Содержание
- 2. Химическая кинетика - то раздел химии, изучающий скорость и механизм химических реакций.
- 3. 6.1 Понятие о скорости и механизме химических реакций. 6.2 Влияние концентрации реагирующих веществ на скорость химических
- 4. Большинство биохимических реакций являются гомогенными (протекающими в одной фазе). Они могут быть как быстрыми (реакции, лежащие
- 5. Средняя скорость гомогенной реакции (υ) равна изменению концентрации вещества в единицу времени: υ = [A] -
- 6. [A]0_ и [A] – исходная и конечная концентрация вещества, моль/л τ - время реакции, с., мин.,
- 7. Средняя скорость гетерогенной реакции, протекающей на границе раздела фаз, равна изменению количества вещества в единицу времени
- 8. где ν0 и ν – количество вещества в начальный и конечный момент времени, моль S –
- 9. Чтобы произошла химическая реакция, необходимо взаимодействие между молекулами реагирующих веществ. Это взаимодействие происходит в форме столкновения
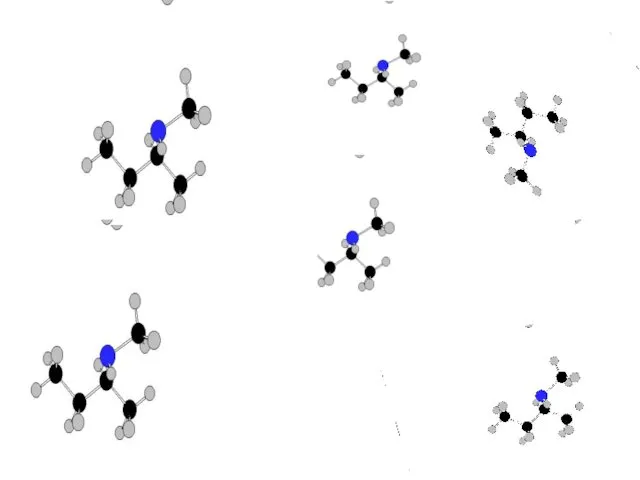
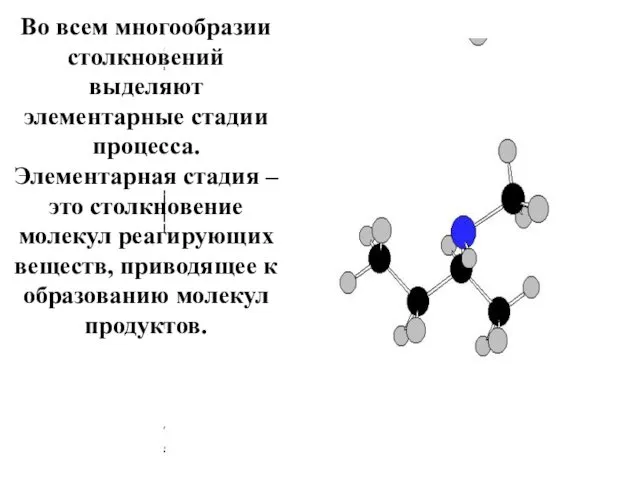
- 11. Во всем многообразии столкновений выделяют элементарные стадии процесса. Элементарная стадия – это столкновение молекул реагирующих веществ,
- 12. Характеристикой элементарной стадии является ее молекулярность, т.е. число участвующих в ней частиц. Стадии могут быть: мономолекулярными
- 13. Механизм химической реакции – это число и последовательность элементарных стадий процесса.
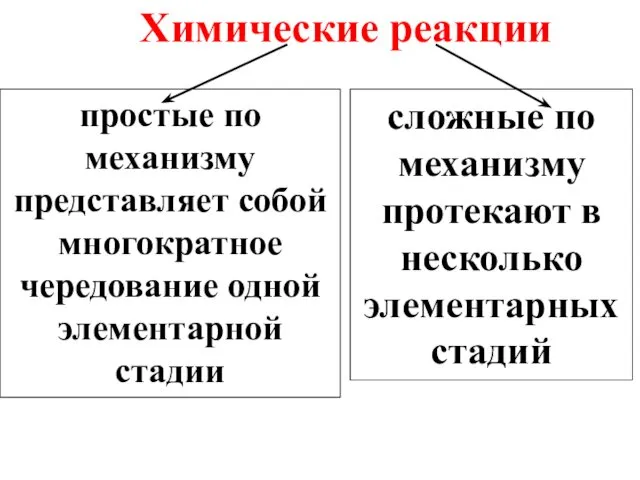
- 14. Химические реакции простые по механизму представляет собой многократное чередование одной элементарной стадии сложные по механизму протекают
- 15. 6.2 Уравнения, описывающие влияние концентрации реагирующих веществ на скорость химических реакций, называются кинетическими уравнениями.
- 16. Кинетические уравнения составляют на основе закона действующих масс (Гульдберг и Вааге,1867): скорость химических реакций прямо пропорциональна
- 17. Математическое выражение ЗДМ для реакции: аА + bВ + cС → Р υ = k [A]x
- 18. k зависит от температуры и природы веществ и не зависти от их концентрации; [A], [B], [C]
- 19. Порядок реакции определяется только экспериментально. Он является величиной формальной и может принимать любые значения: положительные, отрицательные,
- 20. Только для простых реакций порядок и молекулярность совпадают: H2 + I2 → 2HI υ = k
- 21. Кинетическое описание простых реакций. Реакции нулевого порядка (n=0) Примеры: фотохимические, каталитические и ферментативные реакции (при высокой
- 22. Условное уравнение: Константа скорости [A]0 - [A] k = τ А → Р Кинетическое уравнение: υ
- 23. [A] Кинетическая кривая реакций нулевого порядка υ
- 24. Время полуреакции (τ ½) –это время, необходимое для уменьшения концентрации исходного вещества в два раза. [A]0
- 25. Реакции первого порядка (n=1) Примеры: каталитические и ферментативные реакции (при низкой концентрации субстрата), радиоактивный распад, выведение
- 26. Условное уравнение: Константа скорости k = 1 τ [A]0 [A] ℓn А → Р Кинетическое уравнение:
- 27. Кинетическая кривая реакции первого порядка [A] υ
- 28. Время полуреакции: τ ½ = ℓn 2 k
- 29. Кинетика сложных реакций 1) обратимые реакции A B k1 k2 Кинетическое уравнение: υ = k1[A] –
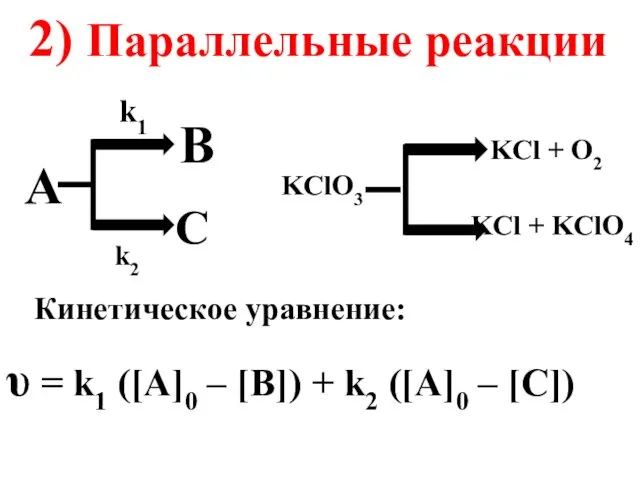
- 30. A B C k1 k2 KClO3 2) Параллельные реакции KCl + O2 KCl + KClO4 Кинетическое
- 31. Скорость реакции равна скорости ее лимитирующей стадии: υ = k2 [B] 3) Последовательные реакции A B
- 32. υ T 6.3 Влияние температуры на скорость может быть различным. Скорость тримолекулярных реакций с ростом температуры
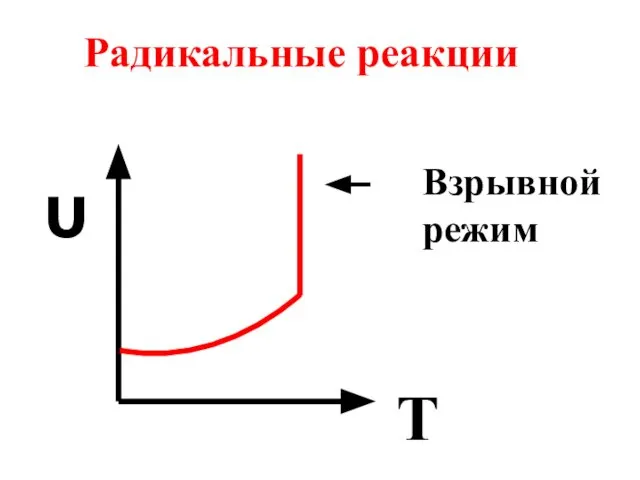
- 33. υ T Взрывной режим Радикальные реакции
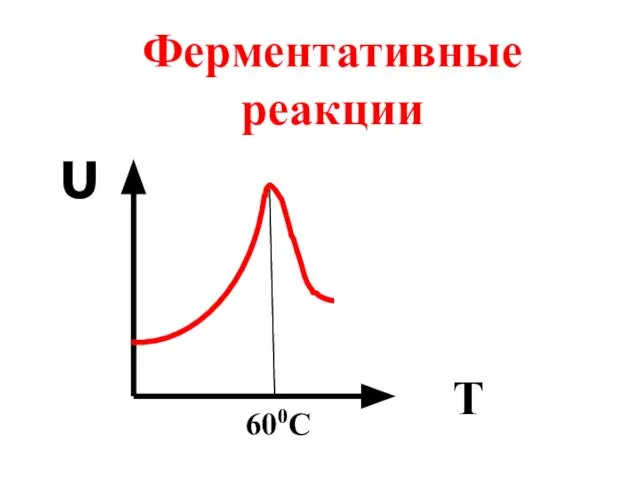
- 34. Ферментативные реакции υ T 600C
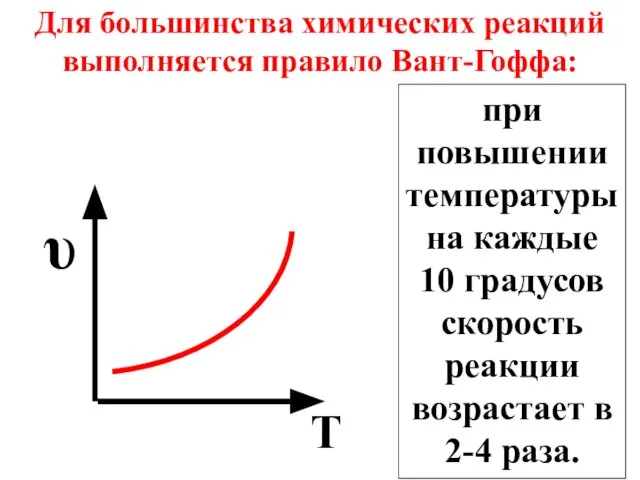
- 35. Для большинства химических реакций выполняется правило Вант-Гоффа: при повышении температуры на каждые 10 градусов скорость реакции
- 36. υT 2 = υT 1 γ T2 – T1 10 где Т1 и Т2 - начальная
- 37. Значительно точнее зависимость скорости и температуры описывается уравнением Аррениуса: -Еак/RT υ = υ 0e k =
- 38. где υ0 и k0 - коэффициенты пропорциональности, называемые предэкспоненциальными множителями, Еак - энергия активации, кДж/моль.
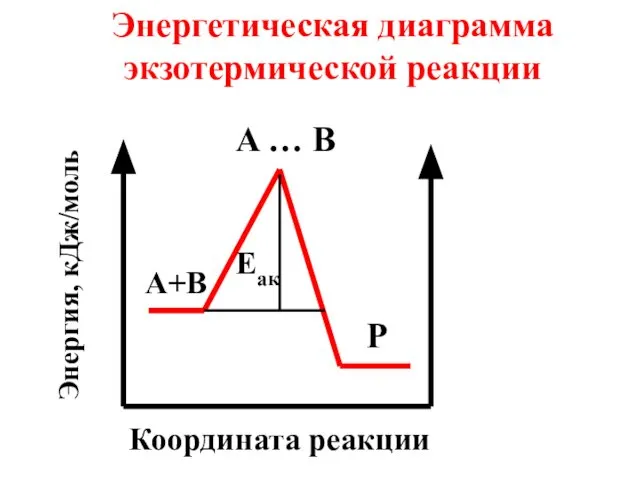
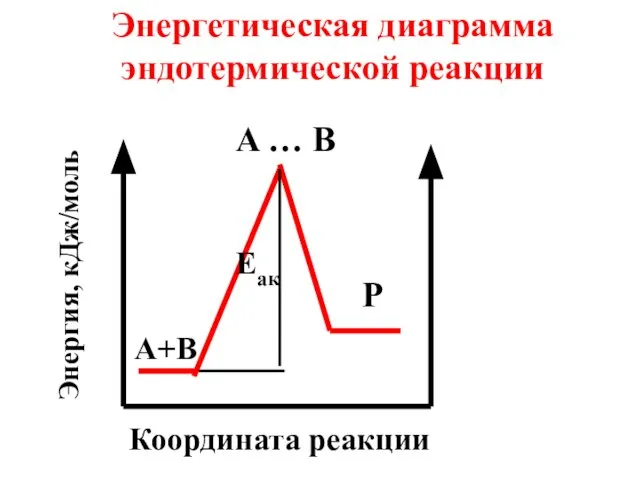
- 39. С точки зрения теории активного комплекса, энергия активации (энергетический барьер химической реакции) - это энергия образования
- 40. Активный комплекс - промежуточная частица, в которой старые связи еще не полностью разорвались, а новые -
- 41. Схема химической реакции : А + В А...В Р А...В - активный комплекс
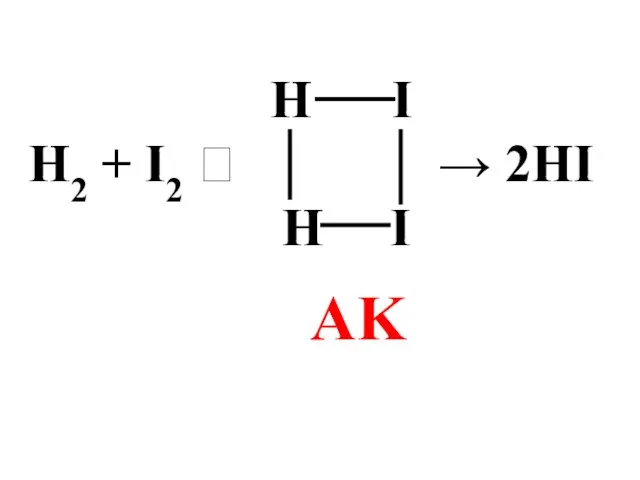
- 42. Н I Н2 + I2 ⮀ → 2HI Н I AK
- 43. Энергетическая диаграмма экзотермической реакции A … B P A+B Eaк Координата реакции Энергия, кДж/моль
- 44. Энергетическая диаграмма эндотермической реакции A … B P A+B Eaк Координата реакции Энергия, кДж/моль
- 45. Энергия активации (Еак) зависит от природы реагирующих веществ и не зависит от температуры.
- 46. С повышением температуры в реакционной смеси возрастает доля активных молекул, способных преодолеть энергетический барьер химической реакции,
- 47. 6.4 Катализаторы – это вещества, изменяющие скорость химической реакции, но не изменяющиеся в ходе процесса ни
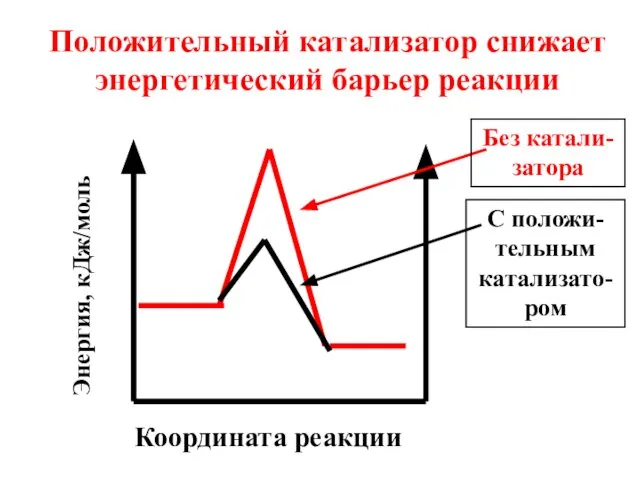
- 48. С точки зрения теории активного комплекса механизм действия катализаторов в том, что они изменяют высоту энергетического
- 49. Координата реакции Положительный катализатор снижает энергетический барьер реакции Энергия, кДж/моль Без катали-затора С положи-тельным катализато-ром
- 50. Под воздействием положи-тельного катализатора в реакционной смеси возрастает доля активных молекул при данной температуре. Скорость реакции
- 51. Координата реакции Отрицательный катализатор повышает энергетический барьер реакции Энергия, кДж/моль Без катали-затора С отрица-тельным ка-тализатором
- 52. Под воздействием отрицательного катализатора в реакционной смеси снижается доля активных молекул при данной температуре. Скорость реакции
- 53. Практически все биохимические реакции являются ферментативными. Фермен-ты (биокатализаторы) – это вещества белковой природы, активированные катионами металлов.
- 54. Ферменты отличаются от обычных катализаторов: а) более высокой каталитической активностью; б) высокой специфичностью, т.е. избирательностью действия.
- 55. Механизм односубстратной ферментативной реакции можно представить схемой: P+ KM k2 Лимитирующая стадия
- 56. Е – фермент, S – субстрат, ЕS – фермент- субстратный комплекс, Р – продукт
- 57. Характеристикой первой стадии ферментативной реакции является КМ – константа Михаэлиса. КМ является величиной, обратной константе равновесия.
- 58. KM KM = 10‾5–10‾3 моль/л Чем меньше КМ, тем устойчивее комплекс .
- 59. Кинетическое уравнение ферментативной реакции: υ = k2 [ES], (1) где k2 – константа скорости, называемая числом
- 60. k2 равна числу молекул субстрата, превращающихся в продукт под воздействием одной молекулы фермента за 1 минуту
- 61. Из-за невозможности экспериментального определения [ES], уравнение (1) преобразовали, выразив [ES] через легко измеряемые параметры реакции.
- 62. υ = [E]общ [S] KM + [S] k2 Кинетическое уравнение ферментативных реакций (уравнение Михаэлиса-Ментен) 1913
- 63. Произведение k2×[E]общ является величиной постоянной, которую обозначают υmax (максимальная скорость) υ = υmax [S] KM +
- 64. При низкой концентрации субстрата KM >> [S], поэтому υ = υmax KM [S] Кинетическое уравнение реакции
- 65. 2) При высокой концентрации субстрата Км Кинетическое уравнение реакции 0-го порядка υ = υmax
- 66. Кинетическая кривая ферментативной реакции [S] υ Реакция нулевого порядка Реакция первого порядка
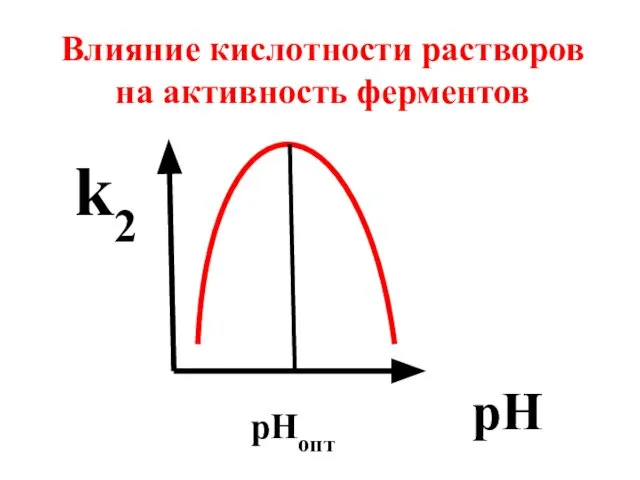
- 67. На активность ферментов оказывают влияние: а) температура, б) кислотность среды, в) наличие ингибиторов
- 68. pH рНопт Влияние кислотности растворов на активность ферментов k2
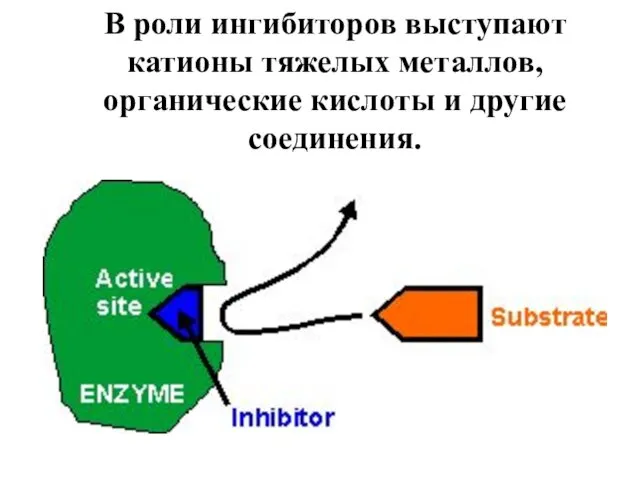
- 69. Ингибиторы ферментов – это вещества, занимающие часть активных центров молекул фермента, в результате чего скорость ферментативной
- 70. В роли ингибиторов выступают катионы тяжелых металлов, органические кислоты и другие соединения.
- 72. Скачать презентацию




![[A]0_ и [A] – исходная и конечная концентрация вещества, моль/л τ](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-5.jpg)












![Условное уравнение: Константа скорости [A]0 - [A] k = τ А](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-21.jpg)
![[A] Кинетическая кривая реакций нулевого порядка υ](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-22.jpg)


![Условное уравнение: Константа скорости k = 1 τ [A]0 [A] ℓn](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-25.jpg)
![Кинетическая кривая реакции первого порядка [A] υ](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-26.jpg)


![Скорость реакции равна скорости ее лимитирующей стадии: υ = k2 [B]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-30.jpg)




















![Кинетическое уравнение ферментативной реакции: υ = k2 [ES], (1) где k2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-58.jpg)

![Из-за невозможности экспериментального определения [ES], уравнение (1) преобразовали, выразив [ES] через легко измеряемые параметры реакции.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-60.jpg)
![υ = [E]общ [S] KM + [S] k2 Кинетическое уравнение ферментативных реакций (уравнение Михаэлиса-Ментен) 1913](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-61.jpg)
![Произведение k2×[E]общ является величиной постоянной, которую обозначают υmax (максимальная скорость) υ](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-62.jpg)
![При низкой концентрации субстрата KM >> [S], поэтому υ = υmax](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-63.jpg)

![Кинетическая кривая ферментативной реакции [S] υ Реакция нулевого порядка Реакция первого порядка](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/464741/slide-65.jpg)


 Эколого-геохимическая оценка состояния компонентов природной среды особо охраняемых территорий. Парк Смоленское Поозерье
Эколого-геохимическая оценка состояния компонентов природной среды особо охраняемых территорий. Парк Смоленское Поозерье Аттестационная работа. Мини-проекты на уроках химии. 8 класс
Аттестационная работа. Мини-проекты на уроках химии. 8 класс Химическая кинетика, химическое равновесие и катализ
Химическая кинетика, химическое равновесие и катализ Простой борный суперфосфат
Простой борный суперфосфат Майкл Фарадей и его открытия в электрохимии
Майкл Фарадей и его открытия в электрохимии Презентация по Химии "МЕТАЛЛИЧЕСКАЯ СВЯЗЬ" - скачать смотреть бесплатно
Презентация по Химии "МЕТАЛЛИЧЕСКАЯ СВЯЗЬ" - скачать смотреть бесплатно Презентация по Химии "Химический КВН" - скачать смотреть
Презентация по Химии "Химический КВН" - скачать смотреть  Current Condition(Revision C)
Current Condition(Revision C) Качество питьевой воды
Качество питьевой воды Галогены. Химические свойства галогенов
Галогены. Химические свойства галогенов Классификация и свойства природных энергоносителей
Классификация и свойства природных энергоносителей Материаловедение. Свойства материалов. (Тема 2)
Материаловедение. Свойства материалов. (Тема 2) Медико-биологическое значение неметаллов. Йод
Медико-биологическое значение неметаллов. Йод Титан. Технология титана
Титан. Технология титана Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы
Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы Алюминий и бор
Алюминий и бор Галогены
Галогены Внеурочная работа по химии. Краеведение
Внеурочная работа по химии. Краеведение Уравнения реакций в молекулярном, полном ионном и сокращенном ионном виде
Уравнения реакций в молекулярном, полном ионном и сокращенном ионном виде Отчет по элективному курсу по химии Тема: «Окислительные свойства концентрированной серной и азотной кислот». Выполнила ученица
Отчет по элективному курсу по химии Тема: «Окислительные свойства концентрированной серной и азотной кислот». Выполнила ученица  Термопластичні Термореактивні
Термопластичні Термореактивні  Гидрогеохимия урана и тория
Гидрогеохимия урана и тория Непредельные углеводороды. Алкины. Уроки 25-26
Непредельные углеводороды. Алкины. Уроки 25-26 Химическая связь
Химическая связь Спирты. Классификация спиртов
Спирты. Классификация спиртов Комплексные соединения
Комплексные соединения Теоретические основы металлургии. Благородные металлы
Теоретические основы металлургии. Благородные металлы Цепная сополимеризация
Цепная сополимеризация