Содержание
- 2. Электрохимия - раздел физической химии, изучающий процессы превращения энергии химической реакции в электрическую и, наоборот, электрической
- 3. Учение об электролитах (главным образом о водных растворах электролитов) Термодинамика электродных процессов(учение об электрохимических равновесиях на
- 4. Глубокая очистка веществ с помощью электролиза Электросинтез Получение тонких пленок, контактов, защитных покрытий Создание химических источников
- 5. Превращение химической энергии питательных (органических) веществ в электрохимическую энергию (зарядка клеточных аккумуляторов) Возникновение биопотенциалов и перенос
- 6. Биоэлектрохимия — изучение электрохимических основ работы живых систем: биоэлектрохимии мембран, биоэлектрокатализа, электрохимии функционирования нервной системы, электропунктурной
- 7. Проводники 1 рода — носителями электричества являются электроны (электронная проводимость). К ним относятся металлы. Проводники 2
- 8. Величина, характеризующая способность вещества проводить электрический ток, называется электропроводимостью. Величина, обратная сопротивлению. Электропроводимость Сопротивление ρ
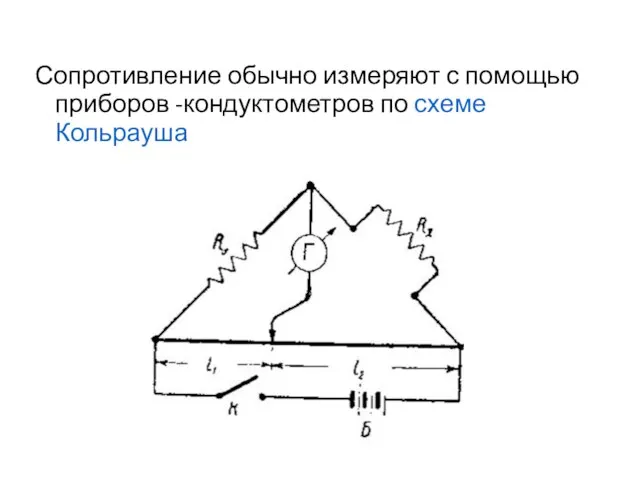
- 9. Сопротивление обычно измеряют с помощью приборов -кондуктометров по схеме Кольрауша
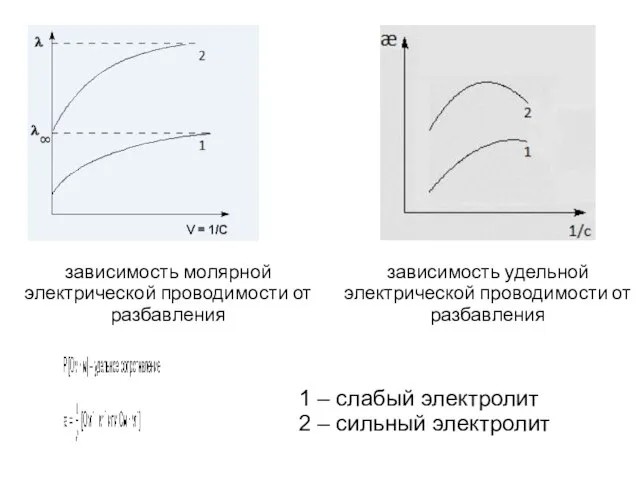
- 10. зависимость удельной электрической проводимости от разбавления зависимость молярной электрической проводимости от разбавления 1 – слабый электролит
- 11. Электропроводимость зависит от: Природы электролита Свойств растворителя Температуры Концентрации раствора Молярная электропроводимость (λ) – электрической проводимость
- 12. молярная электропроводимость Ом-1 ∙ м2∙ моль-1 K= C λ __ 2 Константа диссоциации λ∞(λ∞ - λ)
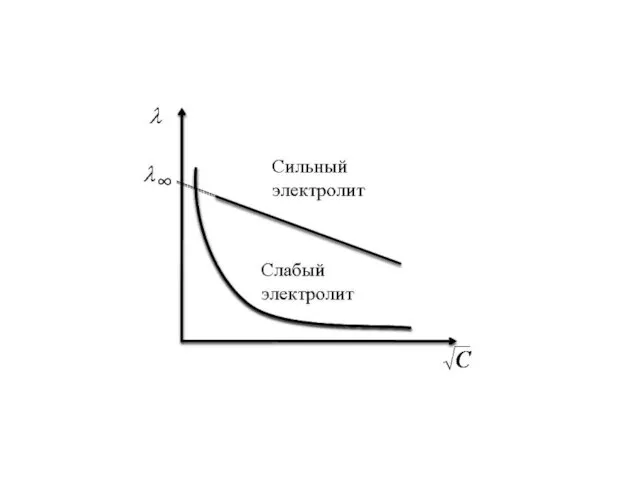
- 13. λ уменьшается при увеличении концетрации раствора: для слабых электролитов это связано с уменьшением количества ионов в
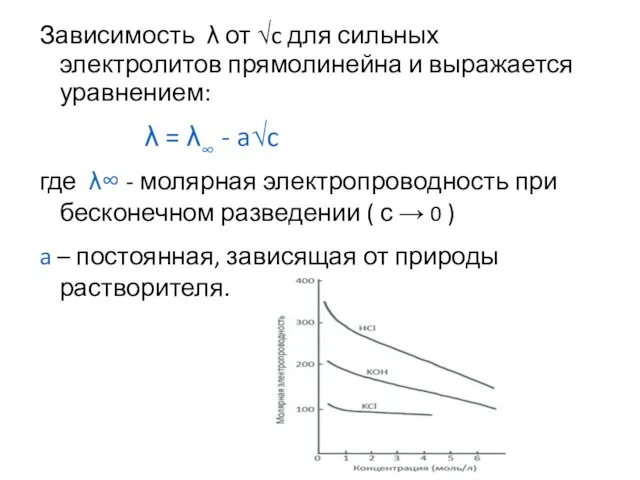
- 14. Зависимость λ от √c для сильных электролитов прямолинейна и выражается уравнением: λ = λ∞ - a√c
- 15. Закон Кольрауша: λ∞ = l∞An + l∞Kt Предельная молярная электрическая проводимость- (λ∞) раствора электролита равна сумме
- 16. ∞
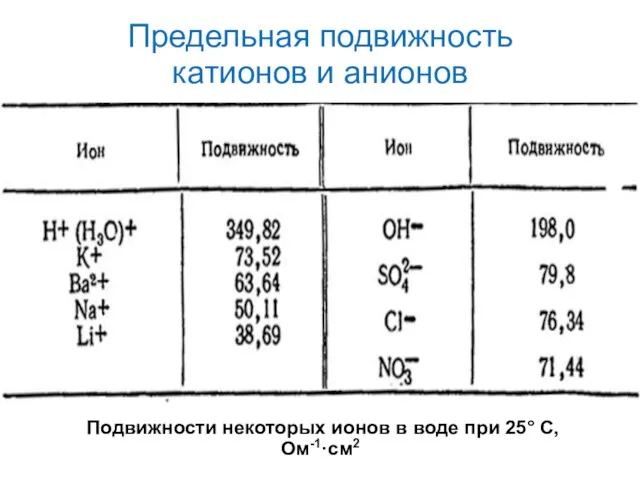
- 17. Предельная подвижность катионов и анионов Подвижности некоторых ионов в воде при 25° C, Ом-1·см2
- 18. Кондуктометрия – физико-химический метод исследования различных систем,основанный на измерении их электрической проводимости. Прямые и косвенные кондуктометрические
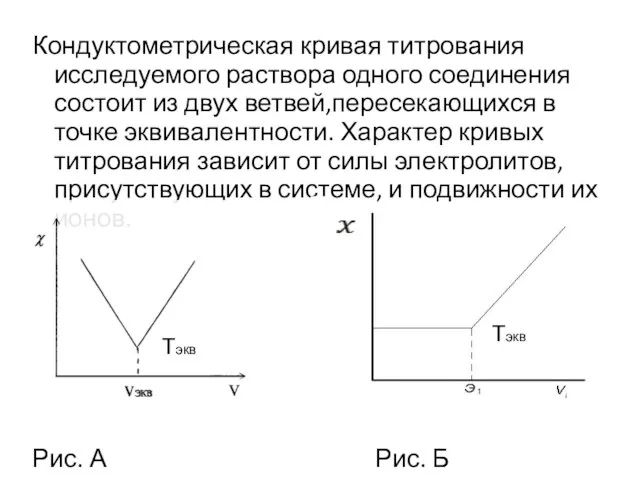
- 19. Кондуктометрическая кривая титрования исследуемого раствора одного соединения состоит из двух ветвей,пересекающихся в точке эквивалентности. Характер кривых
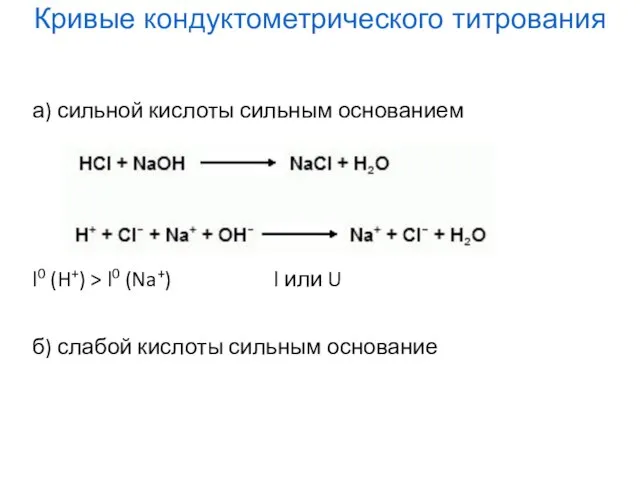
- 20. а) сильной кислоты сильным основанием l0 (H+) > l0 (Na+) l или U б) слабой кислоты
- 21. Электродные потенциалы
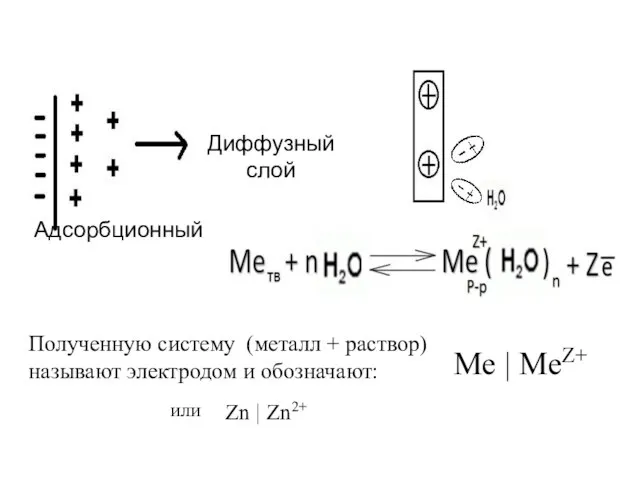
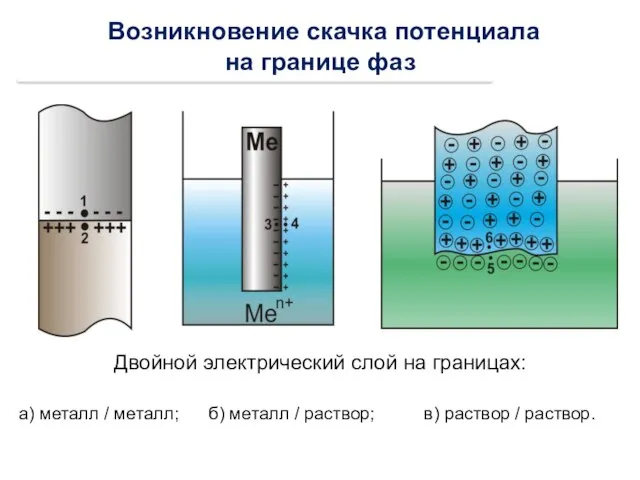
- 22. Диффузный слой Адсорбционный Полученную систему (металл + раствор) называют электродом и обозначают: Zn | Zn2+ Ме
- 23. Возникновение скачка потенциала на границе фаз Двойной электрический слой на границах: а) металл / металл; б)
- 24. 2+
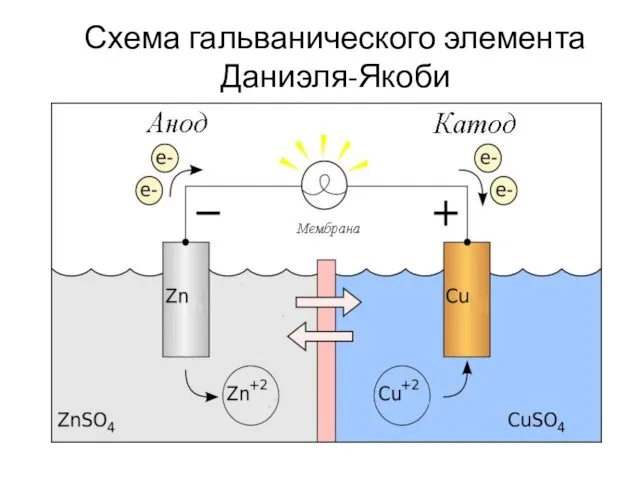
- 25. Схема гальванического элемента Даниэля-Якоби
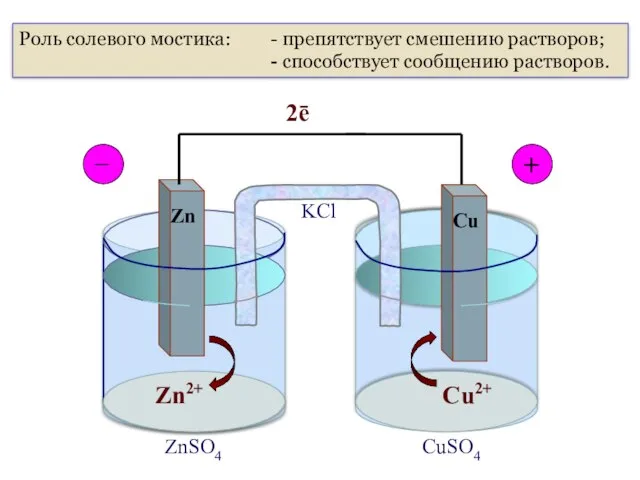
- 26. 4.1. Электрохимические ГЭ Гальванический элемент Даниэля-Якоби Zn2+ Cu2+ 2ē Zn Cu _ + ZnSO4 CuSO4 KCl
- 27. ПРАВИЛО ЗАПИСИ ГЭ: Слева всегда пишется электрод с меньшим стандартным потенциалом, этот электрод называется АНОДОМ (А)
- 28. (тв) (тв) (тв)
- 29. (B) Уравнение НЕРНСТА φ (Mez+, Me) – электродный потенциал металла Me в растворе, содержащем катионы Men+,
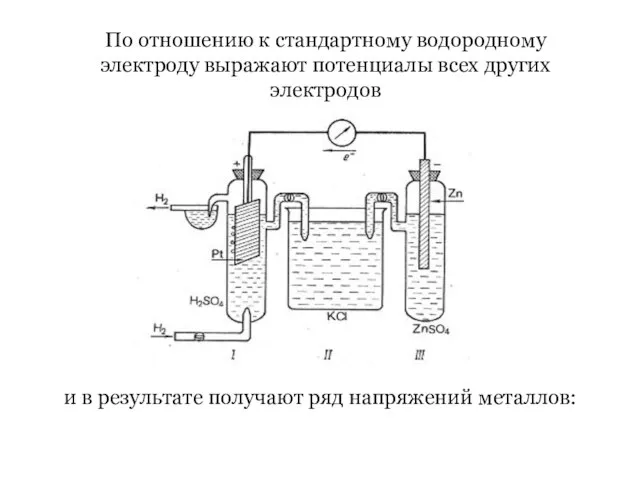
- 30. Измерение электродных потенциалов Электродные потенциалы измеряют с помощью стандартного водородного электрода. При стандартных условиях (t =
- 31. Уравнение Нернста для водородного электрода:
- 32. По отношению к стандартному водородному электроду выражают потенциалы всех других электродов и в результате получают ряд
- 33. Электрохимический ряд напряжений металлов Увеличение потенциала Усиление окислительных свойств Уменьшение химической активности металла Активные Средней активности
- 34. Окислительно – восстановительные системы
- 35. в кислой среде: ,
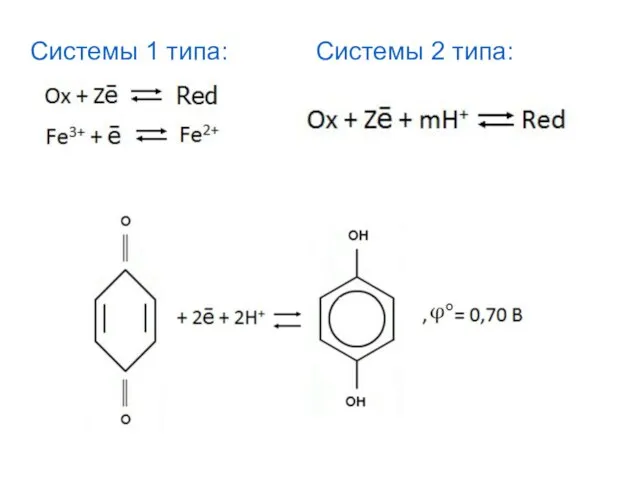
- 36. Системы 1 типа: Системы 2 типа:
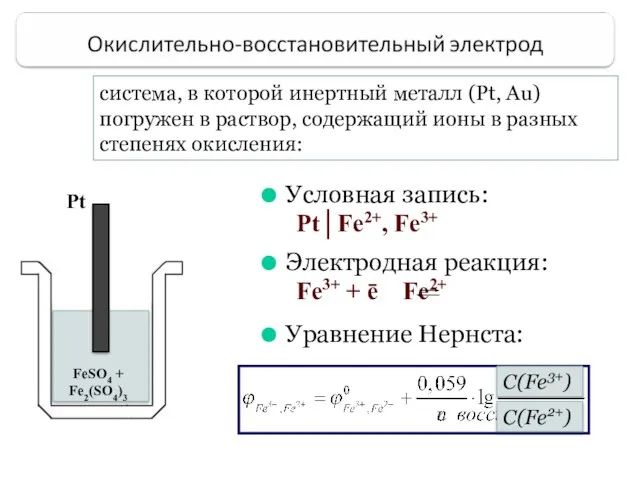
- 38. система, в которой инертный металл (Pt, Au) погружен в раствор, содержащий ионы в разных степенях окисления:
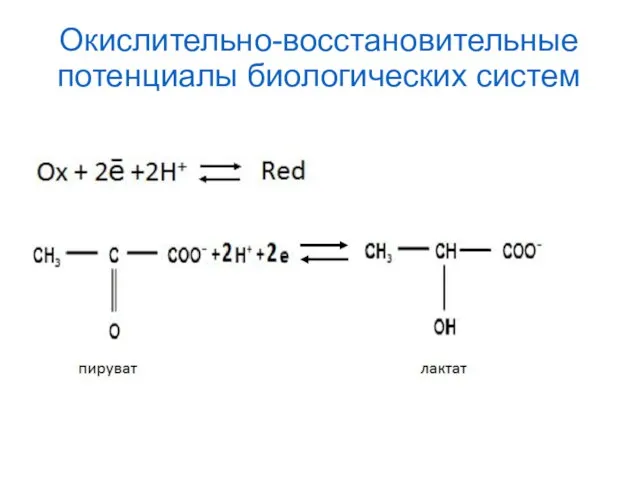
- 39. Окислительно-восстановительные потенциалы биологических систем
- 42. Расчет ЭДС гальванического элемента Электродвижущая сила (ЭДС) – это разность электродных потенциалов катода и анода в
- 43. Направление протекания окислительно-восстановительных реакций Е° = 0 – условие возникновения хим. равновесия Δ G° = -2,3RT
- 44. Электроды: a) I рода Ионно-металлические водородный показатель и б) II рода в) Окислительно-восстановительные эл-ды г) мембранные
- 45. Потенциометрия Потенциометрические методы анализа основаны на измерение электрохимических потенциалов,возникающих на погруженных в раствор индикаторных электродах. Индикаторным
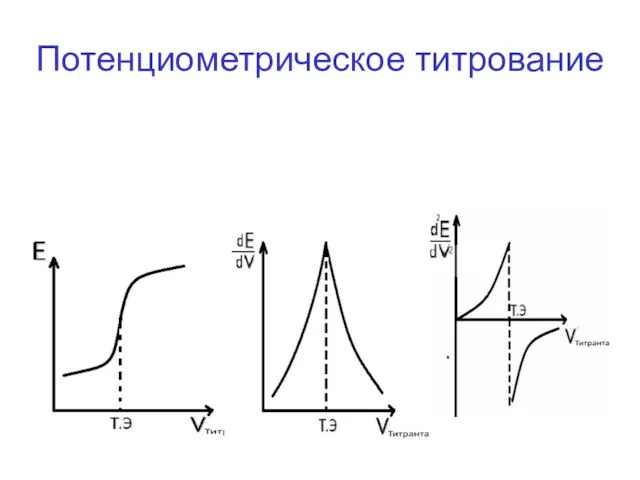
- 46. Потенциометрическое титрование
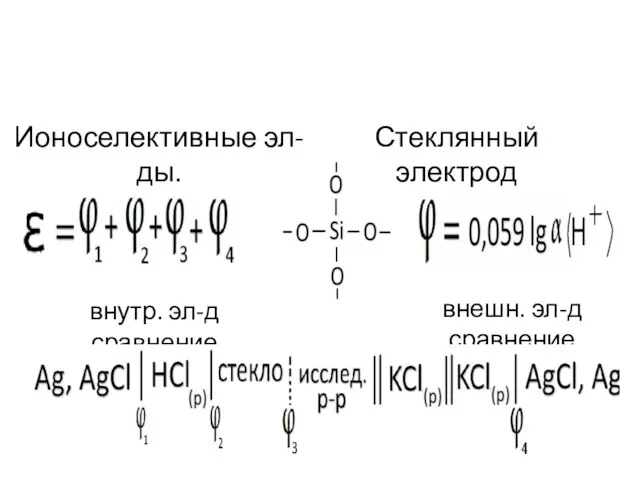
- 48. внешн. эл-д сравнение Ионоселективные эл-ды. Стеклянный электрод внутр. эл-д сравнение
- 49. Хлорсеребряный электрод Для насыщ. KCl:
- 50. Хлорсеребряный электрод - электрод сравнения В насыщенном растворе KCl при температуре 25оС потенциал хлорсеребряного электрода φ
- 52. Скачать презентацию













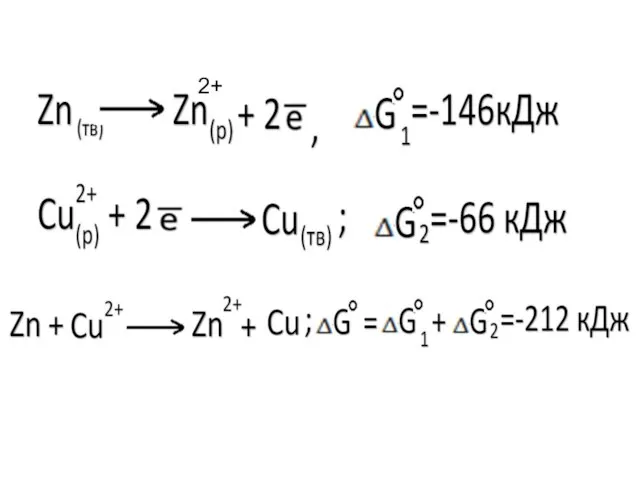







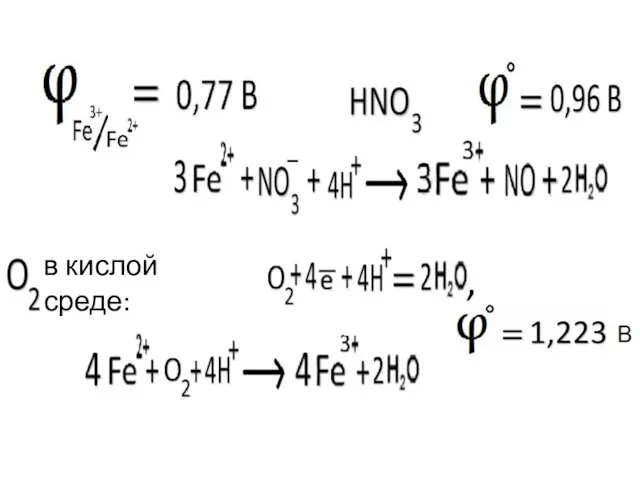










 Аммофос өндірісі. Алыну әдісі
Аммофос өндірісі. Алыну әдісі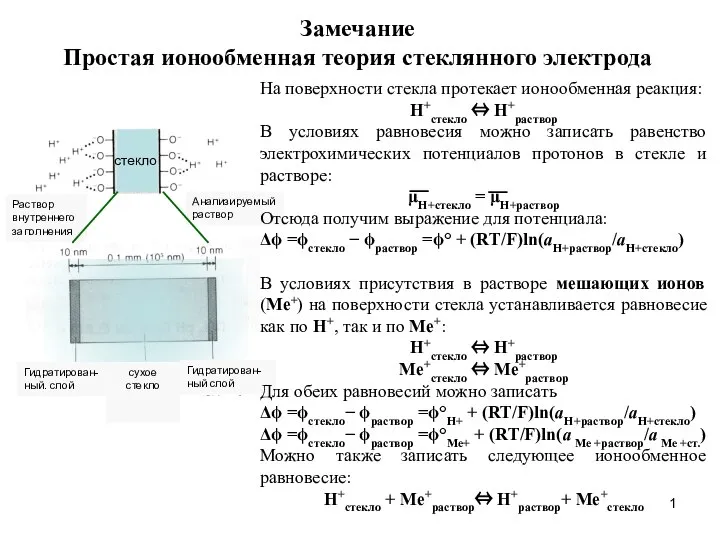 Простая ионообменная теория стеклянного электрода
Простая ионообменная теория стеклянного электрода Марганец. Роль марганца в организме
Марганец. Роль марганца в организме Решение задач Скорость химических реакций 11 класс
Решение задач Скорость химических реакций 11 класс  Парниковий ефект
Парниковий ефект Презентация по Химии "Соли в медицине" - скачать смотреть
Презентация по Химии "Соли в медицине" - скачать смотреть  Сероводоро́д, сернистый водород (H2S) (физические свойства)
Сероводоро́д, сернистый водород (H2S) (физические свойства) Определение содержания солей в нефти
Определение содержания солей в нефти Понятие о химической реакции. Реакции без изменения состава веществ
Понятие о химической реакции. Реакции без изменения состава веществ Формы кристаллов и агрегаты
Формы кристаллов и агрегаты Алкены
Алкены Непредельные углеводороды. Алкены. 9 класс
Непредельные углеводороды. Алкены. 9 класс Периодический закон и периодическая система химических элементов (турнир знатоков химии)
Периодический закон и периодическая система химических элементов (турнир знатоков химии) Тема урока: Силикатная промышленность
Тема урока: Силикатная промышленность Типы химической связи
Типы химической связи Современные конструкционные материалы
Современные конструкционные материалы Коллигативные свойства растворов
Коллигативные свойства растворов Свойства солей
Свойства солей Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4)
Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4) Диоксины, глобальные экотоксиканты
Диоксины, глобальные экотоксиканты Кинетика гетерогенно-каталитических реакций. (Лекция 22)
Кинетика гетерогенно-каталитических реакций. (Лекция 22) Духи
Духи Углеводы. Классификация углеводов
Углеводы. Классификация углеводов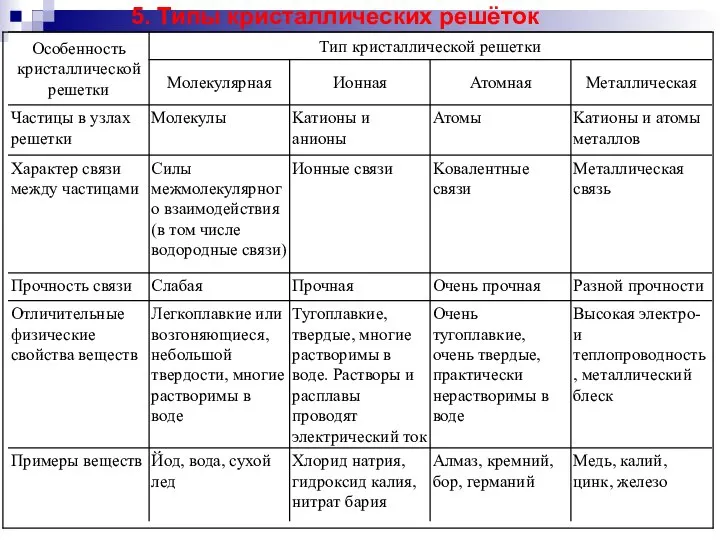 Типы кристаллических решёток. (Лекция 3)
Типы кристаллических решёток. (Лекция 3) Синтетические топлива
Синтетические топлива Основы органической химии. Кислородсодержащие органические соединения
Основы органической химии. Кислородсодержащие органические соединения Биохимия. Химический состав организма
Биохимия. Химический состав организма Углеводороды Выполнили Филаткина Ирина, Филаткина Марина ученица 11 класса МОБУ СОШ № 7 ЛГО
Углеводороды Выполнили Филаткина Ирина, Филаткина Марина ученица 11 класса МОБУ СОШ № 7 ЛГО