Содержание
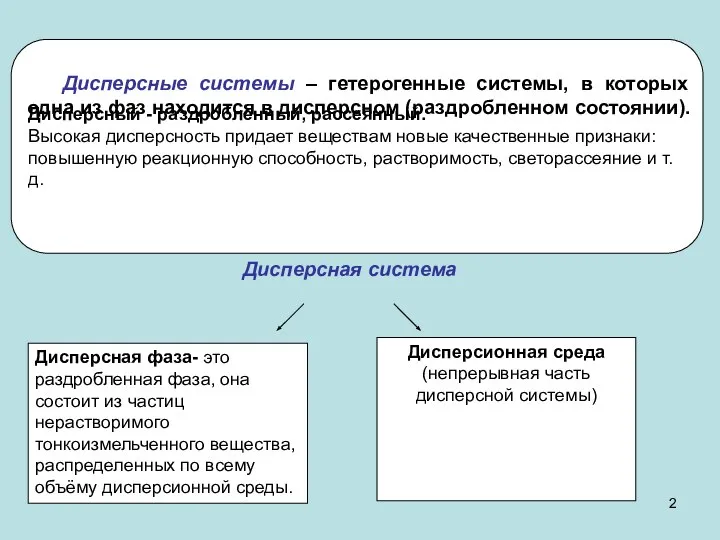
- 2. Дисперсная система Дисперсная фаза- это раздробленная фаза, она состоит из частиц нерастворимого тонкоизмельченного вещества, распределенных по
- 3. Признаки объектов коллоидной химии
- 4. Для коллоидных систем характерно интенсивное броуновское движение частиц дисперсной фазы. По степени взаимодействия между молекулами дисперсной
- 5. Эффект Тиндаля рассеяние света при прохождении светового пучка через оптически неоднородную среду. Обычно наблюдается в виде
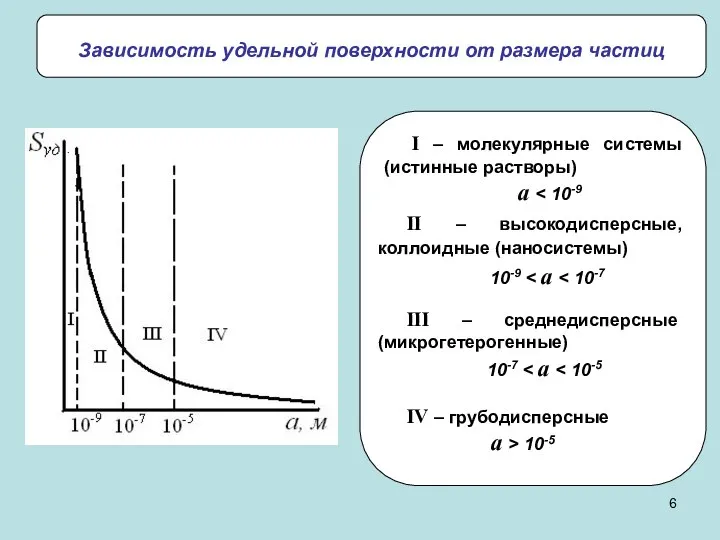
- 6. Зависимость удельной поверхности от размера частиц II – высокодисперсные, коллоидные (наносистемы) 10-9 III – среднедисперсные (микрогетерогенные)
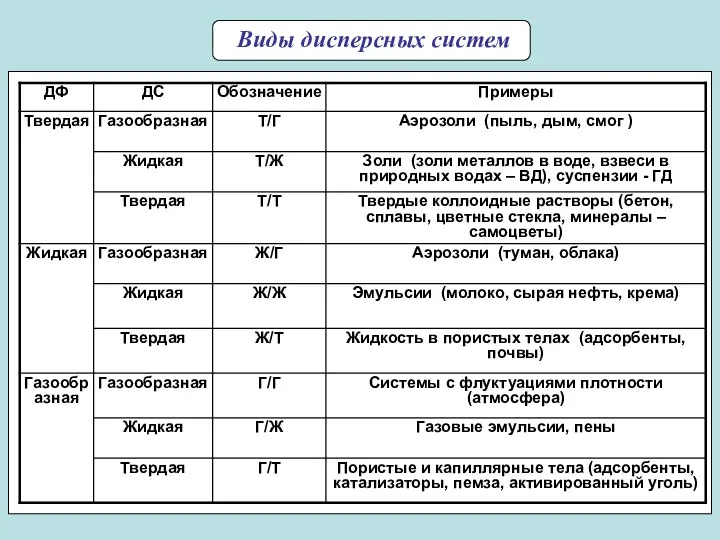
- 7. Виды дисперсных систем
- 8. Дисперсионная среда: ГАЗ Дисперсная фаза: ГАЗ Всегда гомогенная смесь (воздух, природный газ) Дисперсная фаза: Жидкость Туман,
- 9. Дисперсионная среда: Жидкость Дисперсная фаза: ГАЗ Шипучие напитки, пены Дисперсная фаза: Жидкость Эмульсии. Жидкие среды организма
- 10. Дисперсионная среда: Твёрдое вещество Дисперсная фаза: ГАЗ Снежный наст с пузырьками воздуха в нём, почва, кирпич
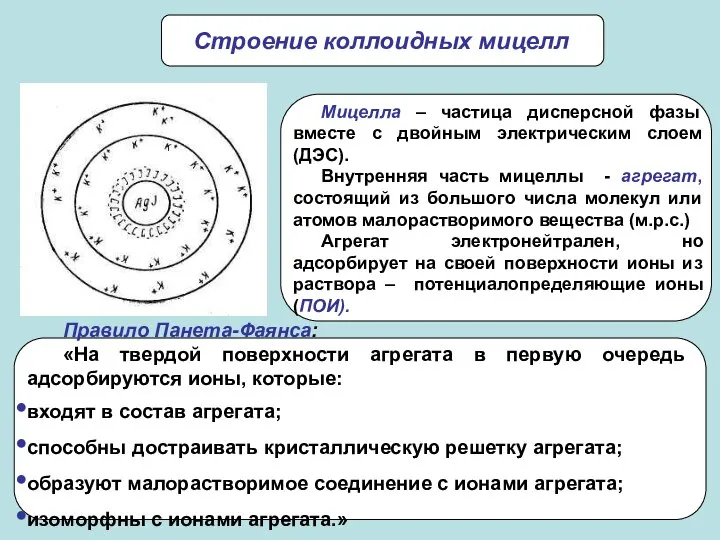
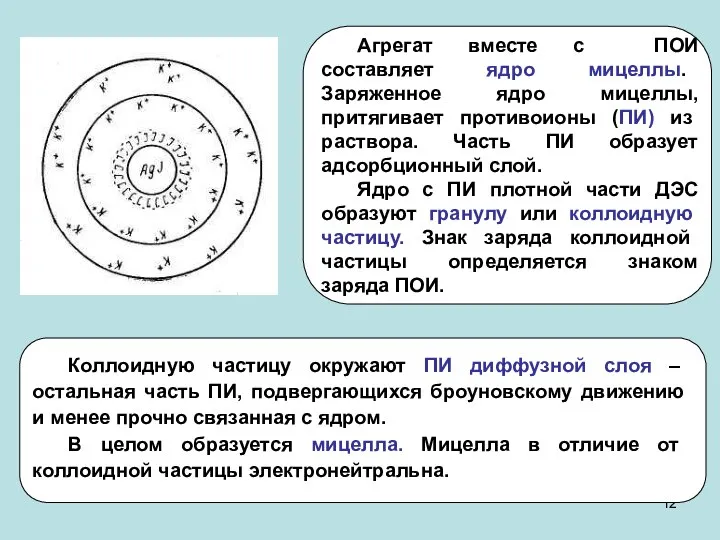
- 11. Строение коллоидных мицелл
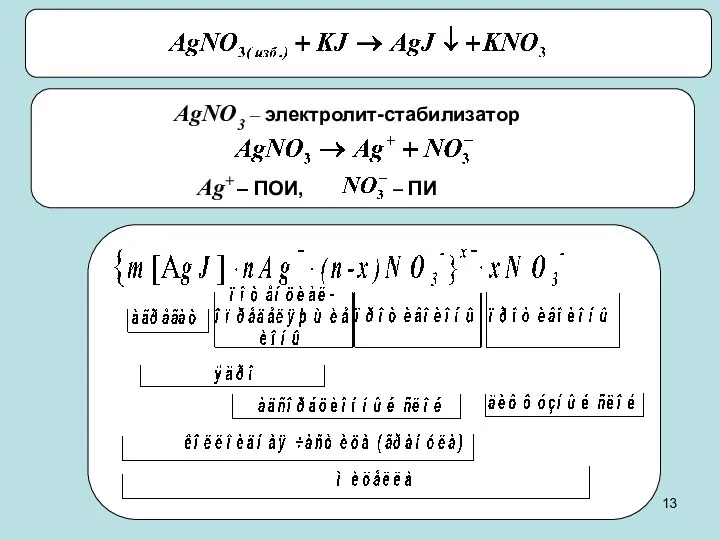
- 14. {m[ AgI ] n I- (n-x) K+}x-x K+
- 15. Получение дисперсных систем измельчение крупных образцов вещества до частиц дисперсных размеров; химический состав и агрегатное состояние
- 16. основаны на ассоциации молекул в агрегаты из истинных растворов; используют для получения высокодисперсных систем; не требуют
- 17. Стадии конденсации 2. Рост зародышей. 3. Формирование слоя стабилизатора (ДЭС).
- 18. Физические конденсационные методы
- 19. Химические конденсационные методы
- 21. 3. Реакции окисления Образование золя серы. 2H2Sр-р + O2 = 2S ↓+ 2H2O Строение мицеллы:
- 22. 4. Реакции гидролиза Получение золя гидроксида железа. FeCl3 + 3H2O = Fe(OH)3 ↓ + 3HCl Cтроение
- 23. Метод пептизации
- 24. Низкомолекулярные примеси (чужеродные электролиты) разрушают коллоидные системы. Диализ – отделение золей от низкомолекулярных примесей с помощью
- 25. Особенности коллоидных растворов Опалесценция (светорассеяние) наблюдается когда λ > d. Чем короче длина волны падающего света,
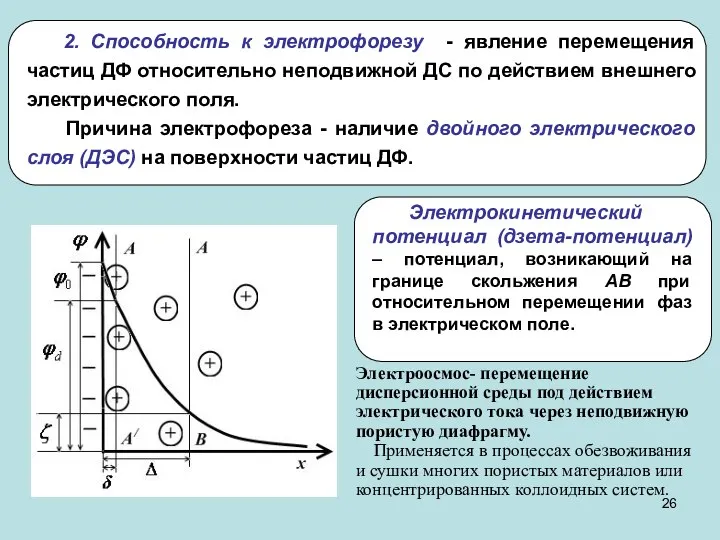
- 26. 2. Способность к электрофорезу - явление перемещения частиц ДФ относительно неподвижной ДС по действием внешнего электрического
- 27. Устойчивость и коагуляция дисперсных систем
- 28. Коагуляция золей электролитами Все электролиты при определенной концентрации могут вызвать коагуляцию золя. Правило знака заряда: коагуляцию
- 29. Порог коагуляции (γ, Спор) – наименьшая концентрация электролита, достаточная для того, чтобы вызвать коагуляцию золя Коагулирующая
- 30. Седиментация Седиментацией называют процесс оседания частиц дисперсной фазы в жидкой или газообразной среде под действием силы
- 31. КОЛЛОИДНЫЕ СИСТЕМЫ В ОРГАНИЗМЕ Можно смело сказать, что весь человек – это ходячий коллоид, а все
- 32. Кости – это коллаген, насыщенный кальцием и фосфором.
- 33. Кровь – это дисперсная система, в которой ферментные элементы эритроциты, тромбоциты, лейкоциты являются фазой, а плазма
- 34. Кожа, мышцы, ногти, волосы, кровеносные сосуды, легкие, весь желудочно-кишечный тракт и многое другое, без чего немыслима
- 36. Скачать презентацию






![{m[ AgI ] n I- (n-x) K+}x-x K+](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1358958/slide-13.jpg)


















 Синильная Кислота - циановодород
Синильная Кислота - циановодород Глюкоза – это спирт, альдегид или альдегидоспирт?
Глюкоза – это спирт, альдегид или альдегидоспирт? Хімічні явища в побуті
Хімічні явища в побуті Валентность химических элементов. 1.Валентность водорода равна единице
Валентность химических элементов. 1.Валентность водорода равна единице Биохимия как наука
Биохимия как наука Кадмий
Кадмий Термодинамическая теория растворов электролитов. Электропроводность растворов электролитов
Термодинамическая теория растворов электролитов. Электропроводность растворов электролитов Аминокилоты. Свойства
Аминокилоты. Свойства Көпатомды спирттер. Химиялық қасиеттері
Көпатомды спирттер. Химиялық қасиеттері Современные проблемы молекулярной биологии
Современные проблемы молекулярной биологии Водород
Водород Кислотно-основные равновесия в растворах
Кислотно-основные равновесия в растворах Свинец. Полезный металл, яд и глобальный загрязнитель
Свинец. Полезный металл, яд и глобальный загрязнитель Предельные углеводороды
Предельные углеводороды Липидтер. Сабынданатын және сабынданбайтын липидтер
Липидтер. Сабынданатын және сабынданбайтын липидтер КАЛЬЦІЙ (Са) Виконала учениця 10-В класу Рахімова Алла
КАЛЬЦІЙ (Са) Виконала учениця 10-В класу Рахімова Алла  Альдегиды и кетоны
Альдегиды и кетоны Презентация по Химии "Уран" - скачать смотреть
Презентация по Химии "Уран" - скачать смотреть  Термодинамічні умови формування природного водню
Термодинамічні умови формування природного водню Многоатомные спирты
Многоатомные спирты Мұнайды өңдеудің химиялық процестерінің теориялық негіздері
Мұнайды өңдеудің химиялық процестерінің теориялық негіздері Алканы. Циклоалканы
Алканы. Циклоалканы Урок-игра. История развития химии
Урок-игра. История развития химии Углеводы. Глюкоза. Простые эфиры. Димедрол
Углеводы. Глюкоза. Простые эфиры. Димедрол Обмен витаминов
Обмен витаминов План выполнения домашней работы по теме «Алкадиены»
План выполнения домашней работы по теме «Алкадиены» Щелочноземельные металлы
Щелочноземельные металлы Витамин A
Витамин A