Содержание
- 2. Введение (цели и задачи курса) Данный курс содержит основные теоретические представления о различных типах реакций полимеризации.
- 3. Практически всё, что окружает нас: одежда, обувь, мебель, продукты питания, книги, строительные и отделочные материалы, да
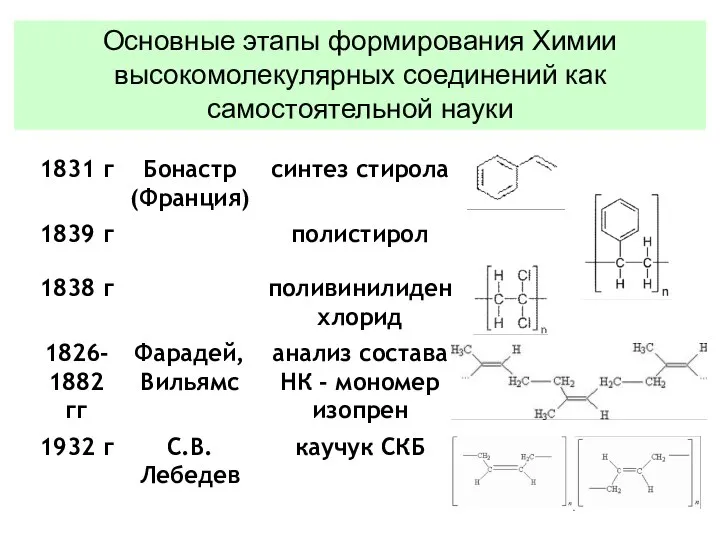
- 4. Основные этапы формирования Химии высокомолекулярных соединений как самостоятельной науки
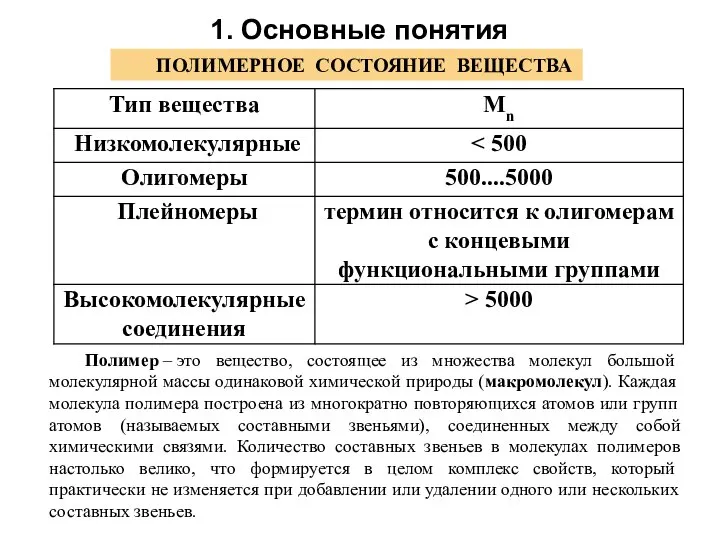
- 6. ПОЛИМЕРНОЕ СОСТОЯНИЕ ВЕЩЕСТВА Полимер – это вещество, состоящее из множества молекул большой молекулярной массы одинаковой химической
- 7. Классификация полимеров по происхождению природные: натуральный каучук, целлюлоза, крахмал, хитин, белки и др. синтетические полимеры (не
- 8. Классификация полимеров по областям применения пластические массы - полимеры, у которых температура стеклования выше температуры эксплуатации
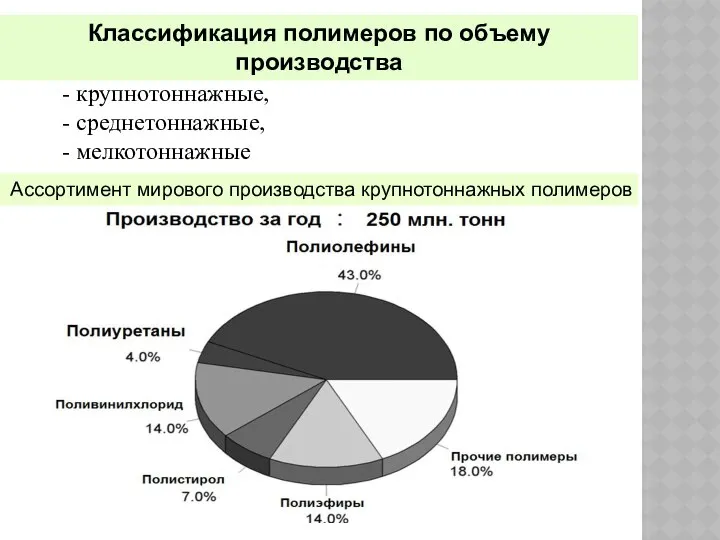
- 9. Ассортимент мирового производства крупнотоннажных полимеров - крупнотоннажные, - среднетоннажные, - мелкотоннажные Классификация полимеров по объему производства
- 10. Мир Европа Динамика производства пластиков млн. т
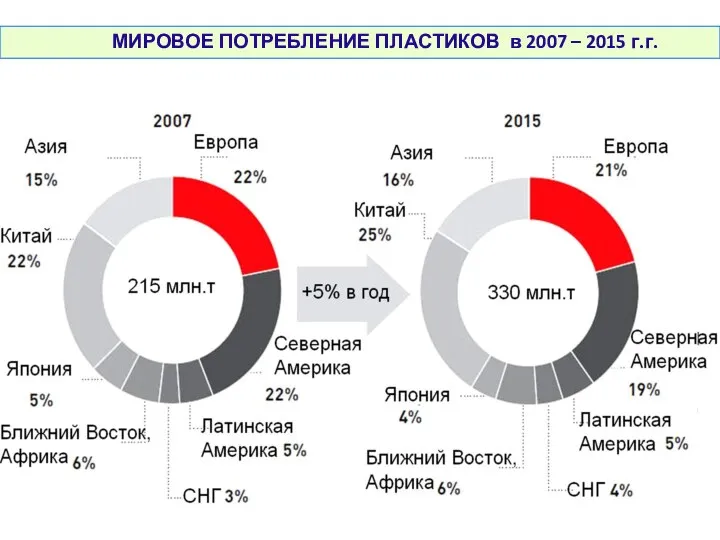
- 11. МИРОВОЕ ПОТРЕБЛЕНИЕ ПЛАСТИКОВ в 2007 – 2015 г.г.
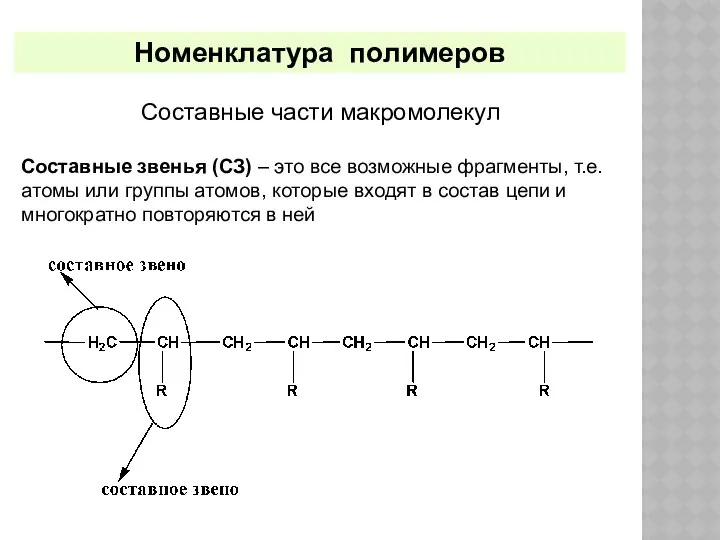
- 12. Номенклатура полимеров Составные части макромолекул Составные звенья (СЗ) – это все возможные фрагменты, т.е. атомы или
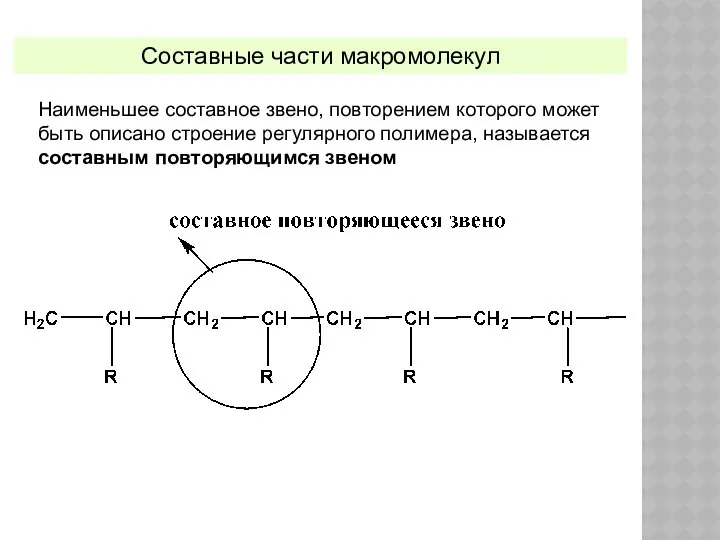
- 13. Наименьшее составное звено, повторением которого может быть описано строение регулярного полимера, называется составным повторяющимся звеном Составные
- 14. Основные виды номенклатуры Номенклатура, основанная на названии мономеров (рациональная номенклатура). Название формируется путем прибавления приставки "поли"
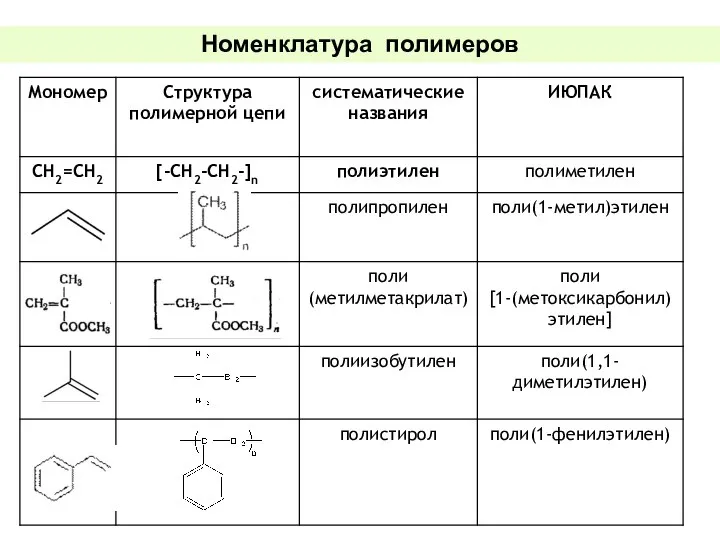
- 15. Номенклатура полимеров
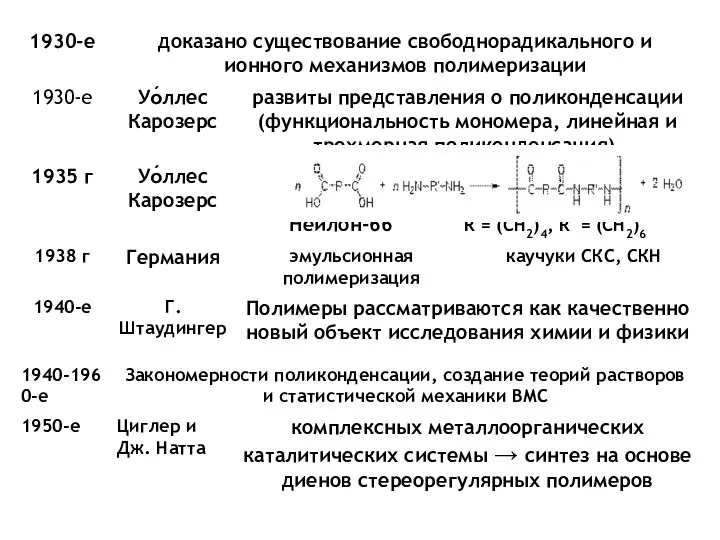
- 17. 2 Введение в теорию полимеризационных процессов Основные типы процесса синтеза полимеров цепная и ступенчатая полимеризация -
- 18. Основные параметры процесса ПМ - термодинамические - кинетические Термодинамические параметры Термодинамические параметры характеризуют возможность протекания процесса
- 20. Для производных этилена 2⋅ЕС-С > ЕС=С, поэтому полимеризация таких мономеров - процесс экзотермический. При T >
- 21. где ΔGо = - RTlnKp - стандартный потенциал при Р = 1 атм и Т =
- 22. Кинетические параметры Кинетические параметры позволяют описать скорость реакции, а также определить характер энергетических затрат, необходимых для
- 23. Длина цепи Полимеризация вызывается первичными активными центрами, образующимися из специально вводимых соединений - инициаторов при радикальной
- 24. Элементарные стадии процесса полимеризации Полимеризационные процессы в общем случае протекают в три этапа: - зарождение цепи,
- 25. Методы проведения процесса Полимеризация мономера может проводиться в растворителе и в отсутствие растворителя. В последнем случая
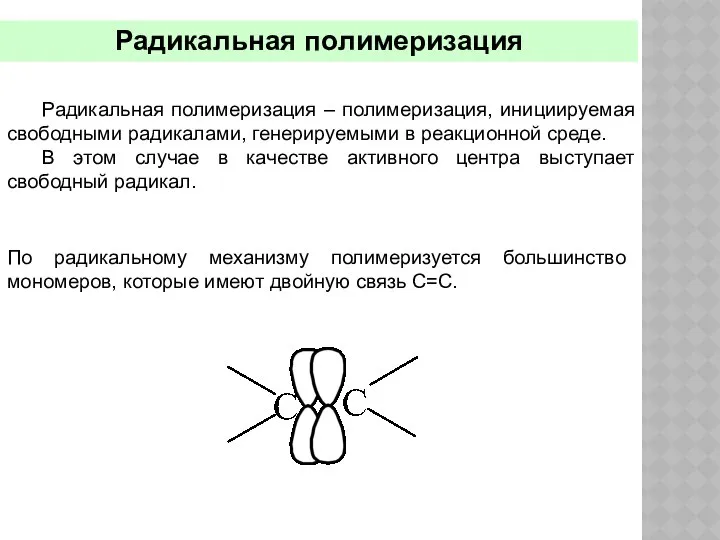
- 26. Радикальная полимеризация Радикальная полимеризация – полимеризация, инициируемая свободными радикалами, генерируемыми в реакционной среде. В этом случае
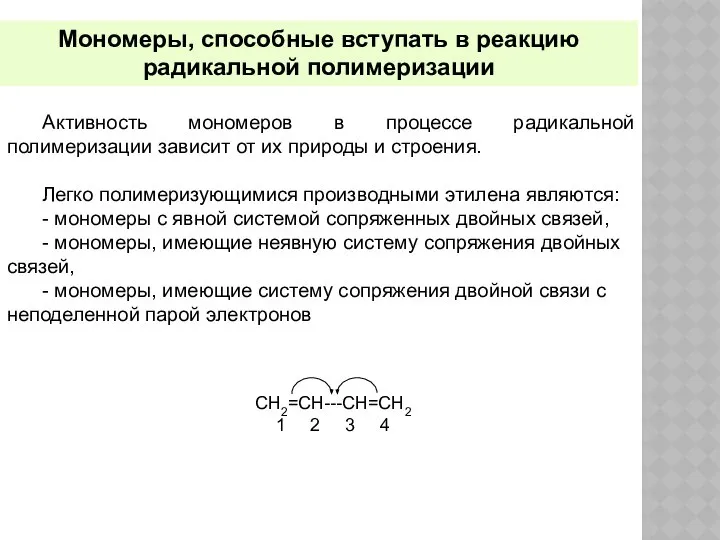
- 28. Мономеры, способные вступать в реакцию радикальной полимеризации Легко полимеризующимися производными этилена являются: - мономеры с явной
- 29. Введение заместителей в молекулу бутадиена приводит к изменению ее активности в реакции полимеризации Введение малополярных заместителей
- 30. Относительные скорости полимеризации различных диеновых мономеров
- 31. Мономеры с неявной системой сопряжения двойных связей стирол, α-метилстирол, нитрил акривой кислоты, CH2=CH-C≡N (НАК), акролеин СН2=СН-С(=О)Н
- 32. Механизм радикальной полимеризации Радикальная полимеризация инициируется свободными радикалами - активными частицами, имеющими неспаренный электрон. Свободные радикалы
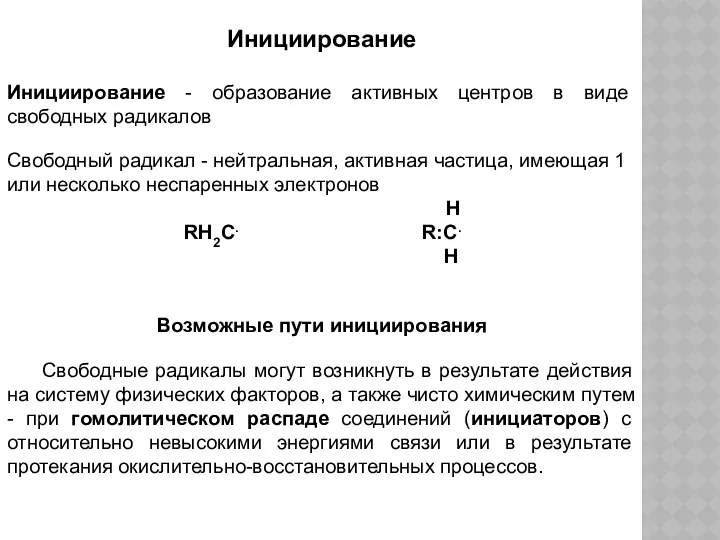
- 33. Инициирование Инициирование - образование активных центров в виде свободных радикалов Свободный радикал - нейтральная, активная частица,
- 34. Гомолитический распад активируется под действием тепла, света, различных активных излучений и других энергетических воздействий. Для того,
- 35. Для перевода молекул в активное состояние существуют следующие методы 1 Инициирование под действием физических факторов: -
- 36. Инициирование под действием физических факторов Термическое инициирование Мономолекулярный механизм инициирования Штаудингера Бимолекулярный механизм инициирования
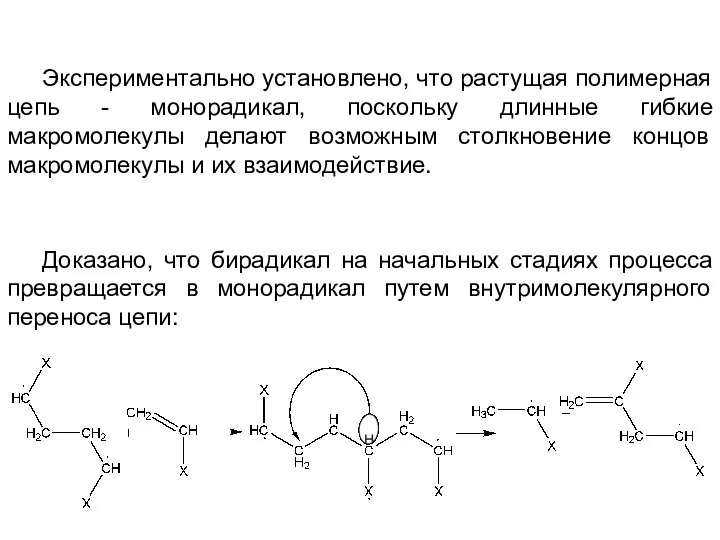
- 37. Экспериментально установлено, что растущая полимерная цепь - монорадикал, поскольку длинные гибкие макромолекулы делают возможным столкновение концов
- 38. Фотохимическое инициирование Инициирование связано с поглощением молекулой мономера кванта световой энергии, энергия которого определяется в виде
- 39. Радиационно-химическое инициирование Протекает под воздействием ионизирующих излучений (α, β, γ-излучение). При этом образуются активные частицы либо
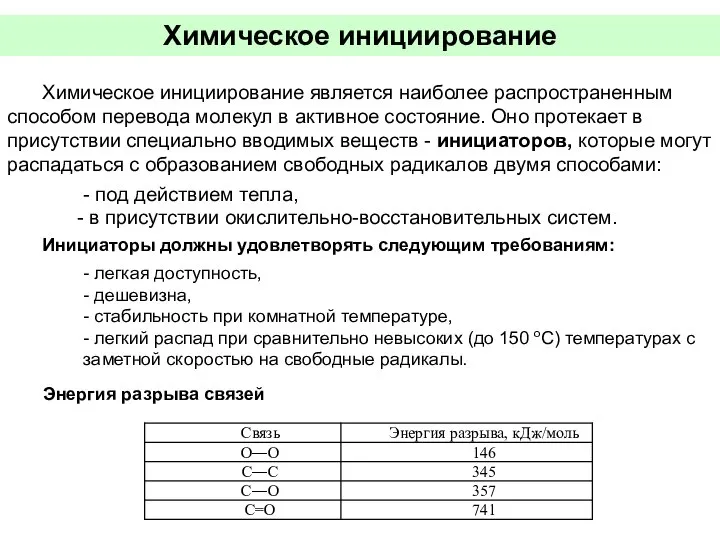
- 40. Химическое инициирование Химическое инициирование является наиболее распространенным способом перевода молекул в активное состояние. Оно протекает в
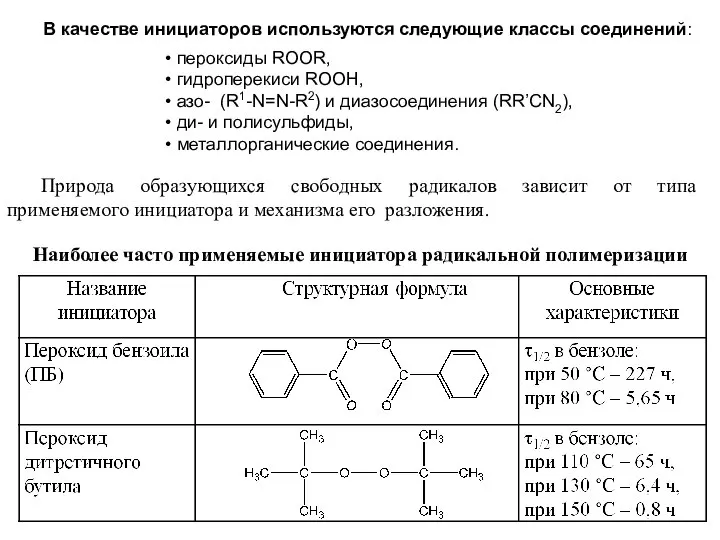
- 41. В качестве инициаторов используются следующие классы соединений: пероксиды ROOR, гидроперекиси ROOН, азо- (R1-N=N-R2) и диазосоединения (RR’CN2),
- 44. Период полураспада (τ1/2): Распад пероксида бензоила Распад третичных гидропероксидов Гидропероксид третичного бутила может распадаться, давая органический
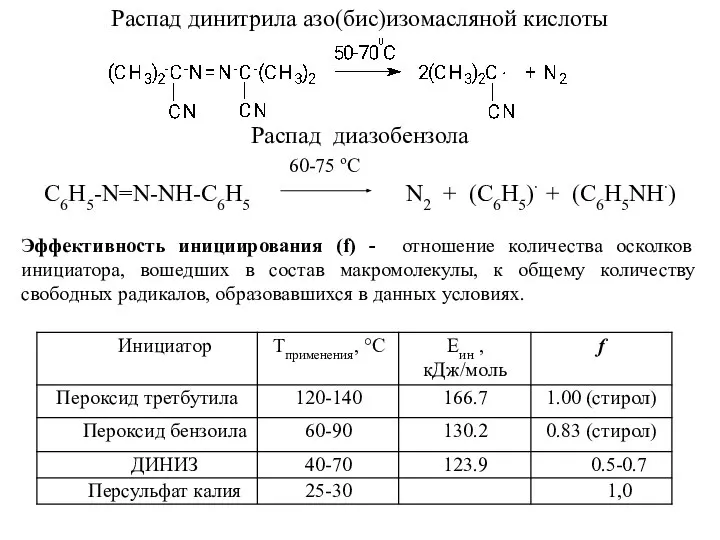
- 45. Распад динитрила азо(бис)изомасляной кислоты Распад диазобензола 60-75 оС С6Н5-N=N-NH-С6Н5 N2 + (С6Н5)∙ + (С6Н5NH∙) Эффективность инициирования
- 46. Эффект клетки (эффект Франко-Рабиновича) Уменьшение количества свободных радикалов в жидкой фазе по сравнению с газовой фазой.
- 47. 3. Выход из клетки: - за счет диффузии [RO∙…O∙R] RO∙ + O∙R - за счет взаимодействия
- 48. Окислительно-восстановительное инициирование 1 При введении в реакционную систему, наряду с основным инициатором – окислителем, достаточно эффективных
- 49. Системы, приводящие к образованию одиночного радикала - Инициирующая система пероксид водорода – соль двухвалентного железа: H-O-O-H
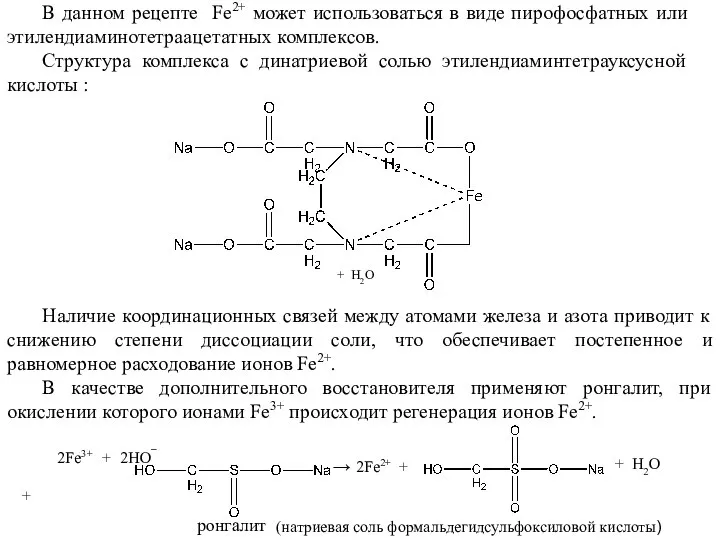
- 50. - Железо-трилон-ронгалитная система. Обратимые окислительно-восстановительные системы нашли широкое применение в процессах синтеза каучуков по технологии низкотемпературной
- 51. В данном рецепте Fe2+ может использоваться в виде пирофосфатных или этилендиаминотетраацетатных комплексов. Структура комплекса с динатриевой
- 52. Первичные свободные радикалы, образовавшиеся по любому из выше перечисленных способов, далее взаимодействуют с молекулой мономера. В
- 53. В ходе реакции происходит выделение тепла. кДж/моль Образование σ = 332,3 кДж/моль Разрыв π-связи = -
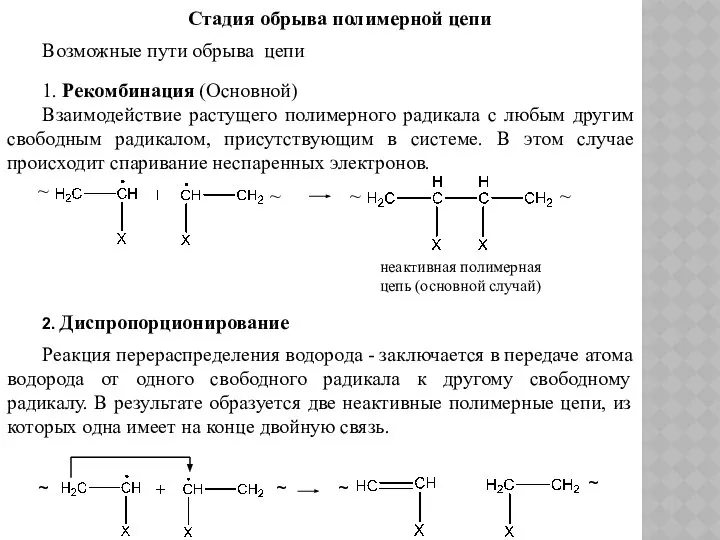
- 54. Стадия обрыва полимерной цепи Возможные пути обрыва цепи 1. Рекомбинация (Основной) Взаимодействие растущего полимерного радикала с
- 55. 3. Столкновении свободных полимерных радикалов с примесями, находящимися в реакционной среде. В результате образуется новый свободный
- 56. При этом могут возникнуть следующие ситуации: а) активность нового свободного радикала может быть равна активности предшествующего
- 57. Способность к участию в передаче цепи при полимеризации характеризуют константами передачи цепи на мономер, на растворитель,
- 58. Передача цепи на мономер ~ ~ Для большинства мономеров значение См невелико (0.1÷5)⋅10-4. Однако при полимеризации
- 59. Бис(изопропилксантоген)дисульфид, дипроксид CBr4 (СS=1.4) Дипроксид, как регулятор ММ, является более активным, чем трет-ДДМ. В то же
- 60. Передача цепи на инициатор Различные инициаторы обладают различной константой передачи цепи. Азонитрилы не участвуют в реакции
- 61. Передача цепи на полимер В том случае, когда мономера в реакционной среде немного, обычно происходит процесс
- 62. 1/Pn 1/Pо [S]/[M] tgϕ = ks ks оценивают для полимеров, полученных при низких степенях превращения мономера.
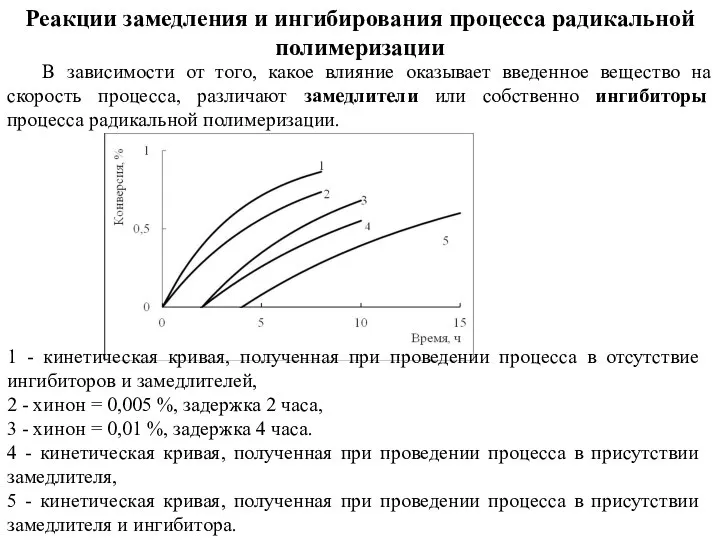
- 63. Реакции замедления и ингибирования процесса радикальной полимеризации В зависимости от того, какое влияние оказывает введенное вещество
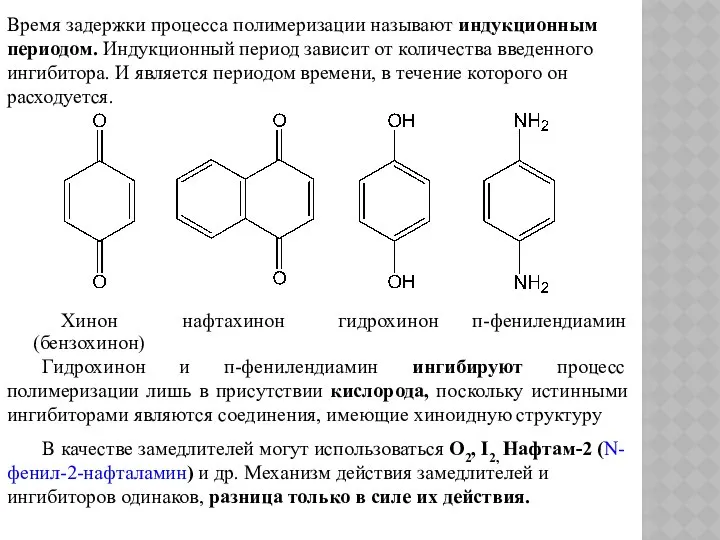
- 64. Время задержки процесса полимеризации называют индукционным периодом. Индукционный период зависит от количества введенного ингибитора. И является
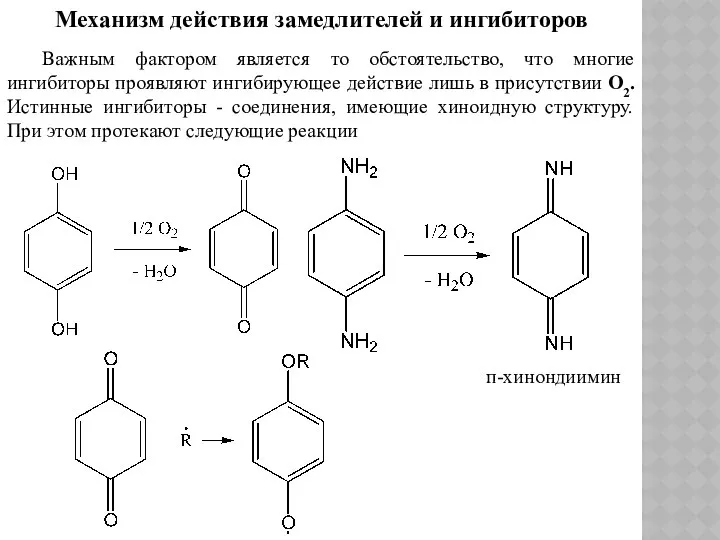
- 65. Механизм действия замедлителей и ингибиторов Важным фактором является то обстоятельство, что многие ингибиторы проявляют ингибирующее действие
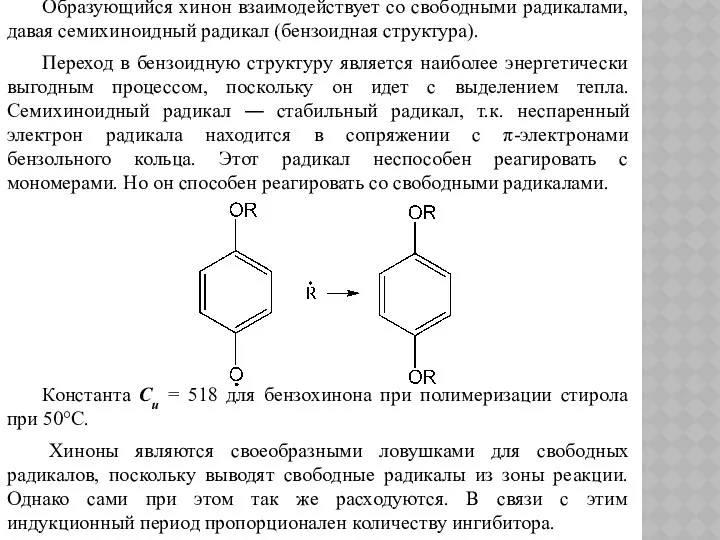
- 66. Образующийся хинон взаимодействует со свободными радикалами, давая семихиноидный радикал (бензоидная структура). Переход в бензоидную структуру является
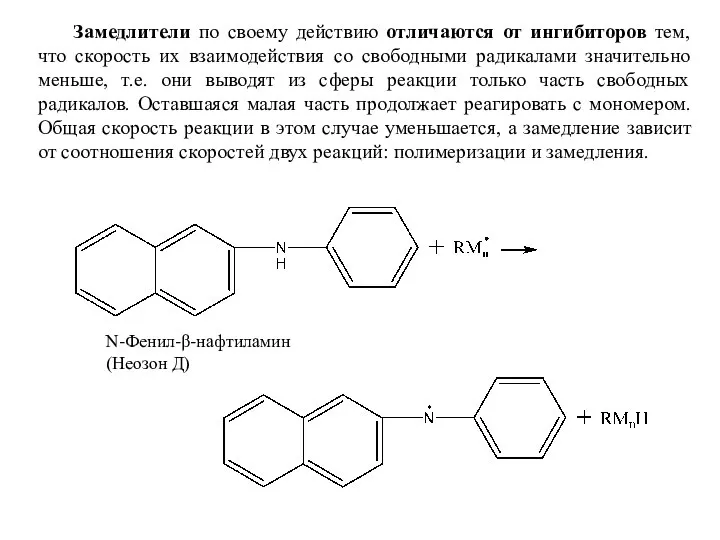
- 67. Замедлители по своему действию отличаются от ингибиторов тем, что скорость их взаимодействия со свободными радикалами значительно
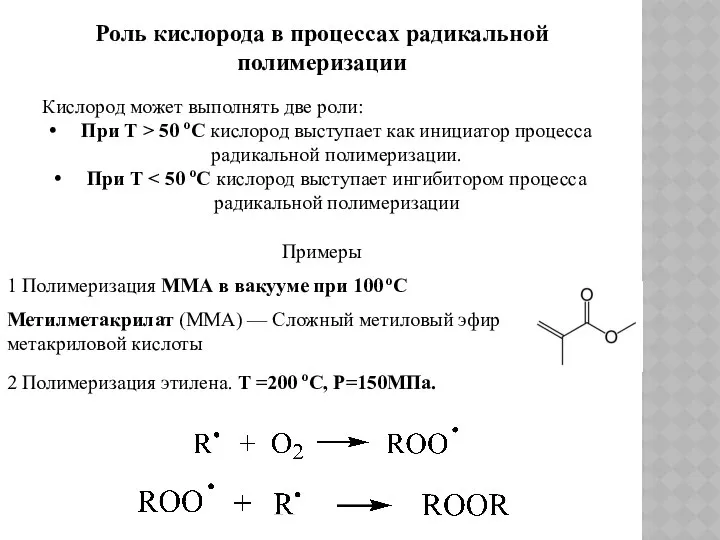
- 68. Роль кислорода в процессах радикальной полимеризации Кислород может выполнять две роли: При Т > 50 оС
- 69. Реакции разветвления и перекрещивания цепей Реакции разветвления и перекрещивания цепей обычно называют вторичными (побочными) реакциями. Образующиеся
- 70. Некоторые особенности полимеризации диенов При полимеризации диенов в зависимости от условий проведения процесса могут получаться полимеры
- 71. Аутополимеризация (самопроизвольная полимеризация) Аутополимеризация - процесс самопроизвольной полимеризации, протекающий без специального внешнего воздействия. При этом образуются
- 72. Передача цепи на полимер Кроме всего прочего возможна передача цепи на полимер, особенно при полимеризации до
- 73. Гель-эффект (эффект Тромсдорфа) Время жизни растущих макрорадикалов мало (10-6-10-9 с), однако при снижении температуры и увеличении
- 74. Кинетический анализ реакции инициированной радикальной полимеризации На кинетике реакции полимеризации и свойствах образующегося полимера отражается множество
- 75. Концентрацию радикалов, которую трудно измерить, можно исключить из рассмотрения, используя принцип Боденштейна или принцип стационарности. Согласно
- 76. Длина кинетической цепи ν (т.е. количество присоединившихся молекул мономера, приходящееся на один образовавшийся активный центр) находяти
- 77. Во многих случаях встречаются оба эти два варианта обрыва цепи: где λ - доля макрорадикалов, обрывающих
- 78. С учетом реакций передачи цепи: где Выражая концентрацию радикала через скорость полимеризации и используя константы передачи
- 79. Например, отношение определяющее скорость полимеризации различных мономеров при [M]=const, [I]=const при 60°С для полимеризующегося с высокой
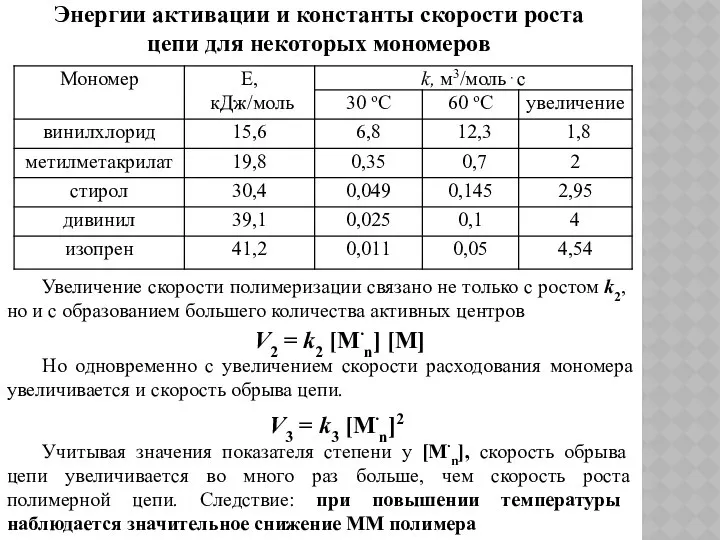
- 80. Влияние различных факторов на процесс радикальной полимеризации Влияние температуры Скорость реакции радикальной полимеризации увеличивается с ростом
- 81. Энергии активации и константы скорости роста цепи для некоторых мономеров Увеличение скорости полимеризации связано не только
- 82. Влияние инициатора С увеличением концентрации инициатора [I] увеличивается число свободных радикалов [R∙]. Следствия: - скорость реакции
- 83. Способы проведения радикальной полимеризации Радикальную полимеризацию проводят в основном: - в блоке (массе), - растворе, -
- 84. Полимеризация в растворе Отсутствуют многие недостатки блочной полимеризации: - устраняется возможность местных перегревов, поскольку теплота реакции
- 85. Полимеризация в суспензии (Бисерная или гранульная полимеризация) широко используется для синтеза различных полимеров. Мономер диспергируют в
- 86. Твердофазная полимеризация Это полимеризация мономеров, находящихся в кристаллическом или стеклообразном состоянии. При этом молекулы мономера жестко
- 87. Полимеризация в эмульсии (Латексная полимеризация - ЛП). Латекс - водная коллоидная дисперсия полимерных частиц размером 10-4-10-5
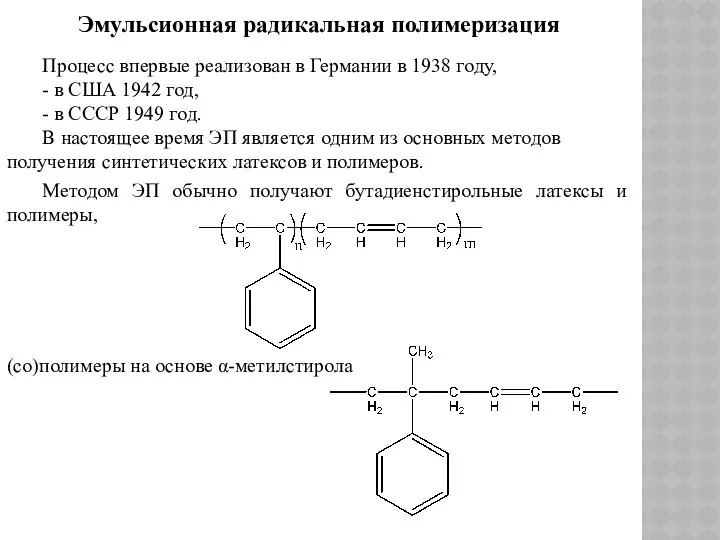
- 88. Эмульсионная радикальная полимеризация Процесс впервые реализован в Германии в 1938 году, - в США 1942 год,
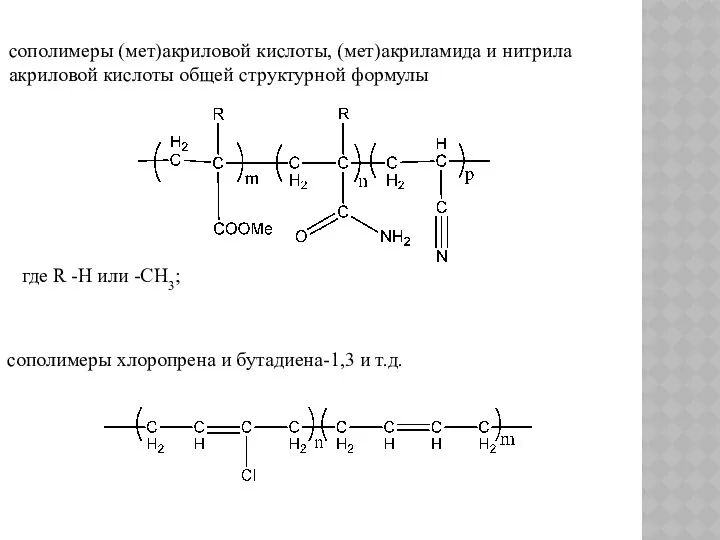
- 89. сополимеры хлоропрена и бутадиена-1,3 и т.д. сополимеры (мет)акриловой кислоты, (мет)акриламида и нитрила акриловой кислоты общей структурной
- 90. Достоинства эмульсионной полимеризации: Возможность осуществления процесса в непрерывном режиме, что обеспечивает однородность получаемого продукта. Низкая вязкость
- 91. Недостатки: Невозможность регулирования микроструктуры полимеров особенно при полимеризации малополярных мономеров. Такие полимеры содержат 80-90 % транс-звеньев.
- 92. Механизм эмульсионной полимеризации и топология процесса Топохимия рассматривает место, где протекают элементарные реакции эмульсионной полимеризации. Образование
- 93. Трудность создания единой теории ЭП обусловливается следующим: Многофазность эмульсионной системы. Многообразие параметров, определяющих механизм и кинетику
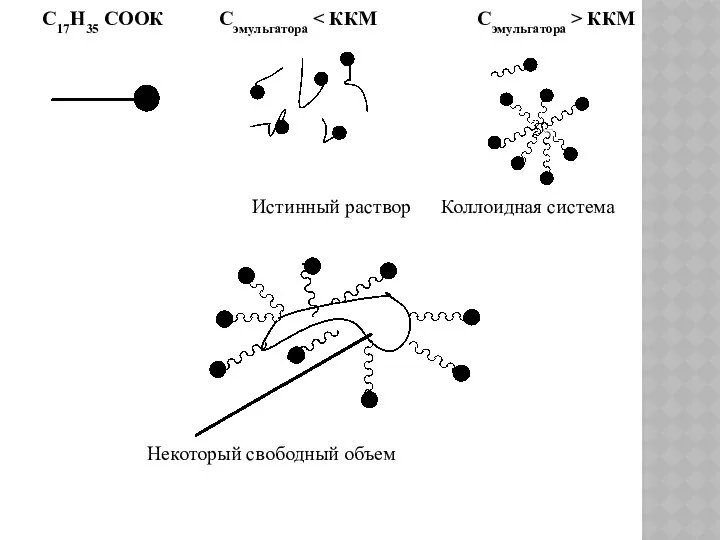
- 94. Минимальная концентрация эмульгатора, при которой наблюдается образование мицелл, называется ККМ. Молекулярная растворимость эмульгатора в воде обычно
- 95. С17Н35 СООК Сэмульгатора ККМ Истинный раствор Коллоидная система Некоторый свободный объем
- 96. С мицеллообразованием тесно связан процесс солюбилизации - коллоидной растворимости мономеров в растворах эмульгаторов. Известно, что большинство
- 97. В том случае, когда в эмульсионной системе процесс протекает в присутствии водорастворимого инициатора, то свободные радикалы
- 98. По ходу полимеризации мицеллы превращаются в ПМЧ, а молекулы мономера первоначально диффундируют и мицеллы, а затем
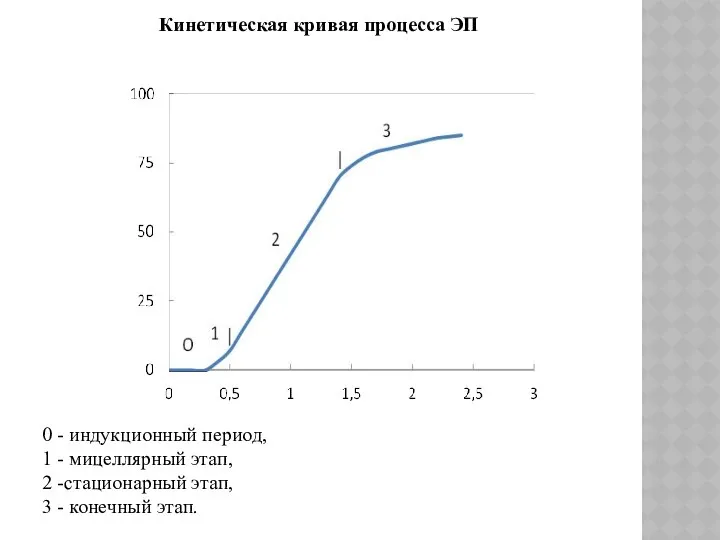
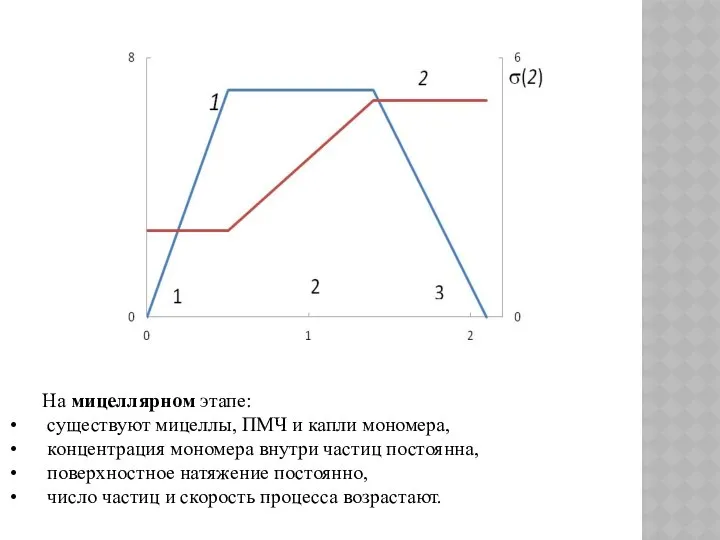
- 99. Кинетическая кривая процесса ЭП 0 - индукционный период, 1 - мицеллярный этап, 2 -стационарный этап, 3
- 100. На мицеллярном этапе: существуют мицеллы, ПМЧ и капли мономера, концентрация мономера внутри частиц постоянна, поверхностное натяжение
- 101. Стационарный этап: существуют ПМЧ и капли мономера, концентрация мономера внутри частиц постоянна, поверхностное натяжение возрастает, поскольку
- 102. Теория Медведева-Хомяковского Согласно этой модели объем ПМЧ не является основной зоной реакции. Адсорбционный слой имеет определенную
- 103. СОПОЛИМЕРИЗАЦИЯ Сополимеризацией называют совместную полимеризацию двух или более мономеров. Она широко используется в практике, поскольку является
- 104. Допущения: - постоянная скорость инициирования; - реакционная способность активного центра постоянна; - все стадии необратимы; -
- 105. Скорости исчерпания мономеров при сополимеризации равны: Поделив эти выражения, получаем отношения концентраций мономерных звеньев в образующемся
- 106. В стационарном состоянии устанавливаются стационарные концентрации активных центров каждого типа. Условием этого вида стационарности является: откуда
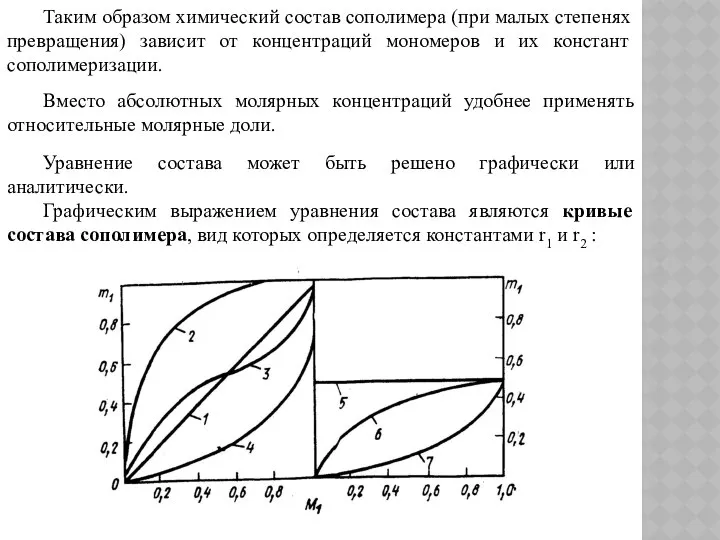
- 107. Параметры r1 и r2 для любой пары мономеров определяются только природой этих мономеров и температурой и
- 108. Таким образом химический состав сополимера (при малых степенях превращения) зависит от концентраций мономеров и их констант
- 110. Статистический анализ чередования звеньев в цепи сополимера указывает на три случая: при r1 r2 =1 звенья
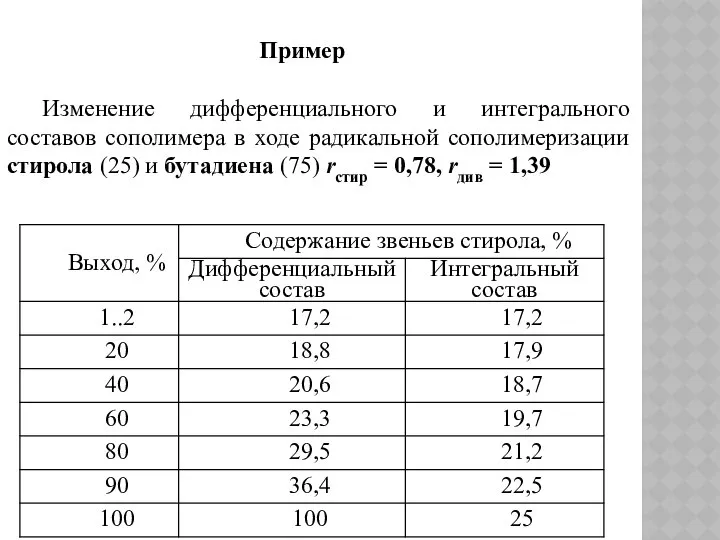
- 111. Дифференциальный и интегральный составы сополимеров Дифференциальный состав сополимера - состав сополимера, образующегося в каждый данный момент
- 112. Изменение дифференциального и интегрального составов сополимера в ходе радикальной сополимеризации стирола (25) и бутадиена (75) rстир
- 113. Константы сополимеризации и их определение Для определения констант сополимеризации необходимо знать: состав сополимера, состав исходной шихты,
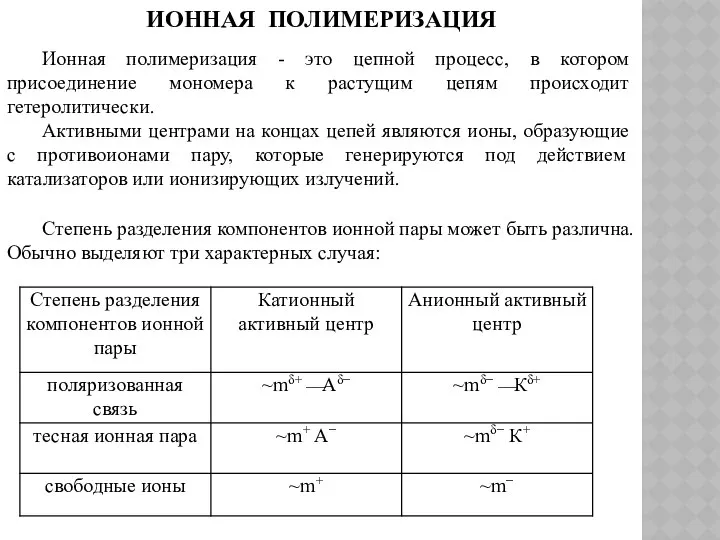
- 114. ИОННАЯ ПОЛИМЕРИЗАЦИЯ Ионная полимеризация - это цепной процесс, в котором присоединение мономера к растущим цепям происходит
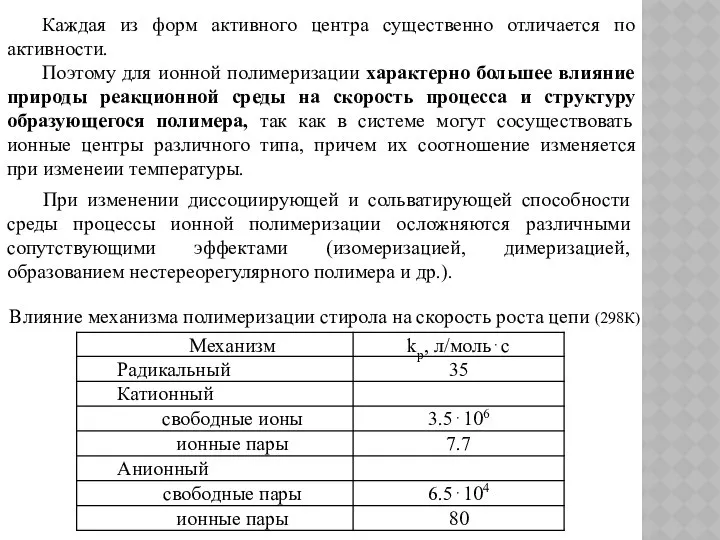
- 115. Каждая из форм активного центра существенно отличается по активности. Поэтому для ионной полимеризации характерно большее влияние
- 116. Внедрение мономера в растущую полимерную цепь осуществляется между заряженным концом растущей макроцепи и противоионом, при этом
- 117. Существенный характер имеет выбор растворителя. Нужен растворитель, который обладает хорошей сольватирующей способностью, не замерзает при понижении
- 118. КАТИОННАЯ ПОЛИМЕРИЗАЦИЯ Впервые катионную полимеризацию осуществил Бутлеров в 1877 году путем полимеризации изобутилена в присутствии серной
- 119. Катализаторы: - протонные кислоты: HClO4, H2SO4, H3PO4, HCl и др.; - апротонные кислоты (кислоты Льюиса, катализаторы
- 120. Реакция инициирования заключается во взаимодействии катиона с мономером. В простейших, но довольно редких случаях, катионы получают
- 121. Рост цепи в катионной полимеризации происходит путем присоединения мономера к макрокатионам или путем его внедрения по
- 122. Обрыв цепи чаще всего происходит в результате мономолекулярной реакции дезактивации активного центра путем внутримолекулярной передачи катиона
- 123. Энергия активации этого процесса положительна, поэтому для увеличения молекулярной массы полимера катионную полимеризация проводят при низких
- 124. Иногда в процессе полимеризации происходит заметное изменение соотношения между активными центрами, находящимися в виде ионных пар
- 125. Отсюда следует, что константа скорости роста цепи kр зависит от концентрации и сольватирующей способности всех компонентов
- 126. АНИОННАЯ ПОЛИМЕРИЗАЦИЯ Систематическое изучение анионной полимеризации ненасыщенных соединений началось в 1920-х годах Лебедевым, Циглером и др.
- 127. Реакция инициирования может осуществляться двумя способами: - по типу кислотно-основного взаимодействия, в результате присоединения к мономеру
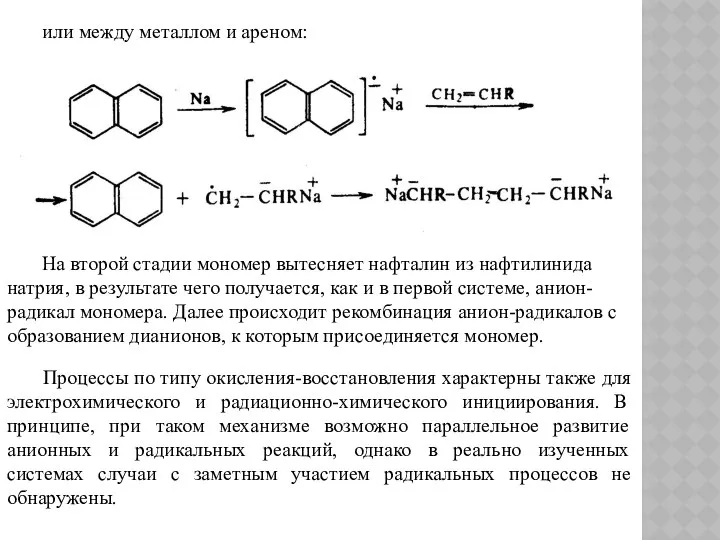
- 128. или между металлом и ареном: На второй стадии мономер вытесняет нафталин из нафтилинида натрия, в результате
- 129. Особенностью анионной полимеризации неполярных мономеров является ассоциация катализатора и растущих цепей в неполярных растворителях и диссоциация
- 130. Полимеризация неполярных мономеров (стирола, бутадиена, изопрена) в углеводородных растворителях нередко сопровождается индукционными эффектами вследствие недостаточной скорости
- 131. Рост цепи для анионной полимеризации характерен относительной стабильностью активных центров. Например, для неполярных полимеров в углеводородных
- 132. В наибольшей степени ориентирующее влияние противоиона проявляется в углеводородной среде, где присутствует Li, наиболее стереоспецифичного из
- 133. Чаще всего общей реакцией обрыва цепи является перенос гидрид-иона на противоион или мономер: ~ ~ ~
- 134. Общая кинетическая картина анионной полимеризации существенно осложнена упомянутой выше множественностью форм существования активных центров. Помимо указанных
- 135. Часто наблюдаются более сложные зависимости общего вида: где учитывается вклад различных форм активных центров. Обычно порядок
- 136. ИОННО-КООРДИНАЦИОННАЯ ПОЛИМЕРИЗАЦИЯ Если акту внедрения мономера в растущую полимерную цепь предшествует акт его координации на активном
- 137. Добавление всего лишь нескольких процентов электронодонорного соединения (эфира, тетрагидрофурана, алкиламина) резко меняет микроструктуру полиизопрена, становится преобладающей
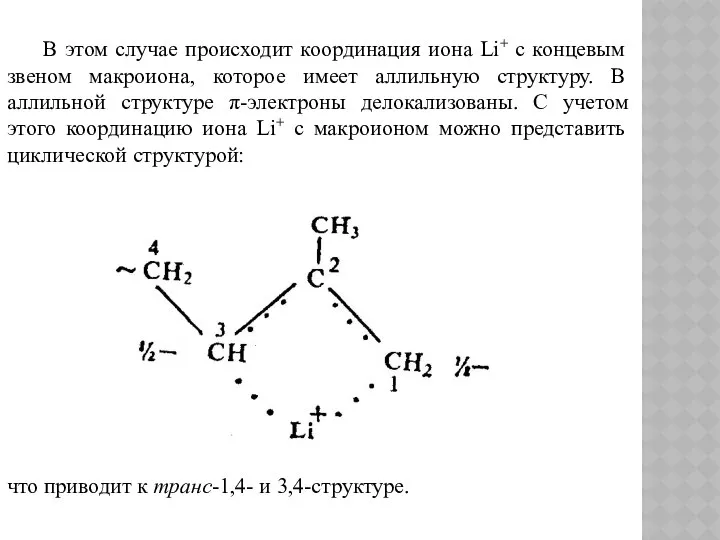
- 138. В этом случае происходит координация иона Li+ с концевым звеном макроиона, которое имеет аллильную структуру. В
- 139. В 1955 году немецкий химик Карл Циглер (для получения полиэтилена в мягких условиях 50-80°С и 1
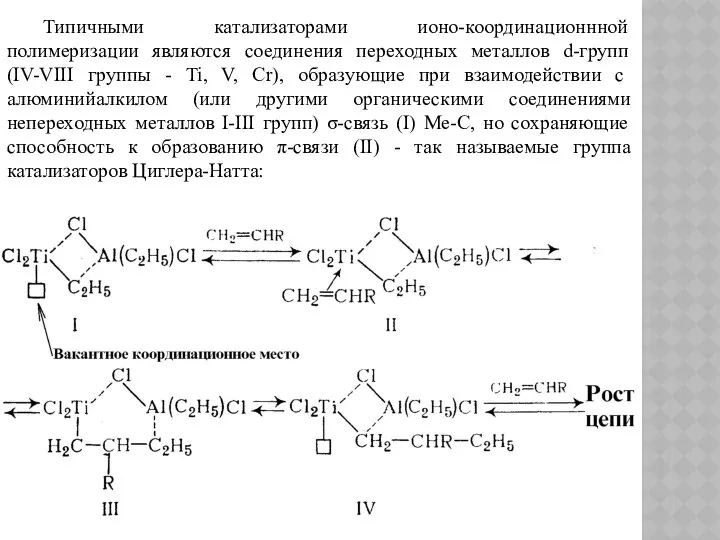
- 140. Типичными катализаторами ионо-координационнной полимеризации являются соединения переходных металлов d-групп (IV-VIII группы - Ti, V, Cr), образующие
- 141. В акте координации мономер выступает в роли донора π-электронов, а переходный металл катализатора Ti, благодаря наличию
- 142. Стереоспецифичность каталитических систем типа Циглера-Натта обусловлена влиянием лигандного окружения в координационной сфере переходного металла, тогда как
- 143. Скорость роста цепи может быть выражена кинетическим уравнением, похожим на подобное для анионной полимеризации: где [I]
- 144. ПОЛИКОНДЕНСАЦИЯ Поликонденсация - это синтез полимеров взаимодействием би- или полифункциональных мономеров или олигомеров, обычно сопровождающийся выделением
- 145. Большой вклад в развитие знаний о процессах поликонденсации внесли отечественнве ученые: В.В. Коршак, Г.С. Петров, К.Д.
- 146. КЛАССИФИКАЦИЯ И ТЕРМИНОЛОГИИ Поликонденсация бифункциональных мономеров называется линейной. Поликонденсация, в которой участвует хотя бы один мономер,
- 147. По типу (и числу) участвующих в реакции мономеров различают: - гомополиконденсацию (участвует один мономер с различными
- 148. При поликонденсации часто возможны обратная и различные обменные реакции. В зависимости от вклада этих реакций различают
- 149. 1) Мономеры (например, диамины или дихлорангидриды дикарбоновых кислот), содержащие в молекулах одинаковые функциональные группы, не способные
- 150. В условиях поликонденсации возможны случаи, когда функциональные группы одного или нескольких мономеров реагируют как друг с
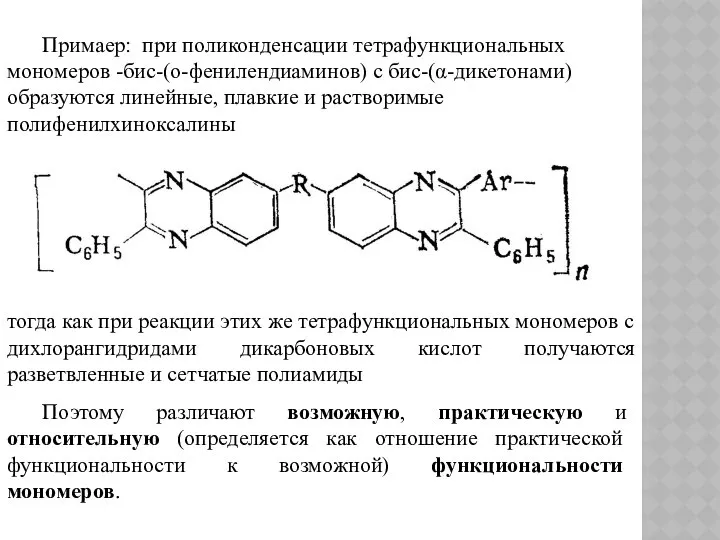
- 151. Примаер: при поликонденсации тетрафункциональных мономеров -бис-(о-фенилендиаминов) с бис-(α-дикетонами) образуются линейные, плавкие и растворимые полифенилхиноксалины тогда как
- 152. Часто ограничиваются рассмотрением средней функциональности: т.е. среднее количество функциональных групп, приходящихся на одну молекулу. Для поликонденсации
- 153. Например, при получении сложных полиэфиров гидроксилсодержащие мономеры могут быть заменены на галогенсодержащие или сложные эфиры, а
- 154. При этом взаимодействие мономеров или образовавшихся олигомеров друг с другом (и олигомеров и мономеров между собой)
- 155. Таким образом росту полимерной цепи при равновесной поликонденсации сопутствует обратная реакция полимера с выделяющимся низкомолекулярным продуктом,
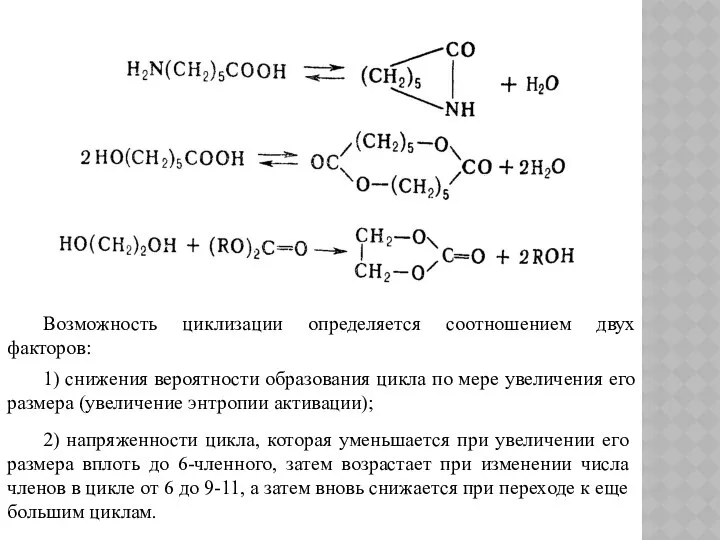
- 156. Возможность циклизации определяется соотношением двух факторов: 1) снижения вероятности образования цикла по мере увеличения его размера
- 157. В результате совместного действия обоих этих факторов при получении методом поликонденсации различных полимеров возможно образование больших
- 158. В ряде случаев обменные реакции положены в основу получения поликонденсационных гомо- и сополимеров, например, синтез полиэтилентерефталата
- 159. КИНЕТИКА, КАТАЛИЗ, МОЛЕКУЛЯРНО-МАССОВОЕ РАСПРЕДЕЛЕНИЕ Своеобразие поликонденсации, существенно отличающее ее от полимеризации, заключается в следующем: исчезновение мономеров
- 160. Поэтому особенно важно изучение кинетики поликонденсации при протекании в гомо- или гетерогенных условиях. Кинетика поликонденсации, включающей
- 161. Во многих случаях указанные допущения перестают быть справедливыми: имеются бифункциональные мономеры, у которых однотипные функциональные группы
- 162. Кинетическая и другие характеристики равновесной и неравновесной поликонденсации сильно различаются. Равновесная поликонденсация характеризуется малыми скоростями [константа
- 163. Из этого соотношения следует, что для получения высокомолекулярных полимеров поликонденсацию следует проводить в условиях, максимально благоприятствующих
- 164. Процессы поликонденсации можно проводить как в одну, так и в несколько стадий, каждая из которых может
- 165. - введение активирующих агентов (например, пиридина и трифенилфосфита при поликонденсации дикарбоновых кислот и диаминов); - катализ.
- 166. Катализаторы применяют как в истинно каталитических количествах (молярные проценты), так и в значительно больших (например, в
- 167. В этом случае справедливо уравнение Карозерса: Например, при поликонденсации глицерина и фталевой кислоты (или фталевого ангидрида):
- 168. Таким образом Если , а х=1, тогда , т.е. полимер не образуется, а только димер. При
- 169. При х = 1 указанное уравнение принимает вид: Поликонденсация при заданном избытке одного из мономеров -
- 177. Скачать презентацию






























![3. Выход из клетки: - за счет диффузии [RO∙…O∙R] RO∙ +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394193/slide-46.jpg)












![1/Pn 1/Pо [S]/[M] tgϕ = ks ks оценивают для полимеров, полученных](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394193/slide-61.jpg)










![Например, отношение определяющее скорость полимеризации различных мономеров при [M]=const, [I]=const при](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394193/slide-78.jpg)

![Влияние инициатора С увеличением концентрации инициатора [I] увеличивается число свободных радикалов](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394193/slide-81.jpg)















































































 Окисно-відновні реакції та їхнє значення
Окисно-відновні реакції та їхнє значення Квантовая механика – теоретическая основа современной химии
Квантовая механика – теоретическая основа современной химии Типы ингибирования и их характерные черты
Типы ингибирования и их характерные черты Иерархия классов методов моделирования. Атомистические и микроскопические методы
Иерархия классов методов моделирования. Атомистические и микроскопические методы Строение молекул некоторых широко распространенных гербицидов
Строение молекул некоторых широко распространенных гербицидов Голубое золото
Голубое золото Кремний. Основа неживой природы
Кремний. Основа неживой природы Химия в нашей жизни
Химия в нашей жизни Клетка элементарная единица живого
Клетка элементарная единица живого Ферменты в пищевой промышленности
Ферменты в пищевой промышленности Фосфор
Фосфор Кислоты и основания
Кислоты и основания Природні джерела органічних речовин Підготувала Учениця 11-Б класу Білик Вікторія
Природні джерела органічних речовин Підготувала Учениця 11-Б класу Білик Вікторія  Классификация химических элементтов
Классификация химических элементтов Геохимия. Геохимическая система элементов
Геохимия. Геохимическая система элементов Классификация аминокислот в зависимости от природы радикалов. (Лекция 3)
Классификация аминокислот в зависимости от природы радикалов. (Лекция 3) Исследовательская работа по теме: « Волшебные жидкости – вещества определители или как определить вкус веществ не пробуя их»
Исследовательская работа по теме: « Волшебные жидкости – вещества определители или как определить вкус веществ не пробуя их»  Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Качественные реакции на функциональные группы
Качественные реакции на функциональные группы Жири. Склад жирів, їх утворення. Жири у природі. Біологічна роль жирів.
Жири. Склад жирів, їх утворення. Жири у природі. Біологічна роль жирів.  Операции термической обработки
Операции термической обработки Состав и основные свойства янтаря и древесных смол
Состав и основные свойства янтаря и древесных смол Горные породы и минералы. Камни-самоцветы
Горные породы и минералы. Камни-самоцветы Презентация по химии Карбоновые кислоты и их производные
Презентация по химии Карбоновые кислоты и их производные  Пигменті в реставрации декоративно-прикладного искусства
Пигменті в реставрации декоративно-прикладного искусства Презентация по Химии "Волшебный сад" - скачать смотреть
Презентация по Химии "Волшебный сад" - скачать смотреть  Система инактивации лекарственных средств в организме человека
Система инактивации лекарственных средств в организме человека Згубний вплив спиртів на організм людини Підготувала Гуцал Наталія 9-Б клас
Згубний вплив спиртів на організм людини Підготувала Гуцал Наталія 9-Б клас