ТИПЫ ХИМИЧЕСКОЙ СВЯЗИ Цели: Дать понятия ионной, ковалентной, металлической, водородной хим.связям; Научить определять и запис
Содержание
- 2. АТОМЫ Na0 - 1s22s22p63s1 Mg0 - 1s22s22p63s2 F0 - 1s22s22p5 Cl0 - 1s22s22p63s23p5 число протонов и
- 3. ИОНЫ Na1+ - 1s22s22p63s0 Mg2+ - 1s22s22p63s0 F1- - 1s22s22p6 Cl1- - 1s22s22p63s23p6 Число протонов и
- 4. ИОНЫ – заряженные частицы, которые образуются в результате присоединения или отдачи электронов. Если е - отдаются
- 5. ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ ЭО атома, условная величина, характеризующая способность атома в молекуле притягивать электроны. ЭО в периоде увеличивается
- 6. Ионная связь образовавшаяся электронная пара полностью принадлежит более электроотрицательному атому. ИОННАЯ СВЯЗЬ, образуемая в результате электростатического
- 7. Физические свойства веществ с ионным типом связи: твердые, тугоплавкие, не имеющие запаха, часто хорошо растворимые в
- 8. Металлическая связь возникает в результате движения свободных электронов, которые достаточно свободно движутся в решетке металлов, электростатически
- 9. Физические свойства. Валентные электроны принадлежат одновременно всем атомам металла, свободно перемещаясь по всему кристаллу. Образуя единое
- 10. Ковалентная связь наиболее общий вид химической связи, возникающий за счет образования общей электронной пары обменный механизм
- 11. ВИДЫ КОВАЛЕНТНОЙ СВЯЗИ ПОЛЯРНАЯ НЕПОЛЯРНАЯ HCl, H2O H2, Cl2, N2.
- 12. Образование полярной и неполярной связи.
- 13. Ковалентная полярная связь образуется между атомами различных неметаллов. Схема образования ковалентной полярной связи: •• •• H*
- 14. ВЕЩЕСТВА С АТОМНОЙ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКОЙ АЛМАЗ(С), КРЕМНИЙ (Si), КВАРЦ (SiO2). Они состоят из атомов, связанных друг
- 15. ВЕЩЕСТВА С МОЛЕКУЛЯРНОЙ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКОЙ В УЗЛАХ – НАХОДЯТСЯ МОЛЕКУЛЫ. УДЕРЖИВАЮТСЯ СЛАБЫМИ МЕЖМОЛЕКУЛЯРНЫМИ СИЛАМИ. ВЕЩЕСТВА ЛЕГКОПЛАВКИ,
- 16. ВОДОРОДНАЯ СВЯЗЬ вид химической связи типа А — Н...А — Н ,образуется в результате взаимодействия атома
- 17. Образование межмолекулярной водородной связи.
- 18. Образование внутримолекулярной водородной связи.
- 20. Скачать презентацию
















 Графическое представление газовых процессов. (10 класс)
Графическое представление газовых процессов. (10 класс) Тканые армирующие материалы
Тканые армирующие материалы Химические опасные аварии с выбросом хлора и аммиака
Химические опасные аварии с выбросом хлора и аммиака Алюминий, его физические и химические свойства
Алюминий, его физические и химические свойства Новые стеклообразные материалы и методы их синтеза. Аморфные и стеклообразные материалы
Новые стеклообразные материалы и методы их синтеза. Аморфные и стеклообразные материалы Материаловедение. Теория сплавов
Материаловедение. Теория сплавов Дисперсные
Дисперсные  Минеральные удобрения
Минеральные удобрения Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Введение в токсикологическую химию. Объекты химико-токсикологического исследования
Введение в токсикологическую химию. Объекты химико-токсикологического исследования Строение атома
Строение атома NaCl – хлорид натрия
NaCl – хлорид натрия Физическая технология топлива. Направления переработки нефти. Классификация нефтепродуктов
Физическая технология топлива. Направления переработки нефти. Классификация нефтепродуктов Клеящие материалы. Классификация и ассортимент клея
Клеящие материалы. Классификация и ассортимент клея Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4)
Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4) Растворы Электролитическая диссоциация
Растворы Электролитическая диссоциация Основные понятия органической химии
Основные понятия органической химии Газообразное состояние вещества
Газообразное состояние вещества Периодическая таблица Д.И. Менделеева. Своя игра
Периодическая таблица Д.И. Менделеева. Своя игра Химические элементы 5-й группы
Химические элементы 5-й группы Сплавы, растворы, смеси
Сплавы, растворы, смеси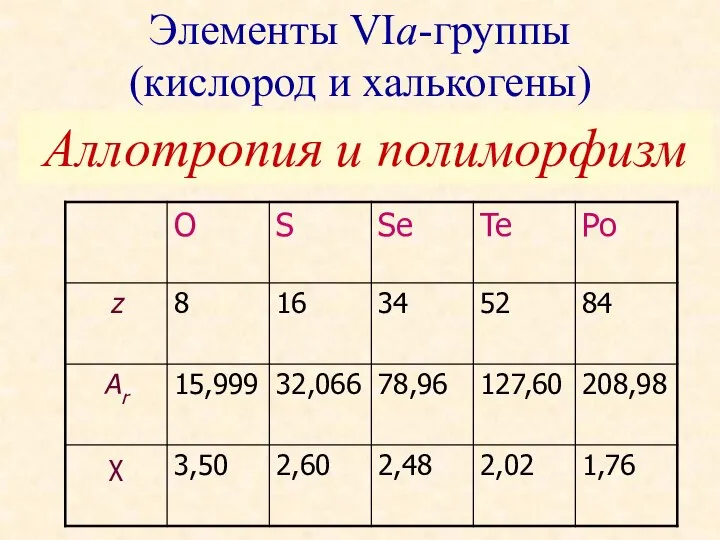 Элементы VIа-группы (кислород и халькогены). Аллотропия и полиморфизм
Элементы VIа-группы (кислород и халькогены). Аллотропия и полиморфизм КИСЛОРОД
КИСЛОРОД  Кислородсодержащие органические соединения. Спирты
Кислородсодержащие органические соединения. Спирты Свойства растворов ВМС
Свойства растворов ВМС Производные фурана, пиррола, тиофена
Производные фурана, пиррола, тиофена Композиционные материалы
Композиционные материалы Самородные элементы
Самородные элементы