Содержание
- 2. Атомные характеристики тяжелых р – элементов s2[__] p2[__]__]__] s2[__] p3[__]__]__] s2[__] p4[__]__]__] IV V VI 937
- 3. Прогнозирование свойств тяжелых р - элементов
- 4. Проявление свойств «металличности» и «неметалличности» у атомов элементов и их соединений. Физические свойства.
- 6. Химические свойства.
- 7. Вывод: Тяжелые р – элементы, называемые полуметаллами, будут сочетать в себе свойства «металличности» и «неметалличности». В
- 8. Литературные данные 1). Общая химия в формулах, определениях, схемах. Под редакцией В.Ф. Тикавого. Минск. Издательство Университетское,
- 9. Для элементов IVA подгруппы ПСЭ
- 10. Для элементов VА подгруппы ПСЭ
- 11. Для элементов VIA подгруппы ПСЭ
- 14. Экспериментальная часть
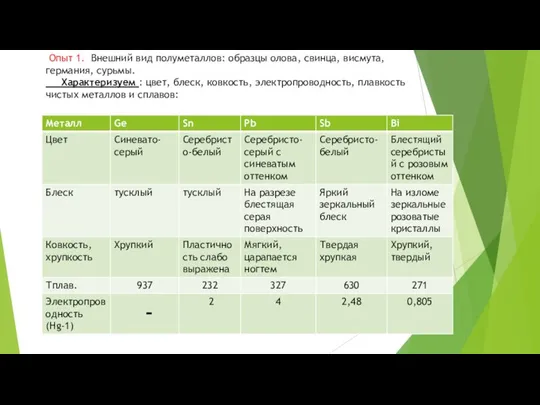
- 15. Опыт 1. Внешний вид полуметаллов: образцы олова, свинца, висмута, германия, сурьмы. Характеризуем : цвет, блеск, ковкость,
- 16. Германий
- 17. Свинец
- 18. Олово
- 19. Сурьма
- 20. Висмут
- 21. Опыт 2. Взаимодействие полуметаллов с простыми веществами. Образование прочных оксидных плёнок на металлах при взаимодействии с
- 22. Опыт 3. Отношение свинца к разбавленным HCl, H2SO4, H3PO4, CH3COOH конц. кислотам. Выполнение опыта: зачистим наждачной
- 24. Отметим наблюдения в таблице. Растворимость свинца в кислотах, окисляющих ионом Н+
- 25. Вывод Свинец нерастворим в соляной, серной и фосфорной кислотах вследствие образования на его поверхности малорастворимых пленок
- 26. Опыт 4. Отношение полуметаллов к кислотам, окисляющим анионом кислоты (HNO3 конц, H2CrO4, H2SO4 конц). Исследуемые полуметаллы
- 28. Опыт 4.1 Sn + 2H2SO4 = SnSO4 + SO2 + 2H2O Sn - 2e = Sn+2
- 29. Опыт 4.2 8Pb + 19 H2SO4 = 8Pb (HSO4)2 + SO2 + 10H2O + S +
- 30. Опыт 4.3 21H2SO4
- 31. Опыт 4.4
- 32. Опыт 4.5
- 33. Опыт 4.6
- 34. Опыт 4.7
- 35. Опыт 4.8
- 36. Опыт 4.9
- 37. Опыт 4.10
- 38. Опыт 4.11
- 39. Опыт 4.12 Sn + H2CrO4 = … Продолжение напишите сами
- 40. Опыт 4.13 Pb + H2CrO4 = … Предлагаем дописать уравнения самостоятельно
- 41. Опыт 5. Склонность солей полуметаллов к гидролизу. Соли: Bi(NO3)3, SnCl2, SbCl3, Pb(NO3)2; лакмус и УИБ. 5а)Выполнение
- 42. Перемешали стеклянным микрошпателем и измерили рН полученных растворов универсальной индикаторной бумажкой
- 44. Уравнения реакций гидролиза катионов полуметаллов.
- 45. Опыт 5.2
- 46. Перемешали стеклянным микрошпателем и измерили рН полученных растворов универсальной индикаторной бумажкой (отметили растворение солей в ацетоне)
- 47. Bi(NO3) PH=1 В ацетоне гидролиз уменьшается, величины pH увеличиваются
- 48. Опыт 6. Исследование окислительно -восстановительных свойств полуметаллов и их соединений. Выполнение опыта: В пробирку поместили 1-2
- 49. Опыт 6.2 Выполнение опыта: В пробирку поместить 1-2 см³ водного раствора CuSO₄ и опустить туда зачищенную
- 50. Опыт 6.3 Выполнение опыта: Получили в пробирке раствор станнита натрия Na₂SnO₂, для чего в пробирку поместили
- 51. Восстановление висмута станнитом натрия в щелочной среде:
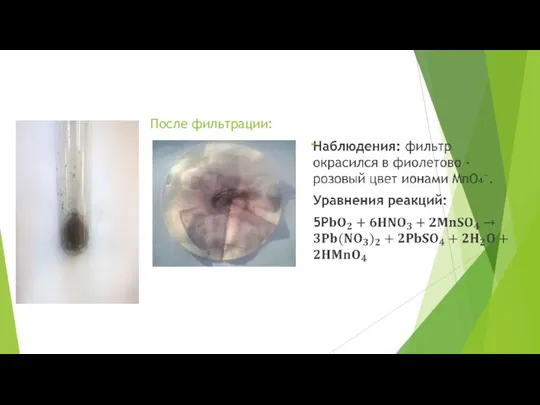
- 52. Опыт 6.4 Выполнение опыта: Поместим в пробирку немного PbO₂ (0,5 микрошпателя), прибавляем 1 см³ концентрированной HNO₃.
- 53. После фильтрации:
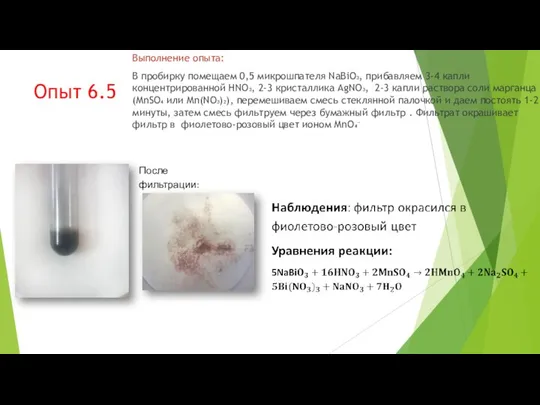
- 54. Опыт 6.5 Выполнение опыта: В пробирку помещаем 0,5 микрошпателя NaBiO₃, прибавляем 3-4 капли концентрированной HNO₃, 2-3
- 55. Опыт 6.6 Выполнение опыта: В пробирку помещаем 2-3 стружки магния, прибавляем 2-3 капли раствора соли сурьмы
- 56. Опыт 7.1 Процессы комплексообразования полуметаллов. Образование комплексной соли висмута.
- 57. Выполнение опыта. В пробирку поместим 2-3 капли соли висмута и 1 каплю разб. KJ, появится черный
- 58. Опыт 7.2 Образование комплекса свинца (II). Выполнение опыта. В пробирку с раствором Pb(NO3)2 вносим 1-2 капли
- 60. Опыт 7.3) Выполнение опыта . Обазование оксалатного комплекса олова (II) В пробирку поместили 2-3 капли ацетонового
- 61. Опыт 7.4 Na2S2O3 осаждает белый осадок из растворов солей свинца ( II ) PbS2O3 , растворимый
- 63. Качественные реакции для распознавания катионов полуметаллов. Sb3+. Выполнение опыта. К 2-3 каплям раствора SbCl3 прибавляем 2-3
- 64. Pb2+. Выполнение опыта. На предметное стекло наносим 1 каплю раствора соли Pb2+ , прибавляем 1 каплю
- 65. Sn2+ и Bi3+ Соль висмута в щелочном растворе восстанавливается станнитом натрия до металлического висмута, который выделяется
- 66. Выполнение опыта. К 3-5 каплям раствора соли олова ( II ) в фарфоровой чашке приливаем около
- 67. Исследование реакций осаждения солей полуметаллов . Опыт 8.1: Образование сульфидов. Выполнение: На полоске фильтровальной бумаги 4
- 68. Когда соли впитаются в бумагу, сверху нанести по 1 капли раствора Na2S.
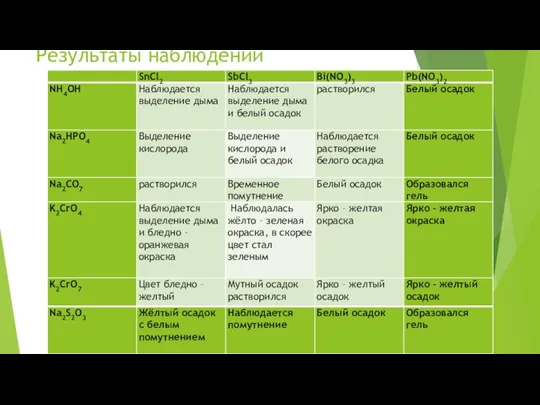
- 74. Результаты наблюдений
- 75. Склонность полуметаллов к полимеризации
- 83. Скачать презентацию
![Атомные характеристики тяжелых р – элементов s2[__] p2[__]__]__] s2[__] p3[__]__]__] s2[__]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/728328/slide-1.jpg)







































































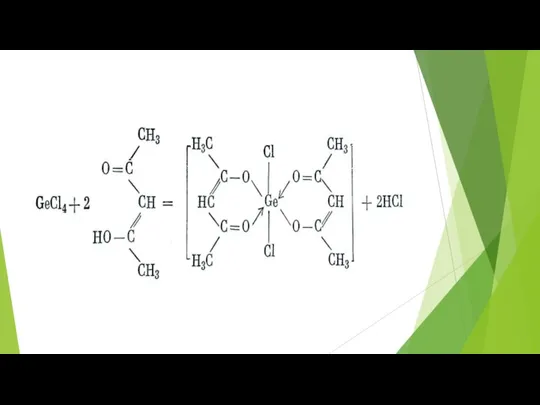
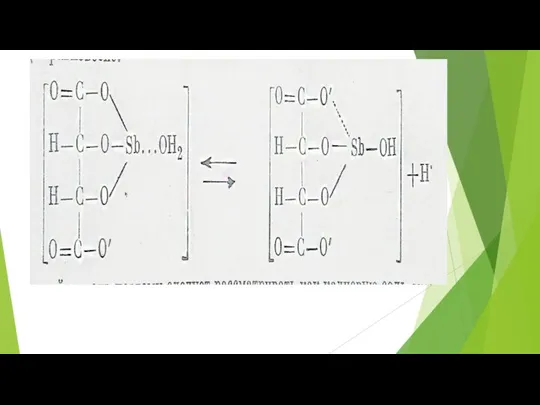


 Миметик глицина на основе производного Гераниола
Миметик глицина на основе производного Гераниола Цеолиты. Свойства и область применения
Цеолиты. Свойства и область применения Химические процессы
Химические процессы Бор (Borum)
Бор (Borum) Химия и стирка
Химия и стирка  Презентация по Химии "Электролиз расплавов и растворов" - скачать смотреть
Презентация по Химии "Электролиз расплавов и растворов" - скачать смотреть  Аттестационная работа. Использование цифровой лаборатории Архимед во внеурочной деятельности по химии
Аттестационная работа. Использование цифровой лаборатории Архимед во внеурочной деятельности по химии д.з.051
д.з.051 Химические и физико-химические методы стандартизации и контроля качества лекарственных. (Лекция 3)
Химические и физико-химические методы стандартизации и контроля качества лекарственных. (Лекция 3) Азотная кислота
Азотная кислота Окислительно-восстановительные реакции. (Лекция 18)
Окислительно-восстановительные реакции. (Лекция 18) Переваривание углеводов в пищеварительном тракте. Гликолиз. Окислительное декарбоксилирование пирувата. (Тема 6)
Переваривание углеводов в пищеварительном тракте. Гликолиз. Окислительное декарбоксилирование пирувата. (Тема 6) Майда еритін витаминдер. А,D,E,K витаминдері
Майда еритін витаминдер. А,D,E,K витаминдері Использование уксусной кислоты в жизни
Использование уксусной кислоты в жизни Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық
Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық Презентация Соли
Презентация Соли Lekcii_ - 2017-lech_ped 11
Lekcii_ - 2017-lech_ped 11 V група періодичної системи Менделєєва
V група періодичної системи Менделєєва Химико-технологические процессы современных производств
Химико-технологические процессы современных производств Органическая химия. Химические свойства и типы реакций. (9 класс)
Органическая химия. Химические свойства и типы реакций. (9 класс) Химия. Вопросы. Практическая работа
Химия. Вопросы. Практическая работа Химическая идентификация
Химическая идентификация Почему протекают химические реакции
Почему протекают химические реакции Презентация по Химии "Солі в природі" - скачать смотреть бесплатно
Презентация по Химии "Солі в природі" - скачать смотреть бесплатно Пегматитовые месторождения
Пегматитовые месторождения Ароматичні вуглеводні Арени Підготував Учень 11-А класу Пазуханич Руслан
Ароматичні вуглеводні Арени Підготував Учень 11-А класу Пазуханич Руслан 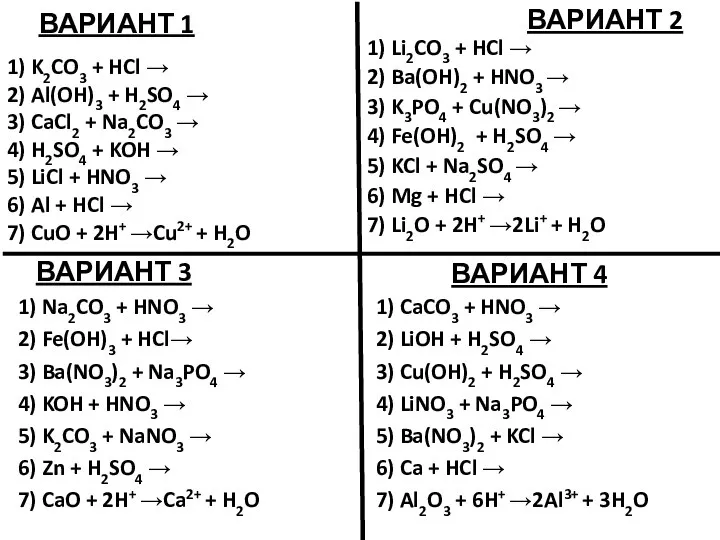 Уравнения возможных реакций. Задание
Уравнения возможных реакций. Задание Методы измерения и приборное обеспечение радиационно-экологического мониторинга. (Лекция 6)
Методы измерения и приборное обеспечение радиационно-экологического мониторинга. (Лекция 6)