Углерод Составил: учитель химии МОУ «Средняя общеобразовательная школа №92 с углубленным изучением отдельных предметов»
- Главная
- Химия
-
Углерод Составил: учитель химии МОУ «Средняя общеобразовательная школа №92 с углубленным изучением отдельных предметов»

Содержание
- 2. Строение атома В периодической таблице химических элементов углерод (С) расположен во втором периоде, в IV группе
- 3. Нахождение в природе Содержание углерода в земной коре 0,1 % по массе. Свободный углерод находится в
- 4. КРУГОВОРОТ УГЛЕРОДА
- 5. Основные и хорошо изученные аллотропные модификации углерода — алмаз и графит. Графит (от др.-греч. γράφω —
- 6. Аллотропия углерода Алма́з (от араб. ألماس, ’almās, тур. elmas, которое идёт через арабск. из др.-греч. ἀδάμας
- 7. Химические свойства Продукты горения углерода в кислороде являются CO и CO2 (монооксид углерода и диоксид углерода
- 8. Применение Графит используется в карандашной промышленности. Также его используют в качестве смазки при особо высоких или
- 9. Углерод играет огромную роль в жизни человека. Его применения столь же разнообразны, как сам этот многоликий
- 11. Скачать презентацию
Строение атома
В периодической таблице химических элементов углерод (С) расположен во втором
Строение атома
В периодической таблице химических элементов углерод (С) расположен во втором
Углерод (С) — неметалл. Возможные степени окисления: -4; 0; +2; +4. Формулы высшего оксида и гидроксида: СО2 и Н2СО3. Оба соединения проявляют кислотные свойства.
Нахождение в природе
Содержание углерода в земной коре 0,1 % по массе. Свободный
Нахождение в природе
Содержание углерода в земной коре 0,1 % по массе. Свободный
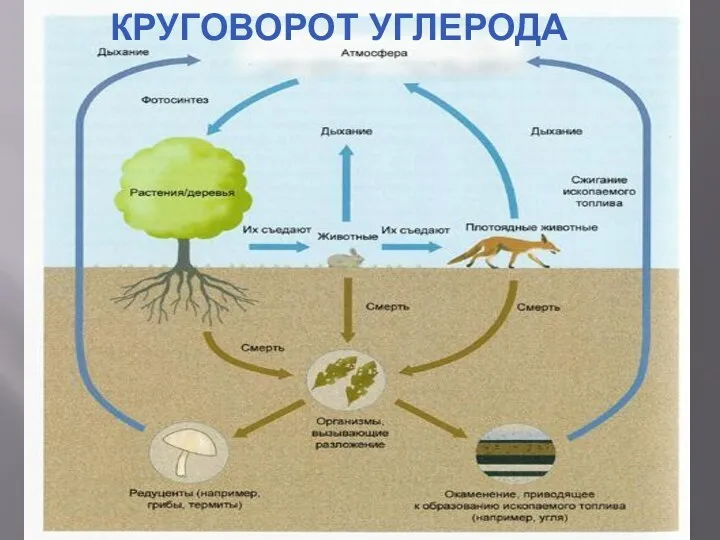
КРУГОВОРОТ УГЛЕРОДА
КРУГОВОРОТ УГЛЕРОДА
Основные и хорошо изученные аллотропные модификации углерода — алмаз и графит.
Графит (от др.-греч. γράφω — пишу) — минерал из класса самородных
Основные и хорошо изученные аллотропные модификации углерода — алмаз и графит.
Графит (от др.-греч. γράφω — пишу) — минерал из класса самородных
Аллотропия углерода
Аллотропия углерода
Алма́з (от араб. ألماس, ’almās, тур. elmas, которое идёт через арабск. из др.-греч. ἀδάμας — «несокрушимый») —минерал, кубическая аллотропная форма
Аллотропия углерода
Алма́з (от араб. ألماس, ’almās, тур. elmas, которое идёт через арабск. из др.-греч. ἀδάμας — «несокрушимый») —минерал, кубическая аллотропная форма
Химические свойства
Продукты горения углерода в кислороде являются CO и CO2 (монооксид углерода и диоксид
Химические свойства
Продукты горения углерода в кислороде являются CO и CO2 (монооксид углерода и диоксид
С + О2=СО2
При реакции углерода с серой получается сероуглерод CS2
С большинством металлов, бором и кремнием углерод образует карбиды, например:
4Al + 3C = Al4C3(карбид алюминия);
Ca + 2C = CaC2(карбид кальция).
Важна в промышленности реакция углерода с водяным паром:
C + H2O = CO + H2
Применение
Графит используется в карандашной промышленности. Также его используют в качестве смазки при
Применение
Графит используется в карандашной промышленности. Также его используют в качестве смазки при
Алмаз, благодаря исключительной твёрдости, незаменимый абразивный материал. Алмазным напылением обладают шлифовальные насадки бормашин. Кроме этого, ограненные алмазы — бриллианты используются в качестве драгоценных камней в ювелирных украшениях. Благодаря редкости, высоким декоративным качествам и стечению исторических обстоятельств, бриллиант неизменно является самым дорогим драгоценным камнем. Исключительно высокая теплопроводность алмаза (до 2000 Вт/м·К) делает его перспективным материалом для полупроводниковой техники в качестве подложек для процессоров. Но относительно высокая цена (около 50 долларов/грамм) и сложность обработки алмаза ограничивают его применение в этой области.
Углерод играет огромную роль в жизни человека. Его применения столь же
Углерод играет огромную роль в жизни человека. Его применения столь же
Углерод является основой всех органических веществ. Любой живой организм состоит в значительной степени из углерода. Углерод — основа жизни. Источником углерода для живых организмов обычно является СО2 из атмосферы или воды. В результате фотосинтеза он попадает в биологические пищевые цепи, в которых живые существа поедают друг друга или останки друг друга и тем самым добывают углерод для строительства собственного тела. Биологический цикл углерода заканчивается либо окислением и возвращением в атмосферу, либо захоронением в виде угля или нефти.
Углерод в виде ископаемого топлива: угля и углеводородов (нефть, природный газ) — один из важнейших источников энергии для человесества.







 Карбоновые кислоты.
Карбоновые кислоты. Степень окисления
Степень окисления Радиохимия. Альфа-бета, және гамма-сәулеленудің табиғаты және қасиеті
Радиохимия. Альфа-бета, және гамма-сәулеленудің табиғаты және қасиеті Лекция 6. Химическая кинетика
Лекция 6. Химическая кинетика Металлы. Общая характеристика
Металлы. Общая характеристика Химический комплекс
Химический комплекс Коллигативные свойства растворов
Коллигативные свойства растворов Полимеры: польза или вред? Выполнила: Ученица 10 «А» класса Архипова Аятэ
Полимеры: польза или вред? Выполнила: Ученица 10 «А» класса Архипова Аятэ № 14.
№ 14.  Производство чугуна. (9 и 11 класс)
Производство чугуна. (9 и 11 класс) Кислородные соединения азота Азотная кислота МБОУ СОШ №30 г.Ростов-на-Дону
Кислородные соединения азота Азотная кислота МБОУ СОШ №30 г.Ростов-на-Дону Невидиме чорнило
Невидиме чорнило Топливо и его химические реакции при сгорании
Топливо и его химические реакции при сгорании Кристаллография. Точечные группы симметрии, принцип их вывода с помощью понятия о группах. Формы кристаллов низшей категории
Кристаллография. Точечные группы симметрии, принцип их вывода с помощью понятия о группах. Формы кристаллов низшей категории Нафта. Класифікація нафти
Нафта. Класифікація нафти Функциональные свойства и анализ каротиноидов в пищевых продуктах
Функциональные свойства и анализ каротиноидов в пищевых продуктах Получение металлов
Получение металлов  Лекарственные формы для глаз в условиях аптечного производства
Лекарственные формы для глаз в условиях аптечного производства Структурная механика композитов. Слоистый композит
Структурная механика композитов. Слоистый композит Основы теории и понятия высокоэффективной жидкостной хроматографии (ВЭЖХ)
Основы теории и понятия высокоэффективной жидкостной хроматографии (ВЭЖХ) Аттестационная работа. Методическая разработка по выполнению исследовательской работы Тайны поваренной соли
Аттестационная работа. Методическая разработка по выполнению исследовательской работы Тайны поваренной соли Конструкционные функциональные волокнистые композиты
Конструкционные функциональные волокнистые композиты Точечные дефекты в кристаллах
Точечные дефекты в кристаллах Свойства химических элементов I и II А подгрупп периодической системы Д.И. Менделеева
Свойства химических элементов I и II А подгрупп периодической системы Д.И. Менделеева Алканы. Циклоалканы
Алканы. Циклоалканы Студенттің өзіндік жұмысы
Студенттің өзіндік жұмысы Алкалоидтар. Алкалоидтар негіздік қасиет
Алкалоидтар. Алкалоидтар негіздік қасиет Основы химической коррозии
Основы химической коррозии