Содержание
- 2. Сульфиды Э = As, Sb, Bi 2ЭCl3 + 3H2S = Э2S3↓ + 6HCl (в р-ре HCl)
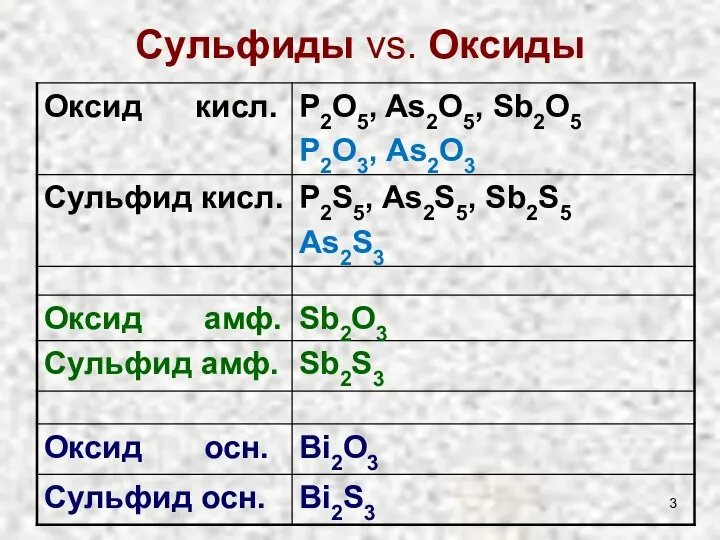
- 3. Сульфиды vs. Оксиды
- 4. Тиосоли Взаимодействие кислых оксидов (сульфидов) As и Sb с основаниями: As2O3 тв. + Na2O тв. =
- 5. Э3+ (Э = P, As, Sb): NaЭS2 и Na3ЭS3 мета- орто- Э5+ (Э = P, As,
- 6. Получение в растворе (Э = As, Sb): Э2S3↓+ Na2S = 2NaЭS2 Э2S5↓+ Na2S = 2NaЭS3 Э2S3↓+
- 7. Побочная подгруппа V группы периодической системы
- 8. Содержание в земной коре и минералы V – 22 место, рассеян, VS2.V2S5 (патронит) Добывают из железных
- 9. Открытие элементов V – 1801г. мексиканец Дель Рио, затем в 1830 Н. Сефстрёмом - «Ванадис» -
- 10. Простые вещества Получение сложное, проблема разделения Nb и Ta M2O5 + 5Ca = 5CaO + 2M
- 11. Известный "автомобильный король" Генри Форд сказал: "Если бы не было ванадия" - не было бы автомобиля".
- 12. Простые вещества Химически инертные 2V + 12HF = 2H[VF6] + 5H2 V + 6HNO3 = [VO2]NO3
- 13. ВАНАДИЙ 2+ VO основные VSO4 3+ V2O3 свойства V2(SO4)3 [VO]SO4 сульфат ванадила 4+ VO2 K4V4O9 ванадит
- 14. Кислородные соединения V5+ V2O5 + H2O = 2HVO3 (V2O5*xH2O↓) (равновесие влево) V2O5 + 2NaOH = 2NaVO3
- 15. IV группа периодической системы
- 16. C, Si, Ge, Sn, Pb
- 17. Распространенность и минералы C – 11 место, CO2, CaCO3 (известняк, кальцит, мрамор), уголь, нефть, прир. газ
- 18. Открытие элементов C –известен с древнейших времен; лат. «карбон» - уголь Si – 1883 г., швед
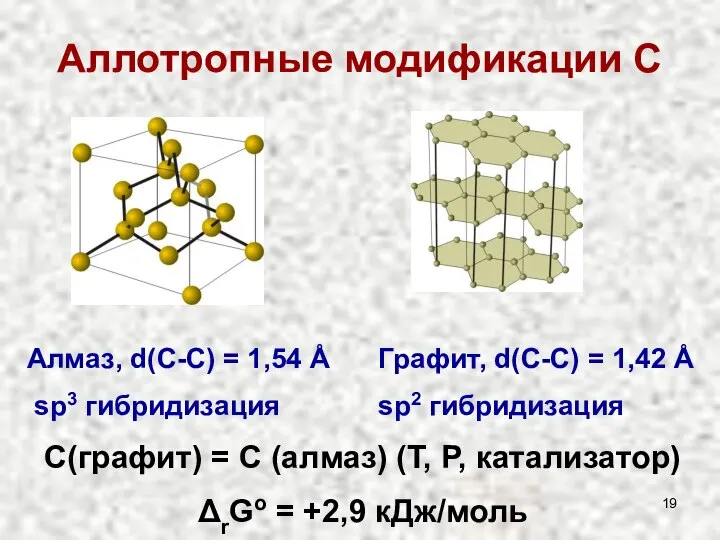
- 19. Аллотропные модификации С Алмаз, d(С-С) = 1,54 Å sp3 гибридизация Графит, d(С-С) = 1,42 Å sp2
- 20. Фуллерены Открыты в 1980 г., Нобелевская премия по химии ПОЛУЧЕНИЕ: Электрическая дуга между угольными электродами, далее
- 21. Фуллерены K3C60 – сверхпроводник при Tc = 18K Gd@C60
- 22. Углеродные нанотрубки и луковицы Углеродные нанотрубки – однослойные и многослойные; открытые и закрытые; модификация поверхности и
- 23. Карбиды Ионные – щелочные и щелочноземельные металлы и Al. Металлоподобные – d и f металлы, металлический
- 24. Карбиды Ионные карбиды – метаниды (Be2C, Al4C3), ацетилениды (MIIC2, MI2C2) 2Al2O3 + 9C = Al4C3 +
- 25. СО (угарный газ) Получение в промышленности CO2 + C кокс = 2CO (при Т) С +
- 26. Cвойства СО Солеобразующий оксид: CO+NaOHр-р= HCOONa (120oC, 5 атм.) Восстановительные свойства: 2CO + O2 = 2CO2
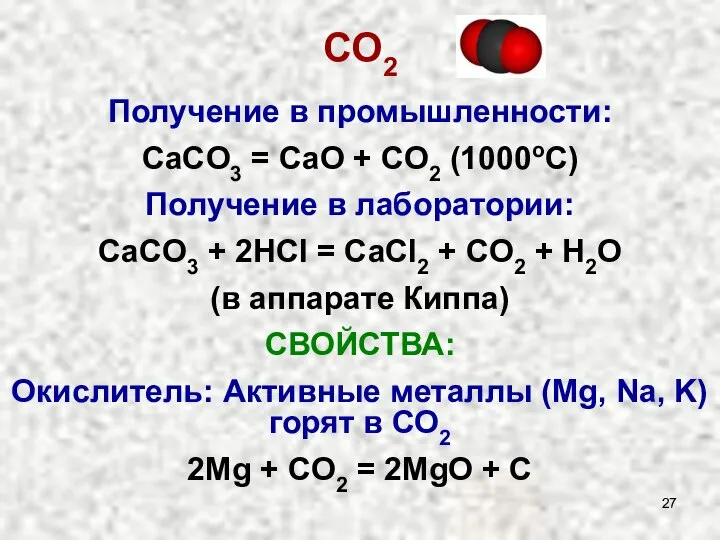
- 27. СO2 Получение в промышленности: СaCO3 = CaO + CO2 (1000oC) Получение в лаборатории: CaCO3 + 2HCl
- 28. Карбонаты и гидрокарбонаты Растворимость в воде: 1V CO2 в 0,9V H2O Кислотные св-ва: СO2 + H2O
- 30. Скачать презентацию









![Простые вещества Химически инертные 2V + 12HF = 2H[VF6] + 5H2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1407083/slide-11.jpg)
![ВАНАДИЙ 2+ VO основные VSO4 3+ V2O3 свойства V2(SO4)3 [VO]SO4 сульфат](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1407083/slide-12.jpg)













 Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Химия в сельском хозяйстве.
Химия в сельском хозяйстве.  Аминспирттер және олардың биологиялық ролі.Элементорганикалық қосылыстар және олардың қасиеті
Аминспирттер және олардың биологиялық ролі.Элементорганикалық қосылыстар және олардың қасиеті Полимеризация бутилена и пропилена
Полимеризация бутилена и пропилена Чистые вещества и смеси (продолжение)
Чистые вещества и смеси (продолжение) Методы анализа вещества
Методы анализа вещества Типы химических реакций в неорганической и органической химии
Типы химических реакций в неорганической и органической химии Синтез и структура медьсодержащих и серебросодержащих соединений пектина и хитозана
Синтез и структура медьсодержащих и серебросодержащих соединений пектина и хитозана Проект – дослідження мило Dove Роботу виконала учениця 11 класу Бабенко Аліна Віталіївна
Проект – дослідження мило Dove Роботу виконала учениця 11 класу Бабенко Аліна Віталіївна  Пена и пенообразователи. Назначение, виды, состав и свойства
Пена и пенообразователи. Назначение, виды, состав и свойства Многоликая уксусная кислота
Многоликая уксусная кислота Распознавание химических соединений
Распознавание химических соединений Формирование ответственного отношения школьников к окружающей среде родного края на уроках химии и во внеурочное время.
Формирование ответственного отношения школьников к окружающей среде родного края на уроках химии и во внеурочное время.  Бионеорганическая химия. Комплексообразование в организме. (Лекция 3)
Бионеорганическая химия. Комплексообразование в организме. (Лекция 3) Глюкоза, ее строение и свойства
Глюкоза, ее строение и свойства Спирты: классификация, изомерия, номенклатура Подготовила учитель химии Несмеянова М.В. МОУ «Сытьковская СОШ»Рузский район М
Спирты: классификация, изомерия, номенклатура Подготовила учитель химии Несмеянова М.В. МОУ «Сытьковская СОШ»Рузский район М Лаки. Эмали. Красочные составы
Лаки. Эмали. Красочные составы Презентация по Химии "ЛИПИДНЫЙ ОБМЕН" - скачать смотреть бесплатно
Презентация по Химии "ЛИПИДНЫЙ ОБМЕН" - скачать смотреть бесплатно Строение атома
Строение атома Коррозия железа
Коррозия железа Презентація на тему: “Нітратна кислота” Підготував: Учень 10-А класу Луцької ЗОШ № 25 Матвійчук Роман
Презентація на тему: “Нітратна кислота” Підготував: Учень 10-А класу Луцької ЗОШ № 25 Матвійчук Роман  Искусственные или технические битумы
Искусственные или технические битумы Роль минеральных веществ в организме человека
Роль минеральных веществ в организме человека Оксид фосфора P2O5
Оксид фосфора P2O5 Методы выращивания кристаллов
Методы выращивания кристаллов Оборудование для дистилляции мисцеллы
Оборудование для дистилляции мисцеллы Химические свойства алкадиенов и алкинов
Химические свойства алкадиенов и алкинов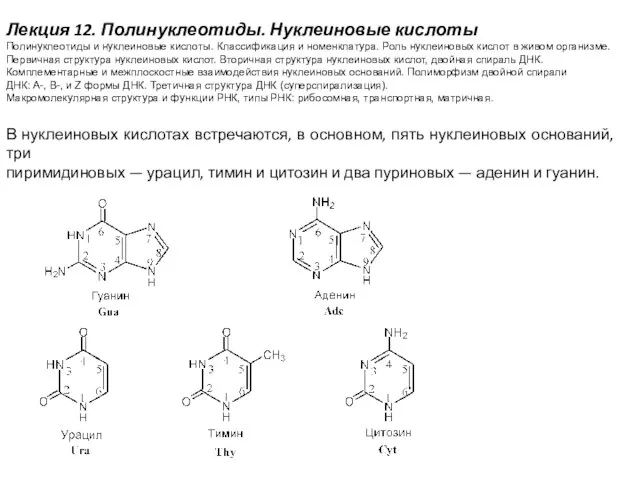 Полинуклеотиды. Нуклеиновые кислоты
Полинуклеотиды. Нуклеиновые кислоты