Содержание
- 2. Общая характеристика элементов
- 3. Общая характеристика элементов F Cl Br I (At) Электронная конфигурация атома: 1s2…ns2np5 1. Окислительные свойства уменьшаются
- 4. Нахождение в природе CaF2 – флюорит (плавиковый шпат) NaCl – каменная соль, галит KCl – сильвин
- 5. Простые вещества F2 Cl2 Br2 I2
- 6. Физические свойства
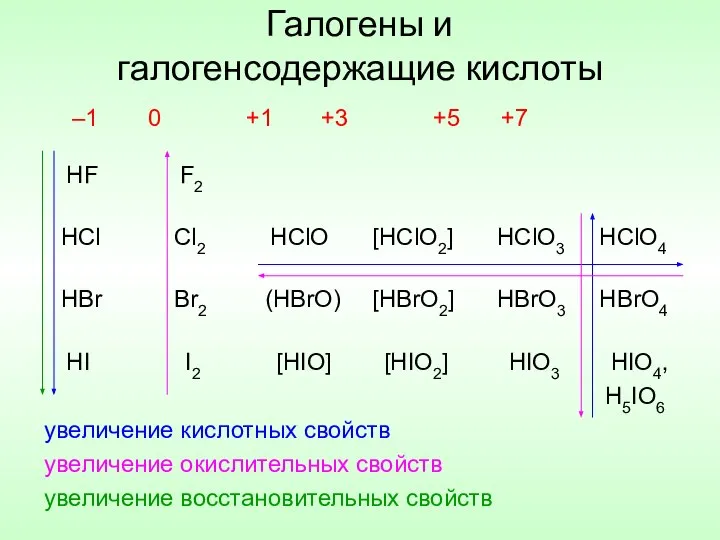
- 7. Галогены и галогенсодержащие кислоты –1 0 +1 +3 +5 +7 HF HCl HI HBr F2 Cl2
- 8. Химические свойства 1. Взаимодействие галогенов с простыми веществами. с неметаллами: H2 + Hal2 = HHal, где
- 9. Химические свойства 2. Взаимодействие галогенов со сложными веществами. с водой: F2 + H2O = HF +
- 10. Химические свойства 3. Гидролиз галогенидов неметаллов. 4. Сопропорционирование. NaCl + NaClO + H2SO4 = Cl2 +
- 11. Химические свойства 5. Взаимодействие галогенидов металлов с H2SO4(конц.). NaF + H2SO4(конц.) = NaCl + H2SO4(конц.) =
- 12. Способы получения галогенов Промышленные. электролиз CaF2 = Ca + F2 NaCl + H2O = NaOH +
- 13. Качественные реакции Ag+ + Cl– = AgCl↓ Ag+ + Br– = AgBr↓ Ag+ + I– =
- 14. Применение F: - производство алюминия и тефлона (авиационная и космическая техника) Br: - лекарственные препараты -
- 16. Скачать презентацию












 Сложные эфиры
Сложные эфиры Фазовое равновесие в насыщенном растворе малорастворимого электролита. (Глава 4. Задача 10)
Фазовое равновесие в насыщенном растворе малорастворимого электролита. (Глава 4. Задача 10) фізичні властивості полімеру спиртів та карбонових кислот
фізичні властивості полімеру спиртів та карбонових кислот  Химические индикаторы
Химические индикаторы Обмен липидов
Обмен липидов Технология производства простых полиэфиров
Технология производства простых полиэфиров Презентация по Химии "Форфор" - скачать смотреть
Презентация по Химии "Форфор" - скачать смотреть  Вода ценный дар природы. Биологическая роль воды
Вода ценный дар природы. Биологическая роль воды Геохимия урана и тория в карбонатитовом процессе
Геохимия урана и тория в карбонатитовом процессе Физическая и коллоидная химия
Физическая и коллоидная химия Физические явления в химии (8 класс)
Физические явления в химии (8 класс) Қабаттағы мұнай
Қабаттағы мұнай Як прості речовини
Як прості речовини  Цинк. Знаходження в періодичній системі і основні характеристики
Цинк. Знаходження в періодичній системі і основні характеристики Адам мен жануар организміне бордың әсері
Адам мен жануар организміне бордың әсері Высокомолекулярные вещества полимеры
Высокомолекулярные вещества полимеры Окислительно-восстановительные процессы. Лекция 8
Окислительно-восстановительные процессы. Лекция 8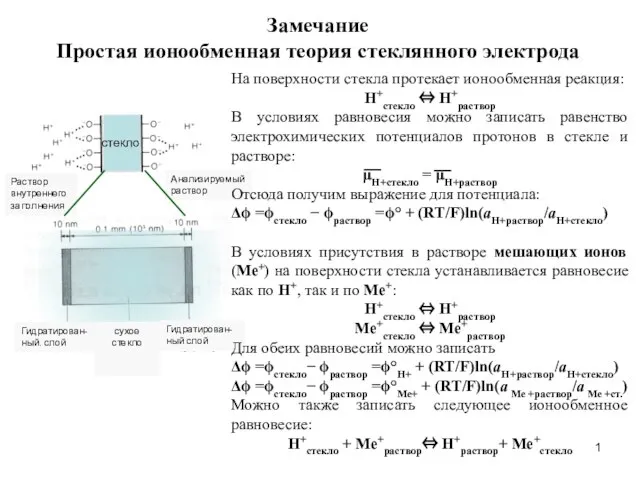 Простая ионообменная теория стеклянного электрода
Простая ионообменная теория стеклянного электрода Биологический метод исследования. Определение патогенности и вирулентности микроорганизмов
Биологический метод исследования. Определение патогенности и вирулентности микроорганизмов Работа выполнена обучающейся 9 «А» класса МОУ «СОШ №2» Мусафировой Анастасией
Работа выполнена обучающейся 9 «А» класса МОУ «СОШ №2» Мусафировой Анастасией Химия, 8. Урок 1
Химия, 8. Урок 1 Биопластики: область применения
Биопластики: область применения Производные карбоновых кислот. Ненасыщенные карбоновые кислоты
Производные карбоновых кислот. Ненасыщенные карбоновые кислоты Caustic Soda
Caustic Soda Презентация по Химии "Неметаллы" - скачать смотреть
Презентация по Химии "Неметаллы" - скачать смотреть  Презентация по Химии "Биополимеры" - скачать смотреть
Презентация по Химии "Биополимеры" - скачать смотреть  Химия в пищевой промышленности
Химия в пищевой промышленности Интересные факты о нефти
Интересные факты о нефти