Содержание
- 2. План лекции
- 3. Предельный случай полярной ковалентной связи. анион А-, катион К+ Ионная связь не обладает: насыщаемостью направленностью повышенной
- 4. Каждый ион окружен сферическим электрическим полем, действующим на любой другой ион. Сила взаимодействия ионов определяются величиной
- 5. Структурный тип NaCl (KBr, AgCl, MgO, TiO, UC) ГЦК упаковка анионов, катионы – в октаэдрических пустотах.
- 6. Структурный тип CsCl (CaS, CsCN, CuZn, NH4Cl) Координация (8,8)
- 7. Структурный тип ZnS (цинковая обманка или сфалерит) CuCl, HgS, GaP ГЦК упаковка анионов, катионы – в
- 8. Структурный тип CaF2 (флюорит) UO2, BaCl2, PbO2 ГЦК упаковка катионов, анионы – в тетраэдрических пустотах. Координация
- 9. Ионные кристаллы − гигантские полимерные молекулы. Формулы (NаСl, СаF2, Аl2(SО4)3 ) − отражают лишь состав. Ионные
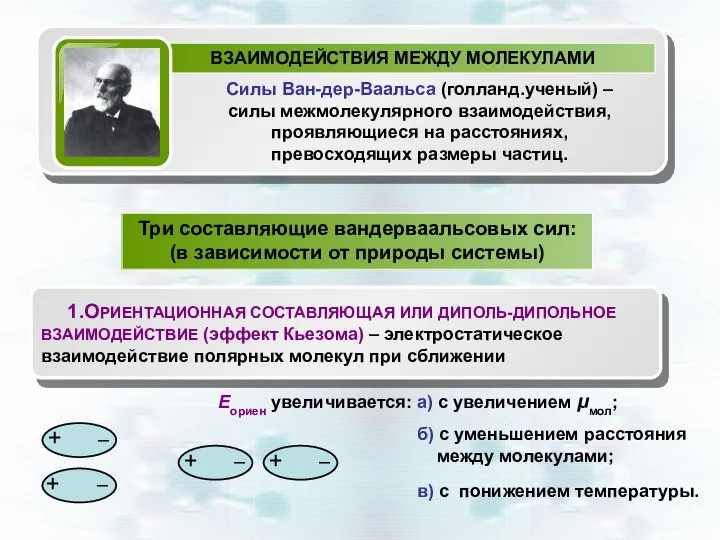
- 10. Три составляющие вандерваальсовых сил: (в зависимости от природы системы) 1.ОРИЕНТАЦИОННАЯ СОСТАВЛЯЮЩАЯ ИЛИ ДИПОЛЬ-ДИПОЛЬНОЕ ВЗАИМОДЕЙСТВИЕ (эффект Кьезома)
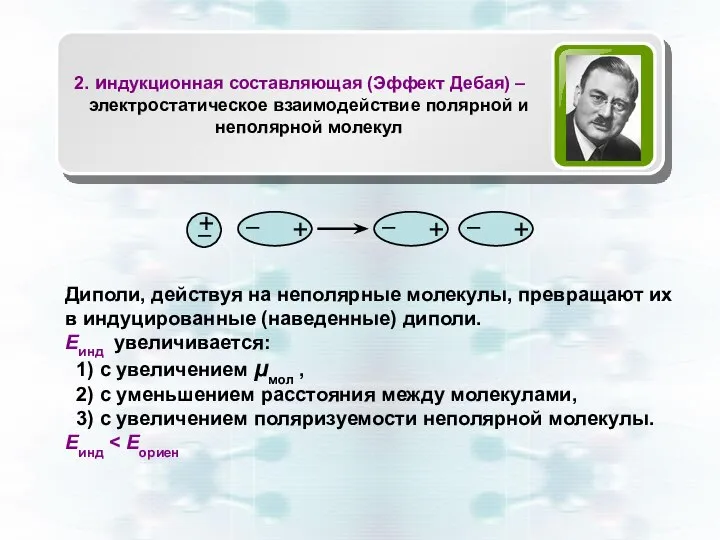
- 11. Диполи, действуя на неполярные молекулы, превращают их в индуцированные (наведенные) диполи. Еинд увеличивается: 1) с увеличением
- 12. В результате взаимодействия мгновенных диполей энергия системы понижается. Едисп увеличивается: с увеличением поляризуемости молекул с уменьшением
- 13. Минимальная энергия системы обеспечивается при расстояниях между центрами молекул 0,4 – 0,5 нм, т. е. существенно
- 14. А – Н + В – R → А – Н⋅⋅⋅В – R водород способен глубоко
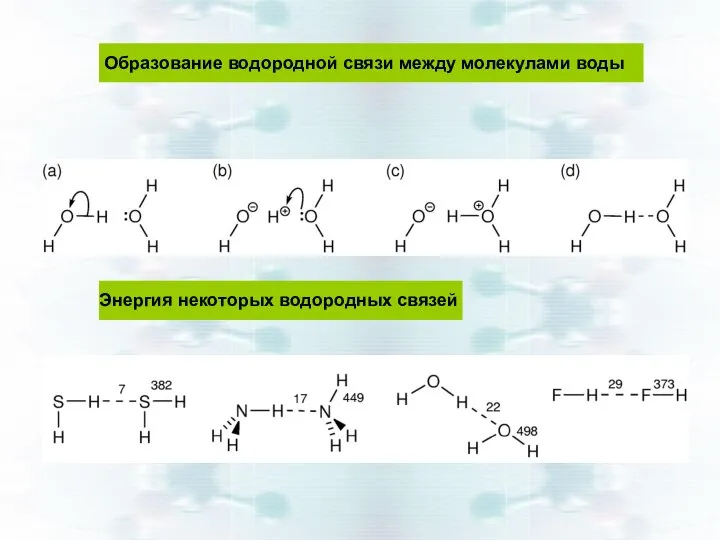
- 15. Образование водородной связи между молекулами воды Энергия некоторых водородных связей
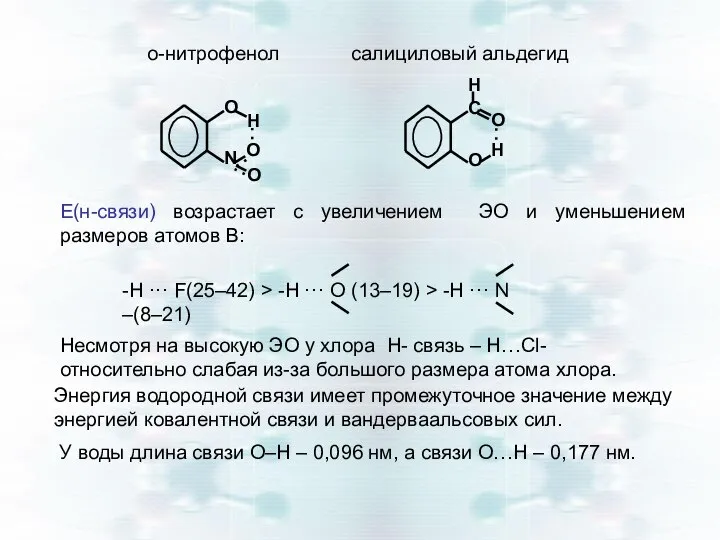
- 16. o-нитрофенол салициловый альдегид O O O N H Е(н-связи) возрастает с увеличением ЭО и уменьшением размеров
- 17. Внутримолекулярная водородная связь - салициловая кислота
- 18. Возникновение водородных связей приводит к образованию димеров, тримеров и других полимерных структур, например, зигзагообразных структур (НF)n,
- 19. Межмолекулярные Н-связи изменяют свойства веществ: повышают вязкость, диэлектрическую постоянную, температуру кипения и плавления, теплоту плавления и
- 20. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ Вещества, в которых элементы проявляют «дополнительные» валентности рассматриваются как соединения высшего порядка и называются
- 21. Структура комплексных соединений внутренняя (координационна ) сфера внешняя сфера [ Аg(NH3) 2 ] Cl Na3 [
- 22. Координационное число: количество лигандов, располагающихся вокруг комплексообразователя [Аg(NH3)2]+ [Al(OH)6]3– Аg+, Аl3+ – комплексообразователи; NН3, ОН– –
- 23. [Zn(CN)4]? Z = Z Zn+2 + 4ZCN– = 2+4(-1) = -2 ⇒ [ Zn(CN)4]2– Химическая связь
- 24. Для комплексов, у которых комплексообразователь s-, p- или d10 – элементы. Теория валентных связей (ВС). Между
- 25. Комплекс [AlBr4]– Атом Аl …3s23р1 комплексообразователь Al3+: неподеленная пара электронов лигандов sp3-гибридизация АО Строение комплексного иона
- 26. Комплекс Fe(CN)6]3- Комплексообразователь Fe3+: 3d54s0. Лиганды CN– – лиганды сильного поля, :CN–:CN–:CN–:CN–:CN–:CN– Fe+3 3d 4s 4p
- 27. Лиганды располагаются вокруг комплексообразователя так, чтобы силы притяжения были максимальны, а силы отталкивания минимальны. Теория кристаллического
- 28. В отсутствии внешнего электростатического поля все d-орбитали – вырожденные (одинаковая энергия). Под воздействием кристаллического поля лигандов
- 29. плоский квадрат Если Еспаривания лиганды сильного поля ⇒ низкоспиновые комплексы. В противном случае – высокоспиновые комплексы.
- 30. Сильное поле лиганда – электроны на d-подуровне комплексообразователя максимально спариваются Для 3d-элементов – спектрохимический ряд лигандов
- 31. Координационное число 6 октаэдрическое расщепление (n-1)d- орбиталей: Δ0 Δ 0,6 Δ 0,4 4 -4 -2 2
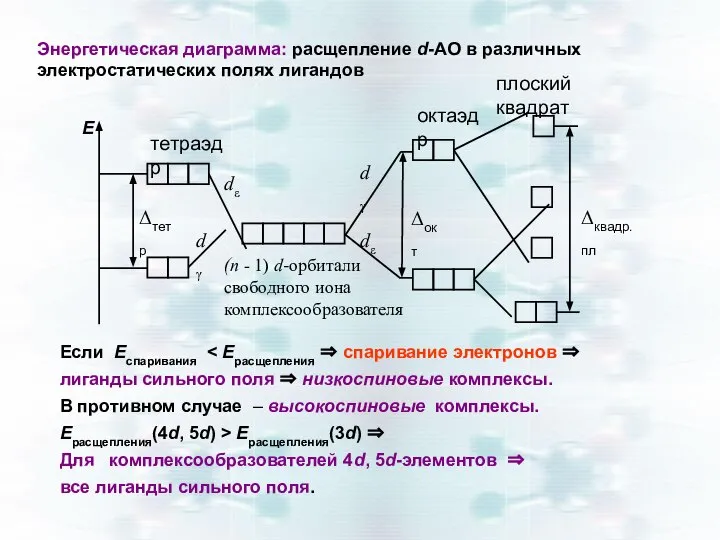
- 32. Комплекс [Co(Н2О)6]2+. Комплексообразователь Со2+: 3d74s0. К.ч. 6 ⇒ октаэдрическое расщепление. центральный атом – 3d – элемент
- 33. sp3d2-гибридизация структура комплекса [Со(Н2О)6]2+ – октаэдр Комплекс – высокоспиновый, внешнеорбитальный, т. к. взаимодействует внешний d- подуровень.
- 34. Комплекс [PtВr6]2- комплексообразователь Pt4+: 5d66s0 Комплексообразователь 5d- элемент ⇒ лиганды сильного поля К. ч. 6 ⇒
- 35. Координационное число – 4 1. Если комплексообразователь 3d – элемент ⇒ лиганды слабого поля ⇒ тетраэдрическое
- 36. Комплексообразователь Au3+: 5d86s0. координационное число – 4 комплексообразователь 5d- элемент ⇒ лиганды сильного поля ⇒ плоско-квадратное
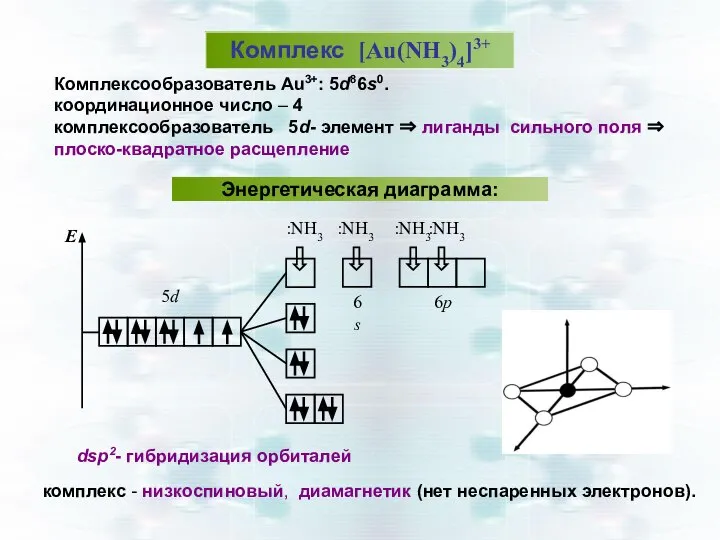
- 37. Комплекс [NiCl4]2- комплексообразователь Ni2+: 3d84s2 координационное число – 4 комплексообразователь – 3d- элемента лиганды ⇒ слабого
- 38. ОКРАСКА КОМПЛЕКСОВ. Т. к. разность энергии (Δ) между dγ- и dε- орбиталями небольшая, возможен переход электрона
- 39. Для большинства двухзарядных комплексообразователей энергия расщепления Δ отвечает ν в пределах от 8000 до 14000 см-1,
- 40. [Cu(H2O)6]2+ [Cu(NH3)4(H2O)2]2+ Окраска комплексов
- 41. РЕАКЦИОННАЯ СПОСОБНОСТЬ. [Fe(NH3)6]2+ – внешняя гибридизация (sp3d2) более реакционноспособен, чем [Fe(CN)6)]4- – «внутренняя гибридизация – d2sp3.
- 43. Скачать презентацию
















![Координационное число: количество лигандов, располагающихся вокруг комплексообразователя [Аg(NH3)2]+ [Al(OH)6]3– Аg+, Аl3+](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392933/slide-21.jpg)
![[Zn(CN)4]? Z = Z Zn+2 + 4ZCN– = 2+4(-1) = -2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392933/slide-22.jpg)

![Комплекс [AlBr4]– Атом Аl …3s23р1 комплексообразователь Al3+: неподеленная пара электронов лигандов](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392933/slide-24.jpg)
![Комплекс Fe(CN)6]3- Комплексообразователь Fe3+: 3d54s0. Лиганды CN– – лиганды сильного поля,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392933/slide-25.jpg)




![Комплекс [Co(Н2О)6]2+. Комплексообразователь Со2+: 3d74s0. К.ч. 6 ⇒ октаэдрическое расщепление. центральный](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392933/slide-31.jpg)
![sp3d2-гибридизация структура комплекса [Со(Н2О)6]2+ – октаэдр Комплекс – высокоспиновый, внешнеорбитальный, т.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392933/slide-32.jpg)
![Комплекс [PtВr6]2- комплексообразователь Pt4+: 5d66s0 Комплексообразователь 5d- элемент ⇒ лиганды сильного](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392933/slide-33.jpg)

![Комплекс [NiCl4]2- комплексообразователь Ni2+: 3d84s2 координационное число – 4 комплексообразователь –](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392933/slide-36.jpg)


![[Cu(H2O)6]2+ [Cu(NH3)4(H2O)2]2+ Окраска комплексов](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392933/slide-39.jpg)
![РЕАКЦИОННАЯ СПОСОБНОСТЬ. [Fe(NH3)6]2+ – внешняя гибридизация (sp3d2) более реакционноспособен, чем [Fe(CN)6)]4-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392933/slide-40.jpg)
 Общие электронные конфигурации элементов главных подгрупп
Общие электронные конфигурации элементов главных подгрупп Аминокислоты. Свойства
Аминокислоты. Свойства Классификация металлов в соответствии с ионным потенциалом и параметром мягкости
Классификация металлов в соответствии с ионным потенциалом и параметром мягкости Сульфаниламидные препараты. (Тема 5)
Сульфаниламидные препараты. (Тема 5) Химия. 8 класс. Подготовка к контрольной работе
Химия. 8 класс. Подготовка к контрольной работе Атомный уровень. Химия простых веществ. Молекулярный уровень. Химия соединений. Живое субклеточный уровень
Атомный уровень. Химия простых веществ. Молекулярный уровень. Химия соединений. Живое субклеточный уровень Присадки к маслам
Присадки к маслам Периодический закон и периодическая система Д.И.Менделеева. Лекция 4
Периодический закон и периодическая система Д.И.Менделеева. Лекция 4 Презентация по Химии "Фосфор" - скачать смотреть бесплатно_
Презентация по Химии "Фосфор" - скачать смотреть бесплатно_ Химия в быту
Химия в быту Химия муравьиной кислоты
Химия муравьиной кислоты Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Генетическая связь основных классов неорганических соединений
Генетическая связь основных классов неорганических соединений Подача питательной воды в парогенератор при запроектной аварии
Подача питательной воды в парогенератор при запроектной аварии Именные реакции в органической химии
Именные реакции в органической химии Презентация по Химии "Оксиды получение, свойства, применение" - скачать смотреть бесплатно
Презентация по Химии "Оксиды получение, свойства, применение" - скачать смотреть бесплатно Презентация по Химии "Металлическая связь" - скачать смотреть
Презентация по Химии "Металлическая связь" - скачать смотреть  Углеводы. Дисахариды и полисахариды
Углеводы. Дисахариды и полисахариды Окислительно-восстановительные реакции . Алканолы
Окислительно-восстановительные реакции . Алканолы Тяжёлая вода
Тяжёлая вода Нитраты и нитриты. Азотные удобрения
Нитраты и нитриты. Азотные удобрения ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»
ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»  Применение неметаллов
Применение неметаллов Бензойная кислота
Бензойная кислота Окислительно- восстановительные процессы
Окислительно- восстановительные процессы Выполнила: Смирнова Маргарита Ученица: 9-а класса
Выполнила: Смирнова Маргарита Ученица: 9-а класса Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..
Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..  Лекция 1. Топливо. Горение топлива
Лекция 1. Топливо. Горение топлива