Содержание
- 2. Термодинамика – это наука, изучающая переходы энергии из одной формы в др., от одних частей системы
- 3. Хим. в-ва, входящие в состав системы, явл-ся её составными частями или компонентами. Системы м.б. одно-, двух-
- 4. Гомогенные системы – это смеси газов, истинные растворы (жидкие или твердые) и др. Гетерогенные системы состоят
- 5. В ходе различных превращений система переходит из одного энергетического состояния в другое. То или иное состояние
- 6. Др. параметры, зависящие от основных, наз-ся ТД функциями состояния системы. В химии наиболее часто используются :
- 7. Внутренняя энергия системы (U) – это полная энергия системы, включающая кине-тическую энергию всех видов движения молекул,
- 8. Запас внутр. энергии системы зависит от параметров состояния системы, природы в-ва и прямо пропорционален массе вещества.
- 9. Изм-ние внутр. энергии системы (ΔU), как и изм-ние любой ТД функции, опр-ся разностью её величин в
- 10. При переходе неизолированной системы из одного состояния в другое изменение её внутренней энергии осуществляется путём обмена
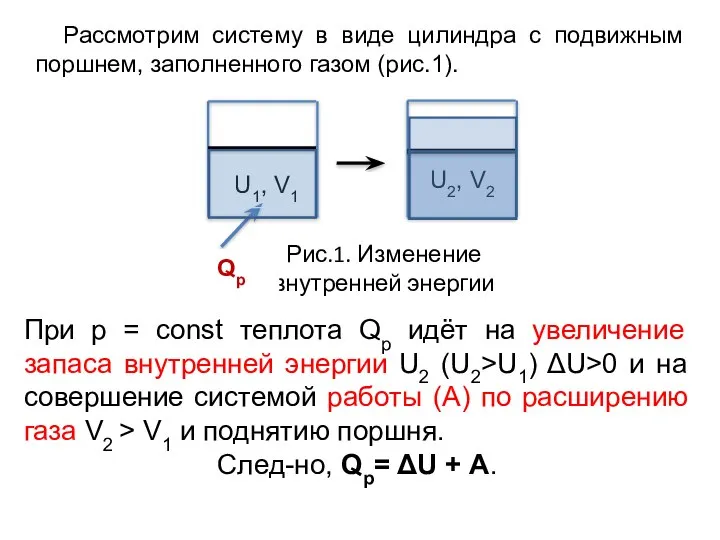
- 11. Рис.1. Изменение внутренней энергии При р = const теплота Qp идёт на увеличение запаса внутренней энергии
- 12. Ур-ние: Qр = ΔU + А выражает суть первого закона ТД: сумма изменений внутренней энергии и
- 13. Это ещё одна важная т.д. ф-ция состояния системы: энтальпия или теплосодержание. Тогда Qp = ΔU +
- 14. В изохорических условиях (V = const и ΔV = 0) вся подведённая к системе теплота (Qv)
- 15. Теплоты хим р-ций, протекающих в изохорно-изотермических и изобарно-изотермических усло-виях, называют тепловыми эффектами. (Дж/моль или кДж/моль). Тепловые
- 16. ТЕРМОХИМИЯ. ТЕРМОХИМ. УРАВНЕНИЯ. ТЕРМОХИМИЧЕСКИЕ РАСЧЁТЫ Раздел химии и хим. ТД, занятый расчётами тепловых эффектов, наз-ся термохимией.
- 17. Поскольку абсолютные значения энергии (т.д. ф-ций) измерить принципиально невозможно, то для проведения термохим. расчётов вводят специальные
- 18. При составлении термохим. ур-ний обр-ния 1 моль некоторых веществ возможно применение нецелочисленных коэффициентов. Поскольку условия получения
- 19. Стандартные условия стандартное давление – 0,1 МПа или 1 атм стандартная температура – 25°C или 298
- 20. Т.к. тепловой эффект р-ций зависит от агре-гатного состояния в-в, то в термохим. ур-ниях указывается и их
- 21. В основе термохимических расчётов реакций лежит закон Гесса (1836 – 1841): Тепловой эффект реакции (ΔНр) не
- 22. 1. Тепловой эффект реакции равен сумме теплот обр-ния продуктов р-ции (Σν2ΔН0обр.прод.) за вычетом суммы теплот обр-ния
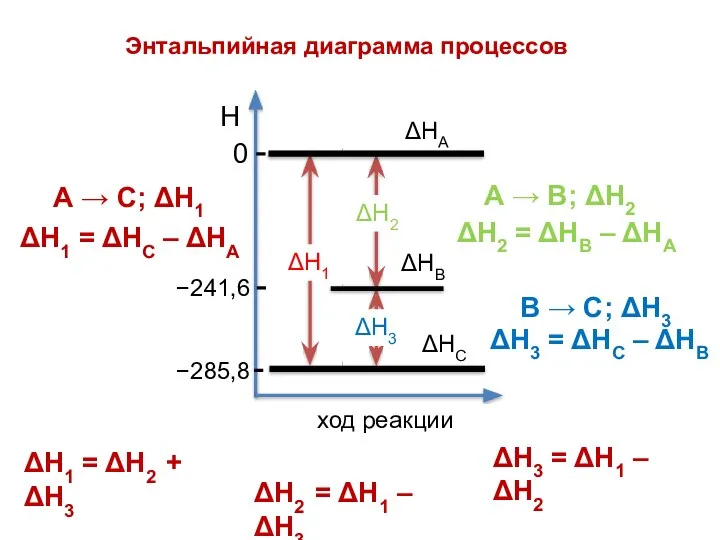
- 23. ΔН2 ΔН1 Н ΔН3 ход реакции 0 −285,8 −241,6 ΔН3 = ΔН1 – ΔН2 ΔН1 =
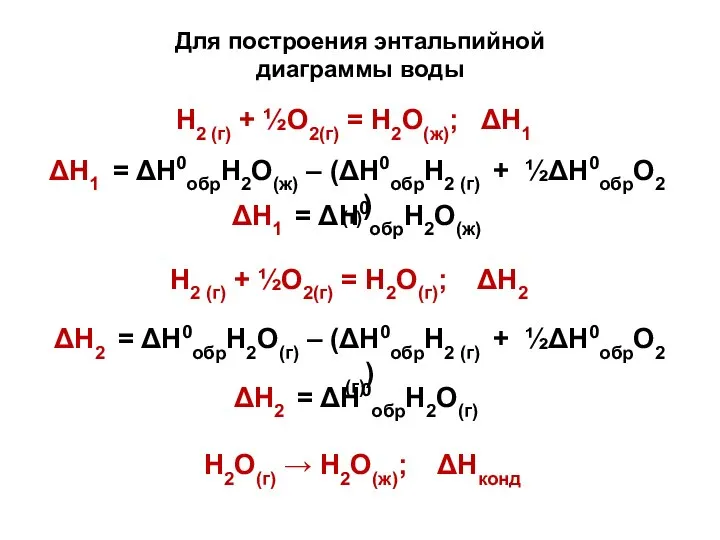
- 24. Н2 (г) + ½О2(г) = Н2О(ж); ΔН1 ΔН1 = ΔН0обрН2О(ж) – (ΔН0обрН2 (г) + ½ΔН0обрО2 (г))
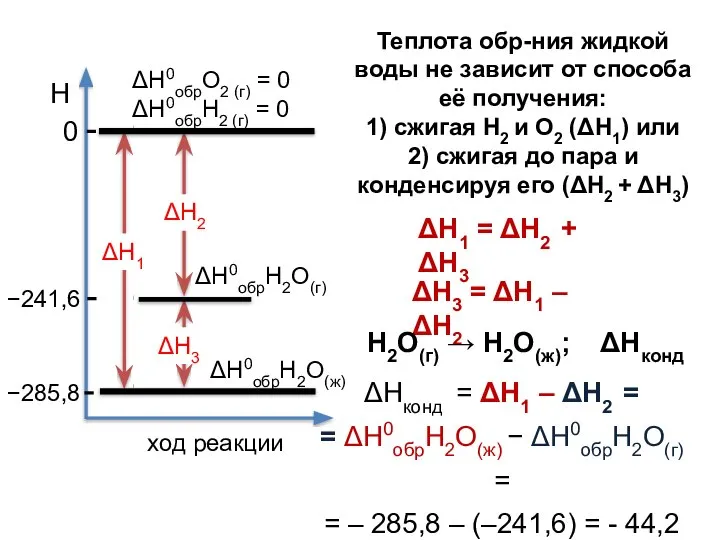
- 25. Теплота обр-ния жидкой воды не зависит от способа её получения: 1) сжигая Н2 и О2 (ΔΗ1)
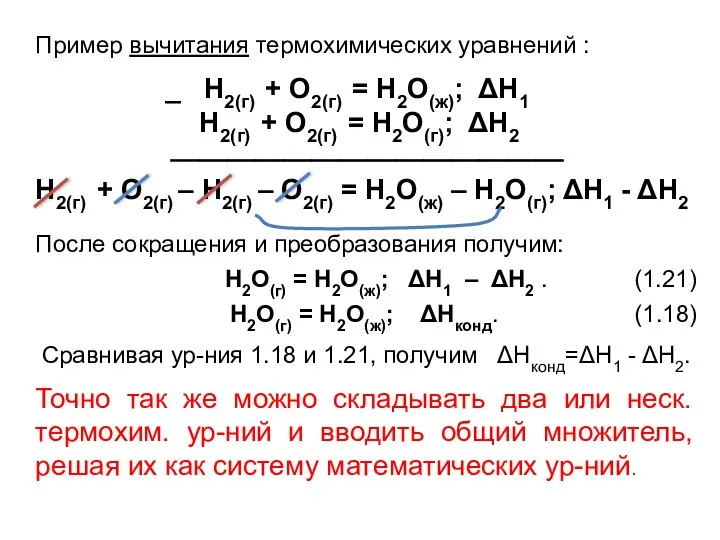
- 26. Пример вычитания термохимических уравнений : _ Н2(г) + О2(г) = Н2О(ж); ΔН1 Н2(г) + О2(г) =
- 27. ЭНТРОПИЯ По з-ну сохранения энергии система может самопроизвольно совершать работу только за счёт собственной энергии, т.е.
- 28. Имеется несколько его формулировок. 1 – Постулат Клаузиуса: теплота не переходит от холодного тела к горячему.
- 29. Из постулатов следует, что в обратимом процессе : Это эквивалентно утверждению, что dQ/T есть дифференциал нек-рой
- 30. Л.Больцман (1877): Т.д. вероятность W состояния системы – это число микросостояний, реализующих данное макросостояние: S =
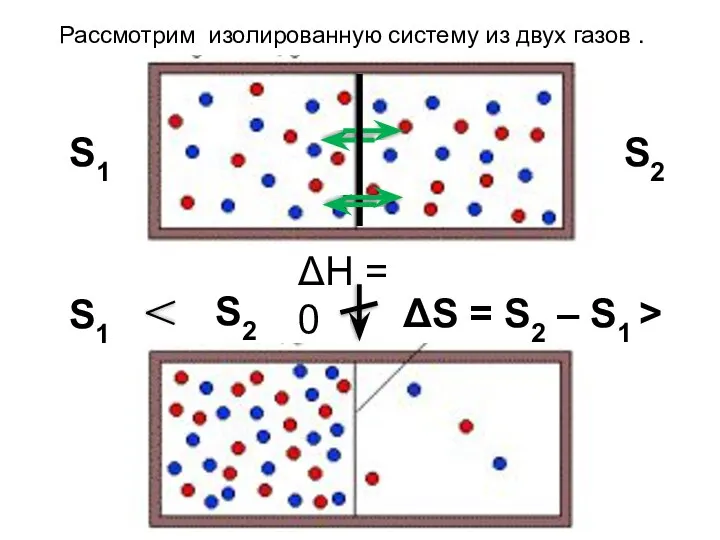
- 31. S1 S2 ΔН = 0 S1 S2 Рассмотрим изолированную систему из двух газов . ΔS =
- 32. Действующая сила процесса связана со стремлением ТД систем к самопроизвольному ув-нию степени хаотичности или ув-нию энтропии.
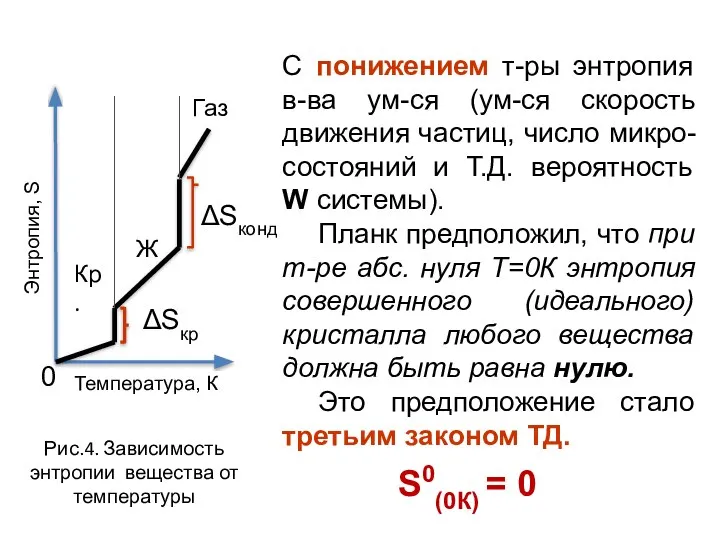
- 33. С понижением т-ры энтропия в-ва ум-ся (ум-ся скорость движения частиц, число микро-состояний и Т.Д. вероятность W
- 34. ΔS хим. реакции также не зависит от пути процесса, а определяется лишь энтропией начального и конечного
- 35. Энтропийный фактор является одной из двух движущих сил процессов и должен иметь размер энергии. Для этого
- 36. ЭНЕРГИЯ ГИББСА С учетом одновременного действия двух противоположных факторов движущей силой для р-ций, протекающих при P,T=const,
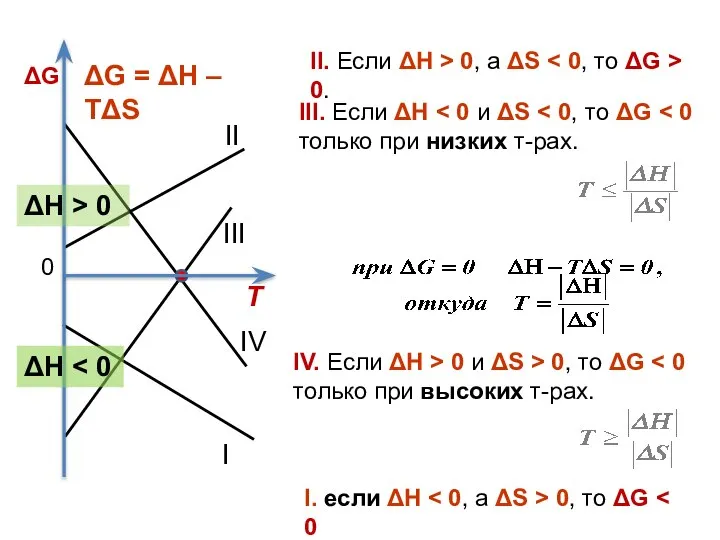
- 37. ΔG ΔG > 0 ΔG = 0 реакция термодинамически возможна При постоянной т-ре и давлении хим.
- 38. Энергия Гиббса связана с энтальпией, энтропией и температурой: G = H – Т⋅S. Её изм-ние ΔG:
- 39. Ι ΙΙΙ ΙΙ ΙV I. если ΔН 0, то ΔG II. Если ΔН > 0, а
- 40. Стандартная энергия Гиббса обр-ния в-ва (ΔG0обр. 298) – изм-ние энергии Гиббса в р-ции обр-ния 1 моль
- 42. Скачать презентацию






























 Презентація на тему: Твердість води Способи усунення твердості води
Презентація на тему: Твердість води Способи усунення твердості води  Карбонові кислоти
Карбонові кислоти Теоретические основы органической химии
Теоретические основы органической химии Алканы (структурная изомерия и систематическая номенклатура)
Алканы (структурная изомерия и систематическая номенклатура) Водородный показатель
Водородный показатель Катарометрический метод контроля
Катарометрический метод контроля Презентация по Химии "Металлическая химическая связь" - скачать смотреть
Презентация по Химии "Металлическая химическая связь" - скачать смотреть  Терпены и стероиды
Терпены и стероиды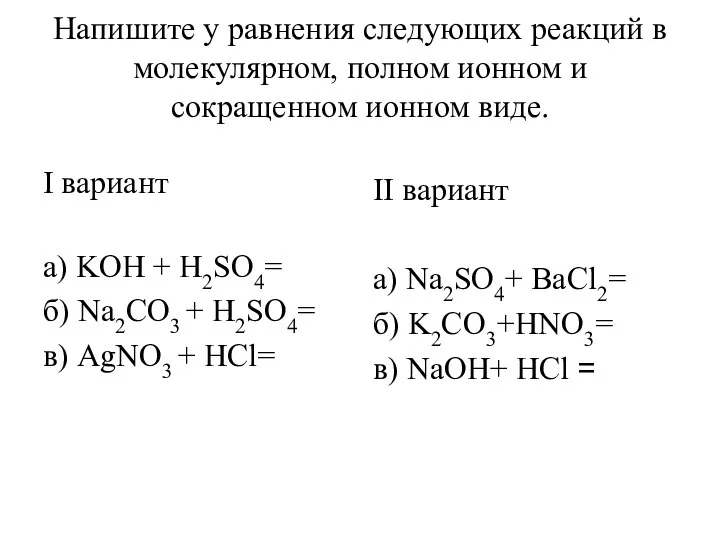 Уравнения реакций в молекулярном, полном ионном и сокращенном ионном виде
Уравнения реакций в молекулярном, полном ионном и сокращенном ионном виде Углерод. Металлы. 9 класс
Углерод. Металлы. 9 класс Азот в природе
Азот в природе Карбоновые кислоты
Карбоновые кислоты Алюміній
Алюміній  Алюминий: свойства и применение
Алюминий: свойства и применение Green chemistry application to intermolecular forces
Green chemistry application to intermolecular forces Валентность связи и локальный баланс валентности
Валентность связи и локальный баланс валентности Лужні метали Підготувала: Анна Сідорова
Лужні метали Підготувала: Анна Сідорова  Аттестационная работа. Элективный курс «Химия в доме»
Аттестационная работа. Элективный курс «Химия в доме» Строение и функция белков
Строение и функция белков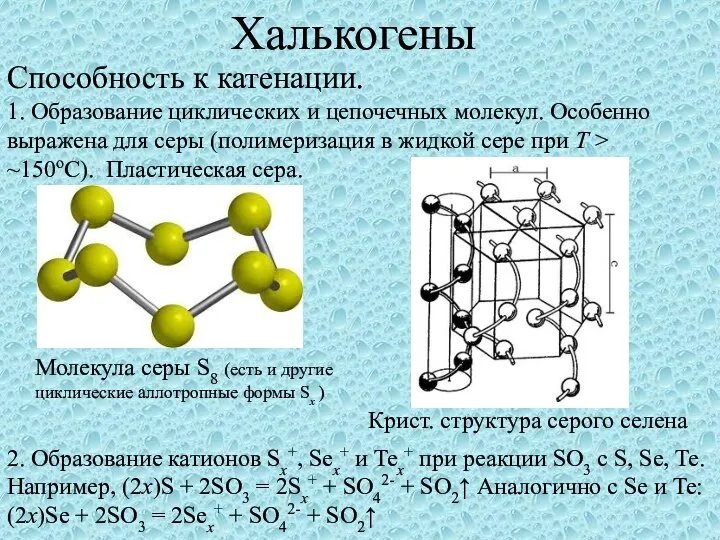 Халькогены. Способность к катенации
Халькогены. Способность к катенации Положение в ПСХЭ Д.И.Менделеева и строение атома
Положение в ПСХЭ Д.И.Менделеева и строение атома Многоликая уксусная кислота
Многоликая уксусная кислота Сверхпроводимость как явление микромира
Сверхпроводимость как явление микромира Алкины. Ацетилен
Алкины. Ацетилен Свойство металлов и сплавов
Свойство металлов и сплавов Фенол Подготовил Ежов Сергей
Фенол Подготовил Ежов Сергей Лекция 4. Методы количественного химического анализа
Лекция 4. Методы количественного химического анализа Адсорбция на твердых телах
Адсорбция на твердых телах