Содержание
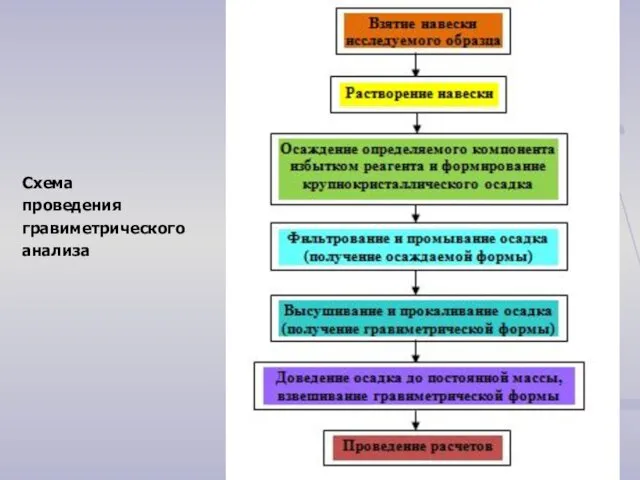
- 3. Схема проведения гравиметрического анализа
- 4. Титриметрические методы Основы титриметрических методов z1Х + z2R → z3Р Для использования в титриметрическом анализе, химические
- 6. Титриметрический метод анализа (титриметрия) основан на измерении объема титранта, пошедшего на реакцию с определяемым веществом. В
- 7. Закон эквивалентов или эквивалентных соотношений Для фиксирования ТЭ применяют индикаторы. Индикаторы – это вещества, которые резко
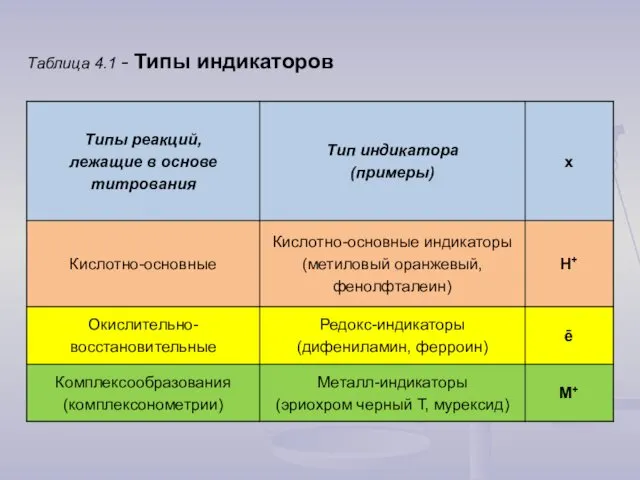
- 8. Таблица 4.1 - Типы индикаторов
- 9. Свойства индикаторов KInd Ind1 ↔ х + Ind2 окраска 1 окраска 2 прологарифмируем и заменим (–lg)
- 10. Основные расчетные формулы титриметрии Расчеты титриметрических определений основаны на использовании закона эквивалентов или эквивалентных соотношений: Данное
- 11. Закон эквивалентов можно выразить и через массу определяемого вещества: Решив последнее выражение относительно m(X), получим вторую
- 13. Метод кислотно-основного титрования Протолитические равновесия Современные представления о кислотах и основаниях: 1. Теория Аррениуса была создана
- 14. Применительно к аналитической химии удобнее всего использовать теорию Брнстеда-Лоури. Обозначим кислоту, способную отдавать протон, как НА,
- 15. Некоторые соединения могут проявлять как свойства кислот, так и свойства оснований; их называют амфипротными соединениями или
- 16. Выражение для константы равновесия автопротолиза воды или При постоянной температуре в воде , поэтому произведение тоже
- 17. Из значения KW получим, что при 25оС в водном растворе [Н+] = [ОН-]= 10-7 моль/л (среда
- 18. Кислоты (НА) и основания (ВОН) в водных растворах способны диссоциировать на ионы: НА + Н2О ↔
- 19. рKа (рKв) – показатель силы кислоты (основания): чем больше рKа (рKв), тем слабее кислота (основание). Между
- 20. Вычисление рН растворов сильных кислот и оснований В водном растворе сильной кислоты имеет место равновесие :
- 21. Вычисление рН растворов слабых кислот и оснований Пусть НА – слабая кислота, которая диссоциирует в водном
- 22. При отрицательном логарифмировании выражения получим уравнение для вычисления рН в растворах слабых кислот: , откуда Проведя
- 24. Скачать презентацию













![Из значения KW получим, что при 25оС в водном растворе [Н+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/495440/slide-16.jpg)





 Ion exchange
Ion exchange Кристалл Гришина Л.А., учитель физики МКС(К) ОУ С (К) ОШ 37 I II вида г. Новосибирск
Кристалл Гришина Л.А., учитель физики МКС(К) ОУ С (К) ОШ 37 I II вида г. Новосибирск Презентація на тему: “Поняття про полімери на прикладі поліетилену”
Презентація на тему: “Поняття про полімери на прикладі поліетилену”  Соли и классы химических веществ
Соли и классы химических веществ Определение разных форм угольной кислоты
Определение разных форм угольной кислоты Строение углеводородов
Строение углеводородов Классификация углеводов. Глюкоза
Классификация углеводов. Глюкоза Синтез новых аллильных производных семикарбазонов и тиосемикарбазонов Пиррол-2-карбальдегидов
Синтез новых аллильных производных семикарбазонов и тиосемикарбазонов Пиррол-2-карбальдегидов Водород
Водород  Валентність
Валентність  Ферроцен. Свойства, получение и применение
Ферроцен. Свойства, получение и применение Основні характеристики атомних електростанцій (АЕС) та підприємств ядерного паливного циклу
Основні характеристики атомних електростанцій (АЕС) та підприємств ядерного паливного циклу Изотермический распад переохлажденного аустенита
Изотермический распад переохлажденного аустенита Презентация по Химии "«Химические волокна»" - скачать смотреть
Презентация по Химии "«Химические волокна»" - скачать смотреть  Три кити нанохімії
Три кити нанохімії Гiдроксикислоти. Номенклатура
Гiдроксикислоти. Номенклатура Комплексные соединения
Комплексные соединения Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха
Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха Конструкция ферментатора
Конструкция ферментатора Электролитическая диссоциация. Устойчивость комплексных соединений
Электролитическая диссоциация. Устойчивость комплексных соединений Щелочные металлы
Щелочные металлы Низкомолекулярные биорегуляторы терпены
Низкомолекулярные биорегуляторы терпены Серная кислота H2SO4
Серная кислота H2SO4 Хроматографические методы анализа
Хроматографические методы анализа Металлы и сплавы, Металлы и сплавы, их свойства и применение в радиоэлектронной аппаратуре Подготовил: учащийся гр.7/8 профессия
Металлы и сплавы, Металлы и сплавы, их свойства и применение в радиоэлектронной аппаратуре Подготовил: учащийся гр.7/8 профессия Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі
Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі Диаграммы состояния двухкомпонентных систем типа твердое тело – жидкость
Диаграммы состояния двухкомпонентных систем типа твердое тело – жидкость