Содержание
- 2. План лекции. 1. Основные термодинамические характеристики. Законы термодинамики. 2. Энергия Гиббса. Критерий самопроизвольного протекания химических реакций.
- 3. Основные термодинамические характеристики Законы термодинамики. 1. Внутренняя энергия (ΔU). 2. Энтальпия (ΔH). 3. Энтропия (ΔS). 4.
- 4. Энергия Гиббса (ΔG) ΔG= ΔH - Т•ΔS ΔH - энтальпийный фактор, Т•ΔS – энтропийный фактор. Критерий
- 5. Тепловой эффект реакции. Закон Гесса. Тепловой эффект реакции- это количество теплоты, которое выделяется или поглощается в
- 6. Скорость химической реакции. Закон действия масс. Скорость химической реакции (V)- это изменение концентрации реагирующих веществ в
- 7. Закон Вант – Гоффа. Зависимость скорости реакции от температуры. Закон Вант-Гоффа: При повышении температуры на каждые
- 8. Катализаторы. Биокатализаторы. Катализаторы – это вещества, которые изменяют скорость реакции, но сами в реакции не расходуются.
- 9. Химическое равновесие с точки зрения кинетики Обратимыми называются реакции, протекающие в двух противоположных направлениях. Самым устойчивым
- 10. Химическое равновесие с точки зрения термодинамики. На протекание химической реакции влияют 2 фактора: энтальпийный (ΔH) и
- 11. Смещение химического равновесия На состояние химического равновесия влияет температура(t), давление(p) и концентрация веществ (C). Предсказать направление
- 13. Скачать презентацию










 Класи неорганічних сполук
Класи неорганічних сполук Изучение стереохимии циклических формалей глицерина методом ЯМР-спектроскопии
Изучение стереохимии циклических формалей глицерина методом ЯМР-спектроскопии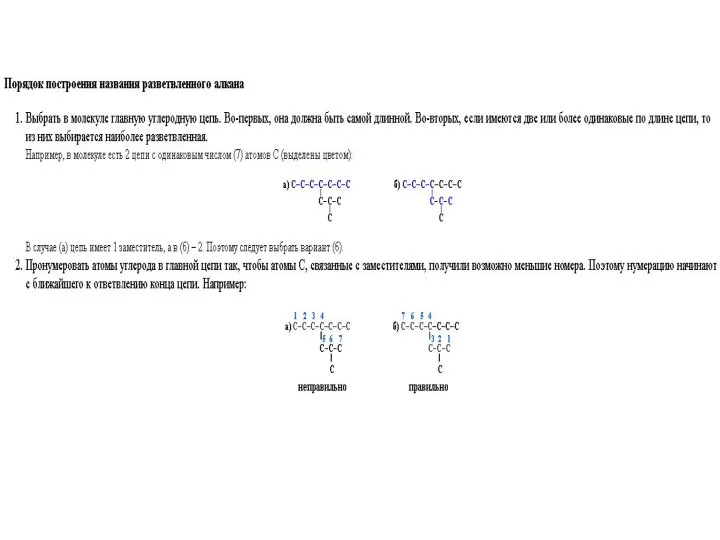 Номенклатура алканов РВЛ
Номенклатура алканов РВЛ Алкины. Гомологический ряд, получение, свойства и применение
Алкины. Гомологический ряд, получение, свойства и применение Тема: Серная кислота, строение, свойства. Выполнила: учитель химии Конохова Елена Дмитриевна
Тема: Серная кислота, строение, свойства. Выполнила: учитель химии Конохова Елена Дмитриевна  Вычисление массы растворённого вещества, содержащегося в определённой массе раствора с известной массовой долей
Вычисление массы растворённого вещества, содержащегося в определённой массе раствора с известной массовой долей Металлы. Электронная конфигурация, нахождение в природе, физические и химические свойства, применение металла
Металлы. Электронная конфигурация, нахождение в природе, физические и химические свойства, применение металла Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине
Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине Скорость химической реакции (химическая кинетика )
Скорость химической реакции (химическая кинетика ) Самостійний газовий розряд
Самостійний газовий розряд  Пищевые добавки в продуктах питания
Пищевые добавки в продуктах питания Презентация по Химии "Сложные эфиры" - скачать смотреть бесплатно
Презентация по Химии "Сложные эфиры" - скачать смотреть бесплатно МУНИЦИПАЛЬНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА №22»
МУНИЦИПАЛЬНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА №22» Электролитическая диссоциация химических элементов Урок - лекция
Электролитическая диссоциация химических элементов Урок - лекция Окислы. Лекция 14
Окислы. Лекция 14 Тема: «Йод в организме человека . Использование его в медицине» Выполнила: Роппельд В.
Тема: «Йод в организме человека . Использование его в медицине» Выполнила: Роппельд В.  Углехимическое сырьё К нему относят: торф, бурые угли, антрацит, горючие сланцы – ископаемые твердые топлива.
Углехимическое сырьё К нему относят: торф, бурые угли, антрацит, горючие сланцы – ископаемые твердые топлива.  Ахрамович Наталья Михайловна учитель химии ГБОУ СОШ № 450 Курортного района Санкт – Петербурга
Ахрамович Наталья Михайловна учитель химии ГБОУ СОШ № 450 Курортного района Санкт – Петербурга Кислородосодержащие органические соединения Cпирты (алканолы)
Кислородосодержащие органические соединения Cпирты (алканолы) Технологічні і біохімічні властивості м‘яса та м‘ясопродуктів. Будова тканин живих організмів
Технологічні і біохімічні властивості м‘яса та м‘ясопродуктів. Будова тканин живих організмів Сабақтың тақырыбы: Сутек. Сутектің табиғатта таралуы және алынуы.
Сабақтың тақырыбы: Сутек. Сутектің табиғатта таралуы және алынуы.  КОРОЗІЯ МЕТАЛІВ ЗАХИСТ ВІД КОРОЗІЇ
КОРОЗІЯ МЕТАЛІВ ЗАХИСТ ВІД КОРОЗІЇ 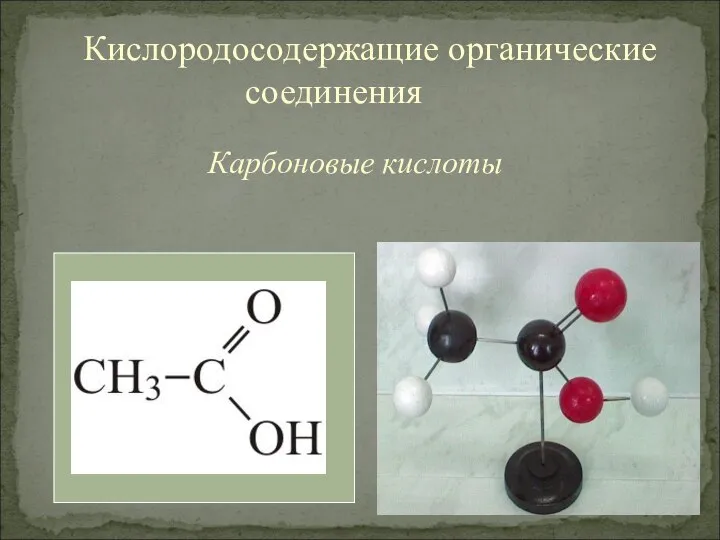 Презентация по Химии "КАРБОНОВЫЕ КИСЛОТЫ" - скачать смотреть
Презентация по Химии "КАРБОНОВЫЕ КИСЛОТЫ" - скачать смотреть  Биологические мембраны
Биологические мембраны Характеристика элементов VIII-В группы. Семейство железа
Характеристика элементов VIII-В группы. Семейство железа Химическая кинетика. Лекция 2
Химическая кинетика. Лекция 2 Аспірин Даниленко, Реутенко 11-А
Аспірин Даниленко, Реутенко 11-А  Соль. Добыча соли
Соль. Добыча соли