Содержание
- 2. План лекции Понятие термодинамической системы. 1 начало термодинамики. Энтальпия. Закон Гесса. Применение 1 начала термодинамики к
- 3. Термодинамика – это наука об энергии, ее свойствах и превращениях. Изучает процессы, связанные с переходом энергии
- 4. Основные понятия: Термодинамическая система – любой объект природы, состоящий из достаточно большого числа структурных единиц, находящихся
- 5. Термодинамические системы (ТДС) подразделяются: По характеру обмена системы с окружающей средой веществом и энергией на: -
- 6. По агрегатному состоянию компонентов на: - гомогенные (однородные) – системы в которых компоненты находятся в одинаковом
- 7. Для термодинамической системы характерен ряд свойств, совокупность которых называют состоянием системы. Состояние системы может быть равновесным,
- 8. Свойства системы могут быть охарактеризованы с помощью термодинамических переменных, которые называются параметрами состояния. Параметры состояния являются
- 9. Система может переходить из одного состояния в другое, что называется процессом. Процесс может быть обратимым и
- 10. При переходе системы из одного состояния в другое происходит изменение параметров состояния системы. Если изменения параметра
- 11. Важнейшей функцией состояния системы является внутренняя энергия (Е). Внутренняя энергия определяет общий запас энергии всех форм
- 12. Δ Е = Е2 – Е1, где Δ Е - изменение внутренней энергии, Е2 и Е1
- 13. I начало термодинамики Это есть обобщенный результат работы многих ученых: Ломоносов, Лаплас, Лавуазье, Майер, Гесс, Джоуль.
- 14. Математическое выражение I начала термодинамики: Q = ∆Е + W теплота, сообщаемая системе, тратится на изменение
- 15. Применение I начала термодинамики Изохорный процесс – характеризуется постоянством объема системы, V – const. Qv =
- 16. Изобарный процесс – характеризуется постоянством давления системы, р – const. Qр = ∆Е + p∙(V2 –
- 17. Энтальпия – функция состояния, которая показывает энергию расширенной системы или теплосодержание системы. Теплота изобарного процесса становится
- 18. Закон Гесса Тепловой эффект реакции при постоянном объеме и давлении не зависит от пути процесса, а
- 19. Тепловой эффект реакции определяют двумя путями: - экспериментальный, проводится в калориметрах; - теоретический, расчетный. Он основан
- 20. Первое следствие закона Гесса – тепловой эффект химической реакции равен разности между суммой теплот образования продуктов
- 21. Второе следствие закона Гесса – тепловой эффект химической реакции равен разности между суммой теплот сгорания исходных
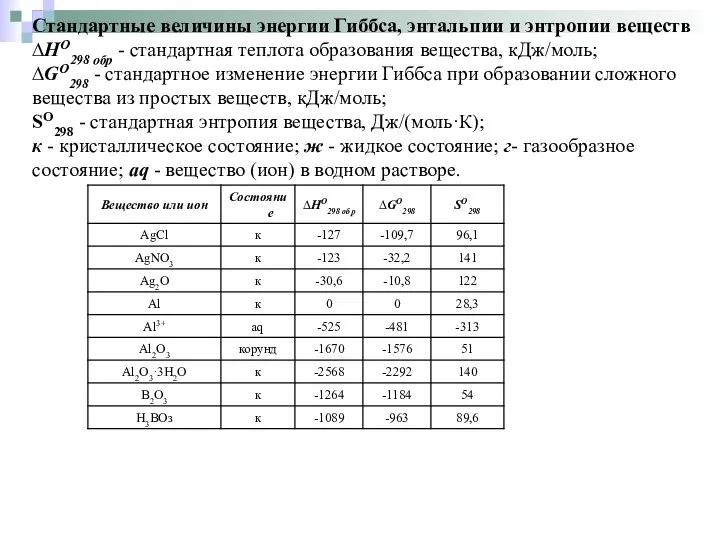
- 22. Стандартная теплота образования (∆Hо298 обр) – тепловой эффект преобразования из простых веществ 1моля соединения при стандартных
- 23. Стандартные величины энергии Гиббса, энтальпии и энтропии веществ ∆HO298 обр - стандартная теплота образования вещества, кДж/моль;
- 24. Биоэнергетика. задача биоэнергетики - изучение законов и механизмов накопления, хранения и использования энергии живыми системами. позволяет
- 25. Первое начало термодинамики для живых организмов все виды работ в организме совершаются за счет эквивалентного количества
- 26. Потребность в калориях можно рассчитать индивидуально, если учитывать 3 основных признака: - интенсивность труда; - возраст;
- 27. Суточная потребность в калориях: для лиц умственного труда (16-60 лет) - 2600-2800 кал; для работников механизированного
- 28. Q=ΔЕ+W. Если в живом организме t°=37°С=const, то ΔЕ=0, тогда первое начало термодинамики для живых организмов: Q=W
- 29. Первичным источником энергии в организме для производства всех видов работ является химическая энергия пищевых веществ. Однако
- 30. Второе начало термодинамики. Свободная энергия Гиббса. Первое начало термодинамики позволяет решать вопросы, связанные с определением теплоты
- 31. Ответ на вопрос о направленности протекания реакции дает второе начало, оно является обобщенным результатом труда многих
- 32. Формулировки второго начала термодинамики: Клаузиус (1850): Теплота не может самопроизвольно переходить от более холодного тела к
- 33. Величина изменения энтропии для обратимых и не обратимых процессов в изолированных системах определяется по уравнению: ∆S
- 34. Только часть теплоты идет на совершение работы, а другая часть является обесцененной или связанной. Связанная энергия
- 35. Термодинамическая вероятность показывает число микросостояний, отвечающих данному макросостоянию системы. К макросостояниям относят следующие свойства веществ: температуру,
- 36. Энтропия увеличивается с увеличением температуры, при переходе из кристаллического состояния в жидкое и газообразное. Чем больше
- 37. Изменение энтропии в реакции можно рассчитать, используя 1 следствие закона Гесса: изменение энтропии равно разности суммы
- 38. Применение II начала термодинамики к живым организмам Теорема Пригожина: в открытой системе в стационарном состоянии прирост
- 39. Истинным критерием направленности процессов является термодинамическая величина – свободная энергия Гиббса - ∆G ( изобарно-изотермический потенциал).
- 40. Процессы, идущие в живых организмах называются: ∆G ∆G > 0 – эндергонические – не самопроизвольные, эти
- 42. Скачать презентацию






































 Презентация по Химии "кристаллические решетки." - скачать смотреть бесплатно_
Презентация по Химии "кристаллические решетки." - скачать смотреть бесплатно_ Показники якості води Онуфреїв Оленка Слухач МАН Секція біологія.
Показники якості води Онуфреїв Оленка Слухач МАН Секція біологія. Оксид азота(2) NO
Оксид азота(2) NO Классификация кислот
Классификация кислот Жидкостная хроматография
Жидкостная хроматография Воздух. Постоянные компоненты воздуха
Воздух. Постоянные компоненты воздуха Тест
Тест Диффузия золота и свинца
Диффузия золота и свинца Синтетические волокна (продолжение)
Синтетические волокна (продолжение) Основи, їх склад, назви, класифікація.
Основи, їх склад, назви, класифікація.  Презентация по Химии "Химия нефти" - скачать смотреть бесплатно
Презентация по Химии "Химия нефти" - скачать смотреть бесплатно Альдегиды и кетоны
Альдегиды и кетоны Электронные представления в химии
Электронные представления в химии Методы выращивания GaAs. Сравнение
Методы выращивания GaAs. Сравнение Химия - основы общей химии (теория)
Химия - основы общей химии (теория) Общие закономерности адсорбции из растворов на поверхности твердого тела. Лекция 05
Общие закономерности адсорбции из растворов на поверхности твердого тела. Лекция 05 Аргентум, или серебро
Аргентум, или серебро Презентация Воздух, его состав и значение.
Презентация Воздух, его состав и значение.  Получение Н2, О2, щелочей
Получение Н2, О2, щелочей Фосфор Материал для повторения и подготовки к ГИА Учитель химии МОУ «Гимназия №1» г. Саратов Шишкина И.Ю.
Фосфор Материал для повторения и подготовки к ГИА Учитель химии МОУ «Гимназия №1» г. Саратов Шишкина И.Ю.  Магний. Магний алудың электролиттік жолы. Магний алудың термиялық жолдары
Магний. Магний алудың электролиттік жолы. Магний алудың термиялық жолдары Калий. Общая информация
Калий. Общая информация ОКИСЛИТЕЛЬНО – ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ Элективный специальный курс углублённого изучения темы для учащихся 11 классов естеств
ОКИСЛИТЕЛЬНО – ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ Элективный специальный курс углублённого изучения темы для учащихся 11 классов естеств Аминокислотный спектр плазмы крови у пациентов с острым миелобластным лейкозом
Аминокислотный спектр плазмы крови у пациентов с острым миелобластным лейкозом Гелий
Гелий Химия. Основные понятия и законы
Химия. Основные понятия и законы Презентация по Химии "Нафта" - скачать смотреть бесплатно
Презентация по Химии "Нафта" - скачать смотреть бесплатно Сероводород. Польза или вред
Сероводород. Польза или вред