Слайд 6

1) Уравнения реакций:
Ca3P2 + 6HCl = 3CaCl2 +2PH3 (1)
CaCl2 + K2CO3
=CaCO3↓ +2KCl (2).
2)Количества реагирующих веществ (количества «чистых» реагирующих веществ):
n =mв-ва /Mв-ва; mв-ва=W ∙ mр-ра; mр-ра=ρ∙V
а) количество HCl:
mр-ра (HCl) = 1,1∙400=440г
m (HCl) =0,05 ∙440=22г
n(HCl) =22/36,5≈0,603≈0,6 моль
n(HCl) = W∙ ρ∙V\ Mв-ва =0,05∙1,1∙400∕36,5=0,6 моль
б) количество K2CO3
m (K2CO3) =0,05∙193,5=9,675г
n (K2CO3)=9,675 ∕138≈0,07 моль
в) количество Ca3P2
n (Ca3P2)=18,2∕ 182= 0,1 моль
3)По уравнению (1) (количество CaCl2 и PH3 можно найти либо по Ca3P2, либо по HCl, следовательно, необходимо будет провести проверку на «избыток – недостаток» и производить расчет по «недостатку»)
а) n (Ca3P2) : n(HCl) : n(CaCl2) : n (PH3)=1:6:3:2, следовательно: Ca3P2 и HCl взяты в количествах, соответствующих уравнению реакции (эквимолярные количества) , и прореагируют полностью.
б) n (CaCl2) =3n(Ca3P2)=0,1∙3=0,3 моль
в) n (PH3)= 2n (Ca3P2)=0,1∙2=).2 моль
V(PH3)= n∙Vм =0,2∙22,4=4,48л
4)По уравнению (2)
n (CaCl2): n (K2CO3): n (CaCO3) =1:1:1, следовательно:
а) в избытке CaCl2 в количестве (0,3-0,07) =0,23 моль и
б) n (CaCO3) = n (K2CO3)= 0,07 моль
m(CaCO3)= n∙ Mв-ва=0,07 ∙100=7г.














 Химический состав и пищевая ценность кофе
Химический состав и пищевая ценность кофе Теоретические основы биоорганической химии
Теоретические основы биоорганической химии Мұнай қалдықтарын гидроөңдеу процестері. Катализаторлары
Мұнай қалдықтарын гидроөңдеу процестері. Катализаторлары Обмен фосфолипидов и стероидов
Обмен фосфолипидов и стероидов Аттестационная работа. Использование цифровой лаборатории Архимед во внеурочной деятельности по химии
Аттестационная работа. Использование цифровой лаборатории Архимед во внеурочной деятельности по химии Презентация Углерод Carboneum происходит от лат. carbo — уголь.
Презентация Углерод Carboneum происходит от лат. carbo — уголь. Взаимное влияние атомов в молекулах
Взаимное влияние атомов в молекулах Соли. Классификация сложных веществ
Соли. Классификация сложных веществ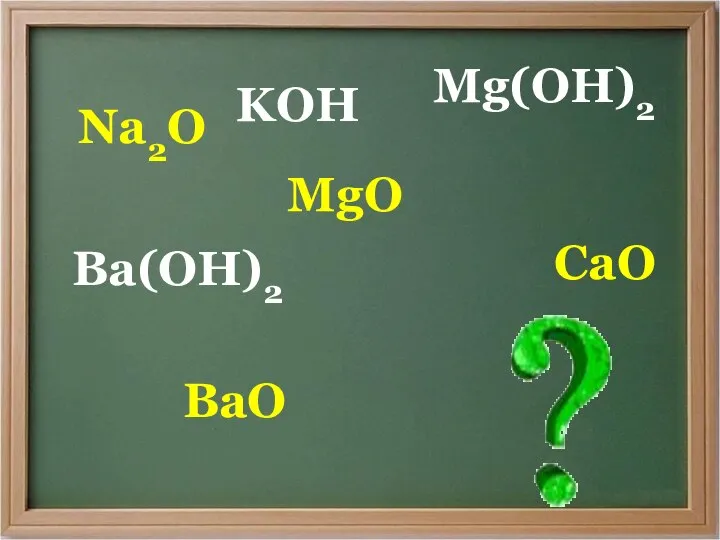 Оксиды и гидроксиды металлов
Оксиды и гидроксиды металлов Предмет органической химии. Основные понятия. Лекция 1
Предмет органической химии. Основные понятия. Лекция 1 Гидроксиды. Основания: способы получения
Гидроксиды. Основания: способы получения III А – топтың элементтері. Бор және алюминий
III А – топтың элементтері. Бор және алюминий Тренировочный тест. Уравнение состояния идеального газа
Тренировочный тест. Уравнение состояния идеального газа Алкалоиды природного происхождения
Алкалоиды природного происхождения Основы кристаллохимии
Основы кристаллохимии Области применения спиртов
Области применения спиртов Химический состав продуктов питания
Химический состав продуктов питания Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ
Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ Алкадиены (диеновые углеводороды)
Алкадиены (диеновые углеводороды) Нейрофизиология. Мембранный потенциал покоя и потенциал действия
Нейрофизиология. Мембранный потенциал покоя и потенциал действия Уран. Получение урана
Уран. Получение урана История получения алюминия
История получения алюминия Углерод и кремний. Лекция №15
Углерод и кремний. Лекция №15 Железо. Строение атома, физические и химические свойства простого вещества
Железо. Строение атома, физические и химические свойства простого вещества Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Адьдегиды
Адьдегиды Минералы. Классификация минералов
Минералы. Классификация минералов Механизмы органических реакций. (Лекция 2)
Механизмы органических реакций. (Лекция 2)