Содержание
- 2. Задания с развернутым ответом в структуре контрольных измерительных материалов для единого государственного экзамена 2017 года по
- 3. Задания 30 Задания 30 ориентированы на проверку следующих умений: определять степень окисления химических элементов, окислитель и
- 4. Задание 30
- 5. Составление электронного баланса: правильно указаны степени окисления элемента-окислителя и элемента-восстановителя; указаны (знаками + и –) процессы
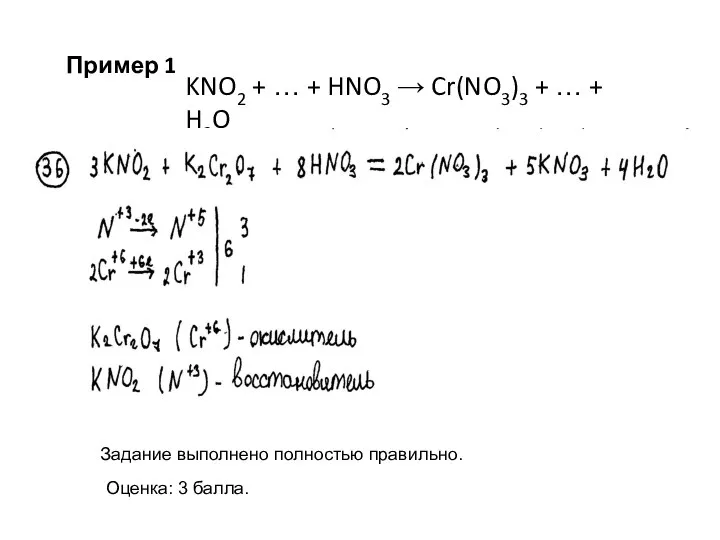
- 6. Задание выполнено полностью правильно. Оценка: 3 балла. Пример 1 KNO2 + … + HNO3 → Cr(NO3)3
- 7. K2Cr2O7 + KBr + H2SO4 → Cr2(SO4)3 + Br2 + … 2Cr+6 + 6ē → 2Cr+3
- 8. 2. Указаны окислитель и восстановитель (1 балл): - окислитель и восстановитель могут быть обозначены даже одной
- 9. В качестве окислителя выбран не дихромат, а хромат калия. Задание выполнено полностью правильно. Оценка: 3 балла.
- 10. В качестве окислителя выбран оксид хрома(IV). Электронный баланс составлен; определены окислитель и восствновитель. Не расставлены стехиометрические
- 11. Электронный баланс не составлен. Окислитель и восстановитель определены. Не расставлены стехиометрические коэффициенты в уравнении реакции. Оценка:
- 12. При составлении электронного баланса допущена ошибка (запись Cr2+3). Окислитель и восствновитель определены. Коэффициенты в уравнении реакции
- 13. Выбрана щелочная среда и Cr2O3 в качестве продукта реакции (при определении продукта не учтен характер среды).
- 14. Указаны окислитель и восстановитель. Определены недостающие веществаи расставлены коэффициенты в уравнении реакции. Электронный баланс составлен неверно.
- 15. Единых требований к оформлению ответа на это задание не предъявляется. Оценка: 3 балла. PCl3 + HNO3
- 16. Неверно составлен электронный баланс; указание окислителя и восстановителя записано неграмотно, но это не может быть основанием
- 17. Удвоены коэффициенты в уравнении реакции. Однако оснований для снижения оценки нет. Оценка: 3 балла
- 18. Задание 31 Выполнение этих заданий предполагает запись четырёх уравнений реакций, описание которых представлено в условии задания.
- 19. ЗаданиЗЗЗЗЗе
- 20. Опираемся на знания: кислотно-основное взаимодействие; реакции ионного обмена; окислительно-восстановительные реакции; комплексообразование (на примере гидроксокомплексов цинка и
- 21. Каждый из четырёх элементов ответа считать верным если: правильно записаны все формулы веществ − участников реакции;
- 22. Задание 31 Хлорид алюминия нагрели с калием. Полученный в результате металл поместили в раствор гидроксида калия.
- 23. Верно записаны 4 уравнения реакций. Оценка: 4 балла.
- 24. Верно записаны 4 уравнения реакций. Оценка: 4 балла.
- 25. При электролизе водного раствора нитрата меди(II) получили металл. Металл обработали концентрированной серной кислотой при нагревании. Выделившийся
- 26. Верно написаны 2, 3 и 4 уравнения реакций. Оценка: 3 балла
- 27. Уравнение 1- пропущен коэффициент перед формулой нитрата меди; Уравнение 2 – неверный коэффициент перед формулой диоксида
- 28. характерные химические свойства органических веществ различных классов генетическая взаимосвязь органических веществ Задание 32 Проверяемые ведущие элементы
- 29. В ответе экзаменуемого допустимо использование структурных формул разного вида (развёрнутой, сокращённой, скелетной), однозначно отражающих порядок связи
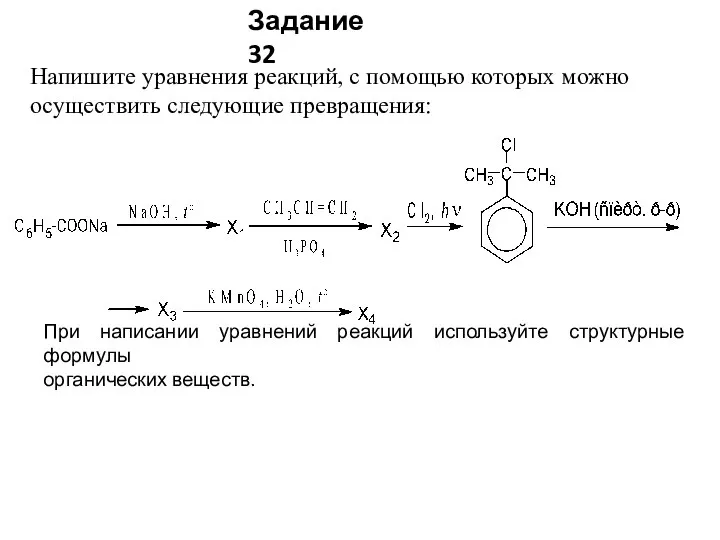
- 30. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: При написании уравнений реакций используйте структурные
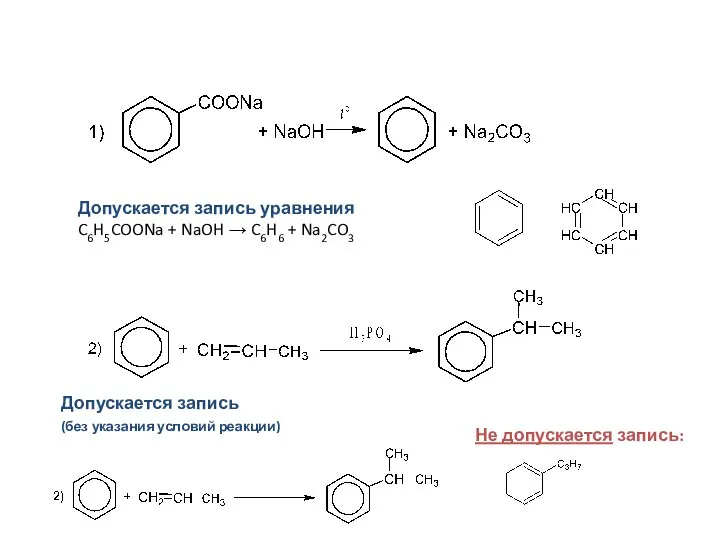
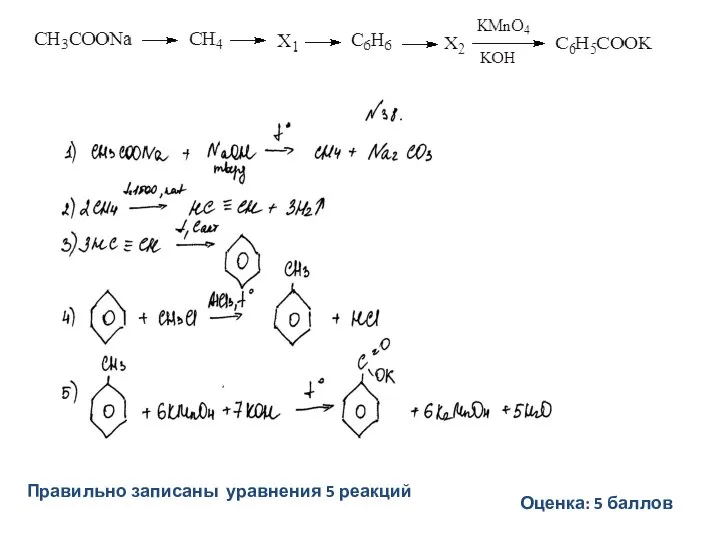
- 31. Допускается запись уравнения C6H5COONa + NaOH → C6H6 + Na2CO3 Допускается запись (без указания условий реакции)
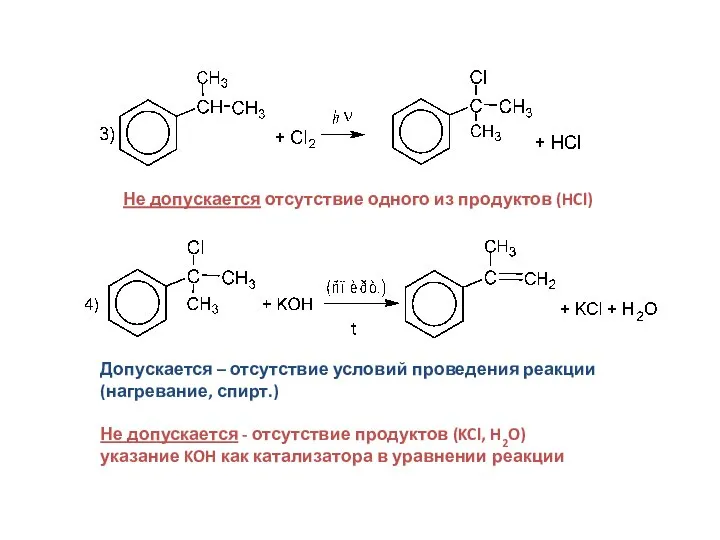
- 32. Не допускается отсутствие одного из продуктов (HCl) Допускается – отсутствие условий проведения реакции (нагревание, спирт.) Не
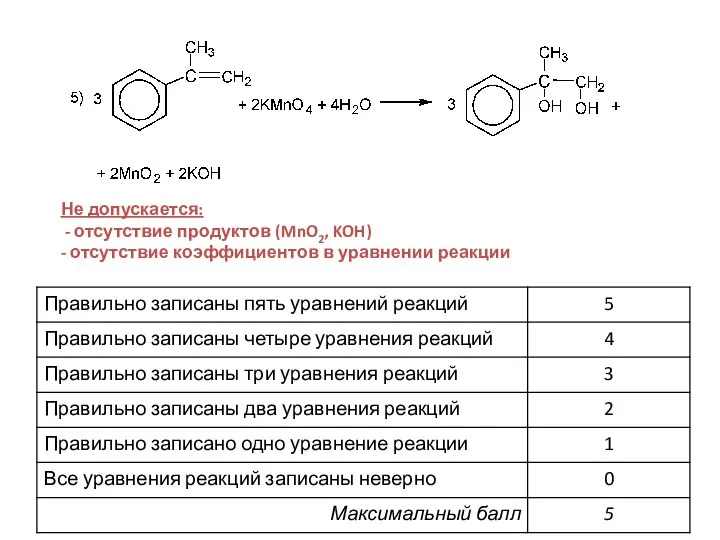
- 33. Не допускается: - отсутствие продуктов (MnO2, KOH) - отсутствие коэффициентов в уравнении реакции
- 35. Правильно записаны уравнения 5 реакций Пример 1 Оценка: 5 баллов
- 36. Пример 4 Оценка: 0 баллов Задание 32-1
- 37. Задание 33 Критерии оценивания
- 38. Задание 33
- 40. Работа 1 Уравнения р-ций – 1 б. Не использованы данные: 44,4 г Mg(NO3)2 Как найдено 0,68
- 41. Работа 2 Уравнения р-ций – 1 б. Данные условия все использованы - 1 б. Логика понятная:
- 42. Задание 34
- 43. Задание 34
- 44. Задание 34
- 45. Работа 8 Вычисления проведены неверно – 0 б. Молекулярная формула не соответствует условию задания – 0
- 46. Задание 34
- 47. Задание 34
- 48. Работа 10 Вычисления проведены верно – 1 б. Молекулярная формула соответствует условию задания – 1 б.
- 49. Работа 11 Вычисления проведены неверно – 0 б. Молекулярная формула соответствует условию и результату вычислений –
- 51. Скачать презентацию










































 Прибор “октис-2”
Прибор “октис-2” Горючие полезные ископаемые, топливно-энергетические ресурсы
Горючие полезные ископаемые, топливно-энергетические ресурсы Гидролиз. Сущность процесса гидролиза
Гидролиз. Сущность процесса гидролиза Определение молекулярной массы белка актина методом электрофореза по Лэммли
Определение молекулярной массы белка актина методом электрофореза по Лэммли Акварельные краски. Их состав и изготовление
Акварельные краски. Их состав и изготовление Учение о растворах. Буферные растворы
Учение о растворах. Буферные растворы Презентация по Химии "Классификация реакций в неорганической химии." - скачать смотреть бесплатно_
Презентация по Химии "Классификация реакций в неорганической химии." - скачать смотреть бесплатно_ Школьный кабинет химии
Школьный кабинет химии α-Аминокислоты. Белки
α-Аминокислоты. Белки Геохимические классификации химических элементов
Геохимические классификации химических элементов Горение жидкого топлива
Горение жидкого топлива ГИДРОЛИЗ СОЛЕЙ 9 класс Учитель биологии и химии Шапошникова Т.С.
ГИДРОЛИЗ СОЛЕЙ 9 класс Учитель биологии и химии Шапошникова Т.С.  Геологические структуры МПИ. Группа доминерализационных структур
Геологические структуры МПИ. Группа доминерализационных структур Вакуумная перегонка мазута
Вакуумная перегонка мазута Резины – эластомеры
Резины – эластомеры Газовая хроматография
Газовая хроматография Азотсодержащие органические соединения
Азотсодержащие органические соединения Алифатические углеводороды. Алканы, их свойства
Алифатические углеводороды. Алканы, их свойства Нефть. Способы её переработки. Продукты переработки нефти
Нефть. Способы её переработки. Продукты переработки нефти Роль ферментов в формировании потребительских свойств продовольственных товаров
Роль ферментов в формировании потребительских свойств продовольственных товаров Клиническая биохимия углеводного обмена. (Лекция 4)
Клиническая биохимия углеводного обмена. (Лекция 4) Щелочные металлы
Щелочные металлы Дисперсные системы Эмульсии. Пены. Порошки
Дисперсные системы Эмульсии. Пены. Порошки Обмен жиров
Обмен жиров Окислительно-восстановительные реакции (ОВР). Часть 2
Окислительно-восстановительные реакции (ОВР). Часть 2 Метод крутого восхождения или метод Бокса-Уилсона. Симплексный метод оптимизации
Метод крутого восхождения или метод Бокса-Уилсона. Симплексный метод оптимизации Мультимедийные иллюстрации по лекционному курсу «Биологическая химия»
Мультимедийные иллюстрации по лекционному курсу «Биологическая химия» Жиры. Общее строение жиров
Жиры. Общее строение жиров