Содержание
- 2. О железе Железо – не только основа всего мира, самый главный элемент окружающей нас природы. Оно
- 3. Немного истории В середине II тысячелетия до н.э. в Египте была основана металлургия железа – получение
- 4. Железо в природе
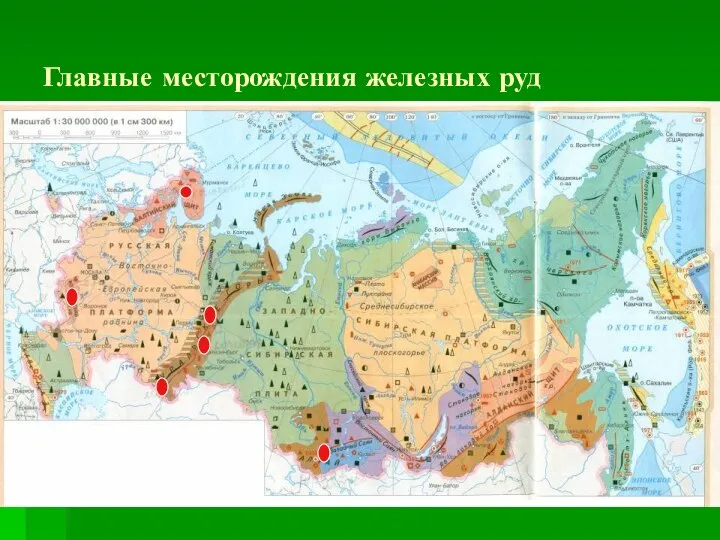
- 5. Главные месторождения железных руд
- 6. Живое железо
- 7. Железо – d-элемент. Порядковый номер 26 Относительная атомная масса 55,847 Валентность переменная II-III
- 8. Физические свойства железа Плотность=7,87 г/см3 Тпл = 1539ْ С Ткип = 3200ْ С Намагничивается Легко обрабатывается:
- 9. Химические свойства железа Металл средней активности в концентрированных серной и азотной кислотах пассивируется
- 10. Железо реагирует : С простыми веществами: Fe + S = FeS 2Fe + 3Cl2 = 2FeCl3
- 11. Коррозия металла Железо разрушается под действием окружающей среды – оно ржавеет 4Fe + 3O2 + 2n·H2O
- 12. Защита железа от коррозии Лако-красочные покрытия Эмаль – силикатное стекло с добавлением оксидов металлов Металлические покрытия:
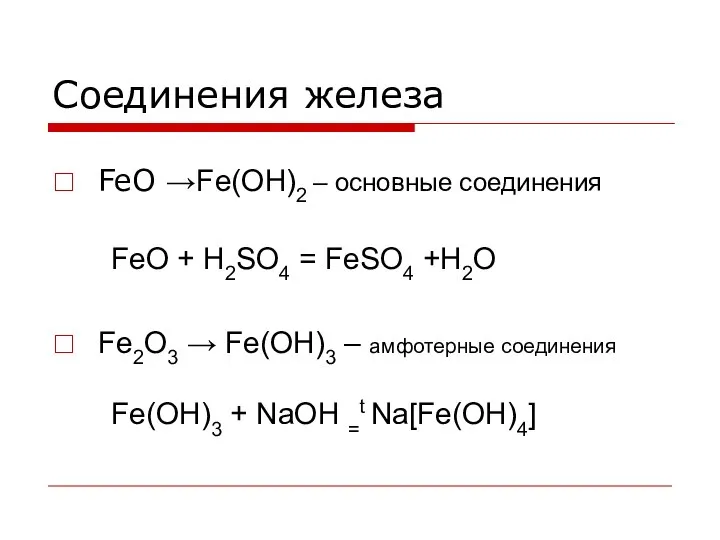
- 13. Соединения железа FeO →Fe(OH)2 – основные соединения FeO + H2SO4 = FeSO4 +H2O Fe2O3 → Fe(OH)3
- 14. Качественные реакции На ион Fe2+ - взаимодействие с красной кровяной солью гексацианоферратом (III)калия Fe+2SO4+K3[Fe(CN)6]=KFe+3[Fe+2(CN)6]↓+K2SO4 синего цвета
- 16. Скачать презентацию











 Химический элемент кремний
Химический элемент кремний Презентация Палладий
Презентация Палладий  Липиды. Структурные компоненты липидов
Липиды. Структурные компоненты липидов Презентация по Химии "Комплексные соединения" - скачать смотреть
Презентация по Химии "Комплексные соединения" - скачать смотреть  Ферменты. Знакомство с ферментами
Ферменты. Знакомство с ферментами Азот и фосфор
Азот и фосфор Синтез, строение и свойства люминесцирующих координационных соединений тербия(III), европия(III) и гадолиния(III) с дикарбоновыми кисло
Синтез, строение и свойства люминесцирующих координационных соединений тербия(III), европия(III) и гадолиния(III) с дикарбоновыми кисло Гидролиз
Гидролиз «Сухая вода» помогла измерить поляризацию ковалентных связей
«Сухая вода» помогла измерить поляризацию ковалентных связей Алексей Евграфович Фаворский и его вклад в победу СССР.
Алексей Евграфович Фаворский и его вклад в победу СССР. Углерод и его соединения
Углерод и его соединения Урок в 8 классе На тему ???
Урок в 8 классе На тему ??? Базовые масла и присадки
Базовые масла и присадки An introduction to the chemistry of alkenes
An introduction to the chemistry of alkenes Синтез (+)-aplykurodinone-1
Синтез (+)-aplykurodinone-1 ГИДРОЛИЗ СОЛЕЙ 9 класс Учитель биологии и химии Шапошникова Т.С.
ГИДРОЛИЗ СОЛЕЙ 9 класс Учитель биологии и химии Шапошникова Т.С.  Определение количества этилендиамина в соединении [Gd(en)x][Fe(CN)6]
Определение количества этилендиамина в соединении [Gd(en)x][Fe(CN)6] Растворение. Растворимость веществ в воде
Растворение. Растворимость веществ в воде Новые научные принципы и технологии извлечения металлов из комплексных руд и техногенных отходов
Новые научные принципы и технологии извлечения металлов из комплексных руд и техногенных отходов Нуклеофильное замещение галогена и других функциональных групп
Нуклеофильное замещение галогена и других функциональных групп Классификация неорганических соединений. Оксиды и их свойства
Классификация неорганических соединений. Оксиды и их свойства Обучающий тест «Виды химической связи»
Обучающий тест «Виды химической связи» Уравнения химических реакций
Уравнения химических реакций Химический элемент гелий
Химический элемент гелий Полиэтилен - термопластичный полимер этилена
Полиэтилен - термопластичный полимер этилена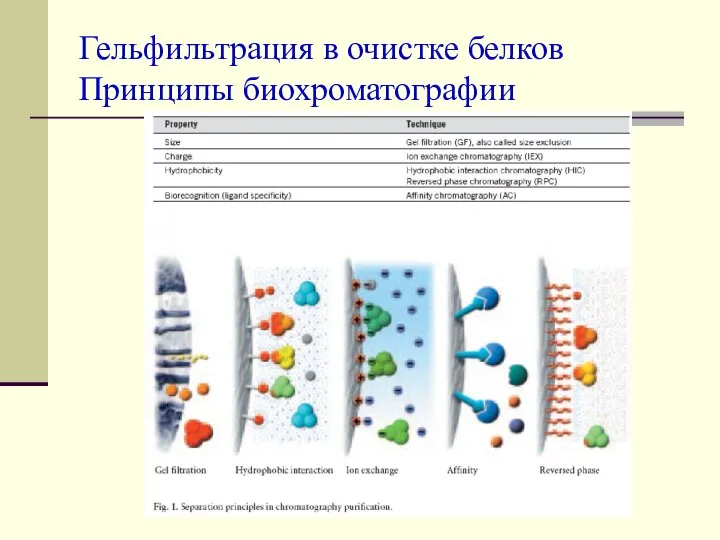 Гельфильтрация в очистке белков. Принципы биохроматографии
Гельфильтрация в очистке белков. Принципы биохроматографии Бальзам-ополаскиватель для волос
Бальзам-ополаскиватель для волос Массообменные процессы
Массообменные процессы