Содержание
- 2. Биоорганическая химия изучает строение и своства веществ, участвующих в процессах жизнедеятельности, в непосредственной связи с познанием
- 3. Электронная структура атома углерода в органических соединениях основное состояние возбужденное состояние
- 8. Классификация по функциональным группам Углеводороды СхНу Кислородсодержащие Азотсодержащие Углеводы Липиды спирты альдегиды кислоты Сложные эфиры амины
- 9. Типы номенклатуры Систематическая Тривиальная Рациональная Систематическая Рациональная
- 10. Правила номенклатуры IUPAC: (IUPAC - Международный союз чистой и прикладной химии, ИЮПАК) префикс корень суффикс Название
- 11. Характеристические группы обозначаемые префиксами и суффиксами.
- 12. Характеристические группы, обозначаемые только префиксами
- 13. Важнейшие углеводородные радикалы, обозначаемыми префиксами.
- 16. Типы химической связи
- 17. Индуктивный эффект Индуктивный эффект - смещение электронной плотности по цепи σ-связей, которое обусловлено различиями в электроотрицательностях
- 18. Индуктивный эффект называют отрицательным (-I), если заместитель смещает электронную плотность ϭ-связи от атома углерода, с которым
- 20. Индуктивный эффект называют положительным (+ I), если заместитель увеличивает электронную плотность на атоме углерода, индуцируя на
- 21. Индуктивный эффект передается по цепи σ-связей с затуханием через 3-4 связи
- 22. Мезомерный эффект Мезомерный эффект – смещение электронной плотности по цепи делокализаванных (сопряженных) π-связей. Системы с открытой
- 23. Системы с замкнутой цепью сопряжения Арены Строение молекулы бензола 6 электронов в делокализованной π связи
- 24. Арены «Ароматичность» – совокупность особых свойств бензола Правило Хюккеля (1931): - плоский замкнутый цикл сопряженная система
- 25. Мезомерный эффект Мезомерный эффект передается по цепи сопряжения без затухания. Мезомерный эффект изображается изогнутыми стрелками
- 26. + М-эффектом обладают заместители, повышающие электронную плотность в сопряженной системе. К ним относятся группы, которые содержат
- 27. +М-эффект заместителя фенол
- 28. -М-эффект заместителя бензальдегид
- 29. Классификация органических реакций 1. По типу разрыва связей. A:B А. + B. Гомолитические реакции – симметричный
- 30. - A:B А: + B Е N Гетеролитические реакции – несимметричный разрыв связи, приводящий к появлению
- 31. Синхронные реакции (согласованные, «реакции без механизма») одно переходное состояние, нет промежуточных соединений
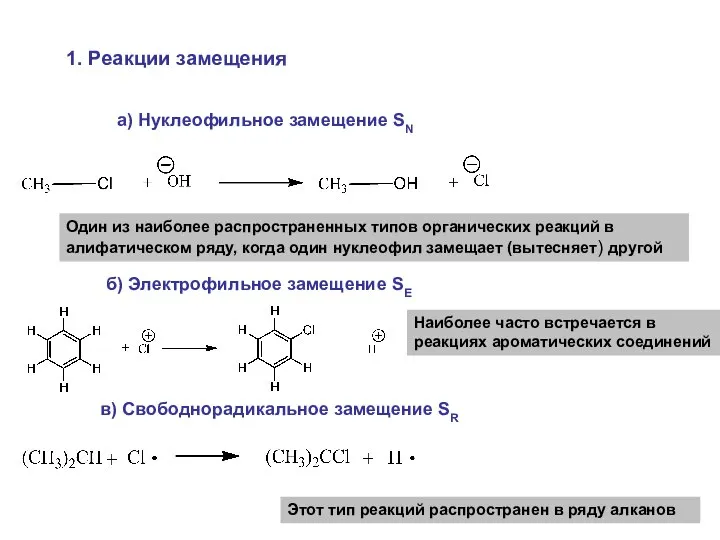
- 32. 2. Классификация по конечному результату 1. Реакции замещения Данный тип реакций обозначают буквой S (от английского
- 33. 1. Реакции замещения а) Нуклеофильное замещение SN Один из наиболее распространенных типов органических реакций в алифатическом
- 34. 2. Реакции присоединения Обозначаются символом A от англйского «Addition» - присоединение. К ним относятся реакции присоединения
- 35. 3. Реакции элиминирования Обозначают символом E от английского «Elimination» - отщепление. Эти реакции приводят к образованию
- 36. 4. Перегруппировки или изомеризации Чрезвычайно характерные для органических соединений реакции, при которых изменяется порядок связывания атомов
- 37. 5. Реакции окисления и восстановления Сопровождаются изменением степени окисления атома углерода, Являющегося реакционным центром. 6. Реакции
- 38. В каждой органической реакции различают: субстрат и реагент. Субстрат – вещество, вступающее в реакцию, в которой
- 39. Виды органических реакций
- 40. Кислотность и основность органических соединений.
- 41. 1. Протонная теория Дж.Бренстеда и Т.Лоури Кислоты Бренстеда – нейтральные молекулы или ионы, способные отдавать протон.
- 42. Оценка кислотности 1. Сила кислоты характеризуется K дисс. 2. Качественно сила кислоты оценивается по стабильности сопряженного
- 43. Факторы, определяющие кислотность (стабильность аниона) а) Влияние ЭО атома в кислотном центре. Чем больше ЭО атома
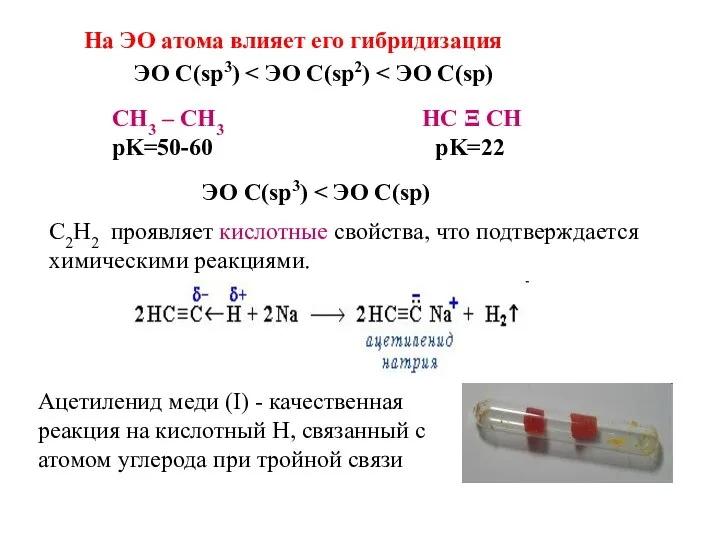
- 44. На ЭО атома влияет его гибридизация СН3 – СН3 НС Ξ СН pK=50-60 pK=22 ЭО С(sp3)
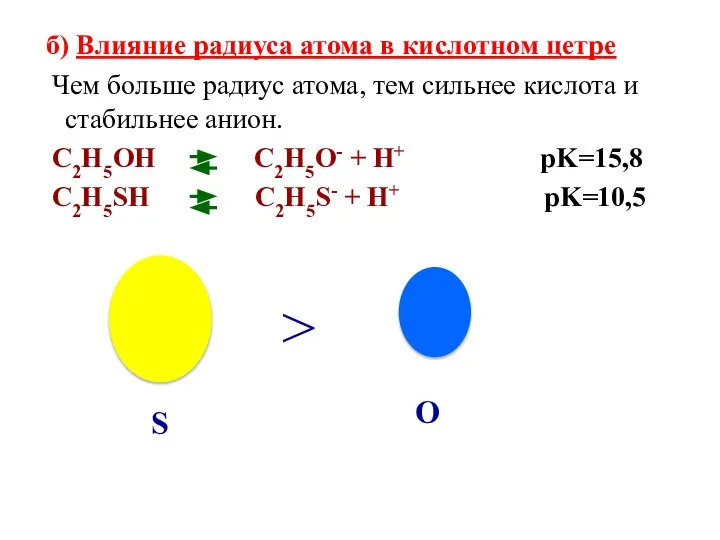
- 45. б) Влияние радиуса атома в кислотном цетре Чем больше радиус атома, тем сильнее кислота и стабильнее
- 46. в) Влияние заместителей Заместители с –I эффектом усиливают кислотность, а с + I эффектом – ослабляют.
- 47. г) Влияние сопряжения Участие в сопряжении усиливает кислотность
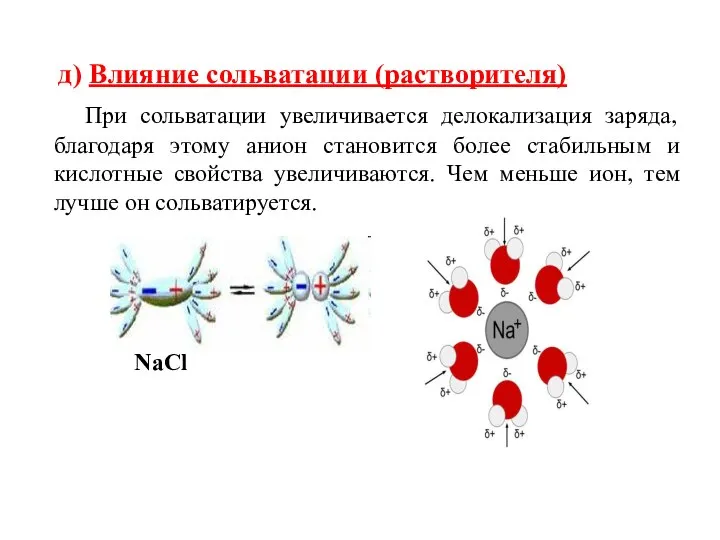
- 48. д) Влияние сольватации (растворителя) При сольватации увеличивается делокализация заряда, благодаря этому анион становится более стабильным и
- 49. Основания Бренстеда – нейтральные молекулы или ионы, способные присоединять протоны (акцепторы Н+). π- основания: молекулы с
- 50. Факторы, влияющие на основность а) Электроотрицательность элемента Чем меньше ЭО, тем сильнее основность б) Размер гетероатома
- 51. 2.Электронная теория Льюиса (1923). Кислота - частица-акцептор электронной пары (H+, BF3, AlCl3). Основание – частица-донор электронной
- 52. Принцип жестких и мягких кислот и оснований (ЖКМО) Пирсона Принцип ЖМКО жесткие кислоты предпочтительно связываются с
- 53. Жесткие кислоты – кислоты, в которых атом-акцептор пары электронов имеет небольшой размер, положительно заряжен, обладает низкой
- 55. Скачать презентацию
















































 Галогенопроизводные. Растворимость, общие закономерности
Галогенопроизводные. Растворимость, общие закономерности Очищение грязной воды
Очищение грязной воды Ароматические углеводороды. Гомологический ряд, изомерия
Ароматические углеводороды. Гомологический ряд, изомерия Биохимия витаминов. Классификация витаминов. Жирорастворимые витамины. (Лекция 20)
Биохимия витаминов. Классификация витаминов. Жирорастворимые витамины. (Лекция 20) Презентация по Химии "Окислительно-восстановительные реакции" - скачать смотреть бесплатно
Презентация по Химии "Окислительно-восстановительные реакции" - скачать смотреть бесплатно d-элементы
d-элементы Классификация реагентов и реакций в органической химии. (Лекция 4)
Классификация реагентов и реакций в органической химии. (Лекция 4) Химические реакции
Химические реакции Гума
Гума  Алюминий. Строение и свойства атома
Алюминий. Строение и свойства атома Свободные радикалы и болезни человека
Свободные радикалы и болезни человека Бензол. Бензол гомологтары. Фенолдар және ароматты аминдер
Бензол. Бензол гомологтары. Фенолдар және ароматты аминдер Алкины. Способы получения
Алкины. Способы получения Витаминдер. Витаминдердің классификациясы. Алиментарлы және екіншілік авитаминоздар. Гипервитаминоздар
Витаминдер. Витаминдердің классификациясы. Алиментарлы және екіншілік авитаминоздар. Гипервитаминоздар Загальні способи добування солей. Класифікація неорганічних речовин
Загальні способи добування солей. Класифікація неорганічних речовин Физико-химические свойства жиров
Физико-химические свойства жиров Алкены «Бутен»
Алкены «Бутен» Презентация по Химии "Великие учёные, внёсшие значительный вклад в развитие химии." - скачать смотреть бесплатно
Презентация по Химии "Великие учёные, внёсшие значительный вклад в развитие химии." - скачать смотреть бесплатно Системный анализ и моделирование процессов. Горение паро-газо-воздушного облака
Системный анализ и моделирование процессов. Горение паро-газо-воздушного облака Нафта, вугілля, природний газ як вуглеводнева сировина. Основні види палива та їх значення в енергетиці країни.
Нафта, вугілля, природний газ як вуглеводнева сировина. Основні види палива та їх значення в енергетиці країни.  Химия и пища
Химия и пища “Су. Ерітінділер” тарауын қорытындылау
“Су. Ерітінділер” тарауын қорытындылау Пластмаси, синтетичні каучуки Виконала: Учениця 11 – А класу Твердохліб Анжеліка
Пластмаси, синтетичні каучуки Виконала: Учениця 11 – А класу Твердохліб Анжеліка  Аммиак
Аммиак Ситуационная задача по биохимии
Ситуационная задача по биохимии Періодичний закон і система хімічних елементів Д.І.Менделєєва. Будова атома.
Періодичний закон і система хімічних елементів Д.І.Менделєєва. Будова атома.  Основы коррозии и защиты металлов. Опасность локальных видов коррозии
Основы коррозии и защиты металлов. Опасность локальных видов коррозии Фенолы: понятие, классификация, номенклатура, изомерия, получение, физические свойства, химические свойства, применение
Фенолы: понятие, классификация, номенклатура, изомерия, получение, физические свойства, химические свойства, применение