Содержание
- 2. Боль в спине: актуальность проблемы Примерно 90% взрослых людей в какой-либо момент жизни испытывают боль в
- 3. Факторы, провоцирующие возникновение боли в спине Избыточный вес Сидячий образ жизни Курение Тяжелая физическая работа Аномалии
- 4. Принципы терапии Учитывая этиологические, патогенетические факторы развития боли в спине, общие принципы обезболивания, данные доказательной медицины
- 5. Применение НПВП Согласно рекомендациям доказательной медицины, для купирования острой боли в спине используют нестероидные противовоспалительные препараты
- 6. Арахидоновая кислота Фосфолипиды мембран Конститутивная циклооксигеназа-1 (ЦОГ-1) Индуцируемая циклооксигеназа-2 (ЦОГ-2) Тромбоксан A2 (тромбоциты) Простациклин (эндотелий, слизистая
- 7. Арахидоновая кислота Фосфолипиды мембран Конститутивная циклооксигеназа-1 (ЦОГ-1) Индуцируемая циклооксигеназа-2 Воспаление, боль, жар Физиологические функции Повышение риска
- 8. Ксефокам®(Лорноксикам): мощный, сбалансированный ингибитор ЦОГ-1/ЦОГ-2 Сбалансированный ингибитор ЦОГ-1 / ЦОГ-2, принадлежащий НПВП класса оксикамов1 Мощное обезболивающее
- 9. Лорноксикам выпускается в трех различных формах Международное непатентованное название – лорноксикам Фармакотерапевтическая группа – нестероидный противовоспалительный
- 10. Лорноксикам: мощный, сбалансированный ингибитор ЦОГ-1 и ЦОГ-2 Berg J et al. Inflamm Res 1999;48:369-79 Лорноксикам –
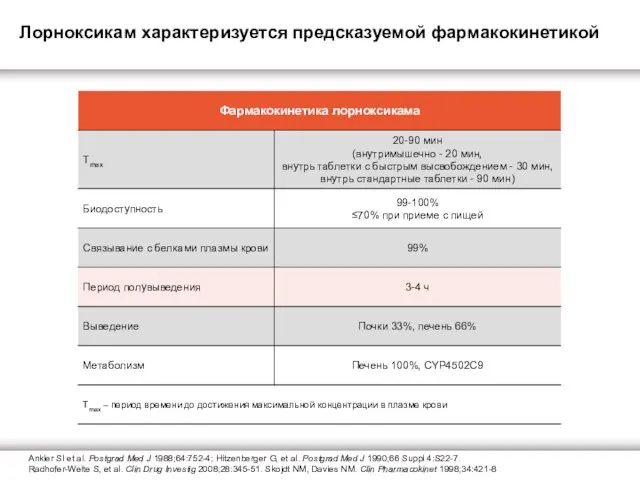
- 11. Ankler SI et al. Postgrad Med J 1988;64:752-4; Hitzenberger G, et al. Postgrad Med J 1990;66
- 12. Лорноксикам быстро всасывается и обеспечивает быстрое ослабление боли Radhofer-Welte S et al. Clin Drug Invest 2008;28:345-51
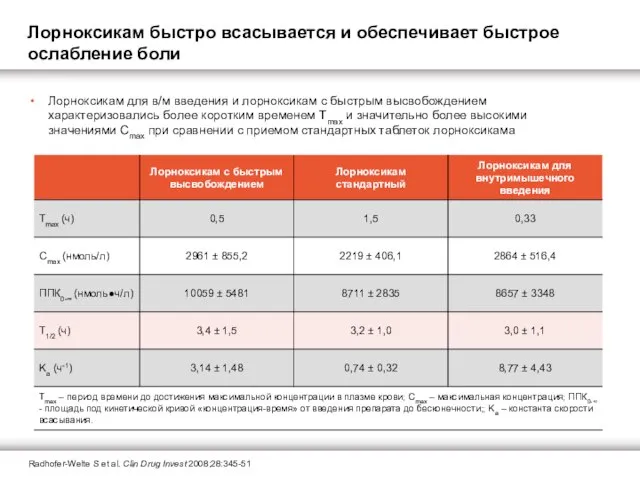
- 13. Radhofer-Welte S et al. Clin Drug Invest 2008;28:345-51 Лорноксикам для в/м введения и лорноксикам с быстрым
- 14. Relative TLR2 mRNA expression Relative TLR4 mRNA expression Gorsky VA et al. Pancreas 2015;V. 44:p. 824–830
- 15. Lipopolysaccharide – TNF-α concentration (pg/ml) Peptidoglycan -TNF-α concentration (pg/ml) Gorsky VA et al. Pancreas 2015;V. 44:p.
- 16. Lipopolysaccharide – IL-6 concentration (pg/ml) Peptidoglycan – IL-6 concentration (pg/ml) Лорноксикам может снижать боль, уменьшая воспаление
- 17. Lipopolysaccharide – IL-8 concentration (pg/ml) Peptidoglycan – IL-8 concentration (pg/ml) *patients with complications of acute pancreatitis
- 18. Ксефокам (лорноксикам): фармакокинетика Метаболизм: Метаболизируется в печени (5-гидроксилорноксикам) Цитохром P450 CYP2C9 Более короткий период полувыведения (3-4
- 19. Ксефокам (лорноксикам): фармакокинетика Быстрое, эффективное всасывание Быстрое достижение равновесной концентрации Короткий период полувыведения (3-4 ч) независимо
- 20. Ксефокам (лорноксикам): безопасность
- 21. Более половины из 83 пациентов (52%) отметили ослабление боли при движении через 1 ч после получения
- 22. Herrmann WA & Geertsen MS. Int J Clin Pract 2009;63:1613-21 Значимые различия в интенсивности боли при
- 23. Медиана времени до начала обезболивающего действия при терапии лорноксикамом с быстрым высвобождением была меньше, чем при
- 24. При терапии лорноксикамом с быстрым высвобождением различия в оценках интенсивности боли за 90-минутный период после введения
- 25. Общее обезболивающее действие (индекс TOTPAR) в течение 90 мин после введения препарата было значимо выше в
- 26. Лорноксикам с быстрым высвобождением хорошо переносился при лечении люмбаго Лорноксикам с быстрым высвобождением и калия диклофенак
- 27. Общая оценка пациентами (по 5-балльной шкале) Лорноксикам с быстрым высвобождением 8 мг (n=110) Калия диклофенак 50
- 28. Схема назначения Лорноксикама при боли в спине
- 29. Цитируемые источники Aabakken L, Osnes M, Frenzel W. Gastrointestinal tolerability of lornoxicam compared to that of
- 30. Цитируемые источники Kocaayan E, Ozkardeşler S, Ozzeybek D, Bayindir S, Akan M. Comparison of effects of
- 32. Скачать презентацию
Боль в спине: актуальность проблемы
Примерно 90% взрослых людей в какой-либо момент
Боль в спине: актуальность проблемы
Примерно 90% взрослых людей в какой-либо момент
Эта патология занимает первое место в списке причин нетрудоспособности у лиц моложе 45 лет
У работающих лиц старше 45 лет боль в спине по частоте находится на третьем месте после сердечно-сосудистых заболеваний и боли в суставах
В 27,5% случаях является причиной обращения амбулаторных больных трудоспособного возраста в поликлинику
У трети пациентов впоследствии острая боль переходит в хроническую, которая сохраняется более 12 нед.
Факторы, провоцирующие возникновение боли в спине
Избыточный вес
Сидячий образ жизни
Курение
Факторы, провоцирующие возникновение боли в спине
Избыточный вес
Сидячий образ жизни
Курение
Тяжелая физическая работа
Аномалии развития скелета
Длительное пребывание в нефизиологической позе
Неудачные, резкие повороты
Длительная вибрация всего тела
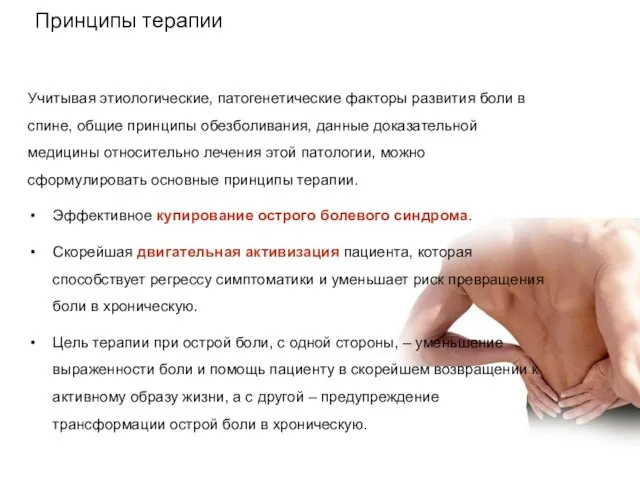
Принципы терапии
Учитывая этиологические, патогенетические факторы развития боли в спине, общие принципы
Принципы терапии
Учитывая этиологические, патогенетические факторы развития боли в спине, общие принципы
Эффективное купирование острого болевого синдрома.
Скорейшая двигательная активизация пациента, которая способствует регрессу симптоматики и уменьшает риск превращения боли в хроническую.
Цель терапии при острой боли, с одной стороны, – уменьшение выраженности боли и помощь пациенту в скорейшем возвращении к активному образу жизни, а с другой – предупреждение трансформации острой боли в хроническую.
Применение НПВП
Согласно рекомендациям доказательной медицины, для купирования острой боли в спине
Применение НПВП
Согласно рекомендациям доказательной медицины, для купирования острой боли в спине
Длительность применения и способ введения НПВП зависят от интенсивности болевого синдрома.
При умеренной боли, не ограничивающей движения пациента, обычно используют низкие дозы пероральных НПВП,
При выраженной боли, существенно ограничивающей передвижение пациента, применяют инъекционное введение в течение 3-7 дней с переходом в дальнейшем на пероральный прием (цель назначения НПВС не только обезболивание, но и противовоспалительное воздействие)
Лечение в среднем составляет 3-4 недели, при радикулопатии – более длительное время.
Арахидоновая кислота
Фосфолипиды мембран
Конститутивная циклооксигеназа-1 (ЦОГ-1)
Индуцируемая циклооксигеназа-2 (ЦОГ-2)
Тромбоксан A2 (тромбоциты)
Простациклин
(эндотелий, слизистая желудка)
Простагландин
Арахидоновая кислота
Фосфолипиды мембран
Конститутивная циклооксигеназа-1 (ЦОГ-1)
Индуцируемая циклооксигеназа-2 (ЦОГ-2)
Тромбоксан A2 (тромбоциты)
Простациклин
(эндотелий, слизистая желудка)
Простагландин
Протеазы
Простагландины
Другие воспалительные медиаторы
Воспаление, боль, жар
Физиологические функции
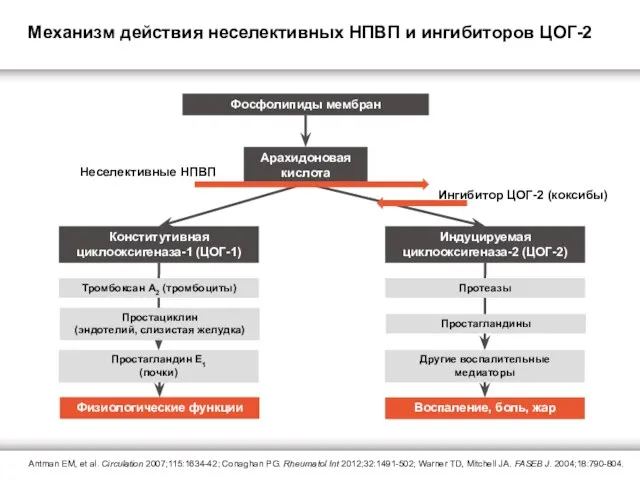
Механизм действия неселективных НПВП и ингибиторов ЦОГ-2
Antman EM, et al. Circulation 2007;115:1634-42; Conaghan PG. Rheumatol Int 2012;32:1491-502; Warner TD, Mitchell JA. FASEB J. 2004;18:790-804.
Арахидоновая кислота
Фосфолипиды мембран
Конститутивная циклооксигеназа-1 (ЦОГ-1)
Индуцируемая циклооксигеназа-2
Воспаление, боль, жар
Физиологические функции
Повышение риска тромботических
Арахидоновая кислота
Фосфолипиды мембран
Конститутивная циклооксигеназа-1 (ЦОГ-1)
Индуцируемая циклооксигеназа-2
Воспаление, боль, жар
Физиологические функции
Повышение риска тромботических
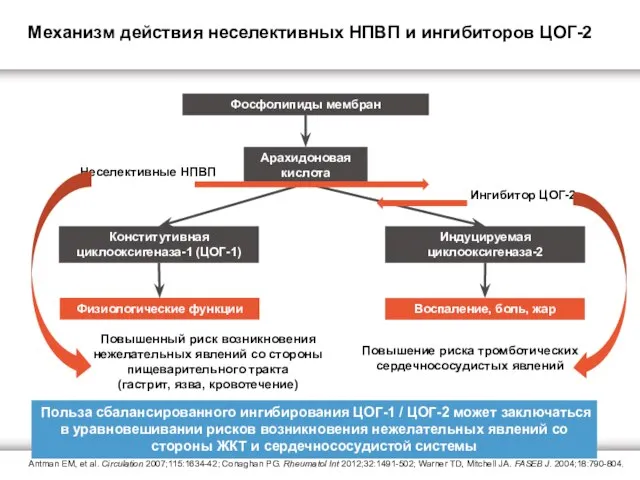
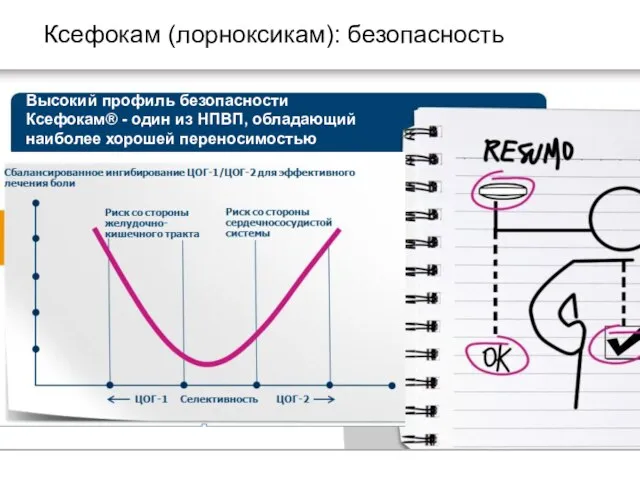
Польза сбалансированного ингибирования ЦОГ-1 / ЦОГ-2 может заключаться в уравновешивании рисков возникновения нежелательных явлений со стороны ЖКТ и сердечнососудистой системы
Antman EM, et al. Circulation 2007;115:1634-42; Conaghan PG. Rheumatol Int 2012;32:1491-502; Warner TD, Mitchell JA. FASEB J. 2004;18:790-804.
Механизм действия неселективных НПВП и ингибиторов ЦОГ-2
Повышенный риск возникновения нежелательных явлений со стороны пищеварительного тракта
(гастрит, язва, кровотечение)
Ксефокам®(Лорноксикам): мощный, сбалансированный ингибитор ЦОГ-1/ЦОГ-2
Сбалансированный ингибитор ЦОГ-1 / ЦОГ-2, принадлежащий НПВП
Ксефокам®(Лорноксикам): мощный, сбалансированный ингибитор ЦОГ-1/ЦОГ-2
Сбалансированный ингибитор ЦОГ-1 / ЦОГ-2, принадлежащий НПВП
Мощное обезболивающее и противовоспалительное действие2
Быстрое всасывание обеспечивает быстрое начало действия3,4
Короткое время полувыведения (3-5 ч) при сравнении с другими оксикамами3-5
Маловероятно накопление в плазме крови
Потенциальная польза в отношении переносимости и снижения риска возникновения нежелательных явлений
Простая предсказуемая фармакокинетика3,5,6
Минимальное влияние на функции почек и печени
Отсутствует необходимость в снижении дозы у пожилых пациентов
Выпускается в трех формах4
Для приема внутрь, для приема внутрь с быстрым высвобождением, флаконы (внутривенное /внутримышечное введение)
1Berg J et al. Inflamm Res 1999;48:369-79; 2Pruss TP et al. Postgrad Med J 1990;66 Suppl 4:S18-21.3Hitzenberger G et al. Postgrad Med J 1990;66 Suppl 4:S22-7.
4Radhofer-Welte S et al. Clin Drug Investig 2008;28:345-51. 5Skojdt NM, Davies NM. Clin Pharmacokinet 1998;34:421-8; 6Ankler SI et al. Postgrad Med J 1988;64:752-4
Лорноксикам выпускается в трех различных формах
Международное непатентованное название – лорноксикам
Фармакотерапевтическая группа
Лорноксикам выпускается в трех различных формах
Международное непатентованное название – лорноксикам
Фармакотерапевтическая группа
Класс – оксикамы
Формы выпуска:
лиофилизат для приготовления раствора для внутривенного и внутримышечного введения 8 мг №5
таблетки покрытые оболочкой 4 мг № 10 и №30
таблетки покрытые оболочкой 8 мг № 10 и №30
Ксефокам рапид таблетки покрытые оболочкой 8 мг № 12 (быстродействующая форма)
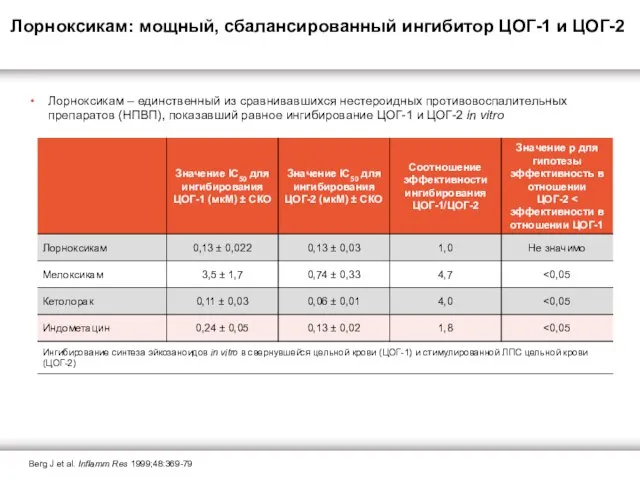
Лорноксикам: мощный, сбалансированный ингибитор ЦОГ-1 и ЦОГ-2
Berg J et al. Inflamm
Лорноксикам: мощный, сбалансированный ингибитор ЦОГ-1 и ЦОГ-2
Berg J et al. Inflamm
Лорноксикам – единственный из сравнивавшихся нестероидных противовоспалительных препаратов (НПВП), показавший равное ингибирование ЦОГ-1 и ЦОГ-2 in vitro
Ankler SI et al. Postgrad Med J 1988;64:752-4; Hitzenberger G, et
Ankler SI et al. Postgrad Med J 1988;64:752-4; Hitzenberger G, et
Лорноксикам характеризуется предсказуемой фармакокинетикой
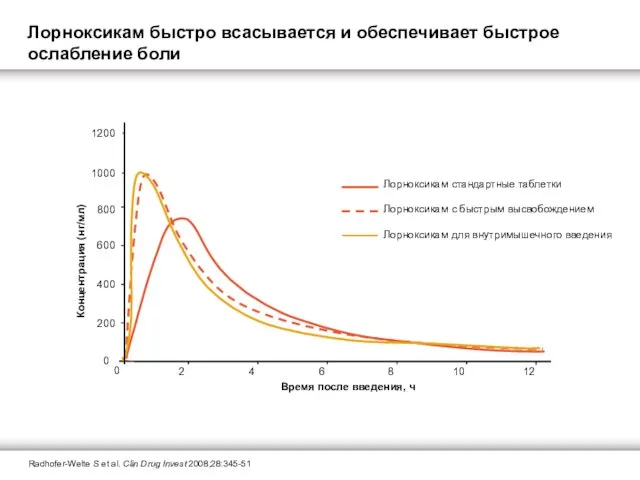
Лорноксикам быстро всасывается и обеспечивает быстрое ослабление боли
Radhofer-Welte S et al.
Лорноксикам быстро всасывается и обеспечивает быстрое ослабление боли
Radhofer-Welte S et al.
Radhofer-Welte S et al. Clin Drug Invest 2008;28:345-51
Лорноксикам для в/м введения
Radhofer-Welte S et al. Clin Drug Invest 2008;28:345-51
Лорноксикам для в/м введения
Лорноксикам быстро всасывается и обеспечивает быстрое ослабление боли
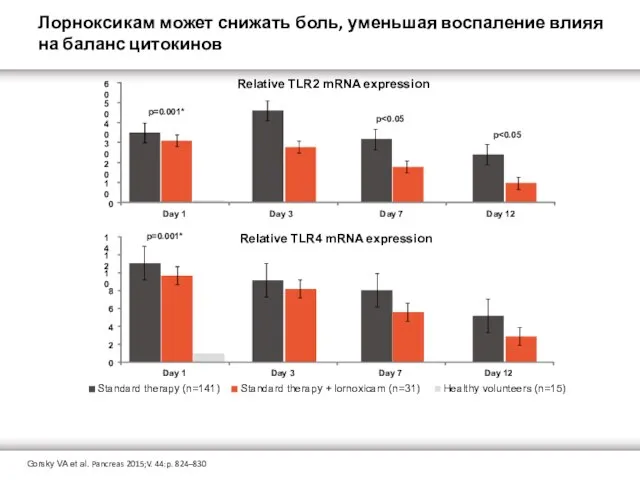
Relative TLR2 mRNA expression
Relative TLR4 mRNA expression
Gorsky VA et al. Pancreas
Relative TLR2 mRNA expression
Relative TLR4 mRNA expression
Gorsky VA et al. Pancreas
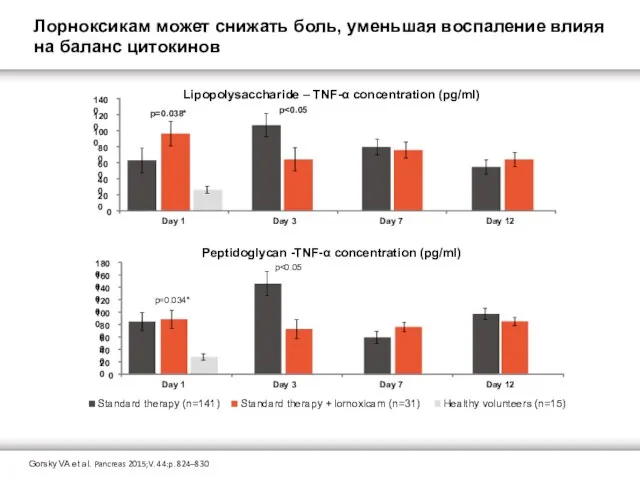
Лорноксикам может снижать боль, уменьшая воспаление влияя на баланс цитокинов
Lipopolysaccharide – TNF-α concentration (pg/ml)
Peptidoglycan -TNF-α concentration (pg/ml)
Gorsky VA et
Lipopolysaccharide – TNF-α concentration (pg/ml)
Peptidoglycan -TNF-α concentration (pg/ml)
Gorsky VA et
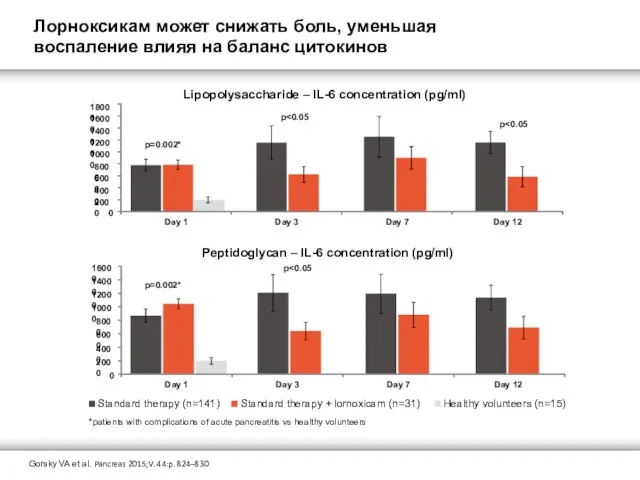
Лорноксикам может снижать боль, уменьшая воспаление влияя на баланс цитокинов
Lipopolysaccharide – IL-6 concentration (pg/ml)
Peptidoglycan – IL-6 concentration (pg/ml)
Лорноксикам может
Lipopolysaccharide – IL-6 concentration (pg/ml)
Peptidoglycan – IL-6 concentration (pg/ml)
Лорноксикам может
*patients with complications of acute pancreatitis vs healthy volunteers
Gorsky VA et al. Pancreas 2015;V. 44:p. 824–830
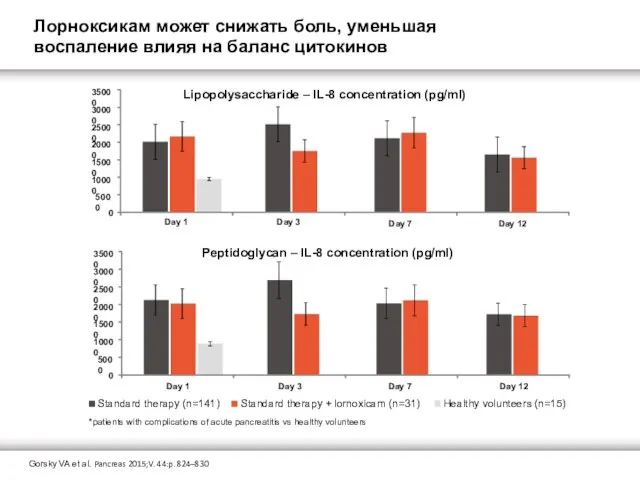
Lipopolysaccharide – IL-8 concentration (pg/ml)
Peptidoglycan – IL-8 concentration (pg/ml)
*patients with
Lipopolysaccharide – IL-8 concentration (pg/ml)
Peptidoglycan – IL-8 concentration (pg/ml)
*patients with
Gorsky VA et al. Pancreas 2015;V. 44:p. 824–830
Лорноксикам может снижать боль, уменьшая воспаление влияя на баланс цитокинов
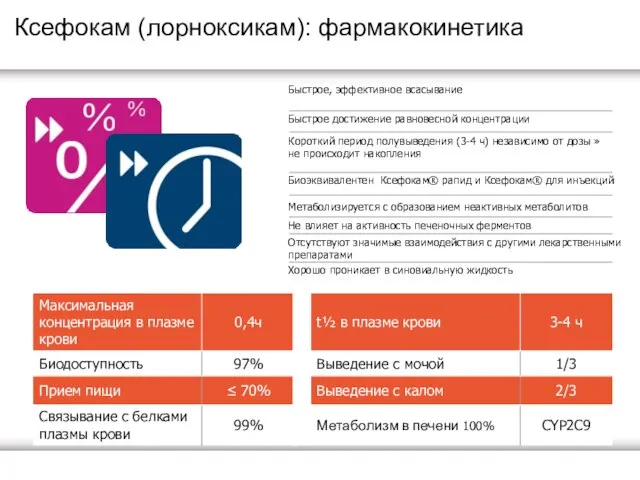
Ксефокам (лорноксикам): фармакокинетика
Метаболизм:
Метаболизируется в печени
(5-гидроксилорноксикам)
Цитохром P450 CYP2C9
Более короткий период полувыведения
Ксефокам (лорноксикам): фармакокинетика
Метаболизм:
Метаболизируется в печени
(5-гидроксилорноксикам)
Цитохром P450 CYP2C9
Более короткий период полувыведения
Не накапливается при многократном приеме
Благодаря короткому периоду
Полувыведения не происходит
накопления Ксефокама в плазме
Ниже риск развития побочных эффектов
Ксефокам (лорноксикам): фармакокинетика
Быстрое, эффективное всасывание
Быстрое достижение равновесной концентрации
Короткий период полувыведения (3-4
Ксефокам (лорноксикам): фармакокинетика
Быстрое, эффективное всасывание
Быстрое достижение равновесной концентрации
Короткий период полувыведения (3-4
Биоэквивалентен Ксефокам® рапид и Ксефокам® для инъекций
Метаболизируется с образованием неактивных метаболитов
Не влияет на активность печеночных ферментов
Отсутствуют значимые взаимодействия с другими лекарственными препаратами
Хорошо проникает в синовиальную жидкость
Ксефокам (лорноксикам): безопасность
Ксефокам (лорноксикам): безопасность
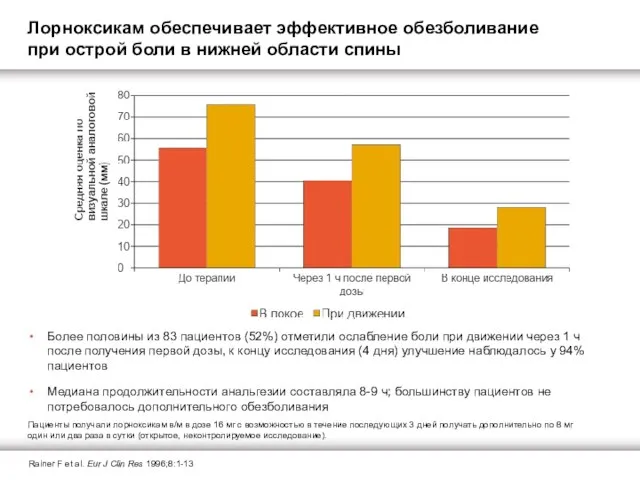
Более половины из 83 пациентов (52%) отметили ослабление боли при движении
Более половины из 83 пациентов (52%) отметили ослабление боли при движении
Медиана продолжительности анальгезии составляла 8-9 ч; большинству пациентов не потребовалось дополнительного обезболивания
Лорноксикам обеспечивает эффективное обезболивание при острой боли в нижней области спины
Rainer F et al. Eur J Clin Res 1996;8:1-13
Пациенты получали лорноксикам в/м в дозе 16 мг с возможностью в течение последующих 3 дней получать дополнительно по 8 мг один или два раза в сутки (открытое, неконтролируемое исследование).
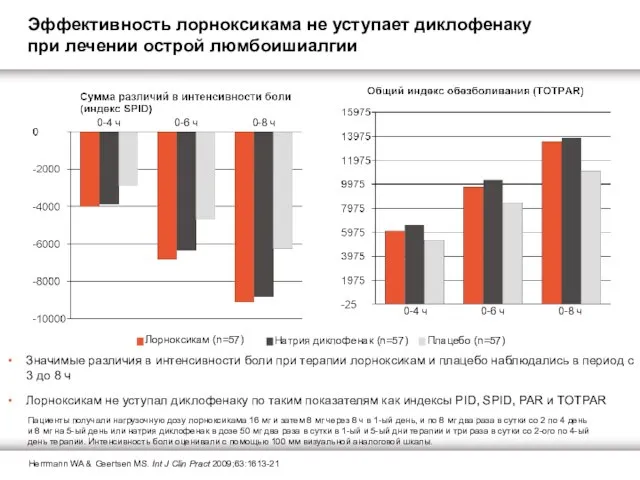
Herrmann WA & Geertsen MS. Int J Clin Pract 2009;63:1613-21
Значимые различия
Herrmann WA & Geertsen MS. Int J Clin Pract 2009;63:1613-21
Значимые различия
Лорноксикам не уступал диклофенаку по таким показателям как индексы PID, SPID, PAR и TOTPAR
Пациенты получали нагрузочную дозу лорноксикама 16 мг и затем 8 мг через 8 ч в 1-ый день, и по 8 мг два раза в сутки со 2 по 4 день и 8 мг на 5-ый день или натрия диклофенак в дозе 50 мг два раза в сутки в 1-ый и 5-ый дни терапии и три раза в сутки со 2-ого по 4-ый день терапии. Интенсивность боли оценивали с помощью 100 мм визуальной аналоговой шкалы.
0-4 ч
0-6 ч
0-8 ч
0-4 ч
0-6 ч
0-8 ч
Лорноксикам (n=57)
Натрия диклофенак (n=57)
Плацебо (n=57)
Эффективность лорноксикама не уступает диклофенаку при лечении острой люмбоишиалгии
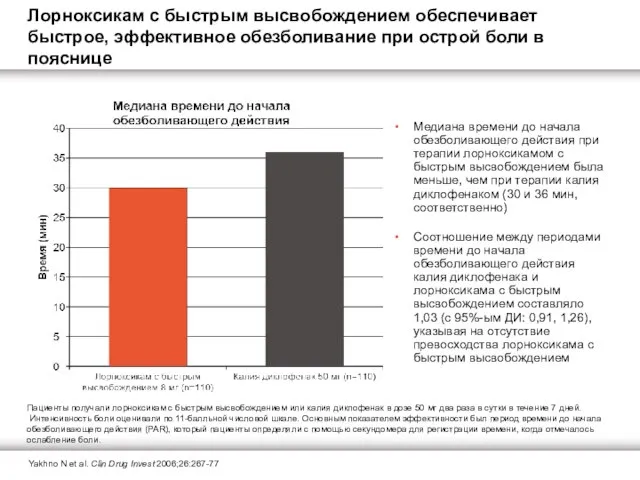
Медиана времени до начала обезболивающего действия при терапии лорноксикамом с быстрым
Медиана времени до начала обезболивающего действия при терапии лорноксикамом с быстрым
Соотношение между периодами времени до начала обезболивающего действия калия диклофенака и лорноксикама с быстрым высвобождением составляло 1,03 (с 95%-ым ДИ: 0,91, 1,26), указывая на отсутствие превосходства лорноксикама с быстрым высвобождением
Лорноксикам с быстрым высвобождением обеспечивает быстрое, эффективное обезболивание при острой боли в пояснице
Yakhno N et al. Clin Drug Invest 2006;26:267-77
Пациенты получали лорноксикам с быстрым высвобождением или калия диклофенак в дозе 50 мг два раза в сутки в течение 7 дней. Интенсивность боли оценивали по 11-балльной числовой шкале. Основным показателем эффективности был период времени до начала обезболивающего действия (PAR), который пациенты определяли с помощью секундомера для регистрации времени, когда отмечалось ослабление боли.
При терапии лорноксикамом с быстрым высвобождением различия в оценках интенсивности боли
При терапии лорноксикамом с быстрым высвобождением различия в оценках интенсивности боли
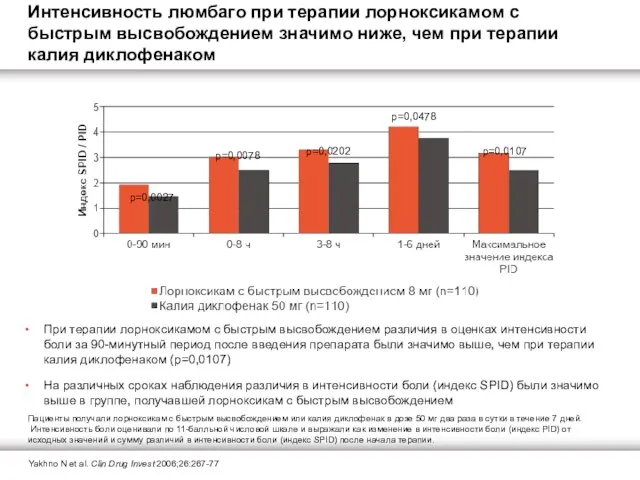
На различных сроках наблюдения различия в интенсивности боли (индекс SPID) были значимо выше в группе, получавшей лорноксикам с быстрым высвобождением
p=0,0027
p=0,0078
p=0,0202
p=0,0478
p=0,0107
Интенсивность люмбаго при терапии лорноксикамом с быстрым высвобождением значимо ниже, чем при терапии калия диклофенаком
Yakhno N et al. Clin Drug Invest 2006;26:267-77
Пациенты получали лорноксикам с быстрым высвобождением или калия диклофенак в дозе 50 мг два раза в сутки в течение 7 дней. Интенсивность боли оценивали по 11-балльной числовой шкале и выражали как изменение в интенсивности боли (индекс PID) от исходных значений и сумму различий в интенсивности боли (индекс SPID) после начала терапии.
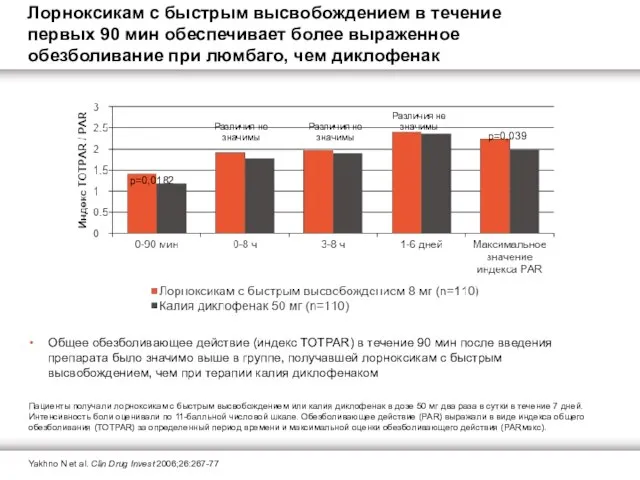
Общее обезболивающее действие (индекс TOTPAR) в течение 90 мин после введения
Общее обезболивающее действие (индекс TOTPAR) в течение 90 мин после введения
p=0,0182
Различия не значимы
Различия не значимы
Различия не значимы
p=0,039
Лорноксикам с быстрым высвобождением в течение первых 90 мин обеспечивает более выраженное обезболивание при люмбаго, чем диклофенак
Yakhno N et al. Clin Drug Invest 2006;26:267-77
Пациенты получали лорноксикам с быстрым высвобождением или калия диклофенак в дозе 50 мг два раза в сутки в течение 7 дней. Интенсивность боли оценивали по 11-балльной числовой шкале. Обезболивающее действие (PAR) выражали в виде индекса общего обезболивания (TOTPAR) за определенный период времени и максимальной оценки обезболивающего действия (PARмакс).
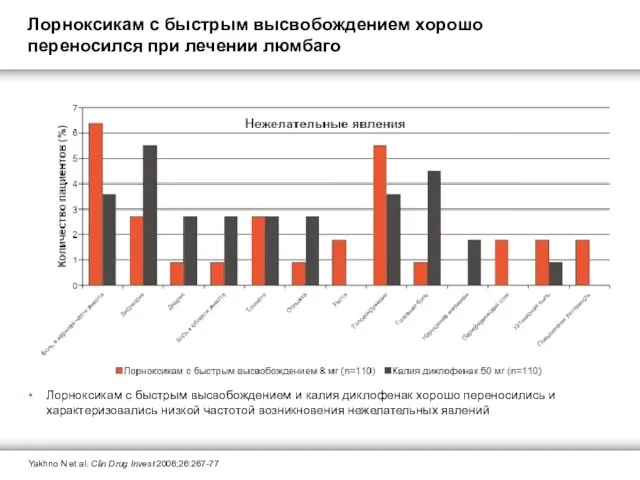
Лорноксикам с быстрым высвобождением хорошо переносился при лечении люмбаго
Лорноксикам с быстрым
Лорноксикам с быстрым высвобождением хорошо переносился при лечении люмбаго
Лорноксикам с быстрым
Yakhno N et al. Clin Drug Invest 2006;26:267-77
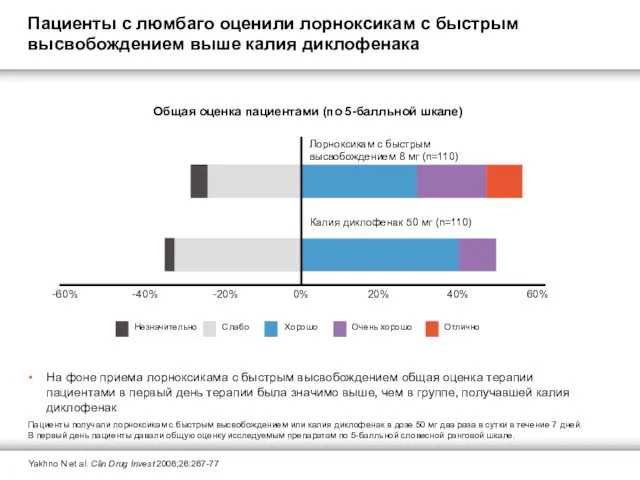
Общая оценка пациентами (по 5-балльной шкале)
Лорноксикам с быстрым высвобождением 8
Общая оценка пациентами (по 5-балльной шкале)
Лорноксикам с быстрым высвобождением 8
Калия диклофенак 50 мг (n=110)
-60%
-20%
0%
40%
60%
Незначительно
Слабо
Хорошо
Очень хорошо
Отлично
-40%
20%
На фоне приема лорноксикама с быстрым высвобождением общая оценка терапии пациентами в первый день терапии была значимо выше, чем в группе, получавшей калия диклофенак
Пациенты с люмбаго оценили лорноксикам с быстрым высвобождением выше калия диклофенака
Yakhno N et al. Clin Drug Invest 2006;26:267-77
Пациенты получали лорноксикам с быстрым высвобождением или калия диклофенак в дозе 50 мг два раза в сутки в течение 7 дней.
В первый день пациенты давали общую оценку исследуемым препаратам по 5-балльной словесной ранговой шкале.
Схема назначения Лорноксикама при боли в спине
Схема назначения Лорноксикама при боли в спине
Цитируемые источники
Aabakken L, Osnes M, Frenzel W. Gastrointestinal tolerability of lornoxicam
Цитируемые источники
Aabakken L, Osnes M, Frenzel W. Gastrointestinal tolerability of lornoxicam
Akcali GE, Iskender A, Demiraran Y, Kayikci A, Yalcin GS, Cam K, Balcioglu YO. Randomized comparison of efficacy of paracetamol, lornoxicam, and tramadol representing three different groups of analgesics for pain control in extracorporeal shockwave lithotripsy. J Endourol 2010;24:615-20.
Amin S, Yosry M, El DI. The effect of the addition of lornoxicam (xefocam) intrarticularly on the WOMAC Scale in patients undergoing arthroscopic anterior cruciate ligament reconstruction. Middle East J Anesthesiol 2011;21:15-21.
Ankier SI, Brimelow AE, Crome P, Johnston A, Warrington SJ, Turner P, Ferber HP. Chlortenoxicam pharmacokinetics in young and elderly human volunteers. Postgrad Med J 1988;64:752-4.
Antman EM, Bennett JS, Daugherty A, Furberg C, Roberts H, Taubert KA; American Heart Association. Use of nonsteroidal antiinflammatory drugs: an update for clinicians: a scientific statement from the American Heart Association. Circulation 2007;115:1634-42.
Arslan M, Ciçek R, Celep B, Yılmaz H, Ustün Kalender H. Comparison of the analgesic effects of intravenous paracetamol and lornoxicam in postoperative pain following thyroidectomies. Agri 2011;23:160-6.
Berg J, Fellier H, Christoph T, Grarup J, Stimmeder D. The analgesic NSAID lornoxicam inhibits cyclooxygenase (COX)-1/-2, inducible nitric oxide synthase (iNOS), and the formation of interleukin (IL)-6 in vitro. Inflamm Res 1999;48:369-79.
Bernstein RM, Frenzel W. A comparative study of 2 dosage regimens of Lornoxicam and a standard dosage of naproxen in patients with rheumatoid arthritis. Eur J Clin Res 1995;7:259-73.
Berry H, Bird HA, Black C, Blake DR, Freeman AM, Golding DN, Hamilton EB, Jayson MI, Kidd B, Kohn H, et al. A double blind, multicentre, placebo controlled trial of lornoxicam in patients with osteoarthritis of the hip and knee. Ann Rheum Dis 1992;51:238-42.
Bilir A, Gulec S, Turgut M, Cetinkaya D, Erkan A, Kurt I. Lornoxicam in extracorporeal shock-wave lithotripsy; comparison with tenoxicam and placebo in terms of analgesic consumption. Scand J Urol Nephrol 2008;42:143-7.
Bölükbasi N, Ersanli S, Basegmez C, Ozdemir T, Ozyalcin S. Efficacy of quick-release lornoxicam versus placebo for acute pain management after dental implant surgery: a randomised placebo-controlled triple-blind trial. Eur J Oral Implantol 2012;5:165-73.
Caruso I, Montrone F, Boari L, Davoli C, Beyene NB, Caporali R, et al. Lornoxicam versus diclofenac in rheumatoid arthritis: a double-blind, multicenter study. Adv Ther 1994;11:132-8.
Cevik E, Cinar O, Salman N, Bayir A, Arziman I, Ardic S, Youngquist ST. Comparing the efficacy of intravenous tenoxicam, lornoxicam, and dexketoprofen trometamol for the treatment of renal colic. Am J Emerg Med 2012;30:1486-90.
Conaghan PG. A turbulent decade for NSAIDs: update on current concepts of classification, epidemiology, comparative efficacy, and toxicity. Rheumatol Int 2012;32:1491-502.
Erdoğan I, Cakan T, Ozcan A, Türkyilmaz E, Baltaci B, Dikmen B. Effect of lornoxicam on postoperative analgesia after myomectomy. Agri 2008;20:26-31.
Herrmann WA, Geertsen MS. Efficacy and safety of lornoxicam compared with placebo and diclofenac in acute sciatica/lumbo-sciatica: an analysis from a randomised, double-blind, multicentre, parallel-group study. Int J Clin Pract 2009;63:1613-21.
Hitzenberger G, Radhofer-Welte S, Takacs F, Rosenow D. Pharmacokinetics of lornoxicam in man. Postgrad Med J 1990;66 Suppl 4:S22-7.
Ilias W, Jansen M. Pain control after hysterectomy: an observer-blind, randomised trial of lornoxicam versus tramadol. Br J Clin Pract 1996;50:197-202.
Işik B, Arslan M, Ozsoylar O, Akçabay M. Effects of preoperative lornoxicam versus tramadol on postoperative pain and adverse effects in adult tonsillectomy patients. Agri 2009;21:113-20.
Karaman S, Gunusen I, Uyar M, Firat V. The effect of pre-operative lornoxicam and ketoprofen application on the morphine consumption of post-operative patient-controlled analgesia. J Int Med Res 2006;34:168-75.
Kidd B, Frenzel W. A multicenter, randomized, double blind study comparing lornoxicam with diclofenac in osteoarthritis. J Rheumatol 1996;23:1605-11.
Цитируемые источники
Kocaayan E, Ozkardeşler S, Ozzeybek D, Bayindir S, Akan M.
Цитируемые источники
Kocaayan E, Ozkardeşler S, Ozzeybek D, Bayindir S, Akan M.
Lanzetta A, Bocchi L, Cherie-Ligniere EL, Letizia G, Melanotte P, Rettagliata F et al. Multicentre clinical double blind study comparing analgesic effect of Lornoxicam and diclofenac in arthrosis. Minverva Ortopedica e Traumatologica 2002;53:165-71.
Lustenberger FD, Grätz KW, Mutzbauer TS. Efficacy of ibuprofen versus lornoxicam after third molar surgery: a randomized, double-blind, crossover pilot study. Oral Maxillofac Surg 2011;15:57-62.
Memedov C, Menteş O, Şimşek A, Keçe C, Yağci G, Harlak A, Coşar A, Tufan T. Comparison of analgesic effects of intraperitoneal lornoxicam and ropivacaine administration in laparoscopic cholecystectomy. Trakya Univ Tip Fak Derg 2010;27:142-149.
Mentes O, Bagci M. Postoperative pain management after inguinal hernia repair: lornoxicam versus tramadol. Hernia 2009;13:427-30.
Møller PL, Nørholt SE. Analgesic efficacy of quick-release versus standard lornoxicam for pain after third molar surgery: a randomized, double-blind, placebo-controlled, single-dose trial. Clin Drug Investig 2008;28:757-66
Mowafi HA, Elmakarim EA, Ismail S, Al-Mahdy M, El-Saflan AE, Elsaid AS. Intravenous lornoxicam is more effective than paracetamol as a supplemental analgesic after lower abdominal surgery: a randomized controlled trial. World J Surg 2012;36:2039-44.
Mowafi HA, Telmessani L, Ismail SA, Naguib MB. Preoperative lornoxicam for pain prevention after tonsillectomy in adults. J Clin Anesth 2011;23:97-101.
Muslu B, Usta B, Muslu S, Yeşilay A, Gözdemir M, Sert H, Demircioglu R. Effect of locally administered lornoxicam in the management of low back pain after lumbar epidural anesthesia: a double-blind, randomized, controlled study. Minerva Anestesiol 2009;75:494-7.
Nørholt SE, Sindet-Pedersen S, Bugge C, Branebjerg PE, Ersbøll BK, Bastian HL. A randomized, double-blind, placebo-controlled, dose-response study of the analgesic effect of lornoxicam after surgical removal of mandibular third molars. J Clin Pharmacol 1995;35:606-14.
Nørholt SE, Sindet-Pedersen S, Larsen U, Bang U, Ingerslev J, Nielsen O, Hansen HJ, Ersbøll AK. Pain control after dental surgery: a double-blind, randomised trial of lornoxicam versus morphine. Pain 1996;67:335-43.
Ozkan F, Erdemir F, Erkorkmaz U, Kaya Z, Senayli Y, Parlaktas BS. Comparison of three different analgesic protocols during shockwave lithotripsy. J Endourol 2012;26:691-6.
Papadima A, Lagoudianakis EE, Antonakis PT, Pattas M, Kremastinou F, Katergiannakis V, Manouras A, Georgiou L. Parecoxib vs. lornoxicam in the treatment of postoperative pain after laparoscopic cholecystectomy: a prospective randomized placebo-controlled trial. Eur J Anaesthesiol 2007;24:154-8.
Patel A, Skelly AM, Kohn H, Preiskel HW. Double-blind placebo-controlled comparison of the analgesic effects of single doses of lornoxicam and aspirin in patients with postoperative dental pain. Br Dent J 1991;170:295-9.
Pleiner J, Nell G, Branebjerg PE, Simin Geersten M, Ilias W. Safety of lornoxicam: an interim meta-analysis of comparative clinical trials. Eur J Pain 2009;13:S55-285 [abstract 659] .
Prasanna N, Subbarao CV, Gutmann JL. The efficacy of pre-operative oral medication of lornoxicam and diclofenac potassium on the success of inferior alveolar nerve block in patients with irreversible pulpitis: a double-blind, randomised controlled clinical trial. Int Endod J 2011;44:330-6.
Pruss TP, Stroissnig H, Radhofer-Welte S, Wendtlandt W, Mehdi N, Takacs F, Fellier H. Overview of the pharmacological properties, pharmacokinetics and animal safety assessment of lornoxicam. Postgrad Med J 1990;66 Suppl 4:S18-21.
Radhofer-Welte S, Dittrich P, Simin M, Branebjerg PE. Comparative bioavailability of lornoxicam as single doses of quick-release tablet, standard tablet and intramuscular injection: a randomized, open-label, crossover phase I study in healthy volunteers. Clin Drug Investig 2008;28:345-51.
Rainer F, Klein G, Mayrhofer F, Singer F, Uray H, Kursten FW. A prospective, multicentre, open-label, uncontrolled phase II study of the local tolerability, safety and efficacy of intramuscular chlortenoxicam in patients with acute low back pain. Eur J Clin Res 1996; 8:1-13.









 История развития психопатологии в России и зарубежных странах
История развития психопатологии в России и зарубежных странах Подросток и наркотики
Подросток и наркотики План саморазвития
План саморазвития Иммунология. Антитела и В-лимфоциты. (Лекция 4)
Иммунология. Антитела и В-лимфоциты. (Лекция 4) Внебольничные роды: неотложные мероприятия на догоспитальном этапе
Внебольничные роды: неотложные мероприятия на догоспитальном этапе Обструктивные заболевания легких. Бронхиальная астма и ХОБЛ в практике участкового врача-терапевта
Обструктивные заболевания легких. Бронхиальная астма и ХОБЛ в практике участкового врача-терапевта Этиология и патогенез туберкулеза
Этиология и патогенез туберкулеза Я выбираю жизнь. Наркотики ломают жизнь людей
Я выбираю жизнь. Наркотики ломают жизнь людей Псориатическая артропатия
Псориатическая артропатия Отбасын жоспарлау
Отбасын жоспарлау Нормальная анатомия пахового канала
Нормальная анатомия пахового канала Депрессия
Депрессия Сравнительная характеристика субъективной оценки детско-родительских отношений детьми с задержкой психического развития
Сравнительная характеристика субъективной оценки детско-родительских отношений детьми с задержкой психического развития Творческий путь и наследие академика рамн Л.А. Дурнова
Творческий путь и наследие академика рамн Л.А. Дурнова Микробиом и вес
Микробиом и вес Остеопатическая помощь
Остеопатическая помощь Тест. Анемии
Тест. Анемии Клиническая классификация туберкулеза. Патогенез первичного туберкулеза. Туберкулезная интоксикация
Клиническая классификация туберкулеза. Патогенез первичного туберкулеза. Туберкулезная интоксикация Психология наших покупок
Психология наших покупок Диагностика беременности
Диагностика беременности Болезнь отложения кристаллов пирофосфата кальция
Болезнь отложения кристаллов пирофосфата кальция Первичная гипертензия
Первичная гипертензия В медицинском кабинете
В медицинском кабинете Проблемы диагностики и коррекции отклонений в развитии в условиях школьного обучения
Проблемы диагностики и коррекции отклонений в развитии в условиях школьного обучения Готовность к школьному обучению
Готовность к школьному обучению Основные способы классификации ядов и отравлений
Основные способы классификации ядов и отравлений Значение правильной осанки в жизнедеятельности человека
Значение правильной осанки в жизнедеятельности человека Особенности влияния различных заболеваний на эмоциональную сферу взрослых и детей
Особенности влияния различных заболеваний на эмоциональную сферу взрослых и детей