Виды металлургических производств
1. Пирометаллургия — восстановление металлов из руд при высоких
температурах с помощью углерода, оксида углерода (II), водорода, металлов — алюминия, магния. Например: Cu2O + CO → 2Cu + CO2
Отраслью пирометаллургии является металлотермия - восстановление металлов из оксидов более активными металлами. Например: 2Al+Cr2O3→2Cr+Al2O3
Сплав железа с углеродом, в котором массовая доля углерода составляет от 2 до 4%, называют чугуном, а если от 0,2 до 2%, называют сталью.
Например, железо восстанавливают из руд коксом в специальных печах, называемых доменными печами или домнами.








 Классификация методов утилизации твердых отходов
Классификация методов утилизации твердых отходов презентация сокращенная
презентация сокращенная Холодильное оборудование. Тепловой расчет холодильной машины
Холодильное оборудование. Тепловой расчет холодильной машины Задание 2. Петрография
Задание 2. Петрография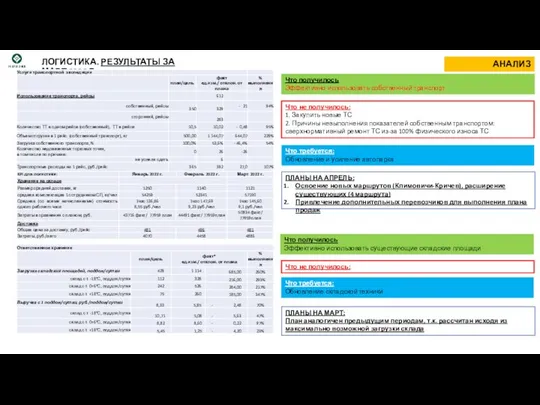 Логистика. Результаты за март 2022 г
Логистика. Результаты за март 2022 г E_Topoleva-Soldunova_Finansirovanie_grazhdanskikh_initsiativ
E_Topoleva-Soldunova_Finansirovanie_grazhdanskikh_initsiativ Картографический метод в экономической географии
Картографический метод в экономической географии Христос - наша Праведность (Оправдание) и наше Освящение - 4
Христос - наша Праведность (Оправдание) и наше Освящение - 4 Ceramics research group
Ceramics research group Электромагнитные переходные процессы в электроэнергетических системах
Электромагнитные переходные процессы в электроэнергетических системах Первый год жизни Насти. Фотоальбом
Первый год жизни Насти. Фотоальбом Картофелеочистительные машины
Картофелеочистительные машины Отделочные материалы
Отделочные материалы Н.А. Заболоцкий: очерк жизни и творчества
Н.А. Заболоцкий: очерк жизни и творчества Опреснительные установки
Опреснительные установки Волшебный мир медиа. Коллекция фотографий
Волшебный мир медиа. Коллекция фотографий ПКРТИ 4.37
ПКРТИ 4.37 20171224_liderstvo
20171224_liderstvo школьная линейка
школьная линейка Lean. Знакомимся с Lean: как создать ценность без потерь
Lean. Знакомимся с Lean: как создать ценность без потерь Техническое обслуживание и ремонт силового электрооборудования станка радиально - сверлильного 2К522
Техническое обслуживание и ремонт силового электрооборудования станка радиально - сверлильного 2К522 Материал бетін ультрадыбыстық өңдеу
Материал бетін ультрадыбыстық өңдеу Холодильные склады
Холодильные склады rezina_1nj37
rezina_1nj37 Пасхальные традиции
Пасхальные традиции Blockchain NFT-кроссовки UniQ
Blockchain NFT-кроссовки UniQ Новий рік 2017
Новий рік 2017 Вязание узлов
Вязание узлов