Содержание
- 2. Атомная физика - это наука об электронном строении вещества. Она призвана объяснить его макроскопические свойства на
- 3. Школа древнегреческих атомистов Демокрит (ок.460-ок.370 до н.э.) Левкипп (V в. до н.э.) Идея атомизма (Ατομος –
- 4. ? Легенда о яблоке
- 5. «… остаётся признать неизбежно Существованье того, что совсем неделимо, являясь По существу наименьшим.» Тит Лукреций Кар
- 6. Закономерности в атомных спектрах. х Итак, что же такое атом? Изолированные атомы в виде разреженного газа
- 7. Линейчатые спектры испускания и поглощения света. Спектральные серии Линейчатые спектры дают все вещества в газообразном атомарном
- 8. Линейчатые спектры испускания и поглощения света. Спектральные серии Обнаружил закономерность в спектральных линиях атома водорода, показав
- 9. Линейчатые спектры испускания и поглощения света. Спектральные серии. Формула Бальмера (первоначальный вид):
- 10. Бальмер установил, что длины волн серии в видимой части спектра водорода могут быть представлены формулой (формула
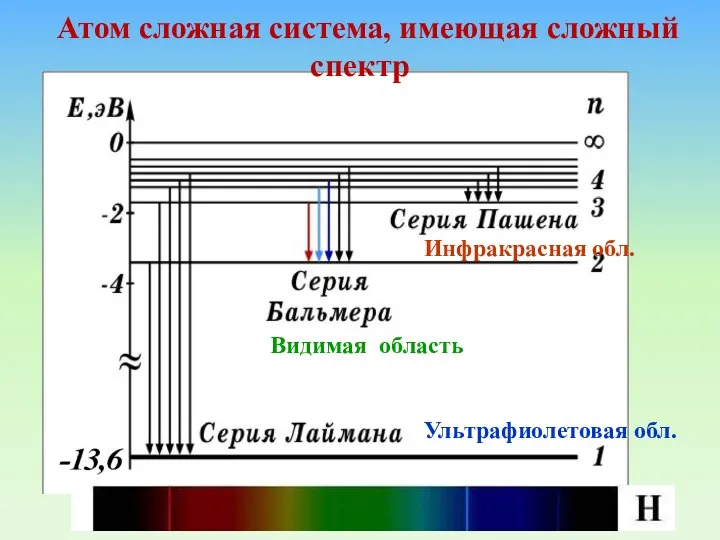
- 11. Дальнейшие исследования показали, что в спектре водорода имеется еще несколько серий:
- 12. Обобщенная формула Бальмера где k = 1, 2, 3,…, n = k + 1, k +
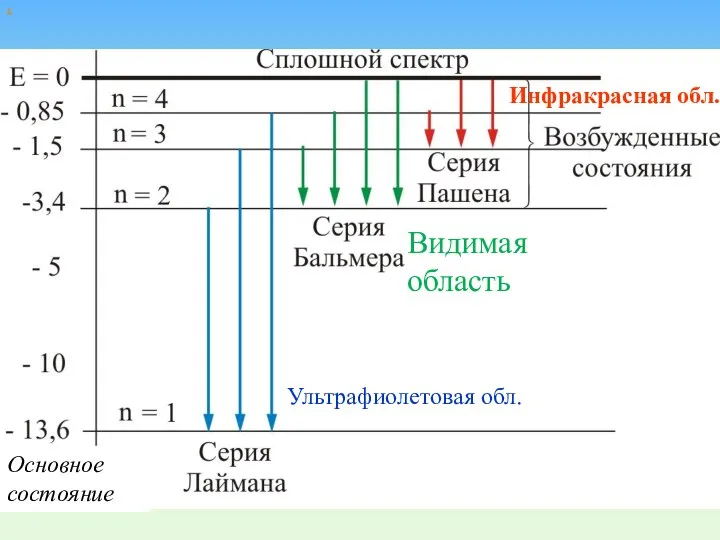
- 13. Атом сложная система, имеющая сложный спектр Видимая область Инфракрасная обл. Ультрафиолетовая обл.
- 14. Были предложены различные модели строения атома. 1 2 3
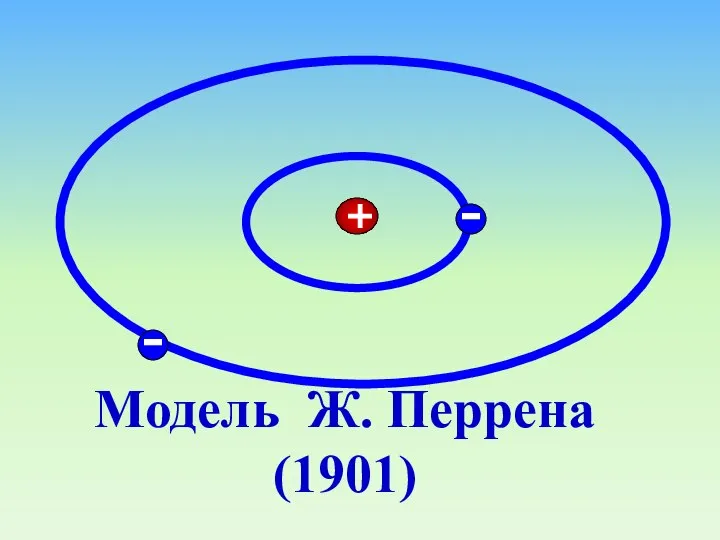
- 15. Модель Ж. Перрена (1901)
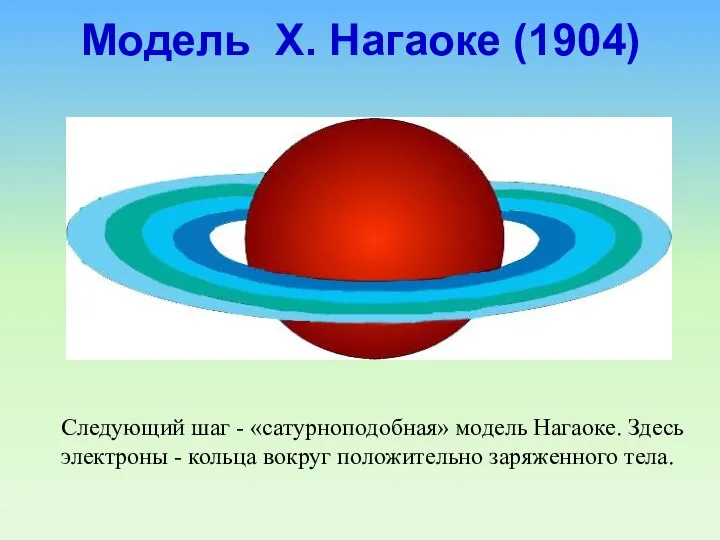
- 16. Следующий шаг - «сатурноподобная» модель Нагаоке. Здесь электроны - кольца вокруг положительно заряженного тела. Модель Х.
- 17. х В 1903 году Дж. Дж. Томсон, предложил модель атома: сфера, равномерно заполненная положительным электричеством, внутри
- 18. Джозеф-Джон Томсон (1856-1940) - английский физик, Нобелевская премия 1906 г. по физике за работы, которые привели
- 19. Какая из моделей верна?
- 20. Эрнест Резерфорд (1871 - 1937). Лауреат Нобелевской премии по химии 1908г. «За проведенные им исследования в
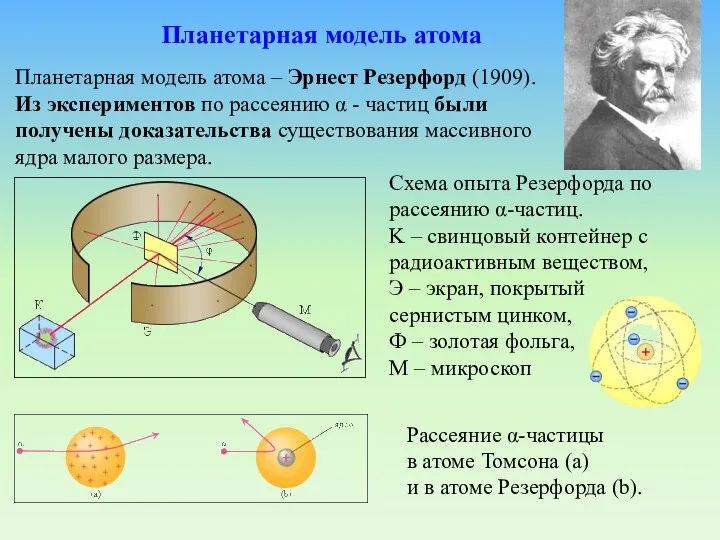
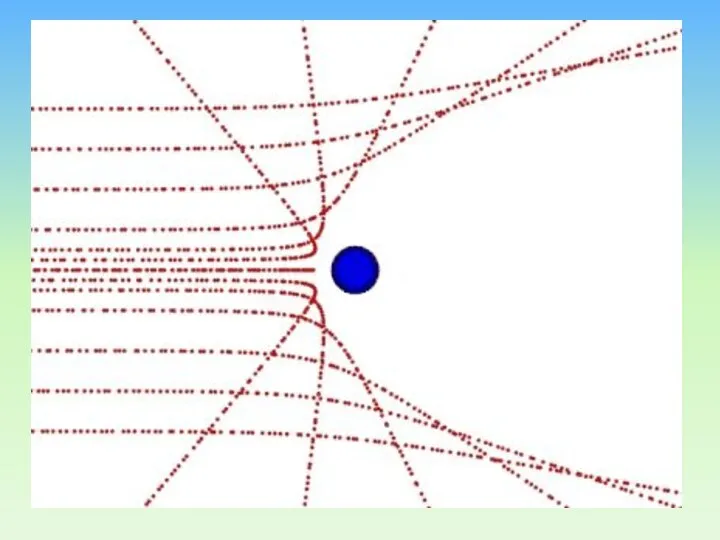
- 21. Схема опыта Резерфорда по рассеянию α-частиц. K – свинцовый контейнер с радиоактивным веществом, Э – экран,
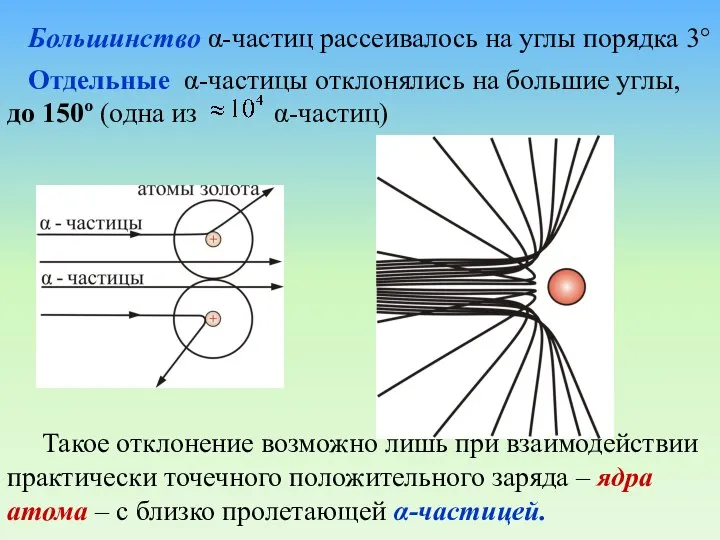
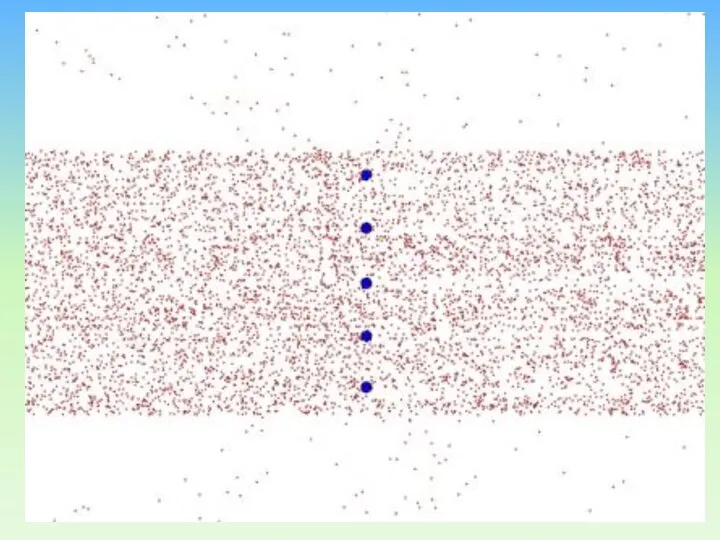
- 22. Большинство α-частиц рассеивалось на углы порядка 3° Отдельные α-частицы отклонялись на большие углы, до 150º (одна
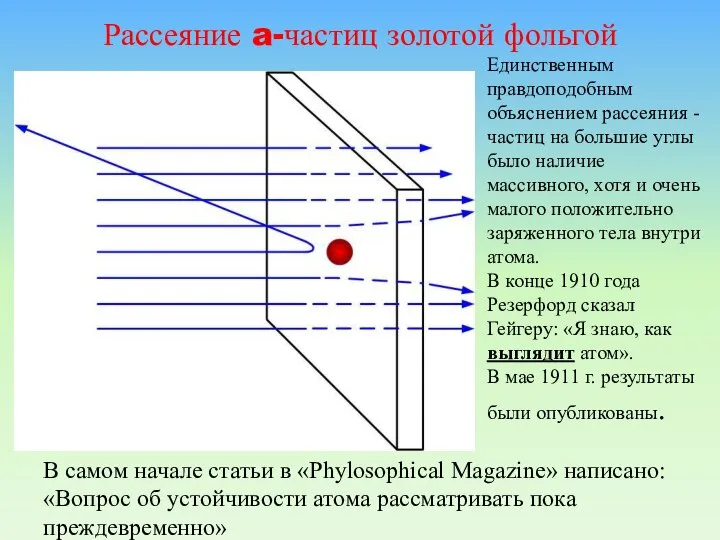
- 23. Рассеяние a-частиц золотой фольгой Единственным правдоподобным объяснением рассеяния -частиц на большие углы было наличие массивного, хотя
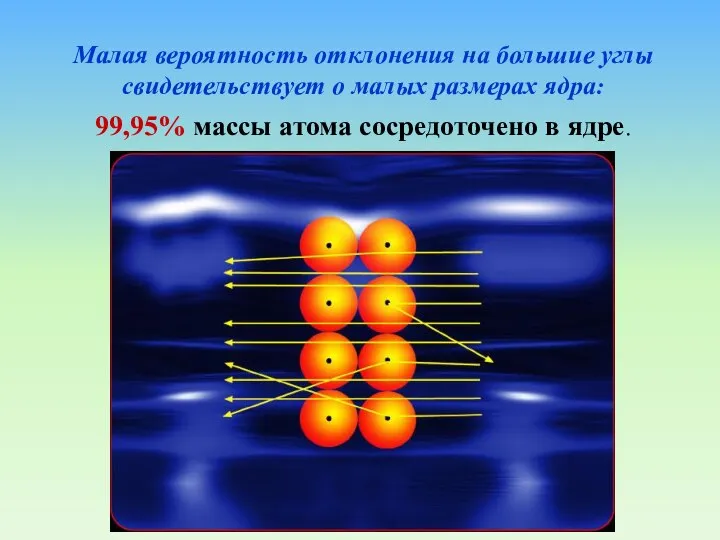
- 24. Малая вероятность отклонения на большие углы свидетельствует о малых размерах ядра: 99,95% массы атома сосредоточено в
- 27. Резерфорд потом вспоминал: "это было самым невероятным событием моей жизни. Это было почти столь же невероятно,
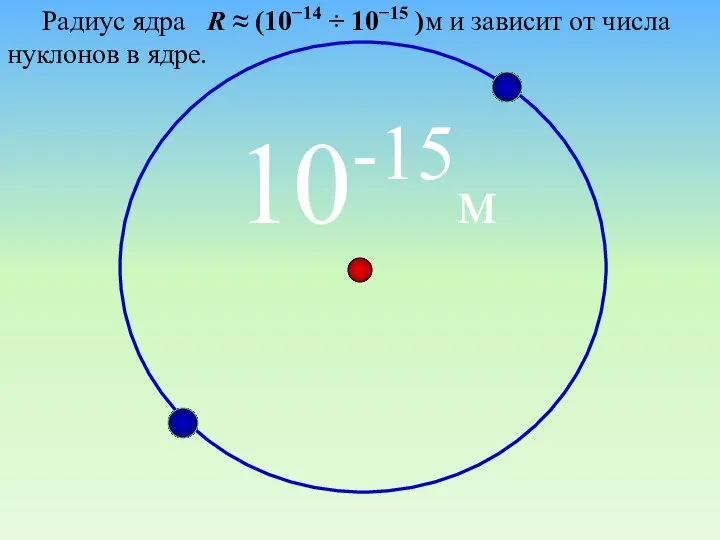
- 28. 10-15м Радиус ядра R ≈ (10−14 ÷ 10−15 )м и зависит от числа нуклонов в ядре.
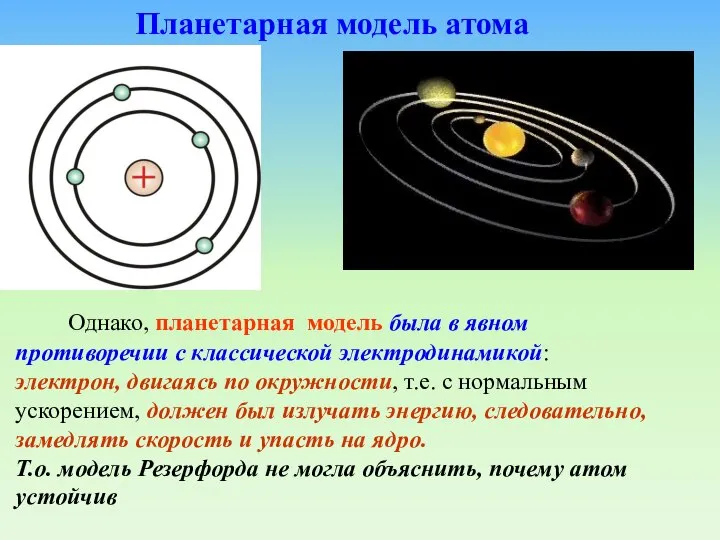
- 29. Однако, планетарная модель была в явном противоречии с классической электродинамикой: электрон, двигаясь по окружности, т.е. с
- 30. К великому сожалению Резерфорда, статья была встречена молчанием. Резерфорд, конечно понимал почему. Его атом был недолговечен.
- 31. Планетарная модель атома противоречит электродинамике Максвелла!!!
- 32. Согласно теории Максвелла, ускоренно движущийся заряд излучает электромагнитные волны.
- 33. При движении по окружности имеется центростремительное ускорение. Поэтому электрон должен терять энергию на электромагнитное излучение и
- 34. Нестабильный атом?! Падать на ядро!
- 35. Попыткой спасения планетарной модели атома стали постулаты Н. Бора
- 36. х Элементарная теория Бора. БОР Нильс Хендрик Давид (1885–1962) – выдающийся датский физик-теоретик, один из создателей
- 37. 1. Атом следует описывать как «пирамиду» стационарных энергетических состояний. Пребывая в одном из стационарных состояний, атом
- 39. 2. При переходах между стационарными состояниями атом поглощает или излучает квант энергии. При поглощении энергии атом
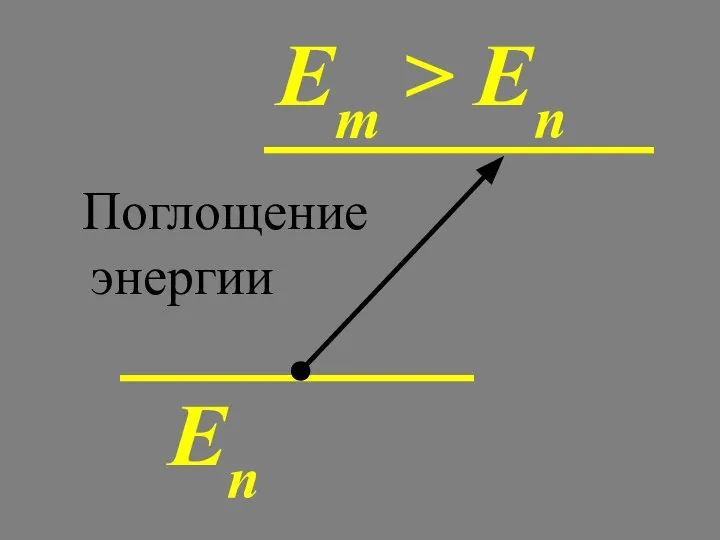
- 40. Еn Em > En Поглощение энергии
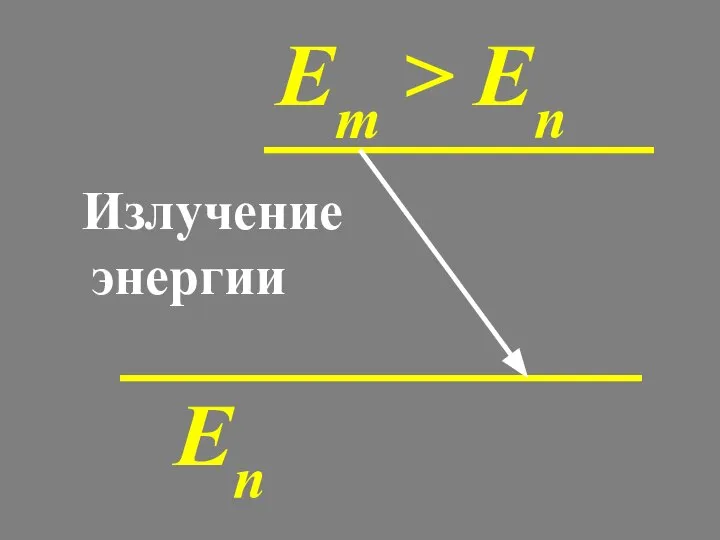
- 41. Еn Em > En Излучение энергии
- 42. Резерфорд в письме Бору сразу же указал на главную трудность новой теории. «Как электрон устанавливает частоту,
- 43. Немного цитат ☺ «Если это правильно, то это означает конец физики как науки» (А. Эйнштейн, 1913
- 44. Немного цитат ☺ «Законы квантования в своей теперешней формулировке носят до некоторой степени теологический характер, для
- 45. Теория Бора
- 46. 1. Электроны движутся только по определенным (стационарным) орбитам. При этом не происходит излучения энергии. Постулаты Бора
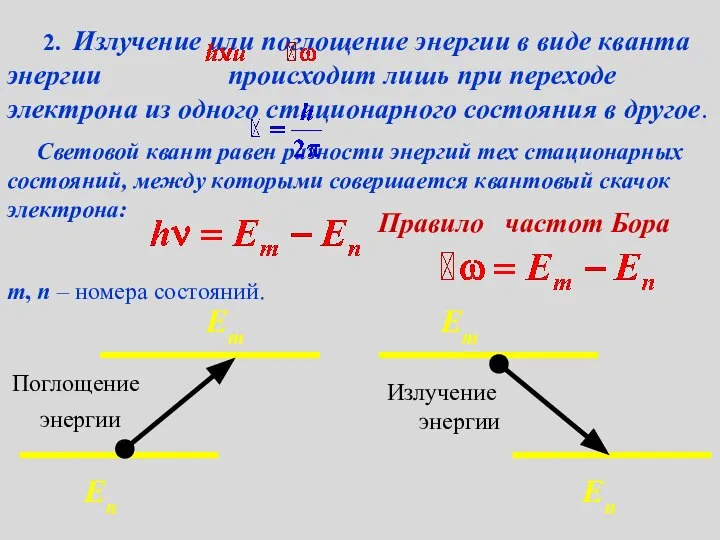
- 47. 2. Излучение или поглощение энергии в виде кванта энергии происходит лишь при переходе электрона из одного
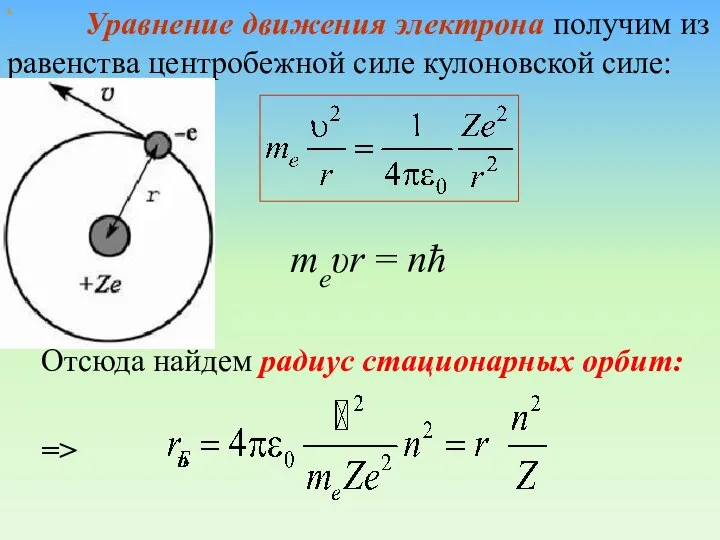
- 48. х Уравнение движения электрона получим из равенства центробежной силе кулоновской силе: => Отсюда найдем радиус стационарных
- 49. Радиус первой орбиты водородного атома называют Боровским радиусом: При n =1, Z = 1 для водорода
- 50. Внутренняя энергия атома слагается из кинетической энергии электрона и потенциальной энергией взаимодействия электрона с ядром: Видно,
- 51. В основном состоянии (n=1) полная энергия электрона в атоме минимальна и равна где Энергию произвольного состояния
- 52. х Видимая область Инфракрасная обл. Ультрафиолетовая обл. Основное состояние
- 53. При переходе электрона в атоме водорода из состояния n в состояние k излучается фотон с энергией
- 54. Лабораторная работа №4 Определение постоянной Ридберга и энергетических уровней атома водорода
- 55. Экспериментальная установка для исследования спектра атома водорода. 1 – спектральная трубка; 2 – источник высокого напряжения;
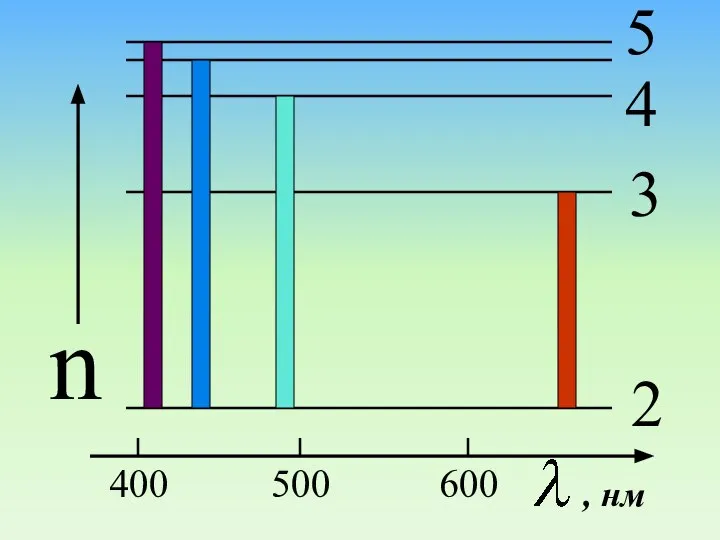
- 56. 400 500 600 n 2 3 4 5 , нм
- 57. В каких пределах должна лежать энергия бомбардирующих электронов, чтобы при возбуждении атомов водорода ударами этих электронов
- 58. Решение (продолжение). При столкновении бомбардирующий электрон не может передать энергию, большую, чем кинетическая энергия этого электрона,
- 60. Бор продемонстрировал объяснительную силу своей модели и другим способом. В конце XIX века гарвардский астроном Эдвард
- 61. Серьезным успехом теории Бора явилось: вычисление постоянной Ридберга для водородоподобных систем и объяснение структуры их линейчатых
- 62. Лабораторная работа №17 Опыт Франка и Герца
- 63. х Опыт Франка и Герца. Существование дискретных энергетических уровней атома и доказательство правильности теории Бора подтверждается
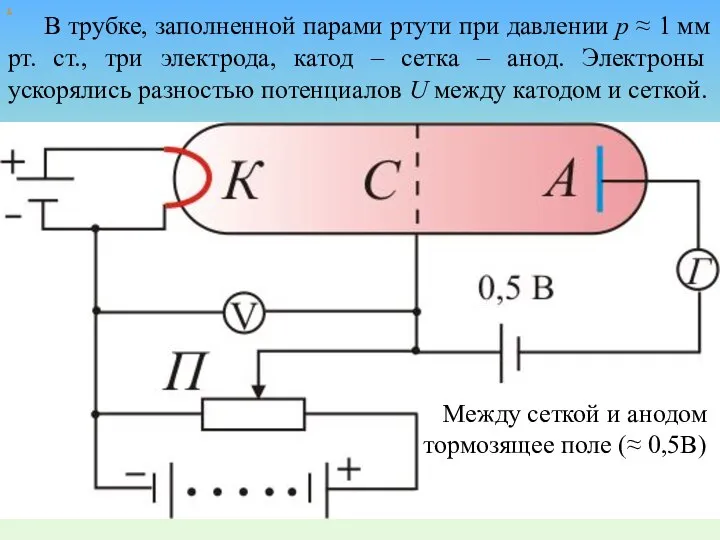
- 64. В трубке, заполненной парами ртути при давлении р ≈ 1 мм рт. ст., три электрода, катод
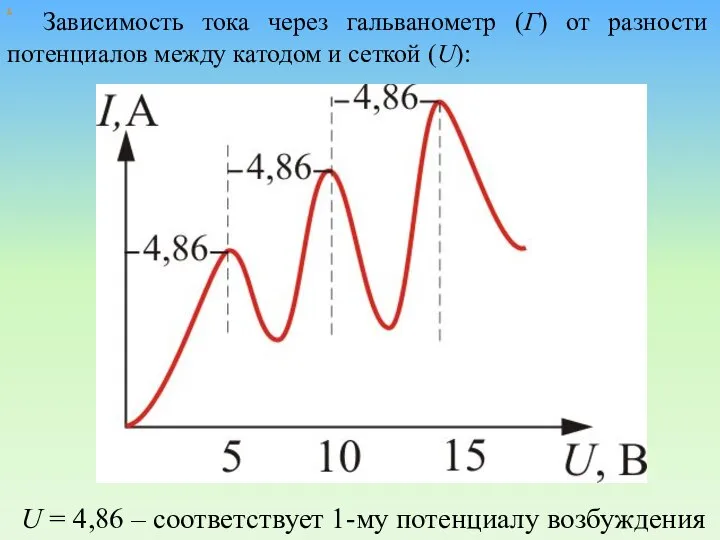
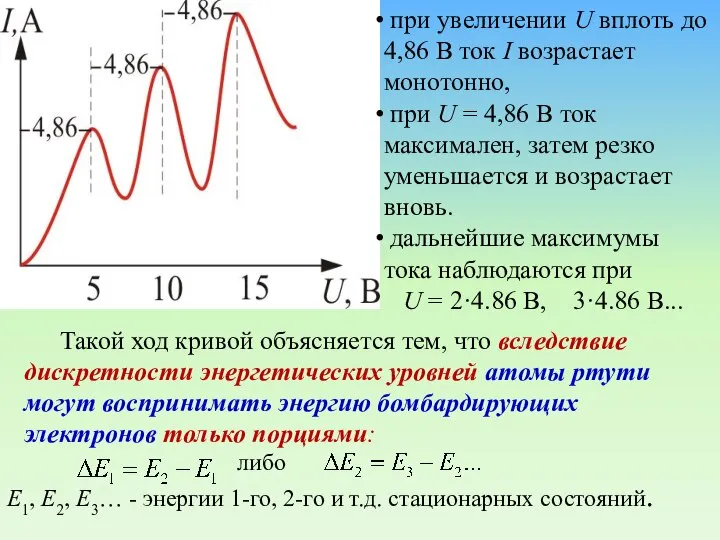
- 65. х Зависимость тока через гальванометр (Г) от разности потенциалов между катодом и сеткой (U): U =
- 66. Такой ход кривой объясняется тем, что вследствие дискретности энергетических уровней атомы ртути могут воспринимать энергию бомбардирующих
- 67. При U энергия электронов меньше ΔЕ1; соударения между электронами и атомами ртути носят упругий характер. При
- 68. Атомы ртути, получившие при соударении с электронами энергию ΔЕ1 и перешедшие в возбужденное состояние, спустя время
- 69. Таким образом, опыты Франка и Герца экспериментально подтвердили не только первый, но и второй постулат Бора.
- 70. х Однако наряду с успехами в теории Бора с самого начала обнаружились существенные недостатки. Главнейшее –
- 71. х Стало ясно, что теория Бора является лишь переходным этапом на пути создания более общей и
- 72. Дальнейшее развитие квантовой механики привело к отказу от механической картины движения электрона в поле ядра.
- 73. КОРПУСКУЛЯРНО-ВОЛНОВОЙ ДУАЛИЗМ «Волна – частица»
- 74. Луи-де- Бройль
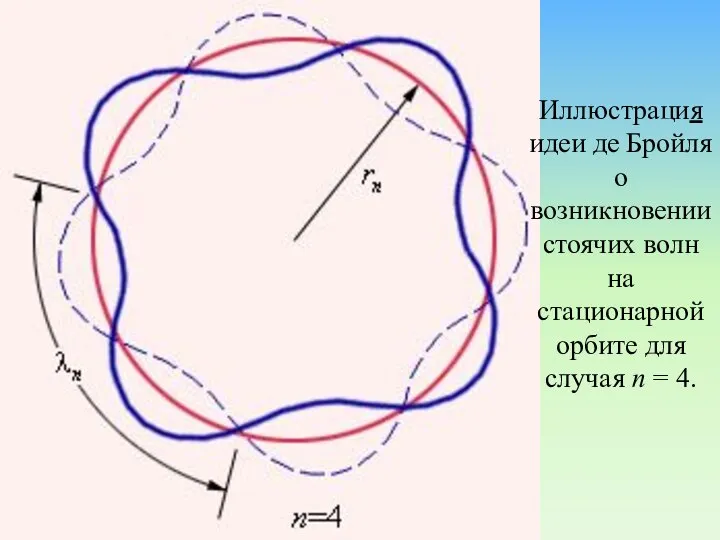
- 75. Иллюстрация идеи де Бройля о возникновении стоячих волн на стационарной орбите для случая n = 4.
- 76. Принцип дополнительности Н.Бора Всем микрообъектам присущи и волновые, и корпускулярные свойства, однако, они не являются ни
- 77. Вернер Гейзенберг Матричная механика Соотношение неопределенностей
- 78. Соотношение неопределенностей В.Гейзенберга Микрочастицы в принципе не имеют одновременно точного значения координаты и соответствующей проекции импульса.
- 79. Эрвин Шредингер Волновая механика Волновое уравнение электрона – уравнение Шредингера
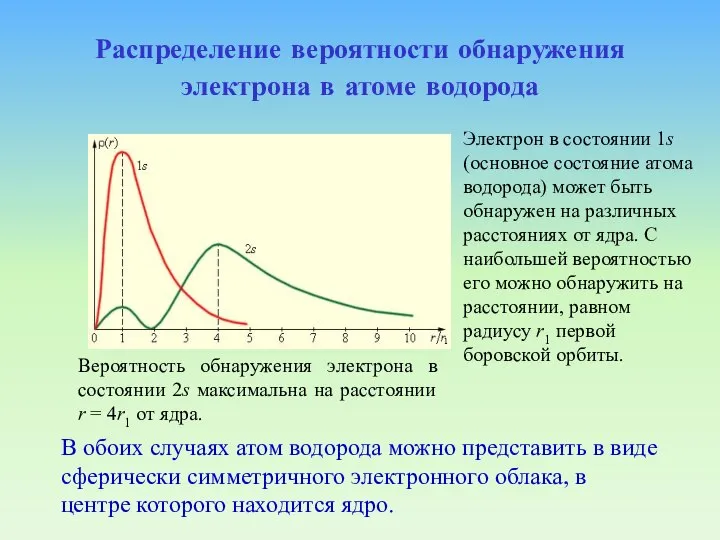
- 80. Распределение вероятности обнаружения электрона в атоме водорода В обоих случаях атом водорода можно представить в виде
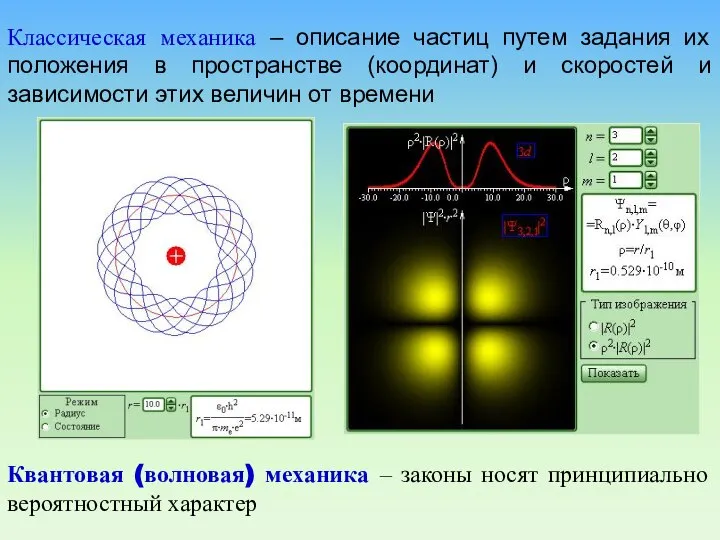
- 81. Классическая механика – описание частиц путем задания их положения в пространстве (координат) и скоростей и зависимости
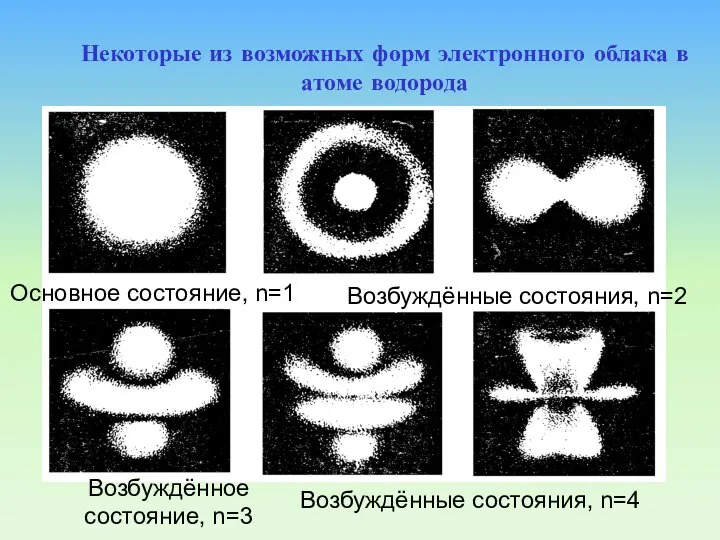
- 82. Возбуждённое состояние, n=3 Некоторые из возможных форм электронного облака в атоме водорода Основное состояние, n=1 Возбуждённые
- 83. 1874 г. - Стони, из чисел Фарадея и Авогадро, определил величину элементарного заряда e и в
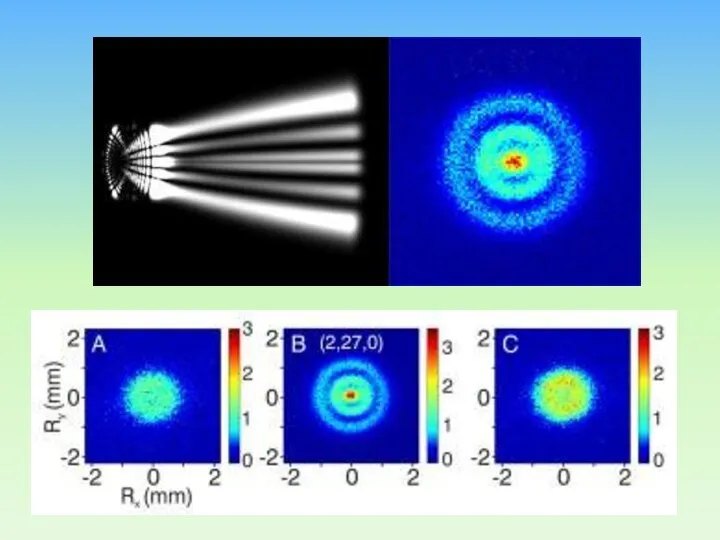
- 84. АТОМУ БОРА 100 ЛЕТ 2013 г. «Квантовый микроскоп» заглядывает в атом водорода Первое прямое наблюдение орбитальной
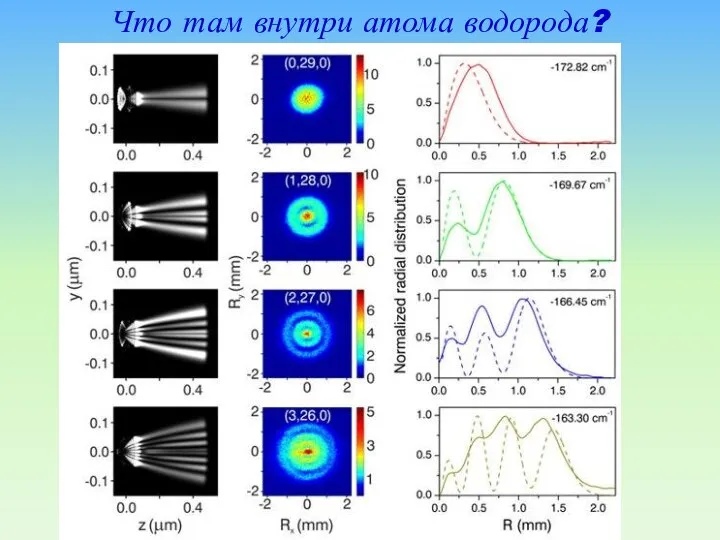
- 85. Что там внутри атома водорода?
- 86. На рисунке показан основной результат - данные видеокамеры за четыре измерения, когда атомы водорода были возбуждены
- 89. Скачать презентацию


















































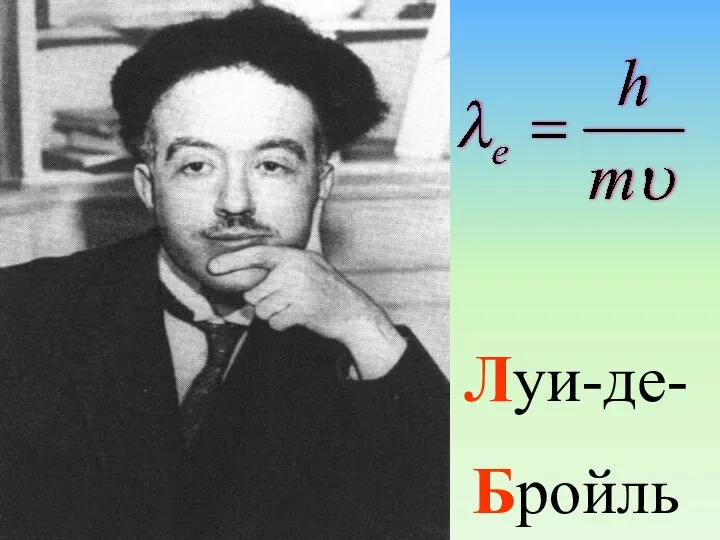







 Рыночная концентрация и монопольная власть
Рыночная концентрация и монопольная власть Электрическая дуга и дугогашение
Электрическая дуга и дугогашение Черлидинг
Черлидинг Единая Россия
Единая Россия Техническое обслуживание и ремонт двигателя ВАЗ2112
Техническое обслуживание и ремонт двигателя ВАЗ2112 Состав архитектурного проекта
Состав архитектурного проекта Налоговый учет
Налоговый учет Организация производства и продаж прибора для неинвазивного (чрезкожного) мониторинга содержания сахара в крови человека
Организация производства и продаж прибора для неинвазивного (чрезкожного) мониторинга содержания сахара в крови человека Теория и методика волейбола
Теория и методика волейбола Научно-исследовательская работа по теме: «Фальсификация алкогольной продукции» Выполнили: студенты 2 курса очной формы обучени
Научно-исследовательская работа по теме: «Фальсификация алкогольной продукции» Выполнили: студенты 2 курса очной формы обучени класс 1 урок
класс 1 урок Секуляризация и секуляризм
Секуляризация и секуляризм Wearing the hair shirt. A retrospective on Haskell
Wearing the hair shirt. A retrospective on Haskell Инфекционные воспалительные заболевания челюстно-лицевой области
Инфекционные воспалительные заболевания челюстно-лицевой области  Основные черты права Древнего Китая Выполнила студентка группы ю104 Рыжкова Анастасия
Основные черты права Древнего Китая Выполнила студентка группы ю104 Рыжкова Анастасия Калтанский городской округ. Проект по продвижению комплекса ГТО среди сверстников
Калтанский городской округ. Проект по продвижению комплекса ГТО среди сверстников Физиологические основы тренировки детей
Физиологические основы тренировки детей Основные понятия делового протокола
Основные понятия делового протокола Работа по системе компьютерной графики
Работа по системе компьютерной графики Мастерская бизнес-планов Практикум по бизнес-планированию Сайт проекта http://infmarket.biz
Мастерская бизнес-планов Практикум по бизнес-планированию Сайт проекта http://infmarket.biz Муниципальное казенное образовательное учреждение Любинского муниципального района Омской области «Любино – Малоросская ср
Муниципальное казенное образовательное учреждение Любинского муниципального района Омской области «Любино – Малоросская ср Брендинг и репутационный менеджмент
Брендинг и репутационный менеджмент Преступления против свободы, чести и достоинства личности
Преступления против свободы, чести и достоинства личности Узбекистан
Узбекистан  История бисера
История бисера Презентация ПРОЦЕССНО-ОРИЕНТИРОВАННЫЙ ПОДХОД
Презентация ПРОЦЕССНО-ОРИЕНТИРОВАННЫЙ ПОДХОД  Операционные системы Введение в файловые системы
Операционные системы Введение в файловые системы Самоблокирующийся дифференциал
Самоблокирующийся дифференциал