Содержание
- 2. Для слабых кислот HClO и H2CO3 в водном растворе при 250С: HClO+H2O=ClO-+H3O+; Kк1 = 2,82*10-8 H2CO3+H2O=HCO3-+H3O+;
- 3. Кислотные свойства ионы NH4+ и Al3+*H2O проявляют после растворения их солей. Например, NH4Cl и Al2(SO4)3. 1-я
- 4. Гидролиз солей - это реакция обмена между водой и растворяемой в ней соли, в результате в
- 5. Гидролиз соли, образованной сильной кислотой и слабым основанием (гидролиз по катиону) Причина гидролиза - образование слабого
- 6. Kо - константа основности - количественная характеристика состояния протолитического равновесия в реакции между основанием B и
- 7. Основные свойства ионов ClO- и CO32- проявляются после растворения в воде их солей. Например, NaClO, K2CO3
- 8. Гидролиз соли, образованной слабой кислотой и сильным основанием (гидролиз по аниону). Причиной гидролиза является образование слабой
- 9. Гидролиз соли, образованной слабой кислотой и слабым основанием (гидролиз и по катиону и по аниону) В
- 10. Многие гидроанионы, в водном растворе являются амфолитами. Например HCO3- : HCO3-+H2O=CO32-+H3O+; Kк = 4,68*10-11 HCO3-+H2O=H2CO3+OH-; Kо=Kв/Kк=2,34*10-8
- 11. Амфолитами являются амфотерные гидроксиды, типа Zn(OH)2, Be(OH)2, Al(OH)3, Cr(OH)3 и другие. В водном растворе они: 1)
- 12. Na2HPO4= 2Na++HPO42- HPO42-+H2O=PO43-+H3O+; Kк = 4,57*10-13 HPO42-+H2O=H2PO4-+OH-; Kо = 1,62*10-7 NaH2PO4 = 2Na+ + H2PO4- H2PO4-+H2O=HPO42-+H3O+;
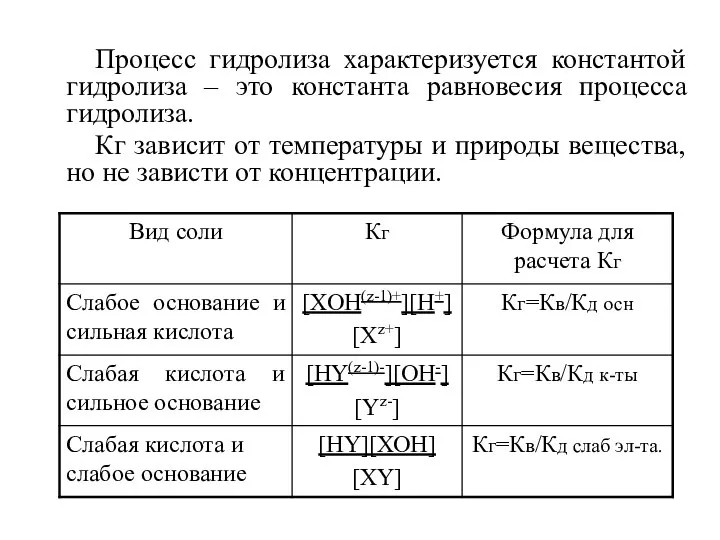
- 13. Процесс гидролиза характеризуется константой гидролиза – это константа равновесия процесса гидролиза. Кг зависит от температуры и
- 14. Глубина протекания гидролиза - степень гидролиза β, представляющая собой отношения концентрации гидролизованных молекул Сгидр. К исходной
- 15. Для подавления гидролиза соли надо добавлять в них при рН 7 – сильное основание. Например, вводя
- 16. Расчет формул для определения рН раствора. 1) Для соли слабой кислоты и сильного основания: рН =
- 18. Скачать презентацию














 Виртуально- информационная выставка
Виртуально- информационная выставка  Аттестационная работа. Совершенствование и проектирование ранее изученных элементов техники акробатических упражнений
Аттестационная работа. Совершенствование и проектирование ранее изученных элементов техники акробатических упражнений Стародавня Індія
Стародавня Індія Физические изменения у подростков
Физические изменения у подростков  40-й чемпионат мира CISM по парашютному спорту
40-й чемпионат мира CISM по парашютному спорту Автор Поддувалова Н.В. Учитель физики МОУ Давыдовская ООШ
Автор Поддувалова Н.В. Учитель физики МОУ Давыдовская ООШ Система имитационного моделирования GPSS World
Система имитационного моделирования GPSS World Презентация "Информационни системи в помощ на стартиращия бизнес" - скачать презентации по Экономике
Презентация "Информационни системи в помощ на стартиращия бизнес" - скачать презентации по Экономике Андромеда ч1 - презентация для начальной школы
Андромеда ч1 - презентация для начальной школы Легенды о полевых и лесных цветах Презентацию для проекта «Благодарю тебя за цветы» подготовила группа «историков»
Легенды о полевых и лесных цветах Презентацию для проекта «Благодарю тебя за цветы» подготовила группа «историков» Рождество. Рождение Иисуса
Рождество. Рождение Иисуса Проектно-исследовательская деятельность учащихся … для всякой вещи есть свое время и устав. Книга Екклезиаста
Проектно-исследовательская деятельность учащихся … для всякой вещи есть свое время и устав. Книга Екклезиаста Разработка технологии и расширение ассортимента блюд и напитков в ресторане с национальной кухней на 280 посадочных мест
Разработка технологии и расширение ассортимента блюд и напитков в ресторане с национальной кухней на 280 посадочных мест Основы техники двигательного действия
Основы техники двигательного действия Информационно-консалтинговая группа
Информационно-консалтинговая группа Презентация на тему "Я учусь в японской школе" - скачать презентации по Педагогике
Презентация на тему "Я учусь в японской школе" - скачать презентации по Педагогике Презентация Лесная промышленность России_
Презентация Лесная промышленность России_ Разборка и сборка системы питания автомобилей Chevrolet Niva
Разборка и сборка системы питания автомобилей Chevrolet Niva Курение - правовой аспект
Курение - правовой аспект Региональная гражданская служба
Региональная гражданская служба Араб каллиграфиясы
Араб каллиграфиясы Общая электротехника. История развития электротехники
Общая электротехника. История развития электротехники Реализация проекта «Аэродинамический комплекс»
Реализация проекта «Аэродинамический комплекс» Гироскопы. Применение в технике
Гироскопы. Применение в технике Избирательное право. Изготовление открытки-стикера молодому избирателю
Избирательное право. Изготовление открытки-стикера молодому избирателю Троица - Зелёные Святки
Троица - Зелёные Святки Система менеджмента безопасности пищевых продуктов
Система менеджмента безопасности пищевых продуктов Управление финансовыми потоками в логистической системе Подготовила Кулик Виктория
Управление финансовыми потоками в логистической системе Подготовила Кулик Виктория