Содержание
- 2. Эксперимент (опыт) в общем случае – общенаучный метод проверки причинно-следственных гипотез с помощью вмешательства (контролируемого воздействия)
- 3. Цель эпидемиологических экспериментальных исследований оценка потенциальной и реальной эффективности и безопасности профилактических и лекарственных средств, способов
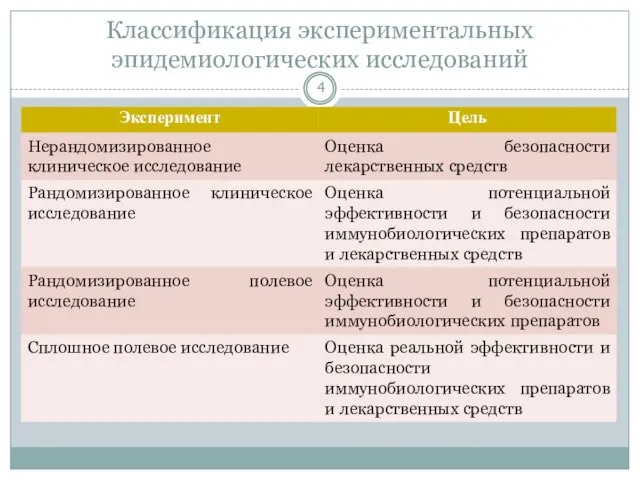
- 4. Классификация экспериментальных эпидемиологических исследований
- 5. Этапы создания лекарственного средства Разработка ЛС Доклинические исследования Клинические исследования
- 7. Медицинская необходимость Системные заболевания Болезнь Альцгеймера ВИЧ инфекция Диабет Злокачественные новообразования Сердечно-сосудистые заболевания Туберкулез Резистентность патогенных
- 8. Good Clinical Practice (GCP) Добросовестная (надлежащая, качественная) клиническая практика
- 9. Лекарственные средства - вещества или их комбинации, вступающие в контакт с организмом человека или животного, проникающие
- 10. Глава 5. Разработка, доклинические исследования лекарственных средств, а также клинические исследования лекарственных препаратов для ветеринарного применения
- 11. Разработчик лекарственного средства организация, обладающая правами на результаты доклинических исследований лекарственного средства, клинических исследований лекарственного препарата,
- 12. Воспроизведенное лекарственное средство лекарственное средство, содержащее такую же фармацевтическую субстанцию или комбинацию таких же фармацевтических субстанций
- 13. Доклиническое исследование лекарственного средства биологические, микробиологические, иммунологические, токсикологические, фармакологические, физические, химические и другие исследования лекарственного средства
- 14. Статья 11. Доклиническое исследование лекарственного средства для медицинского применения проводится путем применения научных методов оценок в
- 15. Доклиническое исследование лекарственного средства для медицинского применения проводится в соответствии с правилами лабораторной практики, утвержденными уполномоченным
- 16. Доклиническое исследование лекарственного средства для медицинского применения разработчики лекарственных средств могут привлекать научно-исследовательские организации, образовательные учреждения
- 17. Доклиническое исследование лекарственного средства для медицинского применения проводится по утвержденному разработчиком лекарственного средства плану с ведением
- 18. Доклиническое исследование лекарственного средства для медицинского применения Результаты доклинического исследования лекарственного средства для медицинского применения могут
- 19. Доклинические исследования
- 20. Статья 22. Решение о проведении клинического исследования лекарственного препарата для медицинского применения 2. Решение о проведении
- 21. Клиническое исследование (испытание) любое систематическое исследование медицинского продукта с участием людей в качестве субъектов (пациентов или
- 22. Клиническое исследование лекарственного препарата изучение диагностических, лечебных, профилактических, фармакологических свойств лекарственного препарата в процессе его применения
- 23. Статья 38 . Клинические исследования лекарственных препаратов
- 24. Статья 38 . Клинические исследования лекарственных препаратов
- 25. Цели клинических исследований Оценка терапевтической эффективности и переносимости нового фармакологического средства Установление наиболее рациональных доз и
- 26. Фазы (этапы) клинических исследований лекарственных средств
- 27. Фаза I (фармакологические-токсикологические) первые исследования на человеке (10-40-80 чел.) Здоровые добровольцы (исключение – онкология, СПИД, психические
- 28. Фаза I (фармакологические-токсикологические) фармакокинетика у человека Фармакодинамика: связь доза/эффект длительность эффекта юридические проблемы – разрешение первого
- 29. Особенности фазы I небольшое число добровольцев, от 4 до 24 человек (до 80 человек в течение
- 30. Преимущества фазы I легче набрать нужное количество здоровых добровольцев здоровые лица более дисциплинированны в соблюдении режима
- 31. Фаза II
- 32. Фаза II первые контролируемые исследования у пациентов (50-300-800 чел.) главная цель – установление эффективности, определение оптимальных
- 33. Фаза IIа Пилотные исследования эффективности (и безопасности) у некоторых отобранных популяций больных с целью лечения, профилактики
- 34. Цели Фазы II оценка краткосрочной безопасности лекарственного средства определение предельных дозировок при новом терапевтическом показании первичная
- 35. Фаза IIb Базисные исследования, т.е. более обширные исследования у пациентов с заболеванием ЦЕЛЬ: привести убедительные доказательства
- 36. Особенности Фаза IIb Плацебо-контролируемые исследования Количество пациентов – 40-300 Ориентировочные исследования у больных Исследования при новых
- 37. Фаза III
- 38. Особенности Фазы III 1000 – 3000 пациентов Исследуются характер и профиль нежелательных лекарственных реакций Изучаются клинически
- 39. Особенности Фазы III условия максимально приближены к обычной медицинской практике Результаты являются основой для создания инструкций
- 40. Задачи Фазы III доказательство эффективности и безопасности демонстрация терапевтических преимуществ фармакоэкономика и качество жизни подтверждение любых
- 42. Фаза IIIb Исследования, проходящие в период от подачи материалов для регистрации препарата в официальные инстанции до
- 43. Фаза IV после начала продажи препарата Постмаркетинговые (пострегистрационные) Цель: получить более подробную информацию об эффективности и
- 44. Субъекты фазы IV Больные заболеванием, для лечения которого данное ЛС зарегистрировано (тысячи чел.) Новые группы больных
- 45. Задачи фазы IV расширение терапевтического профиля дополнительная информация об эффективности различные лекарственные формы, дозы, режимы и
- 46. Особенности проведения КИ для женщин женщины детородного возраста могут принимать участие в КИ при надежном предохранении
- 47. ВИДЫ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ
- 48. Многоцентровое клиническое исследование лекарственного препарата клиническое исследование лекарственного препарата для медицинского применения, проводимое разработчиком лекарственного препарата
- 49. Международное многоцентровое клиническое исследование клиническое исследование лекарственного препарата для медицинского применения, проводимое разработчиком лекарственного препарата в
- 50. Статья 38. Клинические исследования лекарственных препаратов для медицинского применения В отношении воспроизведенных лекарственных препаратов для медицинского
- 51. Исследование биоэквивалентности лекарственного препарата вид клинического исследования лекарственного препарата, проведение которого осуществляется для определения скорости всасывания
- 52. Исследование терапевтической эквивалентности вид клинического исследования лекарственных препаратов, проведение которого осуществляется для выявления одинаковых свойств лекарственных
- 53. Исследование терапевтической эквивалентности Биодоступность отражает количество неизмененного действующего вещества, достигающего системного кровотока (степень всасывания) относительно исходной
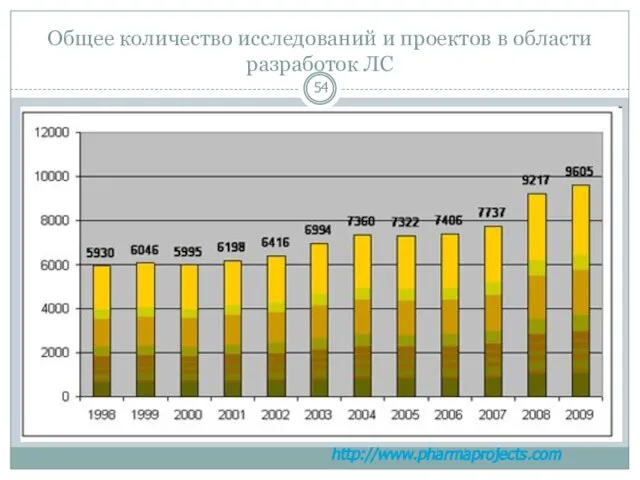
- 54. Общее количество исследований и проектов в области разработок ЛС http://www.pharmaprojects.com
- 55. Особенности исследований медицинских иммунобиологических препаратов
- 56. Фаза I Лабораторные испытания вакцин – исследование физических свойств, химического состава, доклиническое изучение токсичности и безопасности
- 57. Фаза II Ограниченные исследования на иммуногенность и безопасность. Исследование осуществляется только после положительного заключения этического комитета,
- 58. Фаза III Широкомасштабные испытания вакцин-кандидатов на здоровых пациентах (тысячи добровольцев). Определение эффективности вакцины и побочных реакций.
- 59. Фаза IV Постлицензионный контроль качества вакцин. Продолжение исследования частоты и силы побочных реакций, реальной эффективности в
- 60. Дизайн КИ Исследования типа «до – после» Исторический контроль Испытание в параллельных группах: Независимые выборки Связанные
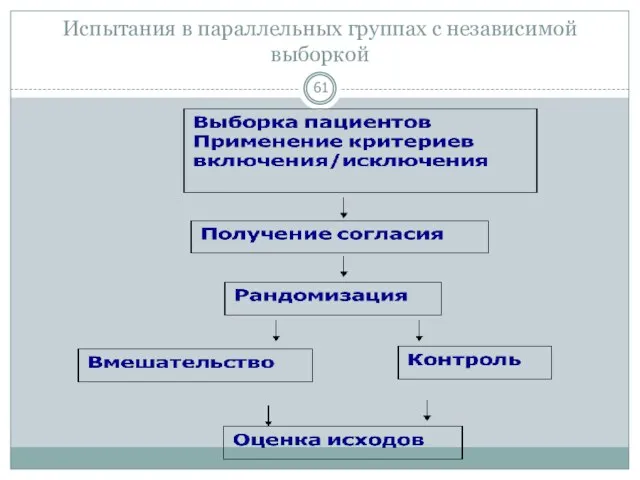
- 61. Испытания в параллельных группах с независимой выборкой
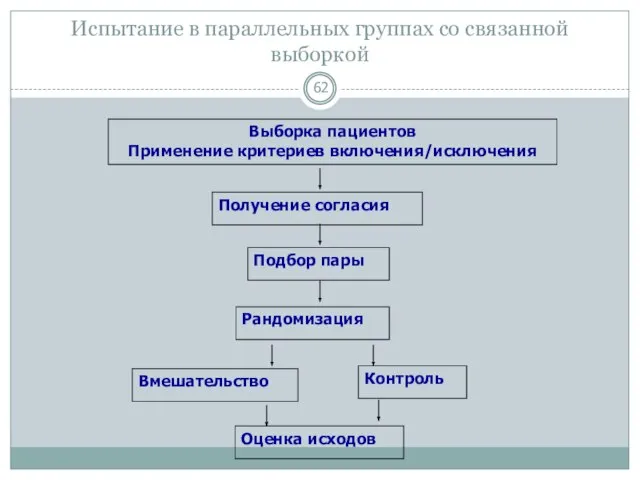
- 62. Испытание в параллельных группах со связанной выборкой Выборка пациентов Применение критериев включения/исключения Получение согласия Рандомизация Вмешательство
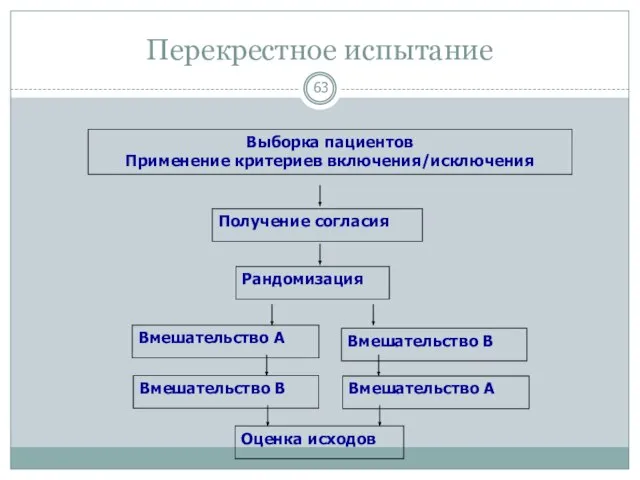
- 63. Перекрестное испытание Выборка пациентов Применение критериев включения/исключения Получение согласия Рандомизация Вмешательство А Оценка исходов Вмешательство В
- 65. Скачать презентацию













































 Цели внутреннего контроля и аудита финансового бизнес-цикла и его функции
Цели внутреннего контроля и аудита финансового бизнес-цикла и его функции Заболевания сосудистого тракта у детей
Заболевания сосудистого тракта у детей Кәсіпкерліктің ұйымдық-құқықтық нысандары. (Такырып 2)
Кәсіпкерліктің ұйымдық-құқықтық нысандары. (Такырып 2) Массивы в C#. Лекция 6
Массивы в C#. Лекция 6 Применение аналоговых перемножителей и балансных модуляторов
Применение аналоговых перемножителей и балансных модуляторов Программирование (Паскаль)
Программирование (Паскаль) Активные методы обучения персонала. Деловая игра, мозговой штурм, кейс-метод, баскет-метод
Активные методы обучения персонала. Деловая игра, мозговой штурм, кейс-метод, баскет-метод РУКОВОДСТВО ОРГАНИЗАЦИОННО-ИСПОЛНИТЕЛЬНАЯ
РУКОВОДСТВО ОРГАНИЗАЦИОННО-ИСПОЛНИТЕЛЬНАЯ  Өндірістік практика бойынша есеп Орал
Өндірістік практика бойынша есеп Орал ПРЕЗЕНТАЦИЯ СИСТЕМЫ © EleWise 2006 – 2010 Управление бизнес процессами. - презентация
ПРЕЗЕНТАЦИЯ СИСТЕМЫ © EleWise 2006 – 2010 Управление бизнес процессами. - презентация Финансовый контроль
Финансовый контроль  Микроциркуляция. Движение крови по венам. Регуляция системы кровообращения
Микроциркуляция. Движение крови по венам. Регуляция системы кровообращения  политология1 лекция
политология1 лекция Природова Ольга Федоровна Декан Факультета усовершенствования врачей ГБОУ ВПО РНИМУ им. Н.И.Пирогова Минздравсоцразвития
Природова Ольга Федоровна Декан Факультета усовершенствования врачей ГБОУ ВПО РНИМУ им. Н.И.Пирогова Минздравсоцразвития Политические роли личности
Политические роли личности Бременские музыканты Художник Сергий Елена
Бременские музыканты Художник Сергий Елена  Творческая работа «Особенности атакующих действий команд в гандболе»
Творческая работа «Особенности атакующих действий команд в гандболе» Материнский (семейный) капитал
Материнский (семейный) капитал Презентация Microsoft PowerPoint
Презентация Microsoft PowerPoint Из истории причесок Учитель технологии МОУ СОШ №1 город Буденновск Салогуб Марина Ивановна
Из истории причесок Учитель технологии МОУ СОШ №1 город Буденновск Салогуб Марина Ивановна  Интерьер
Интерьер Статистика дифференциации доходов
Статистика дифференциации доходов Создание и управление ассортиментом гипермаркета товаров для дома исходя из позиционирования бренда и соответствующей этому ком
Создание и управление ассортиментом гипермаркета товаров для дома исходя из позиционирования бренда и соответствующей этому ком Контроль качества сварных соединений
Контроль качества сварных соединений Страны исламского мира. Саудовская Аравия
Страны исламского мира. Саудовская Аравия Презентация Заполнение таможенной расписки
Презентация Заполнение таможенной расписки Министерство образования и науки РФ Муниципальное казенное общеобразовательное учреждение “Средняя общеобразовательная школа №13” Образовательная область: Мировая Художественная Культура Тема: Творчество И.Е. Репина Выполнил: ученик 9-в класса Бесене
Министерство образования и науки РФ Муниципальное казенное общеобразовательное учреждение “Средняя общеобразовательная школа №13” Образовательная область: Мировая Художественная Культура Тема: Творчество И.Е. Репина Выполнил: ученик 9-в класса Бесене Леонард Эйлер (1707-1783)
Леонард Эйлер (1707-1783)