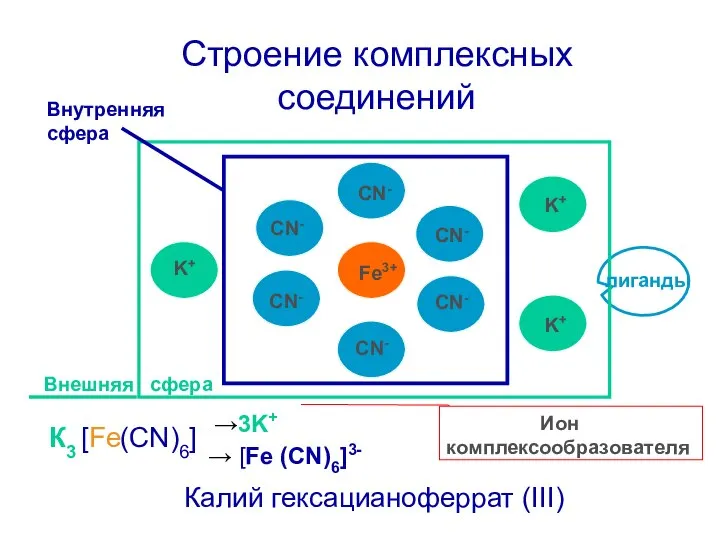
2. Классификация и номенклатура комплексных соединений
Первым называют катион, затем анион. Название
комплекса пишут в одно слово.
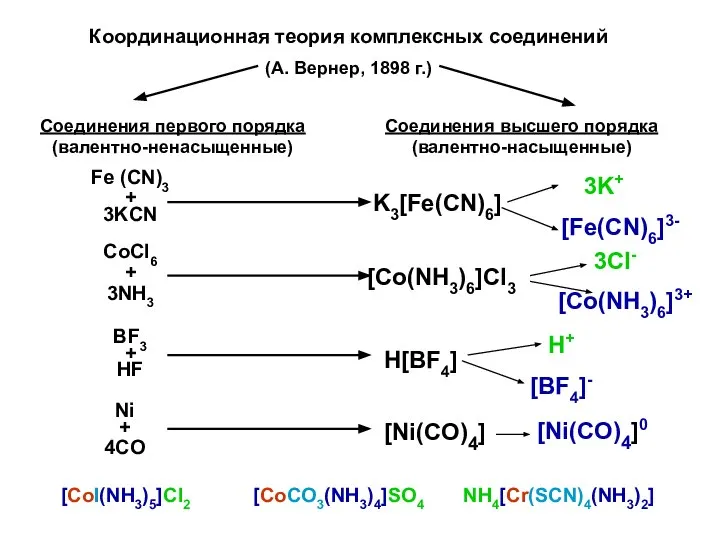
Правила названия комплексных соединений:
2. В названии комплекса сначала перечисляют лиганды (по первым буквам русского алфавита), затем центральный атом.
3. Нейтральные лиганды называют без изменения; к названиям отрицательно заряженных лигандов прибавляют окончание «о».
4. Если одинаковых лигандов в комплексе несколько, перед их названием употребляют соответствующее греческое числительное.
5. Название комплексообразователя зависит от заряда комплекса.
5.1. Для нейтрального и катионного – именительный падеж (рус. яз.)
5.2. Для анионного комплекса - латинский язык (суффикс «ат»)


![Номенклатура комплексных соединений К[Co(CN)(CO)2(NO)] - калий дикарбонил нитрозил циано кобальт (0)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292009/slide-5.jpg)
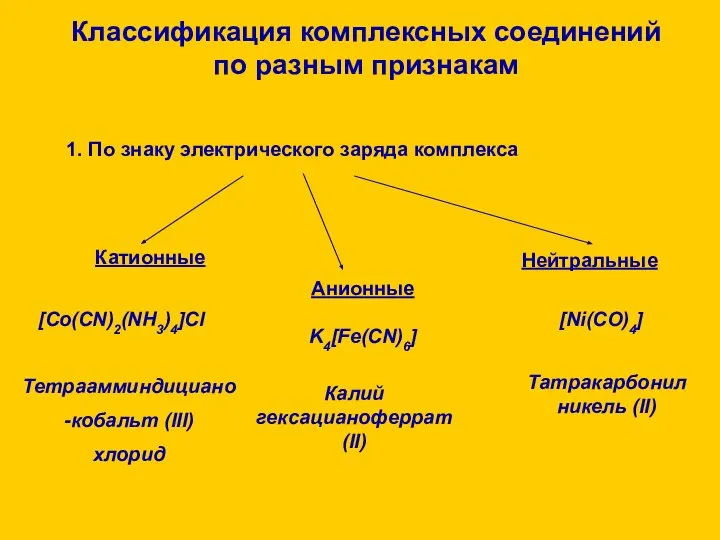
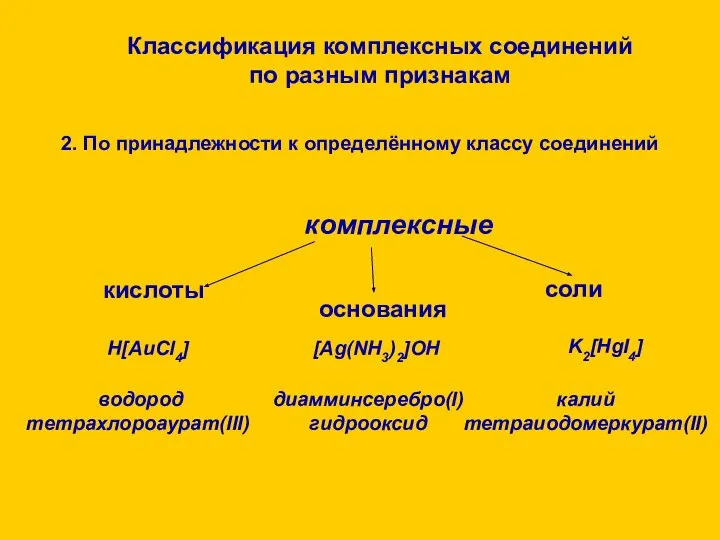
![3. По природе лигандов Аммиакаты [Ni(NH3)6]Cl2 Аквакомплексы [Co(H2O)6]SO4 Ацидокомплексы K[Cu(CN)2] Карбонилы](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1292009/slide-8.jpg)

 Концепция реконструкции и развития Полежаевского парка г. Санкт-Петербурга
Концепция реконструкции и развития Полежаевского парка г. Санкт-Петербурга Aegean and ancient greek architecture. L 5-6
Aegean and ancient greek architecture. L 5-6 Искусство орнамента казахов
Искусство орнамента казахов Презентация Атлас - шелковая ткань
Презентация Атлас - шелковая ткань . Уход за волосами
. Уход за волосами Профессиональные консультанты. Причины и основания для обращения к консультантам. Управленческое консультирование. Тема 2
Профессиональные консультанты. Причины и основания для обращения к консультантам. Управленческое консультирование. Тема 2 Тамақ дәмін тату. Суретпен көрсетілген сөздер
Тамақ дәмін тату. Суретпен көрсетілген сөздер Основы программирования на языке Pascal. Алфавит, типы данных, структура программ. Основные операторы
Основы программирования на языке Pascal. Алфавит, типы данных, структура программ. Основные операторы Тема 8. Инструменты анализа международной торговли Условия торговли Эластичность экспорта и импорта Эффекты дохода и замещения
Тема 8. Инструменты анализа международной торговли Условия торговли Эластичность экспорта и импорта Эффекты дохода и замещения Театральна культура України ХІХ- поч.ХХ ст
Театральна культура України ХІХ- поч.ХХ ст Місцеве самоврядування
Місцеве самоврядування Начертательная геометрия. Пересечение поверхности плоскостью частного положения. (Лекция 5)
Начертательная геометрия. Пересечение поверхности плоскостью частного положения. (Лекция 5) Щелочно-кислотное равновесие. Биохимия мочи.
Щелочно-кислотное равновесие. Биохимия мочи. Механизмдегі күштерді жіктеу
Механизмдегі күштерді жіктеу Grzechy przeciwko Duchowi Świętemu
Grzechy przeciwko Duchowi Świętemu Зачем нужен менеджер продукта при живом проектировщике интерфейсов? Денис Бесков / http://beskov.ru World Usability Day, Москва, 2011
Зачем нужен менеджер продукта при живом проектировщике интерфейсов? Денис Бесков / http://beskov.ru World Usability Day, Москва, 2011  Система отраслевого или корпоративного нормирования
Система отраслевого или корпоративного нормирования Механизмы рынка. Спрос и Предложение
Механизмы рынка. Спрос и Предложение  Ответный бриф. На разработку лендинга для службы доставки еды
Ответный бриф. На разработку лендинга для службы доставки еды Презентация АНОМАЛИИ РОДОВОЙ ДЕЯТЕЛЬНОСТИ Кафедра акушерства и гинекологии №2 КГМУ зав.кафедрой д.м.н., профессор Фаткулли
Презентация АНОМАЛИИ РОДОВОЙ ДЕЯТЕЛЬНОСТИ Кафедра акушерства и гинекологии №2 КГМУ зав.кафедрой д.м.н., профессор Фаткулли МНОГОЧЛЕН - презентация по Алгебре
МНОГОЧЛЕН - презентация по Алгебре „Nim cokolwiek powiesz, dwa razy przemyśl”. Rzecz o ósmym przykazaniu
„Nim cokolwiek powiesz, dwa razy przemyśl”. Rzecz o ósmym przykazaniu Тема 1 ТП
Тема 1 ТП 1992 рік - філіал кібернетико-технічного коледжу Кіровоградського інституту сільськогосподарського машинобудування. 1993 рік -коледж реорганізовано в ліцей. 1999 рік - заклад отримав статус гімназії і назву “Златопільська”.
1992 рік - філіал кібернетико-технічного коледжу Кіровоградського інституту сільськогосподарського машинобудування. 1993 рік -коледж реорганізовано в ліцей. 1999 рік - заклад отримав статус гімназії і назву “Златопільська”. ОСОБО ОПАСНЫЕ ИНФЕКЦИИ (КАРАНТИННЫЕ, КОНВЕНЦИОННЫЕ) Холера. Чума. Геморрагические лихорадки
ОСОБО ОПАСНЫЕ ИНФЕКЦИИ (КАРАНТИННЫЕ, КОНВЕНЦИОННЫЕ) Холера. Чума. Геморрагические лихорадки  Гуманитаризация обучения математики на уроках математики
Гуманитаризация обучения математики на уроках математики  Определение разницы между максимальным и минимальным корнем уравнения y1(x) = y2(x) интервале значений x [0, 10)
Определение разницы между максимальным и минимальным корнем уравнения y1(x) = y2(x) интервале значений x [0, 10) Происхождение государства
Происхождение государства