Содержание
- 2. Потребность в белках и нормы белкового питания Белки – незаменимый компонент пищи, практически единственный источник азота
- 3. Потребности в белковой пище Коэффициент Рубнера (коэффициент изнашивания) = 53 мг N2 /кг массы тела. 23
- 4. Потребность в белках Физиологический минимум = 35 -50 г в сутки. Оптимум – 85 -100 г
- 5. Внешний обмен белка (переваривание, гидролиз) Поэтапный протеолиз белков до аминокислот, лишение их видоспецифичности и антигенности. Главными
- 7. Роль соляной кислоты 1. Создает кислую среду в полости желудка (рН 1,5 -2), условия для самоактивации
- 8. Регуляция синтеза соляной кислоты Гистидин ? гистамин – активация аденилатциклазы – активация фосфопротеинкиназы с участием цАМФ
- 9. ПЕПСИНОГЕН - ПЕПСИН Пепсин – простой одноцепочечный белок, карбоксильная (в активном центре асп-асп) эндопротеиназа. Активируется в
- 10. Панкреатические протеиназы Синтезируются в виде проферментов и активируются лимитированным протеолизом в просвете 12 – перстной кишки.
- 11. Панкреатические протеиназы Трипсин обеспечивает активацию проэластазы, прокарбоксипептидазы, химотрипсиногена, отщепляя N –концевые пептиды. Каскад протеолитических эндо- и
- 12. Всасывание аминокислот в кишечнике В мембранах энтероцитов кишечных ворсинок – несколько систем активного транспорта (Na+ -зависимый
- 15. Гниение белков в кишечнике Реакции дезаминирования и декарбоксилирования аминокислот с участием бактериальных ферментов. В кишечнике накапливаются
- 16. Обезвреживание продуктов гниения в печени Неспецифические, индуцибельные ферменты микросом печени: ФАФС–трансфераза, УДФ-трансфераза образуют парные, нетоксичные, растворимые
- 17. Внутриклеточный протеолиз Лизосомы. Кислые гидролазы: тиоловые и аспартатные протеиназы (катепсины В, L, H, D), гидролизующие белки.
- 18. Защита от протеолиза Как в клетках, так и во внеклеточном пространстве, в крови работают и системы
- 19. Промежуточный обмен аминокислот. Общие пути катаболизма аминокислот (дезаминирование,трансаминирование, декарбоксилирование) Частные реакции превращений аминокислот. Пути синтеза заменимых
- 20. Метаболические функции аминокислот Кроме участия в синтезе пептидов и белков, у большинства аминокислот активная метаболическая «судьба»:
- 21. СИНТЕЗ ЗАМЕНИМЫХ АМИНОКИСЛОТ Источник углеродных скелетов – глюкоза, азота – NH2 – группы аминокислот, NH3. Реакции
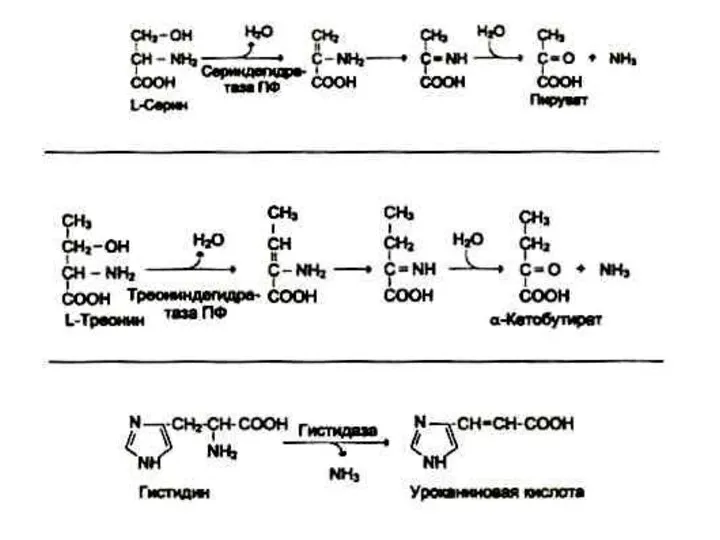
- 22. Дезаминирование аминокислот Механизмы: восстановительный; гидролитический; внутримолекулярный, окислительный. В клетках млекопитающих гис подвергается внутримолекулярному дезаминированию. Сер и
- 24. Окислительное дезаминирование Для каждой аминокислоты есть специфическая оксидаза. FMN –зависимые оксидазы L-аминокислот имеют оптимум рН в
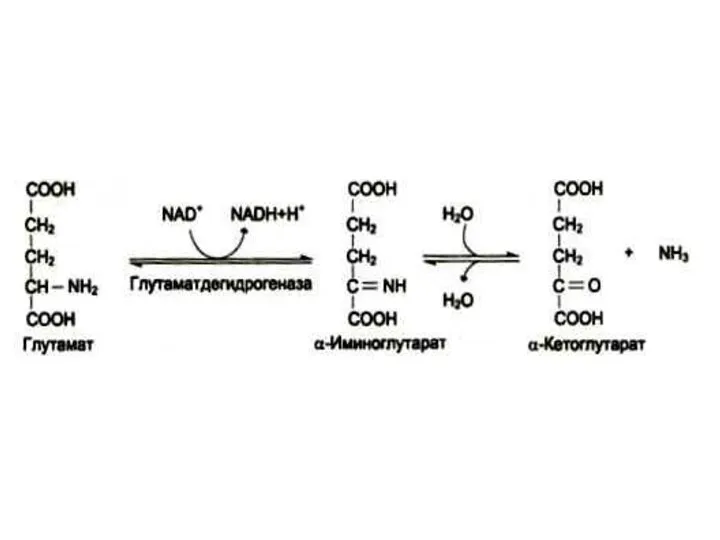
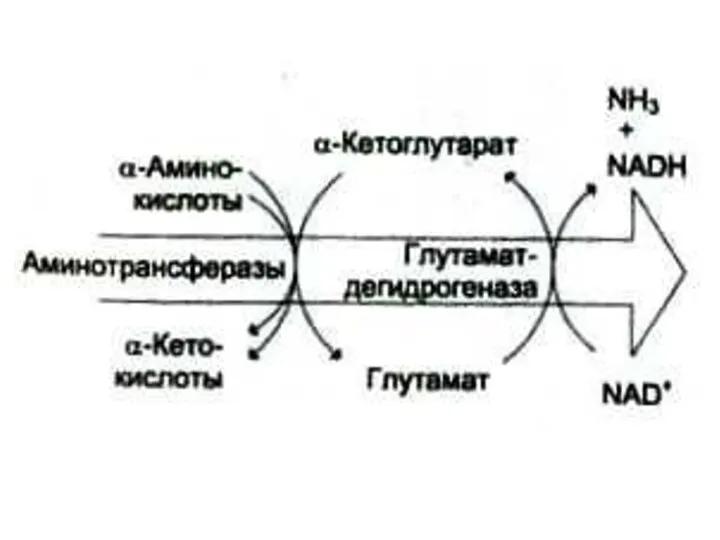
- 25. Окислительное дезаминирование Наиболее активной дезаминазой является глутаматдегидрогеназа (NAD- зависимая) Реакция идет в две стадии: ферментативное окисление
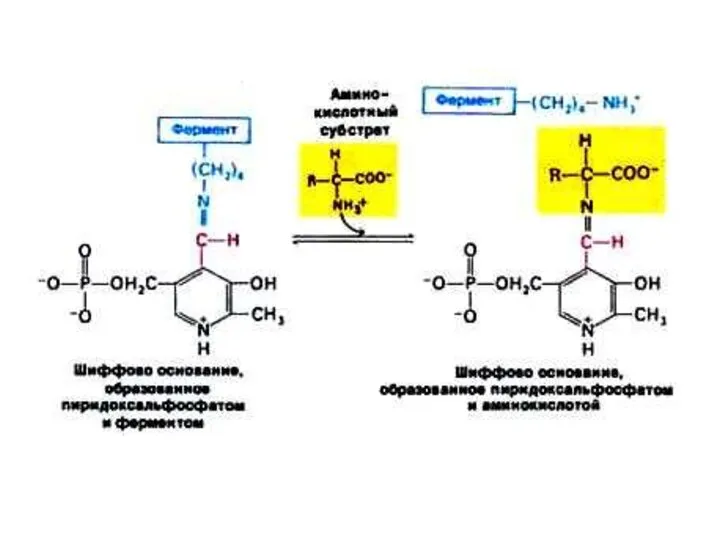
- 27. Трансаминирование Обратимая реакция между кетокислотами и аминокислотами (кофактор – пиридоксальфосфат переносит аминогруппу). На основе кетокислот возникают
- 34. Декарбоксилирование аминокислот При участии пиридоксальзависимых декарбоксилаз образуются биогенные амины. Глу ? γ − аминомасляная кислота Гис
- 38. Конечные продукты белкового обмена Аммиак образуется как результат: дезаминирования аминокислот окисления биогенных аминов утилизация азотистых оснований
- 39. АММИАК В сутки в норме образуется до 20г аммиака, т.е. 4г/л , тем не менее концентрация
- 40. Механизмы токсичности аммиака NH3 проникает через клеточные и митохондриальные мембраны. Увеличение скорости восстановительного аминирования α –кетоглутарата
- 41. Пути обезвреживания аммиака Восстановительное аминирование Образование амидов Синтез азотистых оснований (пиримидинов) Аммониогенез Синтез мочевины «Косвенные» пути,
- 42. Образование амидов дикарбоновых кислот Глутамин- и аспарагин-синтетазы включают аммиак в состав амидов, образуя временную, транспортную нетоксичную
- 43. Восстановительное аминирование кетокислот NADF- зависимая редуктаза восстанавливает кетокислоты до аминокислот. Это путь образования заменимых аминокислот и
- 44. Синтез азотистых оснований (пиримидинов) Синтез пиримидинов начинается с карбамоилсинтетазной реакции: NH3+ CO2+ ATP? NH2COPO32-. Синтез пуринов
- 45. Аммониогенез в почках Глутамин в почках вновь освобождает аммиак Образовавшася с помощью карбангидразы Н2СО3 диссоциирует на
- 46. Синтез креатинина Осуществляется при участии ферментов почек и печени из глицина, аргинина и метионина. Креатин фосфорилируется
- 51. Конечные продукты азотистого обмена У организмов разных видов с мочой выделяются разные продукты: Аммонийтелический тип (NH3)
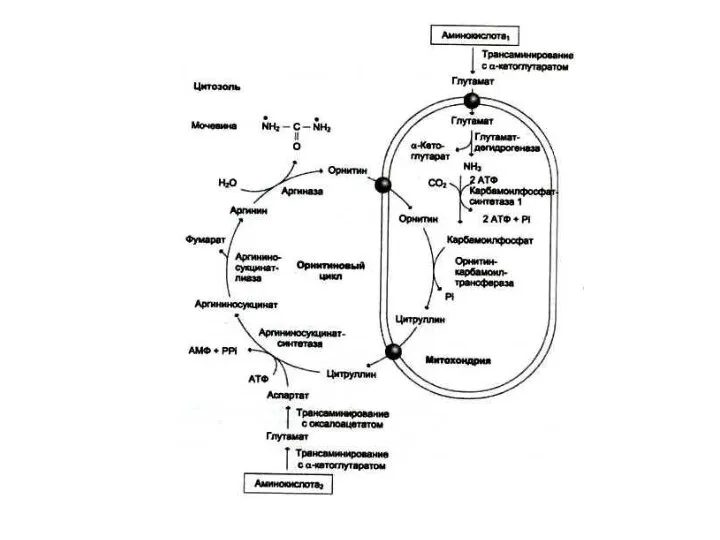
- 52. Орнитиновый цикл синтеза мочевины (цикл Кребса, Ханзеляйта) Гепатоциты, митохондрии, аэробные условия. АТР, СО2, орнитин, цитруллин, аспартат,
- 61. Конечные продукты азотистого обмена Фракции «остаточного» азота в крови: Мочевина (50% N2 крови и 90% N2
- 63. Скачать презентацию























































 Что такое любовь
Что такое любовь Курс обучения тестированию
Курс обучения тестированию Приветствия
Приветствия Модель безопасности рабочего места
Модель безопасности рабочего места Электромобили как элемент интеллектуальных электрических сетей
Электромобили как элемент интеллектуальных электрических сетей Меняющееся общество
Меняющееся общество Пантеон - храм всех богов
Пантеон - храм всех богов Подвеска колес автомобиля
Подвеска колес автомобиля Технология общестроительных работ при возведении жилого дома «Лидия»
Технология общестроительных работ при возведении жилого дома «Лидия» Презентация на тему "Значение сказки в нравственном воспитании детей" - скачать презентации по Педагогике
Презентация на тему "Значение сказки в нравственном воспитании детей" - скачать презентации по Педагогике Нарушение Микроциркуляции
Нарушение Микроциркуляции Позиционирование Nokia
Позиционирование Nokia Презентация по алгебре Типы иррациональных уравнений Примеры решения
Презентация по алгебре Типы иррациональных уравнений Примеры решения  Индустриальное общество новые проблемы и новые ценности 1
Индустриальное общество новые проблемы и новые ценности 1 Классный час «Здоровый ребёнок в здоровой семье» Хвастунова Т.Ф.
Классный час «Здоровый ребёнок в здоровой семье» Хвастунова Т.Ф.  Трудовые отношения между работодателем и работником
Трудовые отношения между работодателем и работником Санкт-Петербург пассажирский, Московская дистанция сигнализации, централизации и блокировки
Санкт-Петербург пассажирский, Московская дистанция сигнализации, централизации и блокировки Центр тестирования ВФСК ГТО «Металлург»
Центр тестирования ВФСК ГТО «Металлург» Музей декоративно-прикладного и народного искусства
Музей декоративно-прикладного и народного искусства Дональд Джон Трамп
Дональд Джон Трамп Designing & Deploying Connected Device Solutions for Small and Medium Business
Designing & Deploying Connected Device Solutions for Small and Medium Business ОБЩИЕ ПОНЯТИЯ ТЕОРИИ ОШИБОК ИЗМЕРЕНИЙ
ОБЩИЕ ПОНЯТИЯ ТЕОРИИ ОШИБОК ИЗМЕРЕНИЙ Развитие договора банковского вклада в российском и советском законодательстве
Развитие договора банковского вклада в российском и советском законодательстве Аттестация рабочих мест
Аттестация рабочих мест  Особенности договора контрактации сельскохозяйственной продукции Подготовил: Михайлов Владимир Крылов Максим
Особенности договора контрактации сельскохозяйственной продукции Подготовил: Михайлов Владимир Крылов Максим ИНСТИТУЦИОНАЛЬНАЯ ЭКОНОМИКА
ИНСТИТУЦИОНАЛЬНАЯ ЭКОНОМИКА  Крутые машины
Крутые машины Технологии власти. Власть технологий
Технологии власти. Власть технологий