Полный момент импульса электрона в атоме. Символические обозначения термов. Правила отбора для оптических переходов.
Содержание
- 2. Операции с векторами L и S можно производить с помощью следующего полуклассического мето-да. Вектора складываются по
- 3. Во-вторых, полный момент J, как всякий момент импульса в квантовой механике имеет свое квантовое число j,
- 4. Проекция вектора J на какое либо направление Z (ось квантования, направление внешнего маг-нитного или электрического поля
- 5. Эти правила сложения векторов L и S со-ставляют векторную модель атома, имеющую большое практическое значе-ние: модель
- 6. Различные состояния атома (термы) принято обо-значать специальными символами, по которым сразу можно указать все квантовые числа.
- 7. Т.к. терм - это характеристика всего атома, то ис-пользуются прописные буквы вместо строчных (которые применяются для
- 8. Правила отбора для оптических переходов Согласно комбинационному принципу, волновое число любой спектральной линии (в испускании и
- 9. Эти правила связаны с законами сохранения мо-мента импульса и четности в квантовых пере-ходах. В частности установлено,
- 10. Если условие (17.10) соблюдается, то такие пере-ходы называются разрешенными. Другие пере-ходы маловероятны, и их называют запрещен-ными.
- 11. Вероятность перехода определяется так называ-емым матричным элементом: интегралом вида (17.11) который представляет собой дипольный момент ex,
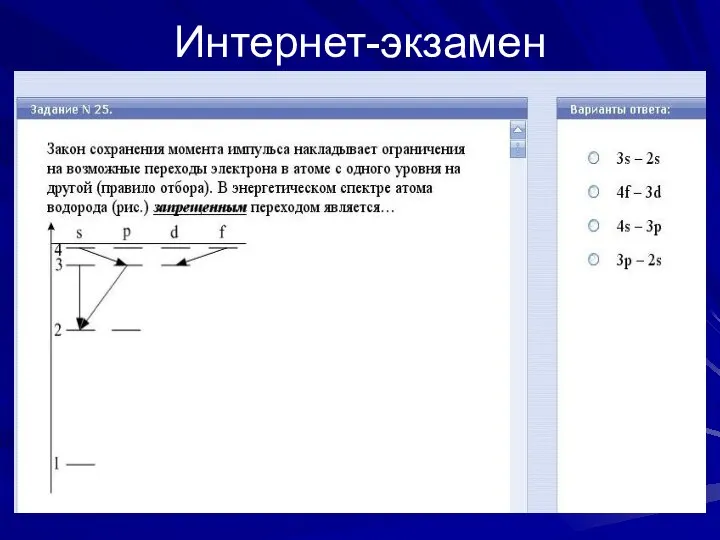
- 12. Интернет-экзамен
- 14. Скачать презентацию










 Файловый ввод-вывод
Файловый ввод-вывод Аффективные психические образования
Аффективные психические образования  Презентация Рынок зерна в российской федерации
Презентация Рынок зерна в российской федерации  _ ___________________ __ _____ 283
_ ___________________ __ _____ 283 Либерально-демократическая партия России (ЛДПР)
Либерально-демократическая партия России (ЛДПР) Азбука предпринимательства. Юридические аспекты и налоги
Азбука предпринимательства. Юридические аспекты и налоги Зримая музыка. 8 класс
Зримая музыка. 8 класс Усиление растянутой зоны строительных конструкций
Усиление растянутой зоны строительных конструкций Дневник классного руководителя Класс 7 Б &nb
Дневник классного руководителя Класс 7 Б &nb Спинномозговые нервы
Спинномозговые нервы  Презентация "Карл Брюллов" - скачать презентации по МХК
Презентация "Карл Брюллов" - скачать презентации по МХК Т.Г. Шевченко – видатний український художник
Т.Г. Шевченко – видатний український художник Тоталитаризм. Общие сведения и понятие
Тоталитаризм. Общие сведения и понятие Халықаралық және ішкі тасымалдаудағы контрактік және келісм шарттық өзара байланыс
Халықаралық және ішкі тасымалдаудағы контрактік және келісм шарттық өзара байланыс Господарський контроль в Україні
Господарський контроль в Україні Контрольная (надзорная) деятельность Федеральной службы по надзору в сфере природопользования (Росприроднадзор)
Контрольная (надзорная) деятельность Федеральной службы по надзору в сфере природопользования (Росприроднадзор) Структура Java. Приложения
Структура Java. Приложения Презентация по образовательной программе внеурочной деятельности «Планета Здоровья» по курсу «Земля- наш дом» Составитель: учи
Презентация по образовательной программе внеурочной деятельности «Планета Здоровья» по курсу «Земля- наш дом» Составитель: учи Презентация по МХК Тициан Вечеллио 1488/1490—1576
Презентация по МХК Тициан Вечеллио 1488/1490—1576  Кубинский новый год
Кубинский новый год Квантовые алгоритмы Монте-Карло. Проблема знака Проблема знака. Winding numbers. Связь фермионного знака и winding numbers
Квантовые алгоритмы Монте-Карло. Проблема знака Проблема знака. Winding numbers. Связь фермионного знака и winding numbers Оксосоединения, получение, свойства, таутомерия
Оксосоединения, получение, свойства, таутомерия  Комплексный эколого-краеведческий проект «Создание пеше-водного маршрута «Вниз по речке Василевке в сказку озера Сапшо»
Комплексный эколого-краеведческий проект «Создание пеше-водного маршрута «Вниз по речке Василевке в сказку озера Сапшо» Управление командой в стартап-проекте
Управление командой в стартап-проекте  Износ основных фонов
Износ основных фонов МОУ «Анаткасинская начальная школа-детский сад» Моргаушский район Исследовательский проект Хвостатые гидростроители
МОУ «Анаткасинская начальная школа-детский сад» Моргаушский район Исследовательский проект Хвостатые гидростроители Культура армянского народа
Культура армянского народа Презентация "Введение в экономику" - скачать презентации по Экономике
Презентация "Введение в экономику" - скачать презентации по Экономике