Содержание
- 2. Биохимия - это наука, занимающаяся изучением различных молекул, химических реакций и процессов, протекающих в живых клетках
- 3. Главная задача биохимии состоит в том, чтобы достичь полного понимания на молекулярном уровне природы всех химических
- 4. Основательное знание биохимии совершенно необходимо для успешного развития двух главных направлений биомедицинских наук: решение проблем сохранения
- 5. В живых клетках происходит синтез множества органических молекул, среди которых главную роль играют полимерные макромолекулы –
- 6. Белки являются важнейшим субстратом жизни, т.к. обладают рядом особенностей: молекулы белков отличаются неисчерпаемым разнообразием структуры при
- 7. 4. молекулы белков закономерно изменяют свою структуру под влиянием внешнего воздействия и восстанавливают исходное состояние. При
- 8. Синтез белков очень сложен и трудоемок, поэтому реально лучше выделить белки из природных источников. Белки обладают
- 9. Последовательность операций по выделению белков обычно состоит в следующем: измельчение биологического материала (гомогенизация) 2. извлечение белков,
- 10. МЕТОДЫ ВЫДЕЛЕНИЯ БЕЛКОВ Высаливание (процесс осаждения белка из раствора под действием соли) Электрофорез (основан на способности
- 11. Белки выделяют солевыми растворами (8-10%). Различные соли обладают разным растворяющим действием по отношению к белку. максимальным
- 12. Метод электрофореза основан на способности различных белков перемещаться под действием электрического поля с неодинаковой скоростью в
- 13. Адсорбционная хроматография Разделение компонентов смеси (образца) основано на их различной сорбируемости на твердом адсорбенте. В качестве
- 14. Распределительная хроматография В отличие от адсорбционной твердая фаза служит только опорой (основой) для стационарной жидкой фазы.
- 15. Ионообменная хроматография сводится к вытеснению противоионов, связанных с анионными и катионными центрами ионообменника ионогенными группировками белковых
- 16. Аффинная хроматография Основана на принципе избирательного взаимодействия белков с закрепленными (иммобилизованными) на носителе специфическими веществами –
- 17. Все выделенные белки всегда содержат некоторое количество примесей, особенно ионов солей. Для полного освобождения от этих
- 18. Одним из наиболее распространенных методов исследования химического состава белковых тел является гидролиз. Белок нагревают с растворами
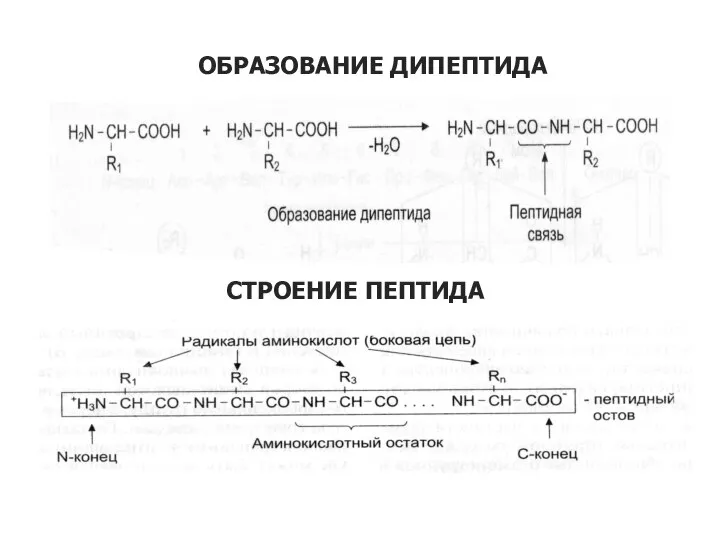
- 19. ОБРАЗОВАНИЕ ДИПЕПТИДА СТРОЕНИЕ ПЕПТИДА
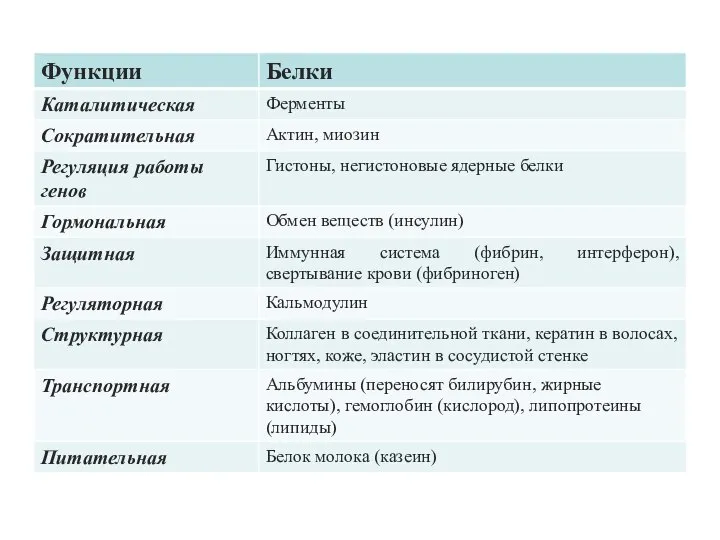
- 20. КЛАССИФИКАЦИЯ БЕЛКОВ Классификация белков, основанная на их растворимости, была введена в 1907—1908 гг. и используется до
- 21. ФОРМА МОЛЕКУЛ Если исходить из отношения осей (продольной и поперечной), можно выделить два больших класса белков.
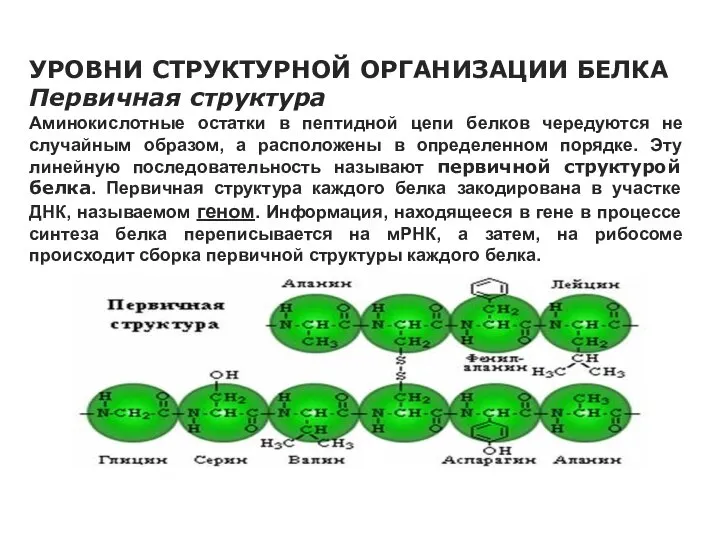
- 23. УРОВНИ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКА Первичная структура Аминокислотные остатки в пептидной цепи белков чередуются не случайным образом,
- 24. Вторичная структура Пространственная структура, образующаяся в результате взаимодействий между функциональными группами, входящими в состав белка. Вторичная
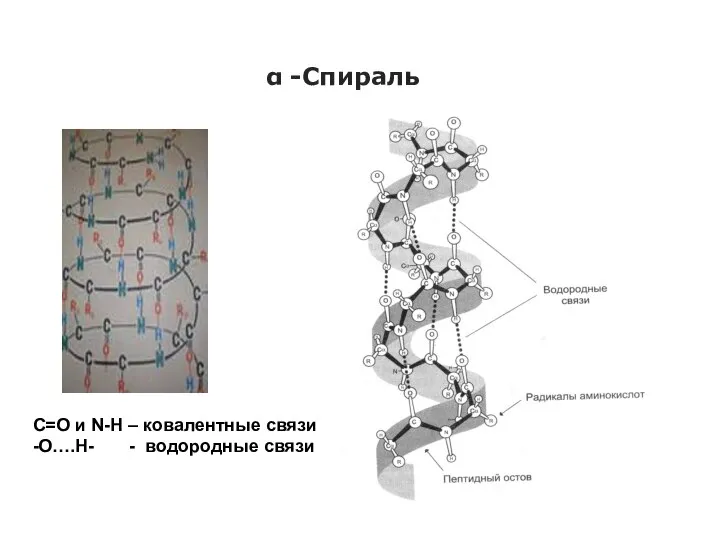
- 25. Основные характеристики α-спирали 1. α-Спираль стабилизируется водородными связями между атомом водорода, присоединенным к атому азота пептидной
- 26. Основные характеристики α-спирали 4. α-Спираль образуется самопроизвольно и является наиболее устойчивой конформацией полипептидной цепи, отвечающей минимуму
- 27. α -Спираль С=О и N-Н – ковалентные связи -О….Н- - водородные связи
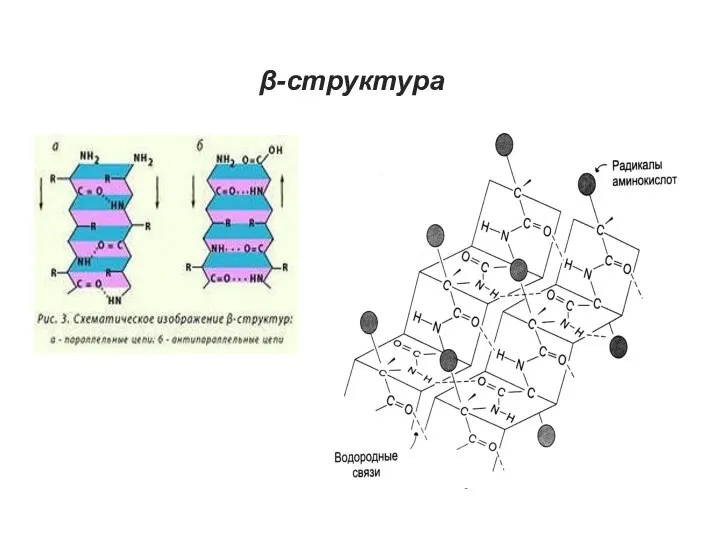
- 28. β-структура Это слоистые структуры, образуемые при сочетании участков полипептидной цепи, находящихся в β-конформации, т.е. в виде
- 29. β-структура
- 30. Третичная структура Это трехмерная пространственная структура, образующаяся за счет взаимодействий между радикалами аминокислот, которые могут располагаться
- 31. Гидрофильные радикалы аминокислот стремятся образовать водородные связи с водой и поэтому располагаются на поверхности белков. Они
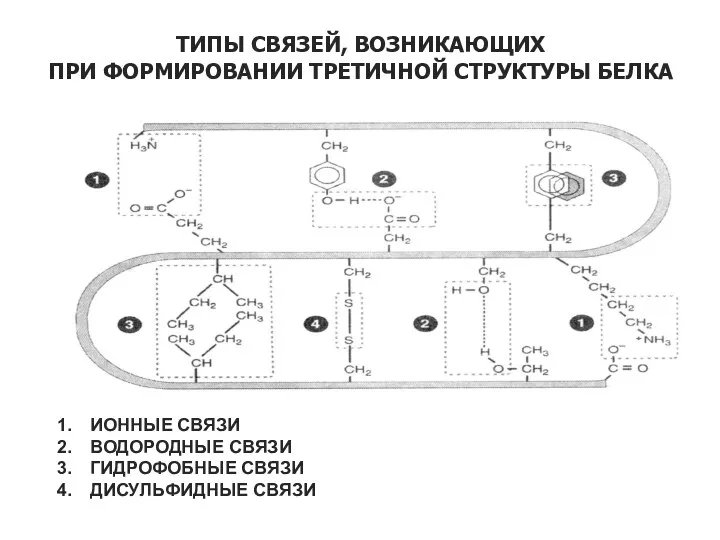
- 32. ТИПЫ СВЯЗЕЙ, ВОЗНИКАЮЩИХ ПРИ ФОРМИРОВАНИИ ТРЕТИЧНОЙ СТРУКТУРЫ БЕЛКА ИОННЫЕ СВЯЗИ ВОДОРОДНЫЕ СВЯЗИ ГИДРОФОБНЫЕ СВЯЗИ ДИСУЛЬФИДНЫЕ СВЯЗИ
- 33. Четвертичная структура Если белки состоят из двух и более полипептидных цепей, связанных между собой нековалентными (не
- 34. Многие олигомерные белки содержат два или четыре протомера и называются димерами или тетрамерами соответственно. Олигомерные белки
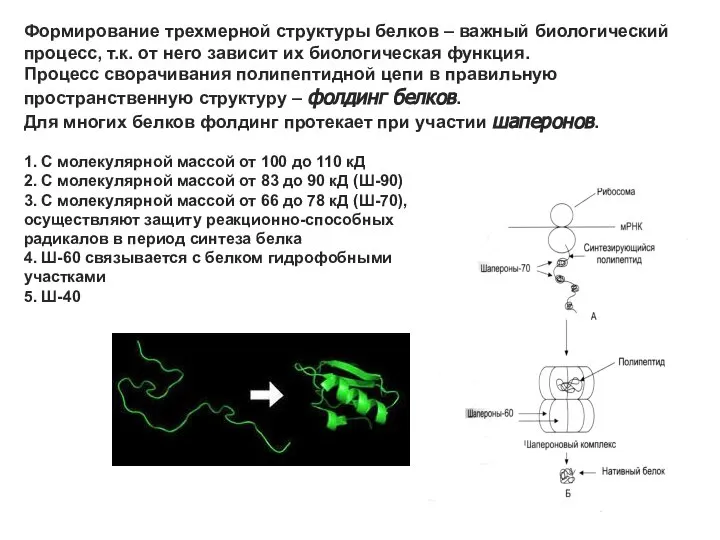
- 35. Формирование трехмерной структуры белков – важный биологический процесс, т.к. от него зависит их биологическая функция. Процесс
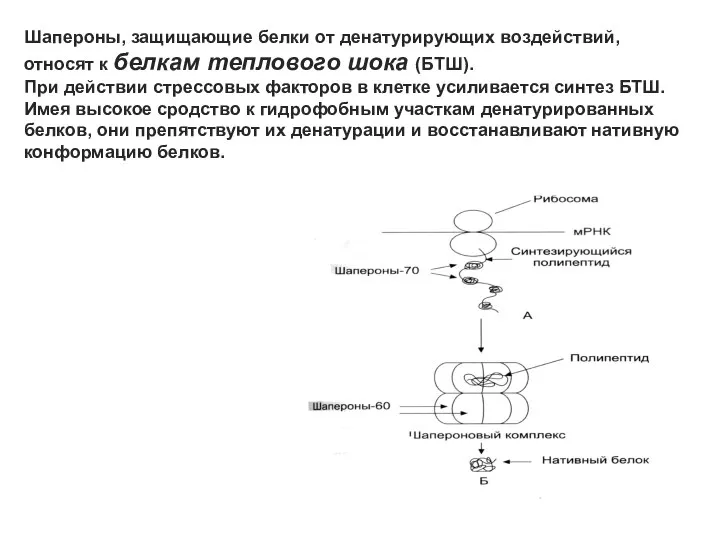
- 36. Шапероны, защищающие белки от денатурирующих воздействий, относят к белкам теплового шока (БТШ). При действии стрессовых факторов
- 37. Наиболее изученный пример белка, имеющего четвертичную структуру - гемоглобин. Молекула гемоглобина построена из 4-субъединиц с молекулярной
- 38. Большой интерес представляет интерес взаимосвязи структуры гемоглобина с его функцией – способностью связывать, переносить и отдавать
- 39. Большой интерес представляет интерес взаимосвязи структуры гемоглобина с его функцией – способностью связывать, переносить и отдавать
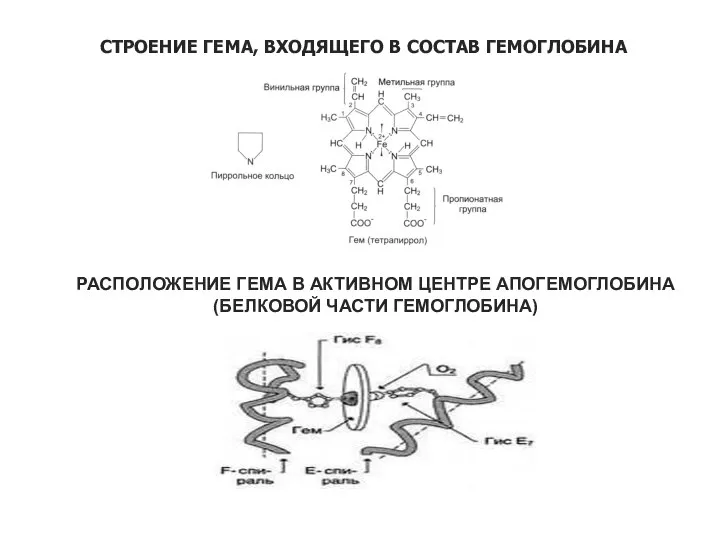
- 40. СТРОЕНИЕ ГЕМА, ВХОДЯЩЕГО В СОСТАВ ГЕМОГЛОБИНА РАСПОЛОЖЕНИЕ ГЕМА В АКТИВНОМ ЦЕНТРЕ АПОГЕМОГЛОБИНА (БЕЛКОВОЙ ЧАСТИ ГЕМОГЛОБИНА)
- 41. ДЕНАТУРАЦИЯ Сравнительно слабые связи, ответственные за стабилизацию вторичной, третичной и четвертичной структуры белка, легко разрушаются, что
- 42. Большинство белков теряют биологическую активность в присутствии кислот или оснований, мочевины, тяжелых металлов (Ag, Pb, Hg),
- 43. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА БЕЛКОВ Белки различаются по своим физико-химическим свойствам. форма молекул (глобулярные и фибриллярные) 2. молекулярная
- 44. Суммарный заряд белковой молекулы зависит от соотношения ионизированных анионных радикалов глутаминовой и аспарагиной кислот и катионных
- 45. Изменение суммарного заряда аминокислот в зависимости от рН среды
- 46. Если полипептидная цепь белка содержит более 200 аминокислот, то ее пространственная структура сформирована в виде двух
- 47. Соединение, с которым взаимодействует белок, называется лигандом (субстраты ферментов, кофакторы (ионы металлов), ингибиторы (ацетилхолин – нейромедиатор,
- 49. Скачать презентацию





































 мочеполовая система
мочеполовая система  Решения для бизнеса. Все адаптив. Landing pages
Решения для бизнеса. Все адаптив. Landing pages Презентация КОВРОВЫЕ ИЗДЕЛИЯ
Презентация КОВРОВЫЕ ИЗДЕЛИЯ знакомство с обощями в стихах - презентация для начальной школы
знакомство с обощями в стихах - презентация для начальной школы Дорожные условия и безопасность движения
Дорожные условия и безопасность движения Античная Философия
Античная Философия Презентация: «Романтизм в западноевропейской культуре XVIII – XIX вв.»
Презентация: «Романтизм в западноевропейской культуре XVIII – XIX вв.» Пуçлансассăн П-пала Шутсăр кирлĕ япала
Пуçлансассăн П-пала Шутсăр кирлĕ япала твёрдые и мягкие звуки - презентация для начальной школы
твёрдые и мягкие звуки - презентация для начальной школы Презентация "Ты украшаешь. Знакомство с Мастером Украшения" - скачать презентации по МХК
Презентация "Ты украшаешь. Знакомство с Мастером Украшения" - скачать презентации по МХК Культура России XVIII века
Культура России XVIII века Узлы элементов
Узлы элементов Саратов и Покровск 19 века.
Саратов и Покровск 19 века. Антенні та фідерні пристрої ЗРЛ. Загальні відомості і принцип дії фідерних пристроїв. (Тема 3.1)
Антенні та фідерні пристрої ЗРЛ. Загальні відомості і принцип дії фідерних пристроїв. (Тема 3.1) Гипоидная передача
Гипоидная передача Энциклопедия слова «Учитель» - презентация для начальной школы_
Энциклопедия слова «Учитель» - презентация для начальной школы_ Презентацию выполил учитель-логопед МК ДОУ «Детский сад № 188» компенсирующего вида Кадырова А.М. г. Новокузнецк 2014
Презентацию выполил учитель-логопед МК ДОУ «Детский сад № 188» компенсирующего вида Кадырова А.М. г. Новокузнецк 2014  Расчетно-графическая работа по системам компьютерной графики
Расчетно-графическая работа по системам компьютерной графики  Педагогика и психология управления
Педагогика и психология управления Самолова Жанна
Самолова Жанна Изобразительный материал-условие развития творческой деятельности дошкольников Педагог доп. образования ГОУ СОШ 2115 Елена
Изобразительный материал-условие развития творческой деятельности дошкольников Педагог доп. образования ГОУ СОШ 2115 Елена  Муса Гареев. Интеллектуальная игра "Что? Где? Когда?"
Муса Гареев. Интеллектуальная игра "Что? Где? Когда?" Раскраска вершин графа
Раскраска вершин графа Питер де Хоох Питер де Хох или де Хоох Родился 20 декабря 1629 в Роттердаме умер после 1684 в Амстердаме — гол
Питер де Хоох Питер де Хох или де Хоох Родился 20 декабря 1629 в Роттердаме умер после 1684 в Амстердаме — гол Презентация на тему "Первая помощь при обморожении и ожоге разных степеней" - скачать презентации по Медицине
Презентация на тему "Первая помощь при обморожении и ожоге разных степеней" - скачать презентации по Медицине Скандинавский календарь
Скандинавский календарь Экологические проблемы Калининградской области
Экологические проблемы Калининградской области Делительные головки
Делительные головки