Содержание
- 2. С пищей в организм поступают разнообразные жирные кислоты, в том числе и незаменимые. Значительная часть заменимых
- 3. Синтез жирных кислот происходит в абсорбтивный период. Активный гликолиз и последующее окислительное декарбоксилирование пирувата способствуют увеличению
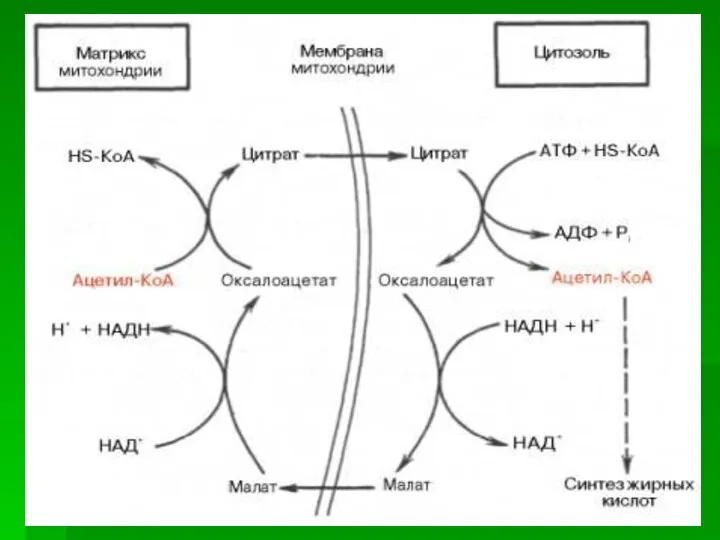
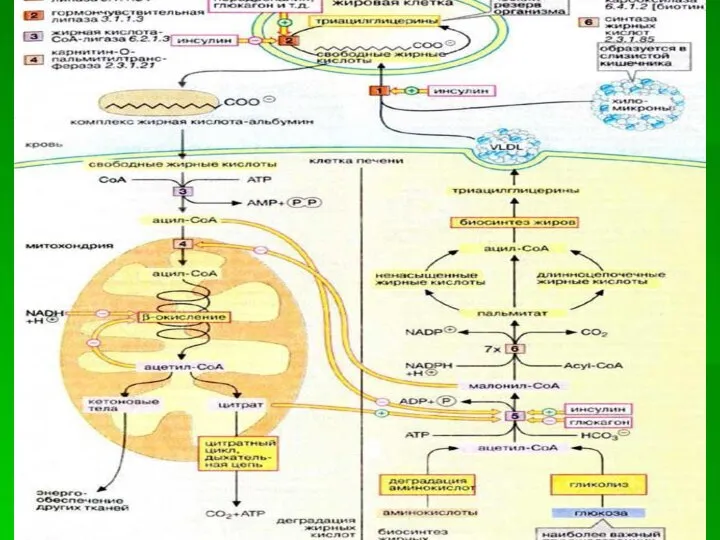
- 4. Синтез жирных кислот происходит в цитозоле клеток, поэтому ацетил-КоА должен транспортироваться через внутреннюю мембрану митохондрий в
- 5. Перенос цитрата в цитоплазму происходит только при увеличении количества цитрата в митохондриях, когда изоцитратдегидрогеназа и α-кетоглутарат-дегидрогеназа
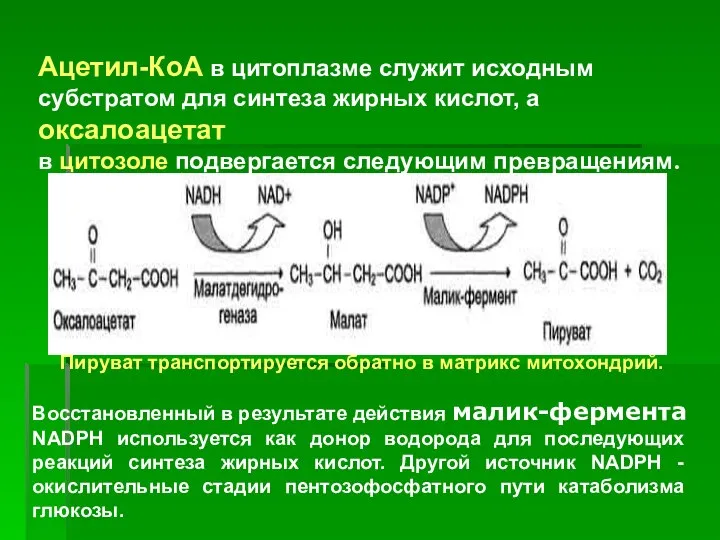
- 6. Ацетил-КоА в цитоплазме служит исходным субстратом для синтеза жирных кислот, а оксалоацетат в цитозоле подвергается следующим
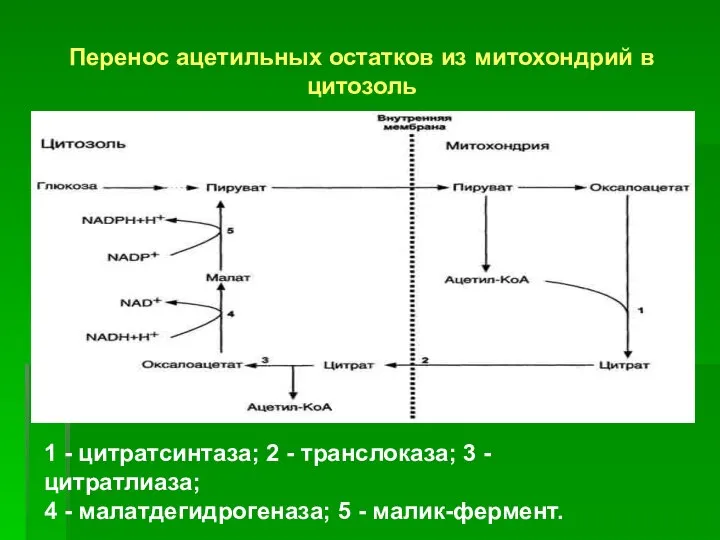
- 7. Перенос ацетильных остатков из митохондрий в цитозоль 1 - цитратсинтаза; 2 - транслоказа; 3 - цитратлиаза;
- 8. Образование малонил-КоА из ацетил-КоА – это первая и регуляторная реакция в биосинтезе жирных кислот. Фермент, катализирующий
- 9. В первой стадии реакции СО2 ковалентно связывается с биотином за счёт энергии АТФ, во второй стадии
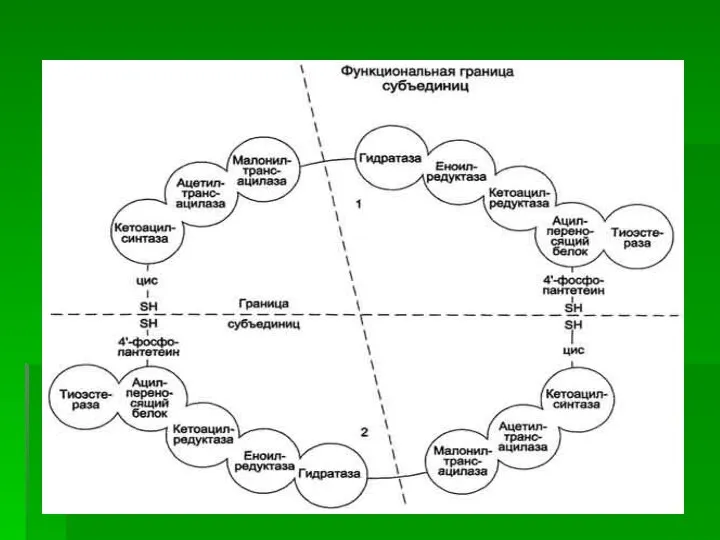
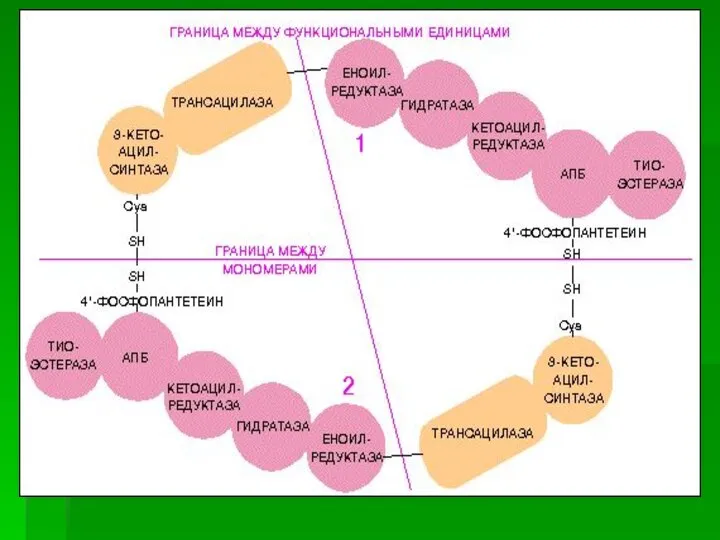
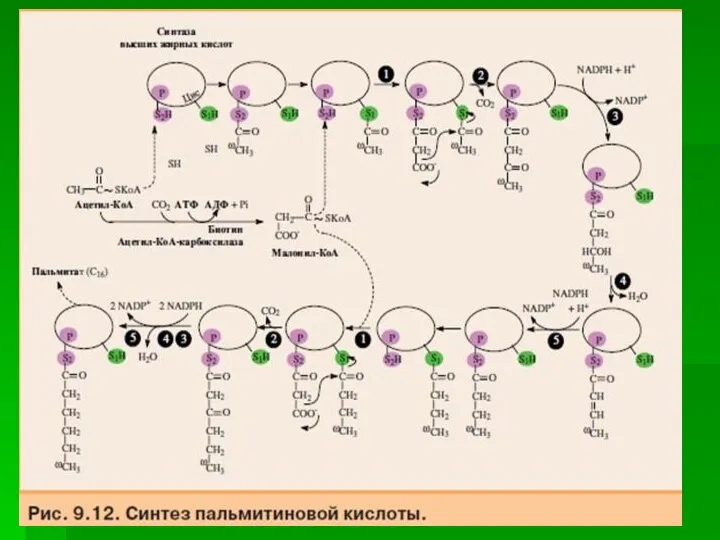
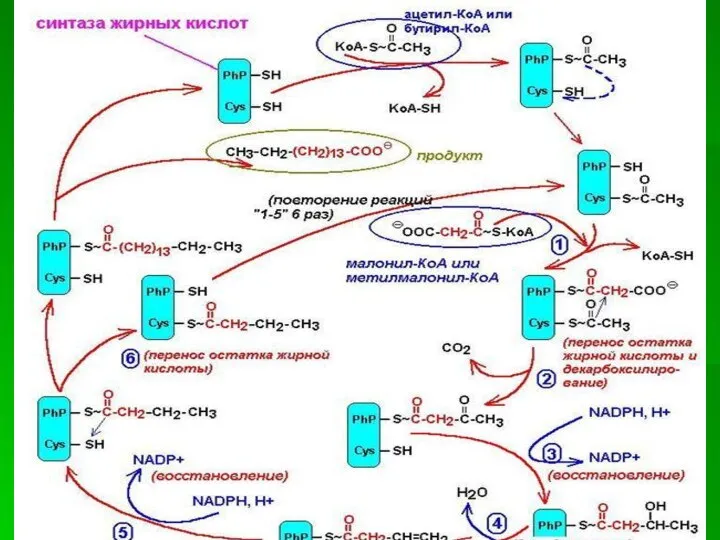
- 10. После образования малонил-КоА синтез жирных кислот продолжается на мультиферментном комплексе - синтазе жирных кислот. Этот фермент
- 14. Суммарная реакция : Ацетил-КоА+7 Малонил-КоА +14 НАДФН2 = ПК+7СО2+7 Н2О + 8 HSKoA +14 НАДФ+
- 18. Каждый мономер содержит все каталитические центры, функционально активен комплекс из 2 протомеров. Поэтому реально синтезируются одновременно
- 19. Этот комплекс последовательно удлиняет радикал жирной кислоты на 2 углеродных атома, донором которых служит малонил-КоА. Конечный
- 20. Первая реакция - перенос ацетильной группы ацетил-КоА на тиоловую группу цистеина ацетилтрансацилазным центром. Затем от малонил-КоА
- 21. Ацетильная группа конденсируется с остатком малонила по месту отделившегося СО2. Реакция катализируется кетоацилсинтазным центром.
- 22. Образовавшийся радикал ацетоацетила последовательно восстанавливается кетоацилредуктазой, затем дегидратируется и опять восстанавливается еноилредуктазой - активными центрами комплекса.
- 23. Перед вторым циклом радикал бутирила переносится туда, где находился ацетил в начале первого цикла реакций. Затем
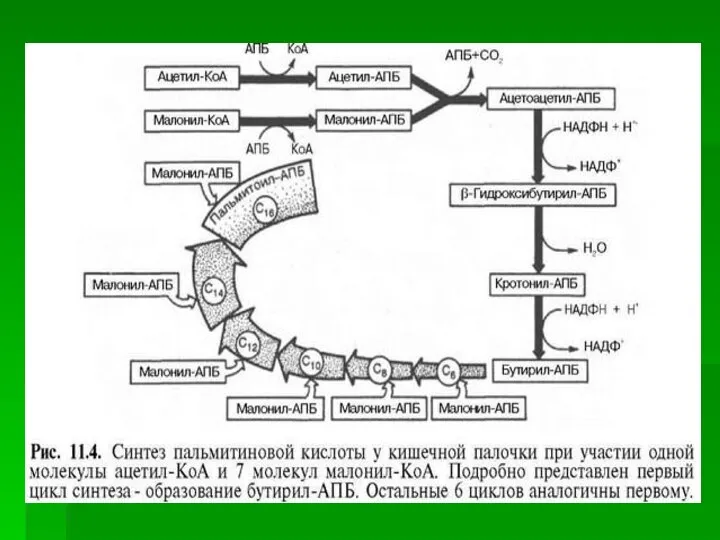
- 24. Аналогичные циклы реакций повторяются до тех пор, пока не образуется радикал пальмитиновой кислоты. Под действием тиоэстеразного
- 25. Суммарное уравнение синтеза пальмитиновой кислоты из ацетил-КоА и малонил-КоА: CH3-CO-SKoA + 7 HOOC-CH2-CO-SKoA + 14 (NADPH
- 27. Основные источники водорода для синтеза жирных кислот В каждом цикле биосинтеза пальмитиновой кислоты проходят 2 реакции
- 28. Общая схема реакций синтеза пальмитиновой кислоты
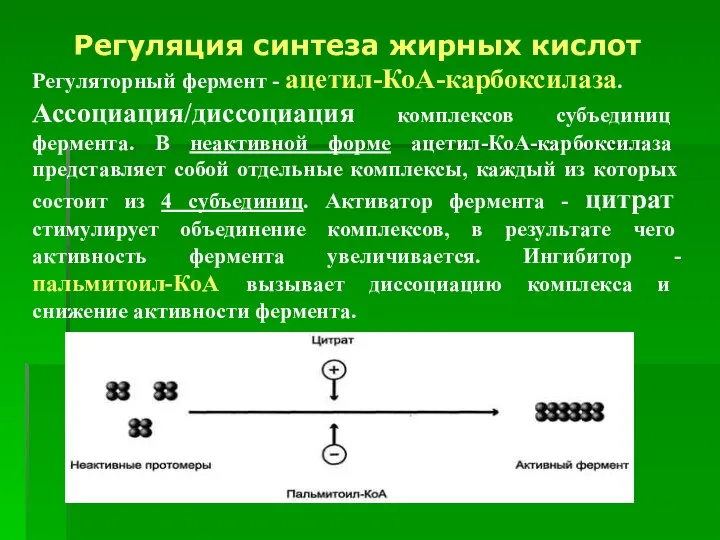
- 29. Регуляция синтеза жирных кислот Регуляторный фермент - ацетил-КоА-карбоксилаза. Ассоциация/диссоциация комплексов субъединиц фермента. В неактивной форме ацетил-КоА-карбоксилаза
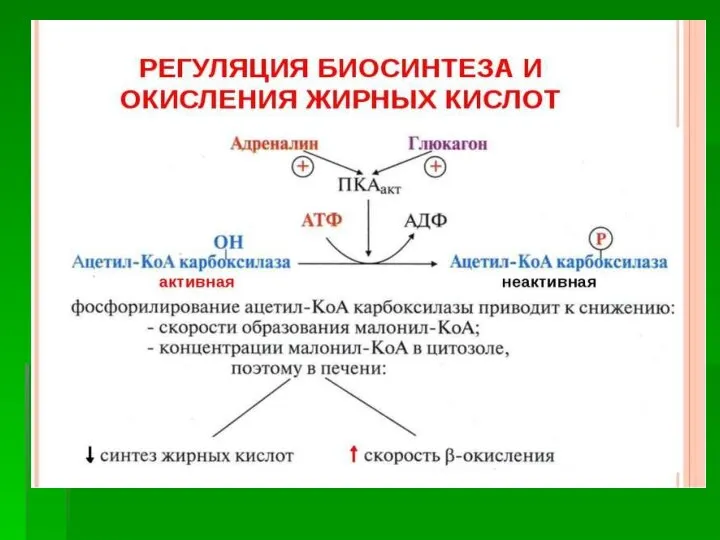
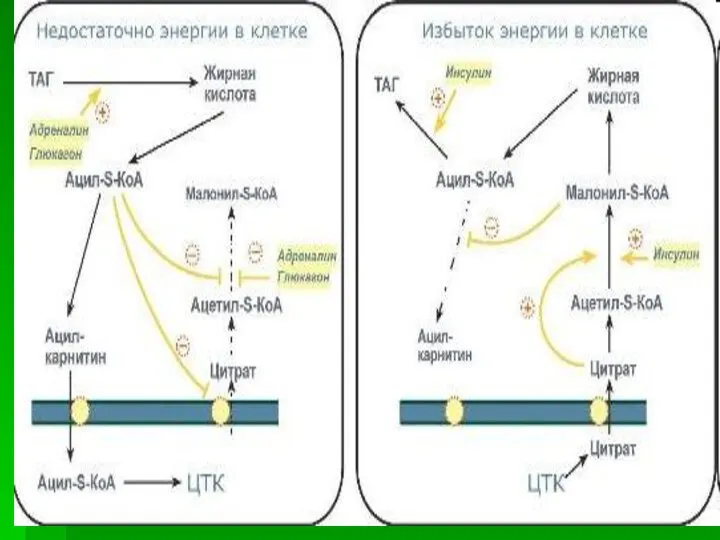
- 30. Фосфорилирование/дефосфорилирование ацетил-КоА-карбоксилазы. В постабсорбтивном состоянии или при физической работе глюкагон/адреналин через аденилат-циклазную систему активируют протеинкиназу А
- 31. Длительное потребление богатой углеводами и бедной жирами пищи приводит к увеличению секреции инсулина, который стимулирует индукцию
- 35. Синтез жирных кислот из пальмитиновой кислоты В ЭР происходит удлинение пальмитиновой кислоты с участием малонил-КоА. Последовательность
- 36. Ферменты могут использовать в качестве субстратов не только пальмитиновую, но и другие жирные кислоты. Поэтому в
- 37. Основной продукт элонгации в печени - стеариновая кислота (С18:0), однако в ткани мозга образуется большое количество
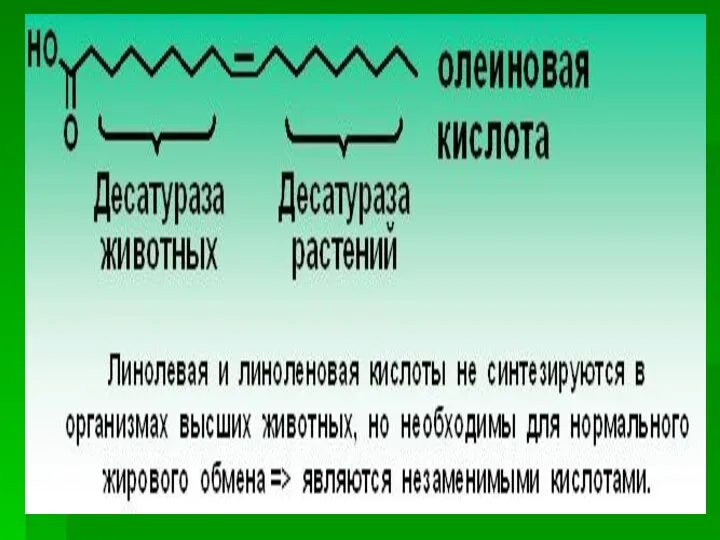
- 38. Включение двойных связей в радикалы жирных кислот называется десатурацией. Основные жирные кислоты, образующиеся в организме человека
- 39. Для образования двойной связи в радикале жирной кислоты требуется молекулярный кислород, NADH, цитохром b5 и FAD-зависимая
- 41. Эйкозаноиды, включающие в себя простагландины - высокоактивные регуляторы клеточных функций. Эйкозаноиды - биологически активные вещества, синтезируемые
- 42. Эйкозаноиды участвуют во многих процессах: регулируют тонус ГМК и вследствие этого влияют на АД, состояние бронхов,
- 43. Такие признаки воспаления, как боль, отёк, лихорадка, в значительной мере обусловлены действием эйкозаноидов. Избыточная секреция эйкозаноидов
- 44. Реакции перекисного окисления липидов
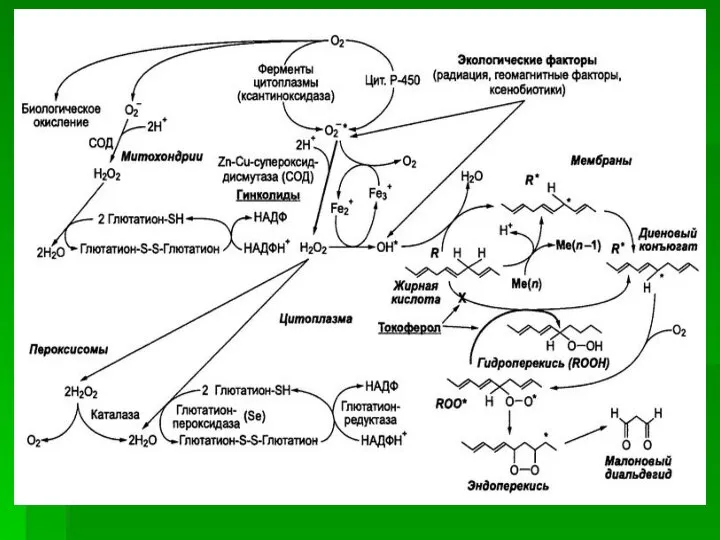
- 45. Перекисное окисление липидов – свободнорадикальное окисление липидов, вызванное пероксидным ионом. При изучении процессов биологического окисления рассматривается
- 46. Перекисное окисление липидов – это цепные реакции, обеспечивающие расширенное воспроизводство свободных радикалов, частиц, имеющих неспаренный электрон,
- 47. Наиболее развита антиоксидантная система в клетках, больше подверженных окислению, где выше парциальное давление кислорода, например, эритроциты,
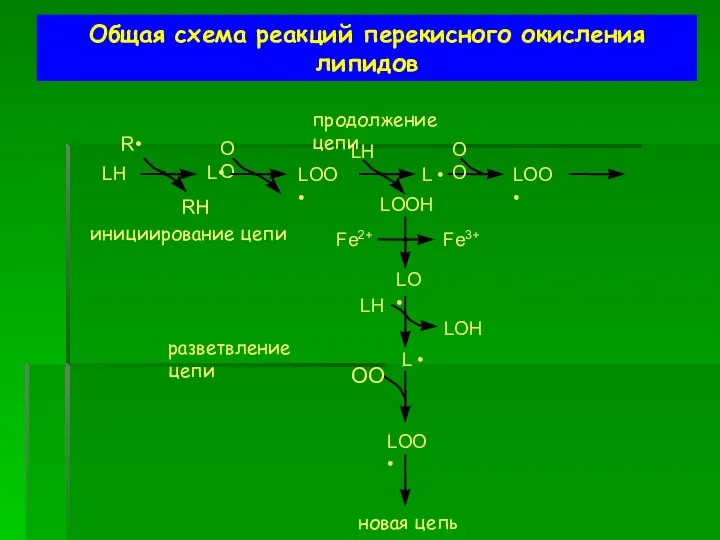
- 48. Общая схема реакций перекисного окисления липидов
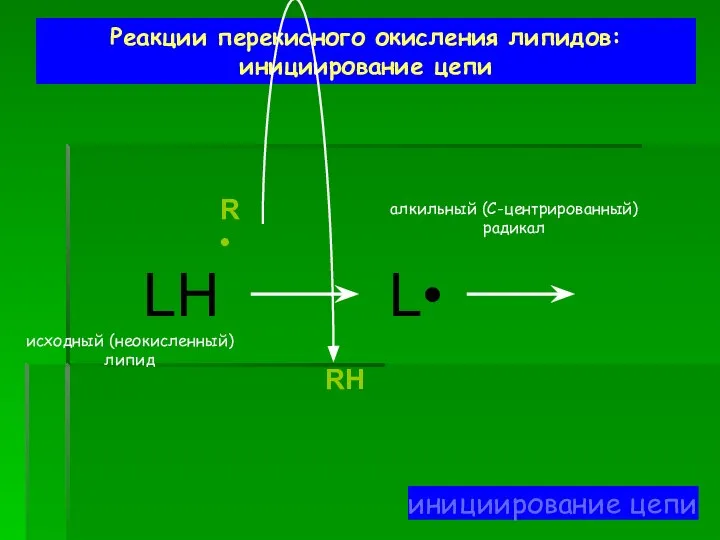
- 49. Реакции перекисного окисления липидов: инициирование цепи
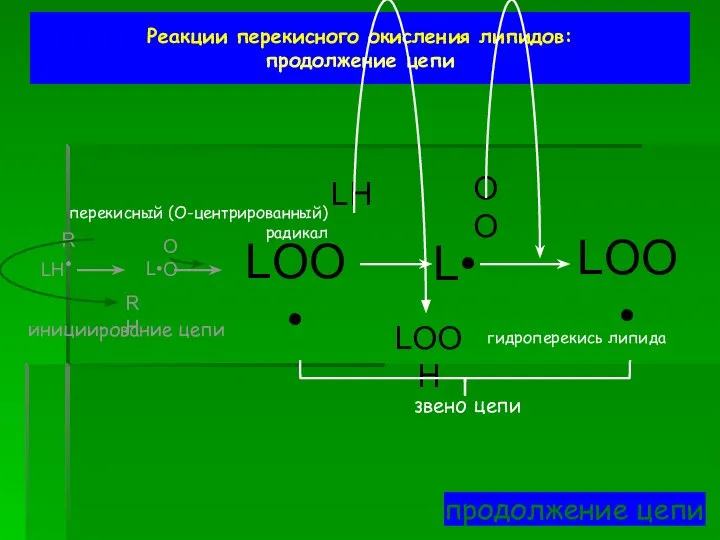
- 50. Реакции перекисного окисления липидов: продолжение цепи
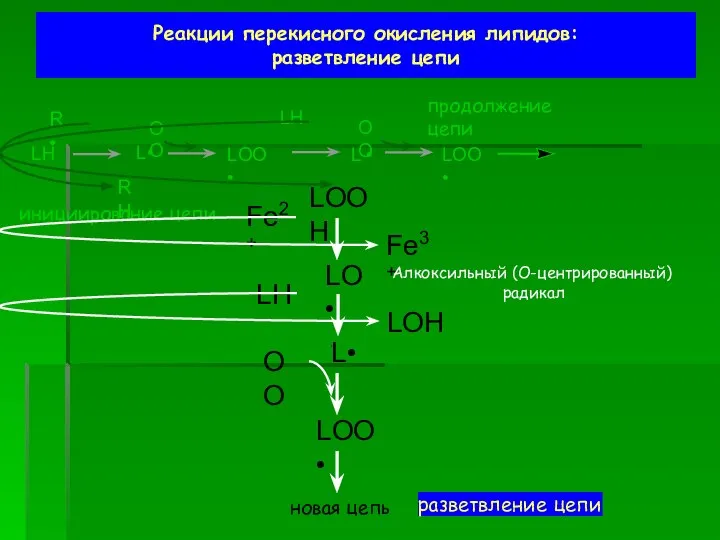
- 51. Реакции перекисного окисления липидов: разветвление цепи
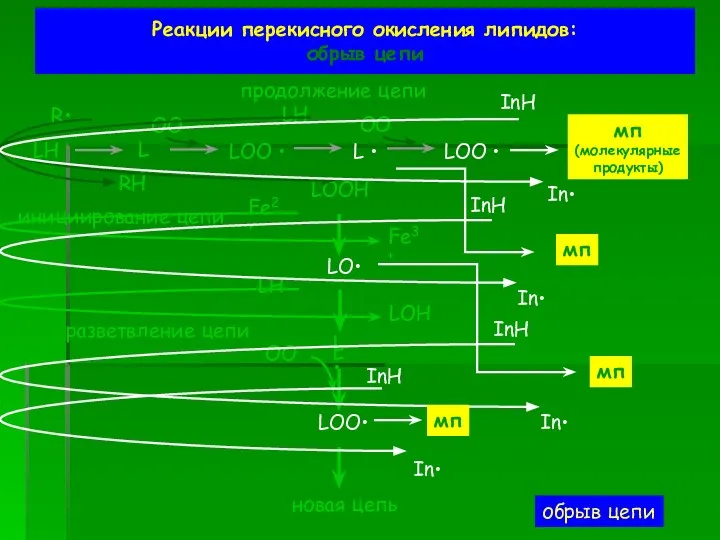
- 52. Реакции перекисного окисления липидов: обрыв цепи
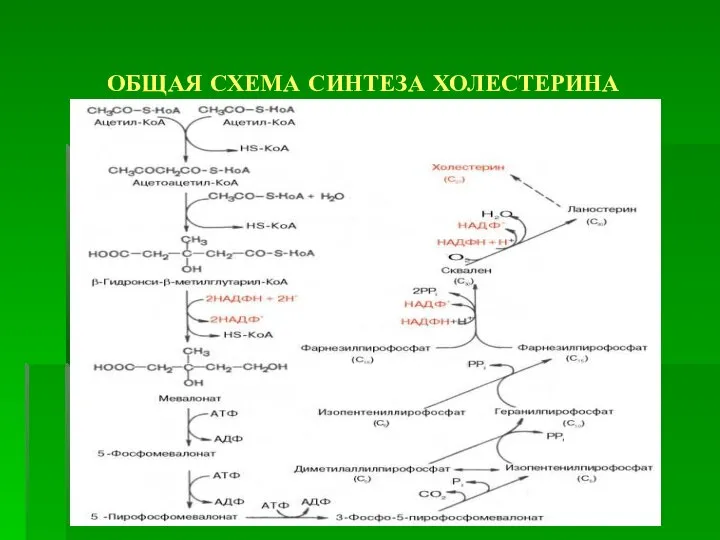
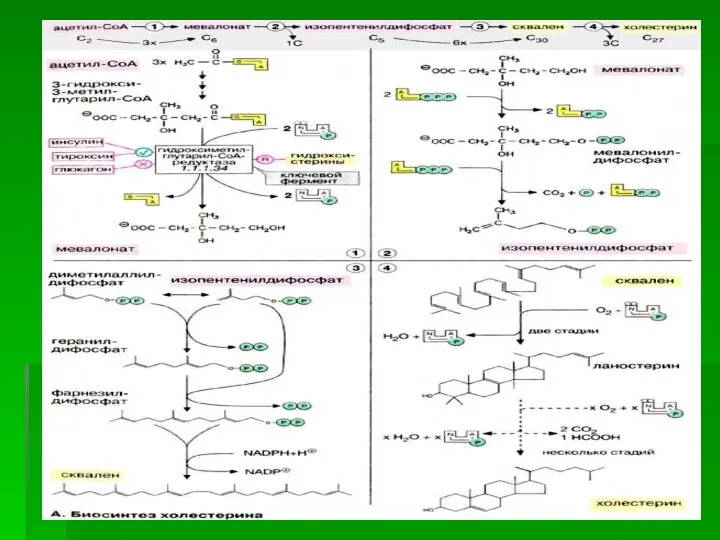
- 54. БИОСИНТЕЗ ХОЛЕСТЕРИНА В синтезе холестерина можно выделить три основные стадии: I – превращение активного ацетата в
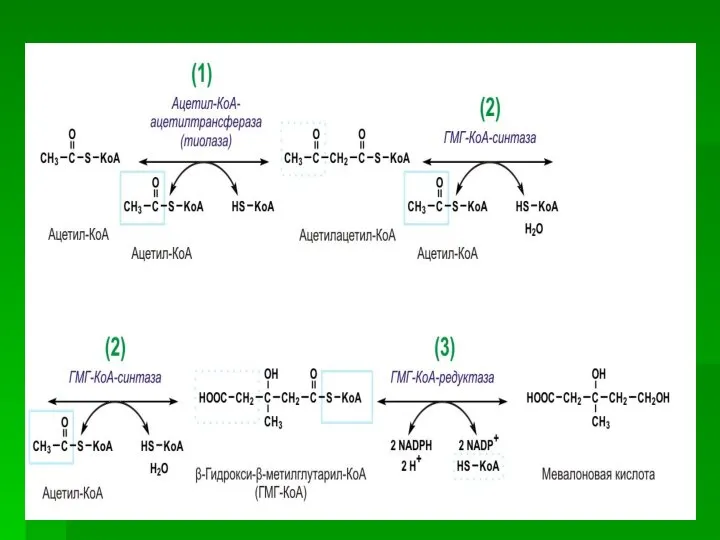
- 55. I стадия Начальным этапом синтеза мевалоновой кислоты из ацетил-КоА является образование ацетоацетил-КоА посредством обратимой тиолазной реакции:
- 56. В результате конденсации ацетоацетил-КоА с 3-й молекулой ацетил-КоА при участии гидроксиметилглутарил-КоА-синтазы (ГМГ-КоА-синтаза) образуется β-гидрокси-β-метилглутарил-КоА:
- 57. β-Гидрокси-β-метилглутарил-КоА под действием регуляторного фермента НАДФ-зависимой гидроксиметилглутарил-КоА-редуктазы (ГМГ-КоА- редуктаза) в результате восстановления одной из карбоксильных групп
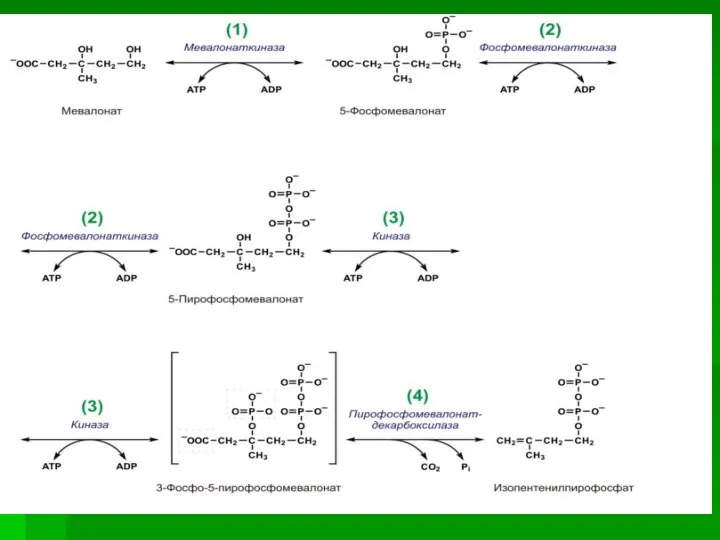
- 59. II стадия Мевалоновая кислота превращается в сквален. Реакции II стадии начинаются с фосфорилирования мевалоновой кислоты с
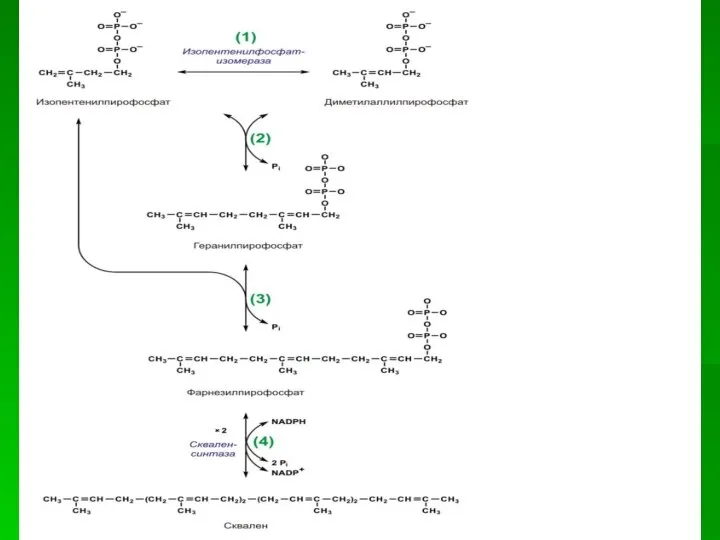
- 60. Оба изомерных изопентенилпирофосфата (диметилаллилпирофосфат и изопентенилпирофосфат) конденсируются с высвобождением пирофосфата и образованием геранилпирофосфата:
- 61. К геранилпирофосфату вновь присоединяется изопентенилпирофосфат. В результате этой реакции образуется фарнезилпирофосфат Фарнезилдифосфат является также исходным соединением
- 63. В заключительной реакции данной стадии в результате НАДФН-зависимой восстановительной конденсации 2 молекул фарнезилпирофосфата образуется сквален:
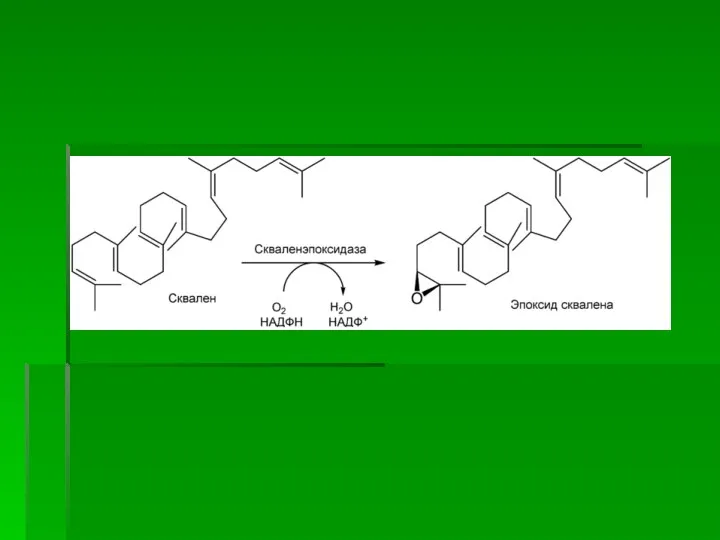
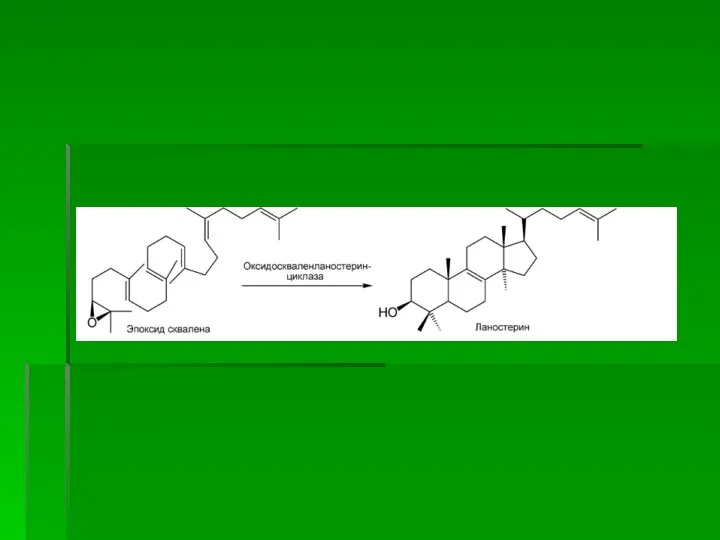
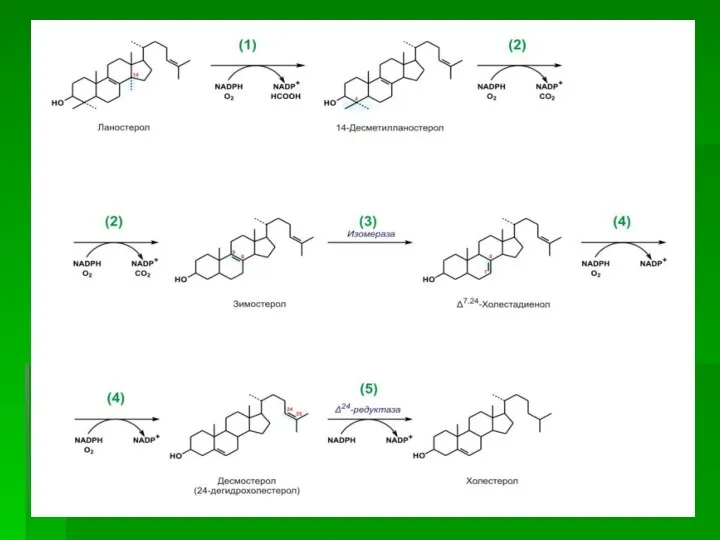
- 65. III стадия Сквален, линейный изопреноид, под влиянием сквален-оксидоциклазы циклизируется с потреблением кислорода в ланостерин, С 30
- 69. ОБЩАЯ СХЕМА СИНТЕЗА ХОЛЕСТЕРИНА
- 71. Липолиз Распад липидов в тканях осуществляют гидролитические ферменты– липазы. Три-, ди- и моноглицеридлипазы действуют на нейтральные
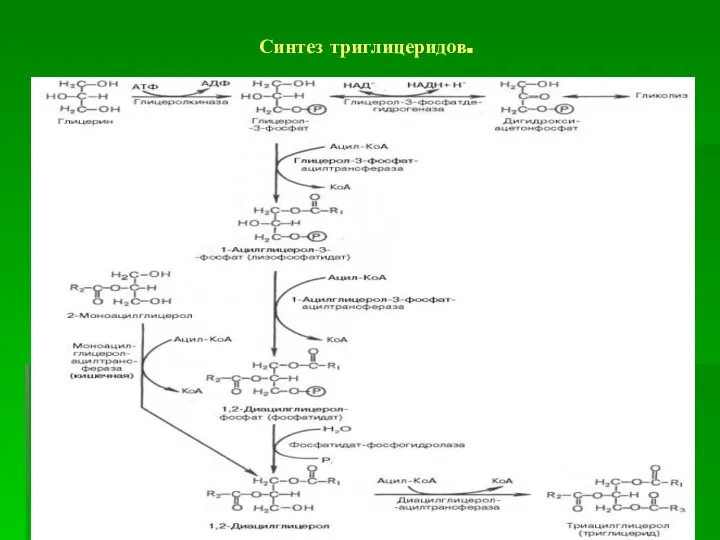
- 72. Синтез триглицеридов.
- 74. Скачать презентацию











































 Религиозная философия
Религиозная философия Доклад «Причины неуспеваемости школьников: анализ отечественного опыта».
Доклад «Причины неуспеваемости школьников: анализ отечественного опыта». Масленица
Масленица Родительское собрание «Как готовить домашнее задание» Редкий родитель не сталкивается с проблемой приготовления уроков дома. - &
Родительское собрание «Как готовить домашнее задание» Редкий родитель не сталкивается с проблемой приготовления уроков дома. - & Спортивно-оздоровительный выезд студентов «Поезд здоровья – 2016»
Спортивно-оздоровительный выезд студентов «Поезд здоровья – 2016» Судебная доктрина деловой цели: применение в российской практике
Судебная доктрина деловой цели: применение в российской практике Доверительный маркетинг Презентацию подготовила Свинарчук Е.И.
Доверительный маркетинг Презентацию подготовила Свинарчук Е.И. Разработка базы для информационной системы брикетировочного цеха завода «Эковер» по утилизации отходов минераловатного произв
Разработка базы для информационной системы брикетировочного цеха завода «Эковер» по утилизации отходов минераловатного произв Политические режимы
Политические режимы Презентация ВАЖНЕЙШИЕ ФАКТОРЫ РАЗВИТИЯ УПРАВЛЕНЧЕСКОЙ МЫСЛИ В РОССИИ XVII в
Презентация ВАЖНЕЙШИЕ ФАКТОРЫ РАЗВИТИЯ УПРАВЛЕНЧЕСКОЙ МЫСЛИ В РОССИИ XVII в Гармонические функции
Гармонические функции Экологическое законодательство Российской Федерации
Экологическое законодательство Российской Федерации Органайзер студента
Органайзер студента Образ учителя
Образ учителя  Ақпаратты енгізу, шығару. Сызықтық программаны құру
Ақпаратты енгізу, шығару. Сызықтық программаны құру Студия Calligraphy Курган. Каллиграфия
Студия Calligraphy Курган. Каллиграфия Внеурочная деятельность образовательного учреждения Внеурочная деятельность образовательного учреждения для реализации ФГОС
Внеурочная деятельность образовательного учреждения Внеурочная деятельность образовательного учреждения для реализации ФГОС 1615-2027
1615-2027 Аттестационная работа. Метеоцентр «Народные приметы»
Аттестационная работа. Метеоцентр «Народные приметы» Презентация на тему "Целиакия" - скачать презентации по Медицине
Презентация на тему "Целиакия" - скачать презентации по Медицине Классификация промзданий. Экзамен
Классификация промзданий. Экзамен Презентация Технологический процесс выхода предприятия на внешний рынок
Презентация Технологический процесс выхода предприятия на внешний рынок  Национализм как идеология
Национализм как идеология Политические партии и движения, их классификация
Политические партии и движения, их классификация Правовое регулирование перевозок груза воздушным транспортом Подготовила студентка группы Ю121б Сутуло Юлия
Правовое регулирование перевозок груза воздушным транспортом Подготовила студентка группы Ю121б Сутуло Юлия Численное интегрирование
Численное интегрирование  Храмовый синтез искусства
Храмовый синтез искусства Ожирение. патогенез, клиника, лечение
Ожирение. патогенез, клиника, лечение