Содержание
- 2. Коррозия – разрушение металла в результате его физико-химического взаимодействия с окружающей средой
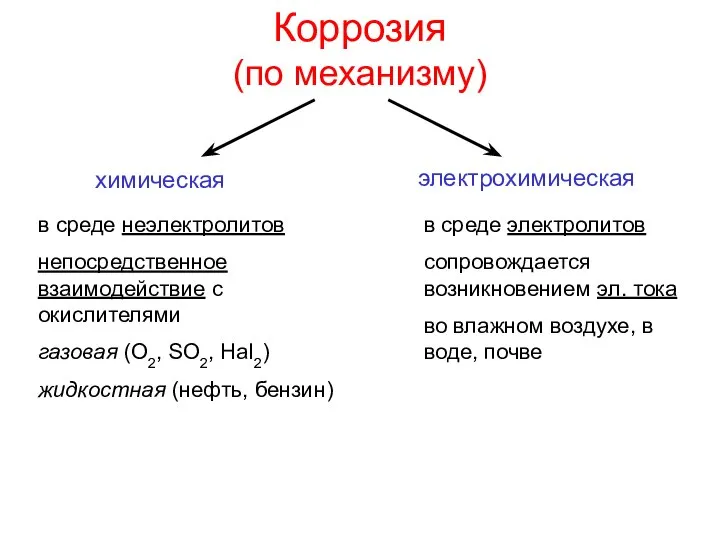
- 3. Коррозия (по механизму) химическая электрохимическая в среде неэлектролитов непосредственное взаимодействие с окислителями газовая (O2, SO2, Hal2)
- 4. Электрохимическая коррозия Микрогальванический элемент анод – более активный металл катод – менее активный металл (электроны связываются
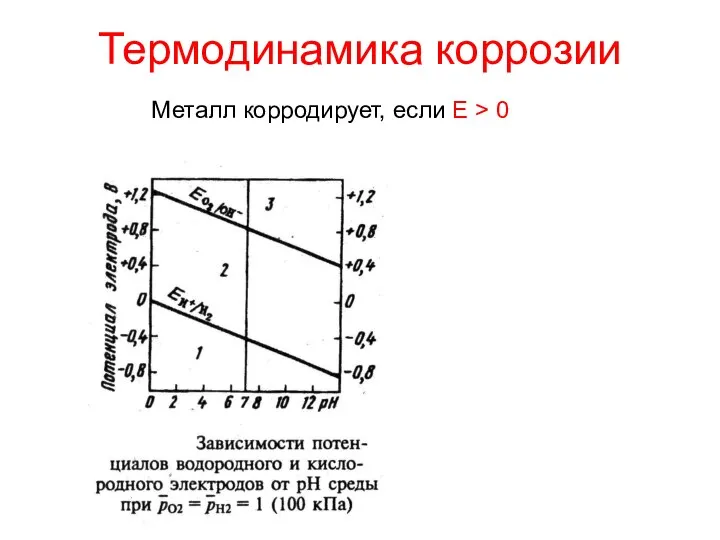
- 5. Термодинамика коррозии Металл корродирует, если E > 0
- 6. Э/х коррозия (по характеру среды) атмосферная солевая (морская, речная) почвенная биокоррозия электрокоррозия
- 7. Э/х коррозия (по характеру разрушений) сплошная – вся поверхность металла местная – отдельные участки поверхности точечная
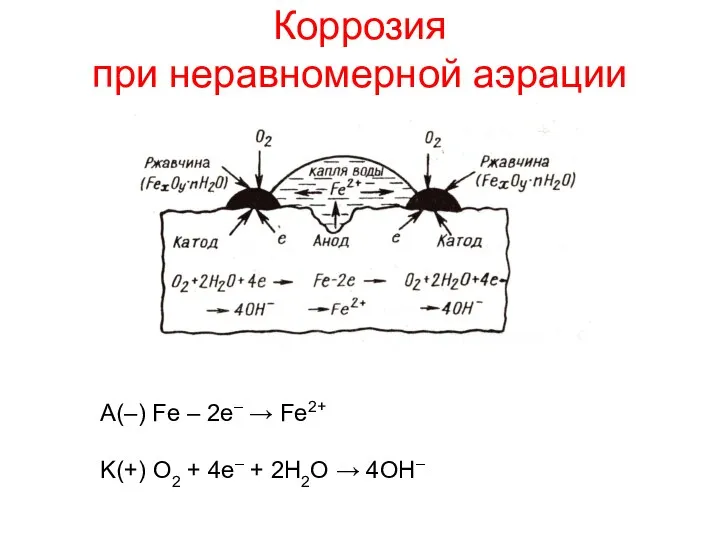
- 8. Коррозия при неравномерной аэрации А(–) Fe – 2e– → Fe2+ K(+) O2 + 4e– + 2H2O
- 9. Способы защиты от коррозии Нанесение покрытий Легирование металлов Электрохимическая защита Изменение свойств коррозионной среды
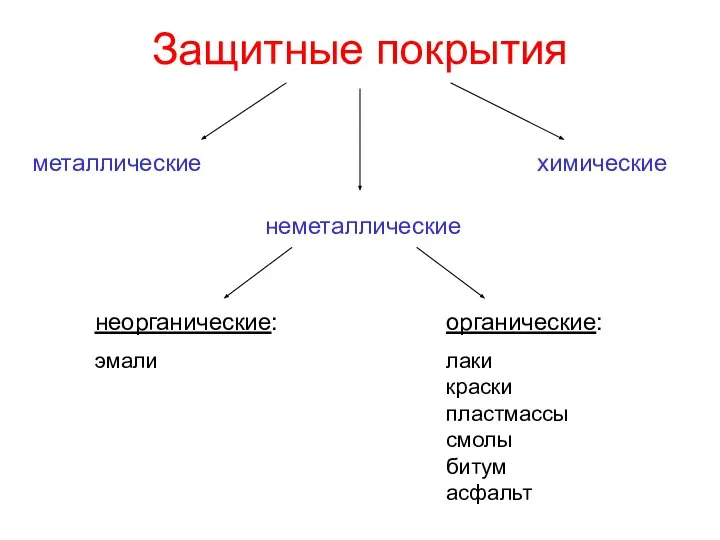
- 10. Защитные покрытия металлические неметаллические химические неорганические: эмали органические: лаки краски пластмассы смолы битум асфальт
- 11. Химические покрытия Химическая обработка поверхности металла с целью получения пленки, устойчивой к коррозии Оксидирование – получение
- 12. Металлические покрытия Анодное покрытие – покрытие металлом, с более отрицательным потенциалом Оцинкованное железо А(–) Zn –
- 13. Легирование металлов Введение в сплав компонентов (Cr, Ni, Al, Pb, Mo, Mn, W), повышающих коррозионную стойкость
- 14. Сплавы
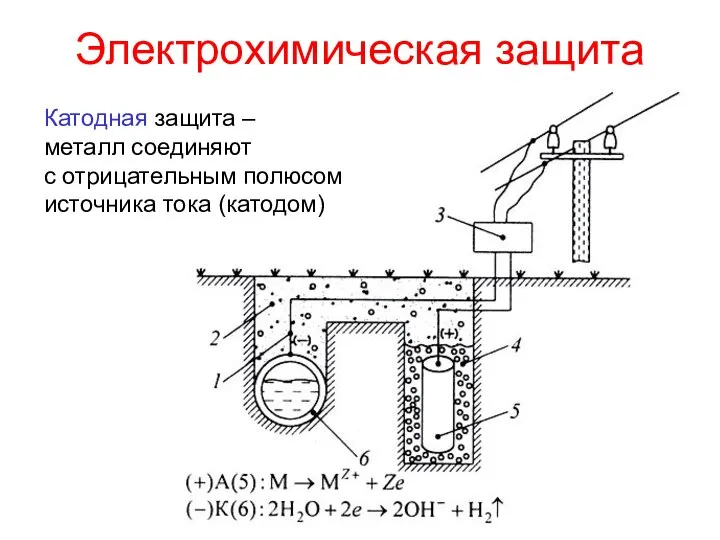
- 15. Электрохимическая защита Катодная защита – металл соединяют с отрицательным полюсом источника тока (катодом)
- 16. Электрохимическая защита Протекторная защита – к изделию присоединяют металл с более отрицательным потенциалом (Zn, Mg, Al)
- 17. Изменение свойств коррозионной среды Введение ингибиторов коррозии Адсорбционные ингибиторы (диэтиламин, уротропин) Пассивационные ингибиторы (Na2Cr2O7, NaNO2, Na2SiO3)
- 18. Коррозия под действием блуждающих токов "Вход" тока – катодный участок, "выход" тока – анодный участок (корродирует)
- 20. Скачать презентацию












 Бизнес-курс. Начало. Этапы прохождения курса
Бизнес-курс. Начало. Этапы прохождения курса Новогодние традиции разных стран мира
Новогодние традиции разных стран мира Деление тяжелых атомных ядер под действием протонов, дейтронов, γ-квантов и -частиц
Деление тяжелых атомных ядер под действием протонов, дейтронов, γ-квантов и -частиц Требования к программному обеспечению и их анализ
Требования к программному обеспечению и их анализ Теория кодирования
Теория кодирования Основные понятия механики материалов (введение в механику материалов)
Основные понятия механики материалов (введение в механику материалов) Презентация Сущность банковского мультипликатора
Презентация Сущность банковского мультипликатора Сборочные чертежи. Разъёмные и неразъёмные соединения деталей
Сборочные чертежи. Разъёмные и неразъёмные соединения деталей Основные направления состояния и развития современной праздничной культуры на Дальнем Востоке
Основные направления состояния и развития современной праздничной культуры на Дальнем Востоке Системы здравоохранения в различных странах мира Системы здравоохранения в различных странах мира Манерова Ольга Александ
Системы здравоохранения в различных странах мира Системы здравоохранения в различных странах мира Манерова Ольга Александ Разработка вертикально-сверлильного станка
Разработка вертикально-сверлильного станка Волейбол. Правила игры
Волейбол. Правила игры Виды обмоток якоря электрических машин постоянного тока
Виды обмоток якоря электрических машин постоянного тока Элементы ЯПВУ. Файлы. И+ПРГ. C/C++
Элементы ЯПВУ. Файлы. И+ПРГ. C/C++ КОНФИДЕНЦИАЛЬНО: УСТАНОВЛЕНИЕ ПРОГРАММЫ ЗАЩИТЫ КОММЕРЧЕСКИХ ТАЙН B КОМПАНИИ д.ю.н. Янушаускайте Кристина ВОИС Программа обуч
КОНФИДЕНЦИАЛЬНО: УСТАНОВЛЕНИЕ ПРОГРАММЫ ЗАЩИТЫ КОММЕРЧЕСКИХ ТАЙН B КОМПАНИИ д.ю.н. Янушаускайте Кристина ВОИС Программа обуч Традиции и обычаи Башкирского народа
Традиции и обычаи Башкирского народа Пористые заполнители для легких бетонов
Пористые заполнители для легких бетонов Портрет Урок на тему:” Портрет.Рисование головы человека”»
Портрет Урок на тему:” Портрет.Рисование головы человека”» Задачи - по двум разностям - презентация для начальной школы
Задачи - по двум разностям - презентация для начальной школы Побережье Тамани. Атамань – этнографический музей под открытым небом
Побережье Тамани. Атамань – этнографический музей под открытым небом Информационные технологии. Visual Basic
Информационные технологии. Visual Basic Алгоритмы и программирование
Алгоритмы и программирование Методическая разработка факультативов по истории Беларуси из опыта работы учителя истории Песенко И.Э. Бобруйск-2009
Методическая разработка факультативов по истории Беларуси из опыта работы учителя истории Песенко И.Э. Бобруйск-2009 КЛАССНЫЙ ЧАС И ЕГО РОЛЬ В ВОСПИТАНИИ УЧАЩИХСЯ Классный час как основной элемент системы работы классного руководителя
КЛАССНЫЙ ЧАС И ЕГО РОЛЬ В ВОСПИТАНИИ УЧАЩИХСЯ Классный час как основной элемент системы работы классного руководителя Lektsia_01_8
Lektsia_01_8 Моделирование на UML. Моделирование использования. Лекция 3
Моделирование на UML. Моделирование использования. Лекция 3 Разминка по философии На тему: «Сферы общественной жизни» Мб 02/1302 Тархов Сергей
Разминка по философии На тему: «Сферы общественной жизни» Мб 02/1302 Тархов Сергей Исследование математических моделей
Исследование математических моделей