Содержание
- 2. Тема 11. Феноменологическая термодинамика (ТД) 1. Термодинамическая система (ТДС). 2. Энергия термодинамической системы, работа и теплота.
- 3. 1 учебный вопрос: Термодинамическая система (ТДС). Пример – газ в цилиндре под поршнем. Параметры состояния ТДС:
- 4. ТДС, в которых параметры состояния имеют определенные значения, одинаковые по всей системе и не меняющиеся со
- 6. Термодинамический процесс (ТДП) – переход ТДС из одного состояния в другое. ТДП изображается графически на диаграммах.
- 7. Равновесные процессы обратимы.
- 9. 2 учебный вопрос: Энергия термодинамической системы, работа и теплота. Энергия – это количественная мера движения материи.
- 10. U газа включает: - кинетическую энергию поступательного и вращательного движения молекул; - кинетическую энергию колебательного движения
- 11. Внутренняя энергия идеального газа: (МКТ17) Работа – это способ передачи энергии, связанный с изменением внешних параметров
- 12. Работа A Элементарная работа Работа при конечном изменении V Геометрический смысл – работу можно представить как
- 13. Теплота Q (количество теплоты) – процесс передачи энергии от одних тел к другим за счет обмена
- 14. Теплоемкость Передача тепловой энергии (теплоты) сопровождается изменением температуры тела. Теплоемкость С – скалярная физическая величина, характеризующая
- 15. Полная теплоемкость (теплоемкость тела) спол численно равна количеству тепла, которое необходимо сообщить системе, чтобы повысить ее
- 16. Молярная теплоемкость С - теплоемкость одного моля вещества: (5) (4) и (5) → (6)
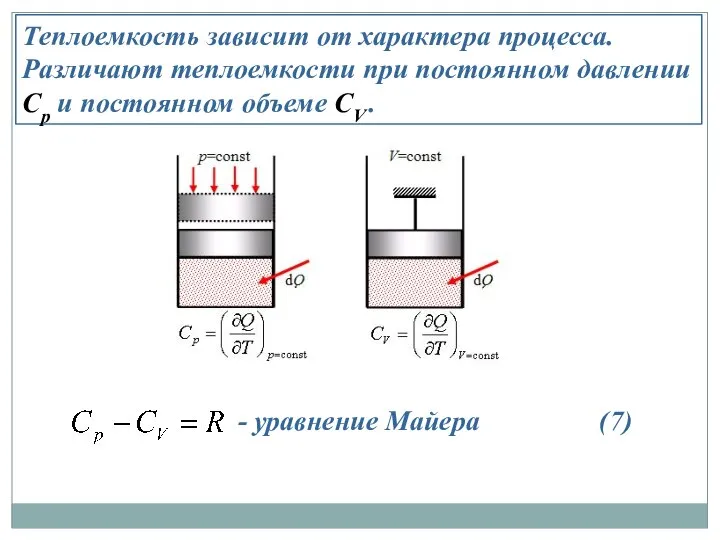
- 17. Теплоемкость зависит от характера процесса. Различают теплоемкости при постоянном давлении Cp и постоянном объеме CV .
- 18. (8) (9) (10)
- 19. 3 учебный вопрос: Первое начало термодинамики В основе термодинамики лежат два закона – два начала термодинамики.
- 20. Количество теплоты, сообщенное системе, идет на приращение ее внутренней энергии и на совершение работы над внешними
- 21. Если система работает по замкнутому термодинамическому процессу (циклу), то В тепловых двигателях невозможно совершить работу, превышающую
- 22. Вычисление теплоемкостей Ср , СV 1. Изохорный процесс (V = const) (МКТ17) (12) (13), (13а) (10)
- 23. 2. Изобарный процесс (p = const) (14) (10) (13) (М-К)
- 24. Пусть (15) (16), (16а) Майер (12), (14)→ (17)
- 27. 4 учебный вопрос: Основные термодинамические процессы(ТДП) идеального газа. Политропный процесс Изотермич. T=const Изобарный p=const Адиабати-ческий Q=0
- 28. Политропным называется равновесный обратимый процесс, удовлетворяющий условиям: 1. рабочее тело – идеальный газ; 2. z −
- 29. 1 начало ТД + ур-е М-К => (19) (20) где (21) уравнения политропы показатель политропы (22)
- 30. Теплота в политропном процессе Работа в политропном процессе (23) (24а) (24б) (10) (22) (19) (М-К)
- 31. Частные случаи политропного процесса а) − изобарный процесс (25а)
- 32. Частные случаи политропного процесса б) − изотермич. процесс Это бесконечно медленный процесс (25б)
- 33. Частные случаи политропного процесса в) − изохорный процесс т.е. все подводимое тепло идет на увеличение внутренней
- 34. Частные случаи политропного процесса г) − адиабатный процесс Это бесконечно быстрый процесс (25г) т.е. работа расширения
- 35. 5 учебный вопрос: Тепловые и холодильные машины. Цикл Карно. Циклом называется круговой процесс, при котором система,
- 36. Nicolas Léonard Sadi Carnot 1 июня 1796 - 24 августа 1832 Теорема Карно: Единственный обратимый процесс
- 37. К.П.Д. цикла Карно Ац = А12 + А23 + А34 + А41 (27)
- 38. КПД тепловой машины, работающей по циклу Карно, не зависит от рода рабочего тела, а зависит только
- 39. 6 учебный вопрос: Энтропия. Второе начало термодинамики. Энтропией называется отношение теплоты, подводимой к термодинамической системе в
- 40. Свойства энтропии 1. В отличие от теплоты, энтропия является функцией состояния, т.е. приращение энтропии не зависит
- 41. Свойства энтропии 2. В ходе необратимого процесса энтропия изолированной системы возрастает: dS>0. 3. Энтропия изолированной системы,
- 42. Теорема Нернста позволяет вычислить энтропию: (30) где c(T) – теплоемкость при заданной температуре
- 43. Второе начало ТД устанавливает направление протекания тепловых процессов. Формулировка немецкого физика Р. Клаузиуса: Невозможен процесс, единственным
- 44. Второе начало ТД – формулировка через энтропию: Все самопроизвольно протекающие процессы в замкнутой системе, приближающие систему
- 45. Энтропия возрастает только в неравновесном процессе. Ее увеличение происходит до тех пор, пока система не достигнет
- 54. Скачать презентацию















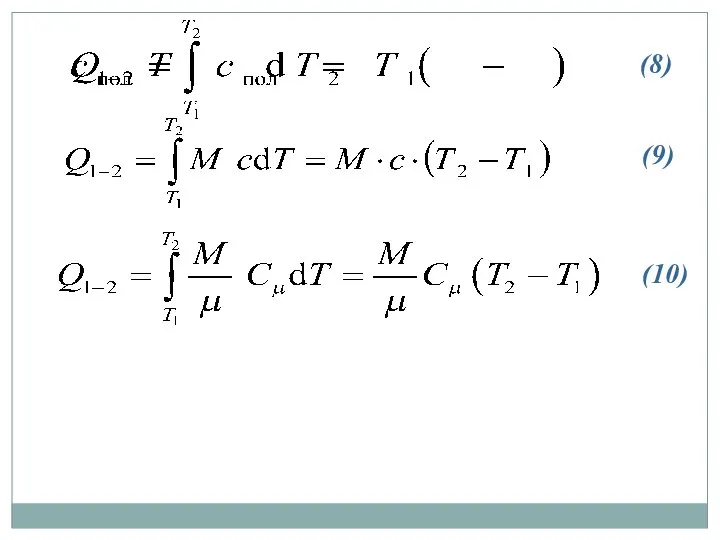


































 Факторы, повышающие интенсивность химического процесса
Факторы, повышающие интенсивность химического процесса Презентация по физике "Сади Карно" - скачать
Презентация по физике "Сади Карно" - скачать  Геометрическая оптика
Геометрическая оптика Торричели Подготовила Ученица 7в класса Толпыгина Виктория
Торричели Подготовила Ученица 7в класса Толпыгина Виктория Кинематика жидкости, как конвенция
Кинематика жидкости, как конвенция Зависимость силы тока от напряжения. Сопротивление проводника
Зависимость силы тока от напряжения. Сопротивление проводника Механическая и электромагнитная картины мира
Механическая и электромагнитная картины мира Экситонные поляритоны в полупроводниковом микрорезонаторе
Экситонные поляритоны в полупроводниковом микрорезонаторе И. Кеплер, его вклад в развитие механики
И. Кеплер, его вклад в развитие механики Тема урока Сообщающиеся сосуды Школа №13 8 класс Васильева М.В. 2008 год
Тема урока Сообщающиеся сосуды Школа №13 8 класс Васильева М.В. 2008 год Презентация Электромагнитная индукция
Презентация Электромагнитная индукция Биологическое действие радиации. Закон радиоактивного распада
Биологическое действие радиации. Закон радиоактивного распада Кривошипно-шатунный механизм двигателя. Назначение и характеристика
Кривошипно-шатунный механизм двигателя. Назначение и характеристика Трехфазные и магнитные цепи. Основные понятия и определения
Трехфазные и магнитные цепи. Основные понятия и определения Квантовая радиофизика. Лекция 4. Спектроскопия ЯМР
Квантовая радиофизика. Лекция 4. Спектроскопия ЯМР Отличии реальных и идеальных газов
Отличии реальных и идеальных газов Электротехника и электроника
Электротехника и электроника Синтез зубчатых передач
Синтез зубчатых передач Определение показателя преломления стекла. Лабораторная работа
Определение показателя преломления стекла. Лабораторная работа Лазер
Лазер Нелинейные геометрии. История создания общей теории относительности. (Часть 1)
Нелинейные геометрии. История создания общей теории относительности. (Часть 1) Влажность воздуха
Влажность воздуха Молекулярно-кинетические свойства коллоидных систем
Молекулярно-кинетические свойства коллоидных систем Ультрафиолетовое излучение
Ультрафиолетовое излучение Газовые законы. Основное уравнение состояния газа
Газовые законы. Основное уравнение состояния газа Юнг тәжірибесі
Юнг тәжірибесі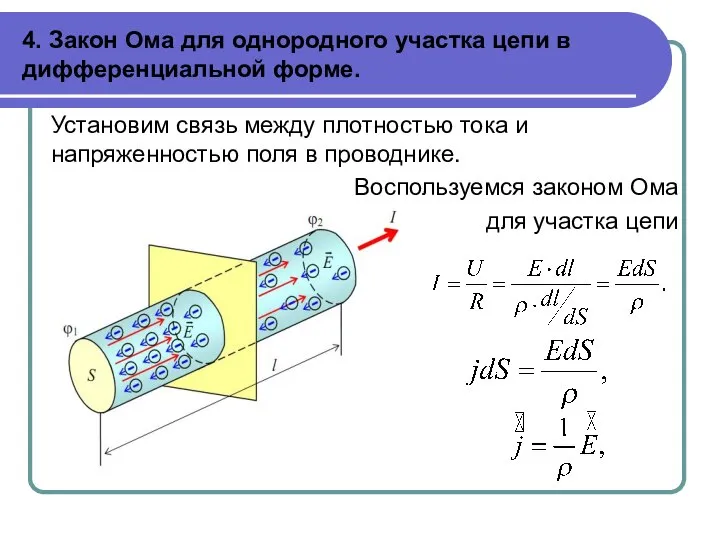 Закон Ома для однородного участка цепи в дифференциальной форме
Закон Ома для однородного участка цепи в дифференциальной форме Изучение астроклиматических характеристик города Петропавловска
Изучение астроклиматических характеристик города Петропавловска