Содержание
- 2. 1. Скорости газовых молекул. Опыт Штерна В средине XIX века была сформулирована молекулярно-кинетическая теория, но тогда
- 3. Теоретики первыми нашли выход. Из уравнения молекулярно-кинетической теории газов известно, что Отсюда среднеквадратичная скорость равна:
- 4. Например, при плотности азота, равной 1,25 кг/м3, при t = 0° С и , скорости молекул
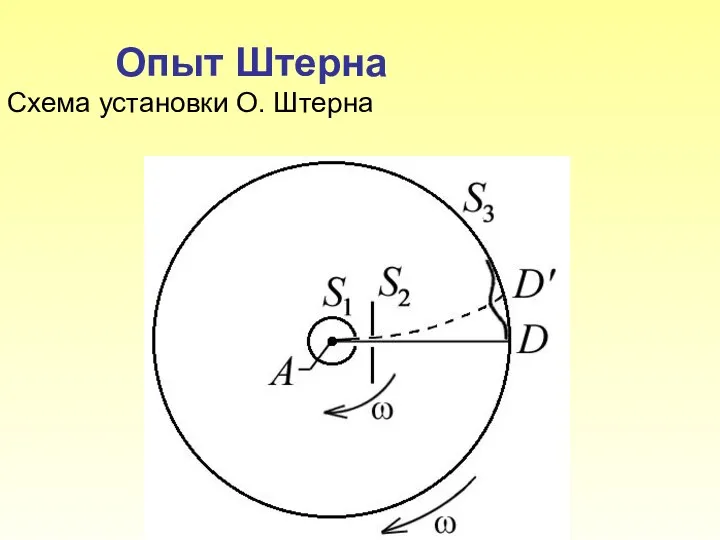
- 5. Опыт Штерна Схема установки О. Штерна
- 6. Платиновая нить А, покрытая снаружи серебром, располагается вдоль оси коаксиальных цилиндров S1, S3. Внутри цилиндров поддерживается
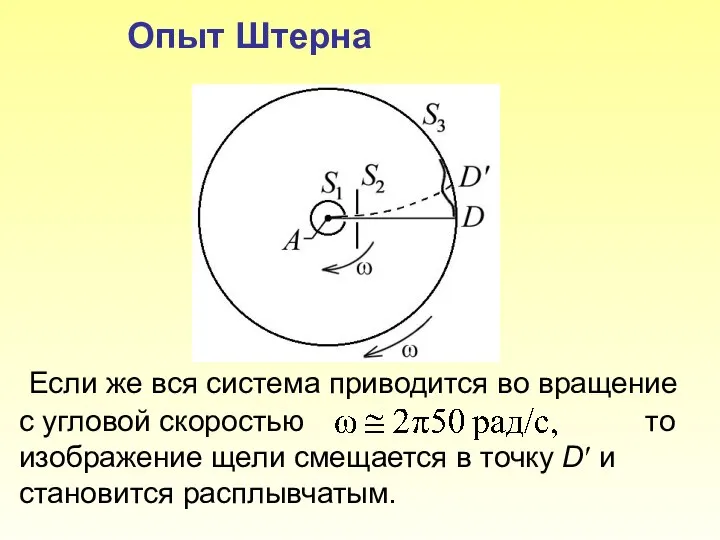
- 7. Опыт Штерна Если же вся система приводится во вращение с угловой скоростью то изображение щели смещается
- 8. Пусть l – расстояние между D и D/, измеренное вдоль поверхности цилиндра S3, где – линейная
- 9. Температура нити в опытах Штерна равнялась 1200°С, что соответствует среднеквадратичной скорости молекул серебра В эксперименте получился
- 10. Ещё в XIX веке Дж. Максвелл утверждал, что молекулы, беспорядочно сталкиваясь друг с другом, как-то «распределяются»
- 11. 2. Вероятность события. Понятие о распределении молекул газа по скоростям С точки зрения атомно-молекулярного строения вещества
- 12. Большое число сталкивающихся атомов и молекул обуславливает важные закономерности в поведении статистических переменных, не свойственные отдельным
- 13. Математическое определение вероятности: вероятность какого-либо события – это предел, к которому стремится отношение числа случаев, приводящих
- 14. Молекулы движутся хаотически. Среди них есть и очень быстрые, и очень медленные. Благодаря беспорядочному движению и
- 15. Будем искать число частиц (Δn) скорости которых лежат в определённом интервале значения скорости Δυ ( т.е.
- 16. Здесь – функция распределения молекул по скоростям, n – концентрация молекул и - интервал значений скоростей.
- 17. Таким образом, f(υ) – имеет смысл вероятности, то есть показывает, какова вероятность любой молекулы газа в
- 18. 3. Функция распределения Максвелла Пусть имеется n тождественных молекул, находящихся в состоянии беспорядочного теплового движения при
- 19. В результате каждого столкновения проекции скорости молекулы испытывают случайное изменение на Δυx, Δυy, Δυz, причем изменения
- 20. Распределение молекул идеального газа по скоростям впервые было получено знаменитым английским ученым Дж. Максвеллом в 1860
- 21. Скорость – векторная величина. Для проекции скорости на ось х (x-ой составляющей скорости), имеем тогда или
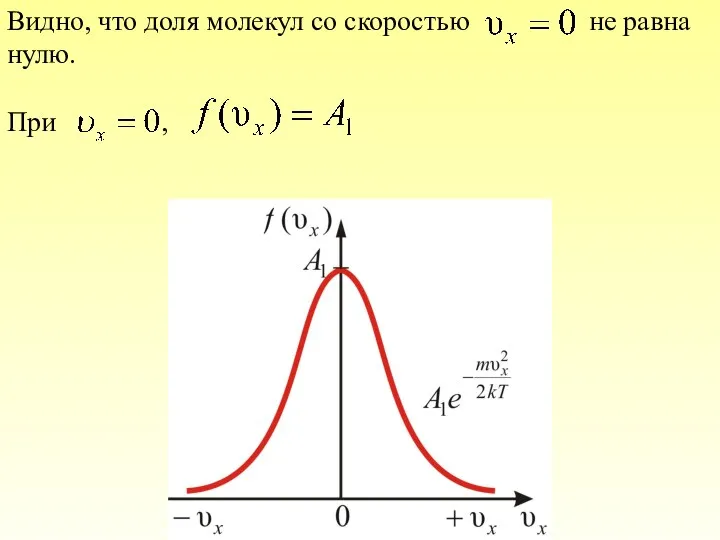
- 22. Видно, что доля молекул со скоростью не равна нулю. При ,
- 23. Приведённое выражение и график справедливы для распределения молекул газа по x-ым компонентам скорости. Очевидно, что и
- 24. Вероятность того, что скорость молекулы одновременно удовлетворяет трём условиям: x – компонента скорости лежит в интервале
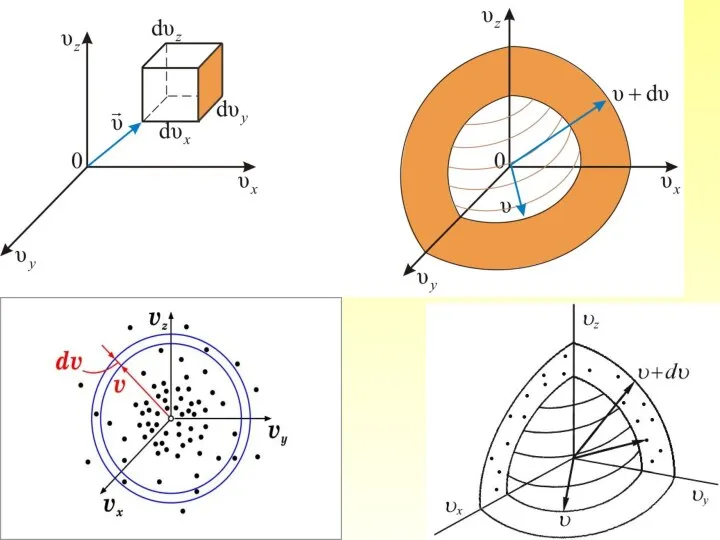
- 25. Или Этой формуле можно дать геометрическое истолкование: dnxyz – это число молекул в параллелепипеде со сторонами
- 27. Величина (dnxyz) не может зависеть от направления вектора скорости. Поэтому надо получить функцию распределения молекул по
- 29. Объём этого шарового слоя: Общее число молекул в слое:
- 30. Отсюда следует закон Максвелла – распределение молекул по абсолютным значениям скоростей: где – доля всех частиц
- 31. При получаем плотность вероятности, или функцию распределения молекул по скоростям: Эта функция обозначает долю молекул единичного
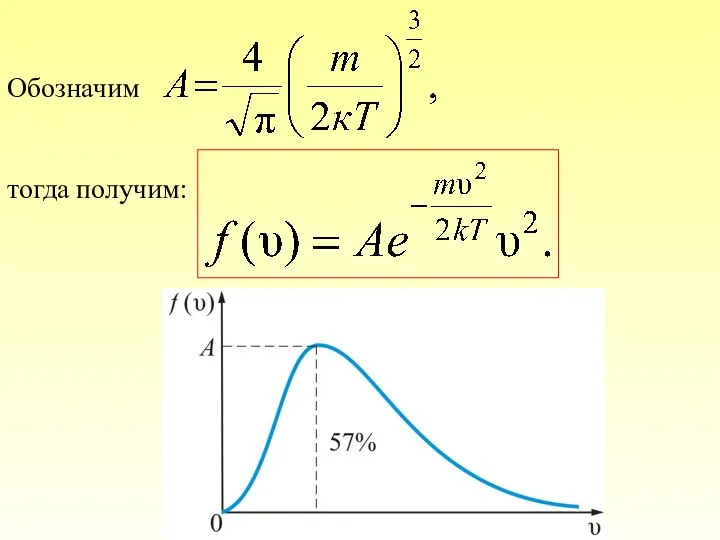
- 32. Обозначим тогда получим:
- 33. Выводы: - Вид распределения молекул газа по скоростям, для каждого газа зависит от массы m и
- 34. Рассмотрим пределы применимости классического описания распределения частиц по скоростям. Для этого воспользуемся соотношением неопределенностей Гейзенберга. Согласно
- 35. Здесь – фундаментальная константа (постоянная Планка), определяющая масштаб квантовых (микроскопических процессов). Таким образом, если частица находится
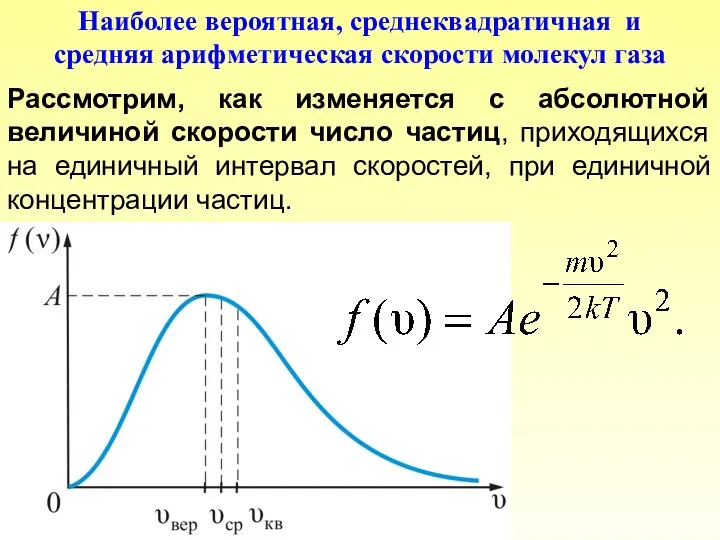
- 36. Рассмотрим, как изменяется с абсолютной величиной скорости число частиц, приходящихся на единичный интервал скоростей, при единичной
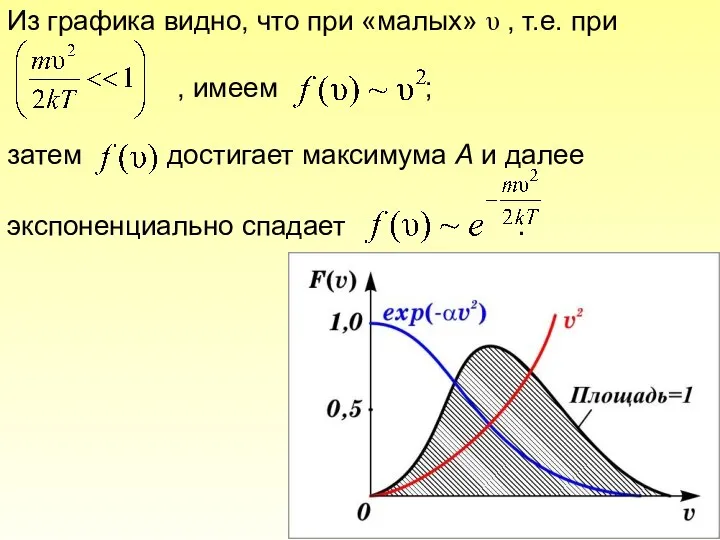
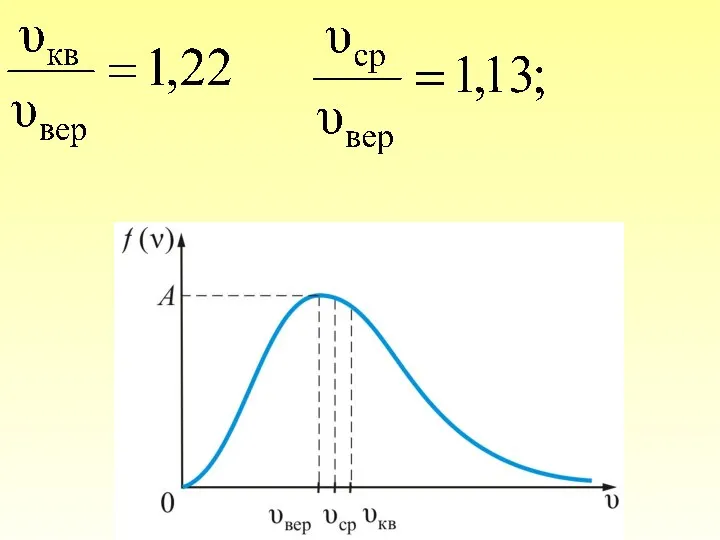
- 37. Из графика видно, что при «малых» υ , т.е. при , имеем ; затем достигает максимума
- 38. Величина скорости, на которую приходится максимум зависимости называют наиболее вероятной скоростью. Величину этой скорости найдем из
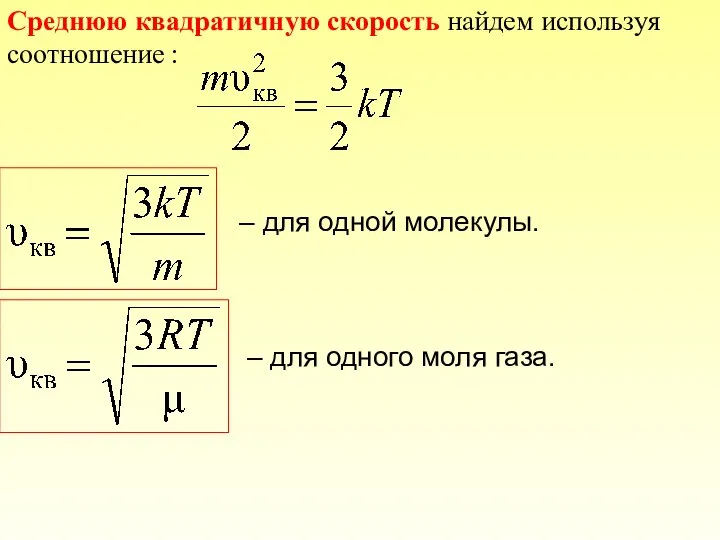
- 39. Среднюю квадратичную скорость найдем используя соотношение : – для одной молекулы. – для одного моля газа.
- 40. Средняя арифметическая скорость − υср где – число молекул со скоростью от υ до . Если
- 42. Формула Максвелла для относительных скоростей Для решения многих задач удобно использовать формулу Максвелла, где скорость выражена
- 43. Формула Максвелла для относительных скоростей Это уравнение универсальное. В таком виде функция распределения не зависит ни
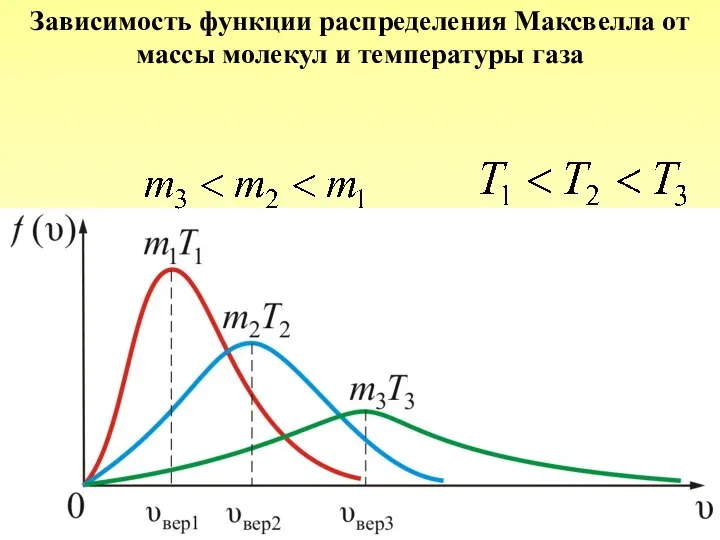
- 45. Зависимость функции распределения Максвелла от массы молекул и температуры газа
- 46. Площадь под кривой величина постоянная, равная единице ( ), поэтому важно знать как будет изменяться положение
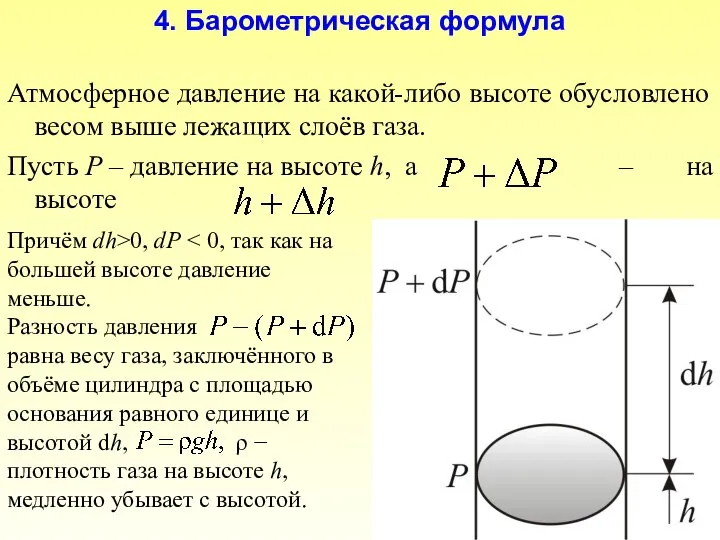
- 47. Атмосферное давление на какой-либо высоте обусловлено весом выше лежащих слоёв газа. Пусть P – давление на
- 48. – плотность газа на высоте h С = Р0 – давление на высоте . - барометрическая
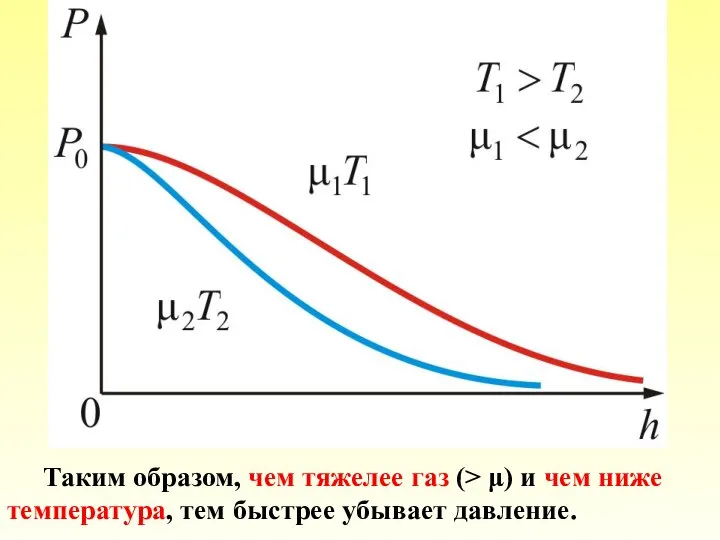
- 49. Из барометрической формулы следует, что P убывает с высотой тем быстрее, чем тяжелее газ (чем больше
- 50. Таким образом, чем тяжелее газ (> μ) и чем ниже температура, тем быстрее убывает давление.
- 51. Распределение Больцмана определяет распределение частиц в силовом поле в условиях теплового равновесия. Пусть идеальный газ находится
- 52. Число молекул в единичном объеме n убывает с удалением от поверхности Земли, значит и давление тоже
- 53. Исходя из основного уравнения молекулярно-кинетической теории: , заменим P и P0 в барометрической формуле на n
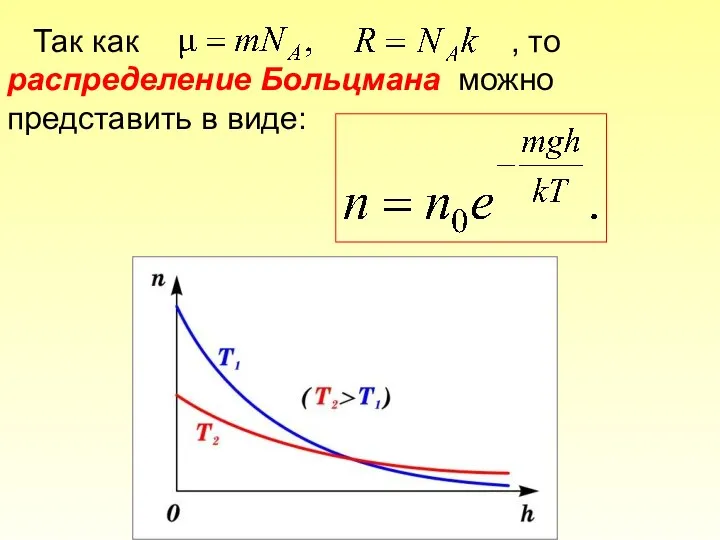
- 54. Так как , то распределение Больцмана можно представить в виде:
- 55. С уменьшением температуры число молекул на высотах, отличных от нуля, убывает. При T=0 тепловое движение прекращается,
- 56. Так как –потенциальная энергия, следовательно, распределение Больцмана характеризует распределение частиц по значениям потенциальной энергии: – это
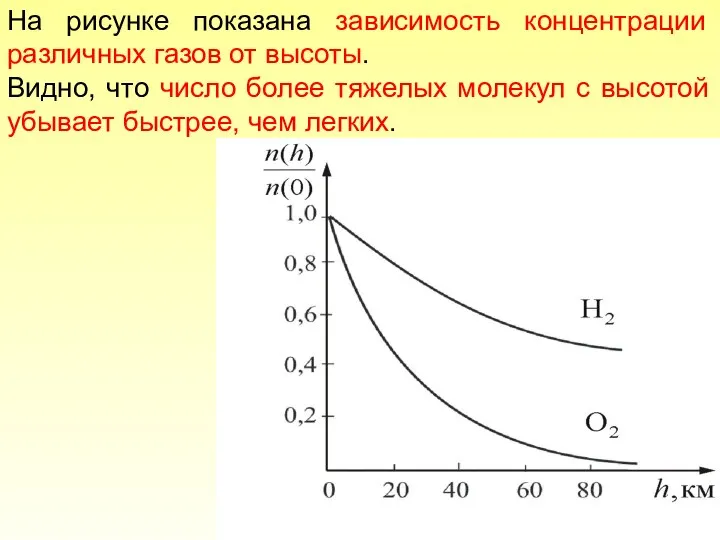
- 57. На рисунке показана зависимость концентрации различных газов от высоты. Видно, что число более тяжелых молекул с
- 58. Можно получить отношение концентраций молекул в точках с U1 и U2 Больцман доказал, что соотношение справедливо
- 59. Из выражения для распределения молекул по скоростям можно найти распределение молекул газа по значениям кинетической энергии
- 60. Отсюда получим функцию распределения молекул по энергиям теплового движения: Средняя кинетическая энергия молекулы идеального газа:
- 61. Итак, закон Максвелла даёт распределение частиц по значениям кинетической энергии а закон Больцмана – распределение частиц
- 62. Обозначим E=U+K – полная энергия. Тогда Это закон распределения Максвелла-Больцмана. Здесь n0 – число молекул в
- 63. Потенциальная и кинетическая энергии, а следовательно и полная энергия Е, могут принимать непрерывный ряд значений. Если
- 64. где Ni – число частиц, находящихся в состоянии с энергией Еi, а А – коэффициент пропорциональности,
- 66. Скачать презентацию

















































 Первое начало термодинамики
Первое начало термодинамики Дифракция. Виды волн
Дифракция. Виды волн Рисунки к методичке по теплообменнику
Рисунки к методичке по теплообменнику Строение и функционирование автомобиля
Строение и функционирование автомобиля Взаимодействие токов. Магнитное поле. Вектор магнитной индукции. Линии магнитной индукции Физика, 11 класс. Физико-математически
Взаимодействие токов. Магнитное поле. Вектор магнитной индукции. Линии магнитной индукции Физика, 11 класс. Физико-математически Основы равновесной термодинамики
Основы равновесной термодинамики Сила трения в природе Выполнила ученица ГОУ ЦО «Школа Здоровья» № 628 Шеина Анна. Руководитель проекта: Лисицкая Елена Владимировн
Сила трения в природе Выполнила ученица ГОУ ЦО «Школа Здоровья» № 628 Шеина Анна. Руководитель проекта: Лисицкая Елена Владимировн Колебания-1. Гармоническое колебание и его характеристики. Модель гармонического осциллятора
Колебания-1. Гармоническое колебание и его характеристики. Модель гармонического осциллятора Коэффициенты токораспределения и потокораспределения
Коэффициенты токораспределения и потокораспределения Камера сгорания
Камера сгорания МОУ СОШ № 13 Г. Новый Уренгой Исследовательская работа на тему: «Использование солнечной энергии для нагревания воды в душе» Раб
МОУ СОШ № 13 Г. Новый Уренгой Исследовательская работа на тему: «Использование солнечной энергии для нагревания воды в душе» Раб Физика и техника
Физика и техника Использование интернет-ресурсов в образовании в области физики учащихся 7-8 классов
Использование интернет-ресурсов в образовании в области физики учащихся 7-8 классов Изучение деления ядра атома урана по фотографиям треков
Изучение деления ядра атома урана по фотографиям треков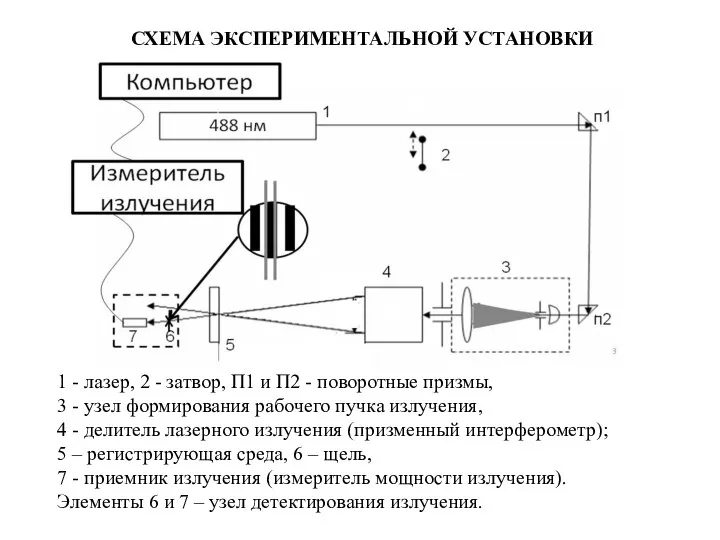 Схема экспериментальной установки
Схема экспериментальной установки Презентация на тему "давление"
Презентация на тему "давление" Methods and technical means for using the energy of waves
Methods and technical means for using the energy of waves ЭНЕРГИЯ И ЕЕ ЗАКОНЫ Тимур Идрисов «Ради Земли»
ЭНЕРГИЯ И ЕЕ ЗАКОНЫ Тимур Идрисов «Ради Земли» Интерференция света
Интерференция света Способы получения изотопов для лучевой диагностики
Способы получения изотопов для лучевой диагностики Физические основы прочности
Физические основы прочности Исследовательский проект Робот-эколог
Исследовательский проект Робот-эколог Переменный ток
Переменный ток Уравнения теории упругости. Закон Гука для изотропного тела. Упругие постоянные. Объемная деформация. (Лекция 4)
Уравнения теории упругости. Закон Гука для изотропного тела. Упругие постоянные. Объемная деформация. (Лекция 4) Презентация по теме: Звуковые волны
Презентация по теме: Звуковые волны Законы Ньютона
Законы Ньютона Основное содержание и задачи воздушной навигации
Основное содержание и задачи воздушной навигации Радиоактивность как свидетельство сложного строения атома
Радиоактивность как свидетельство сложного строения атома