Содержание
- 2. Тема урока Алканы.
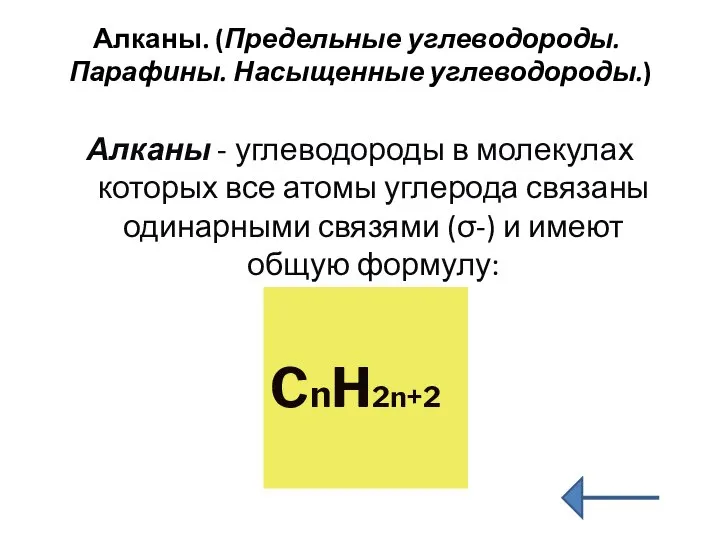
- 3. Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.) Алканы - углеводороды в молекулах которых все атомы углерода связаны
- 4. Гомологический ряд метана СН4 метан С2H6 этан C3H8 пропан C4H10 бутан C5H12 пентан C6H14 гексан C7H16
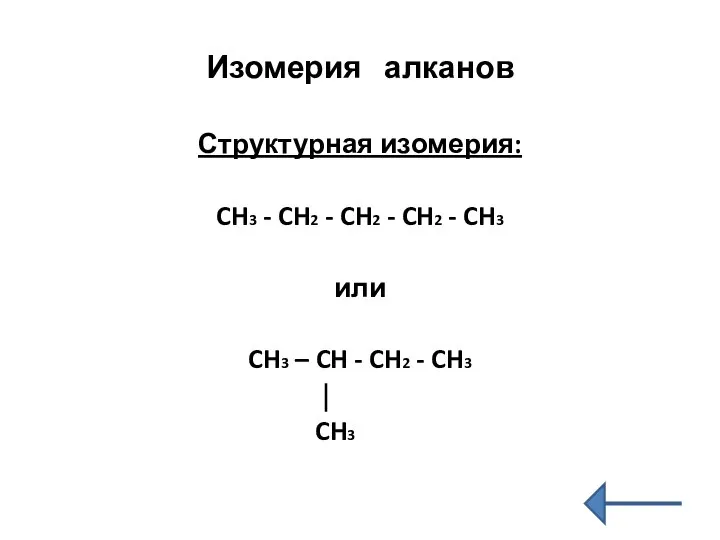
- 5. Изомерия алканов Структурная изомерия: CH3 - CH2 - CH2 - CH2 - CH3 или CH3 –
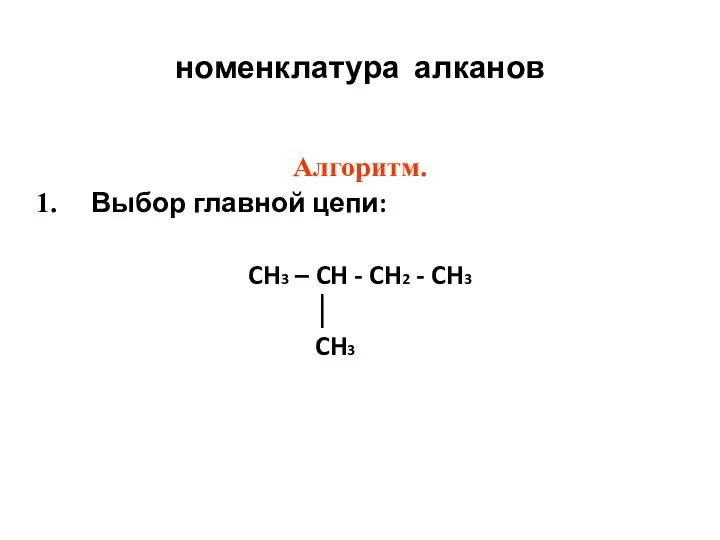
- 6. номенклатура алканов Алгоритм. Выбор главной цепи: CH3 – CH - CH2 - CH3 │ CH3
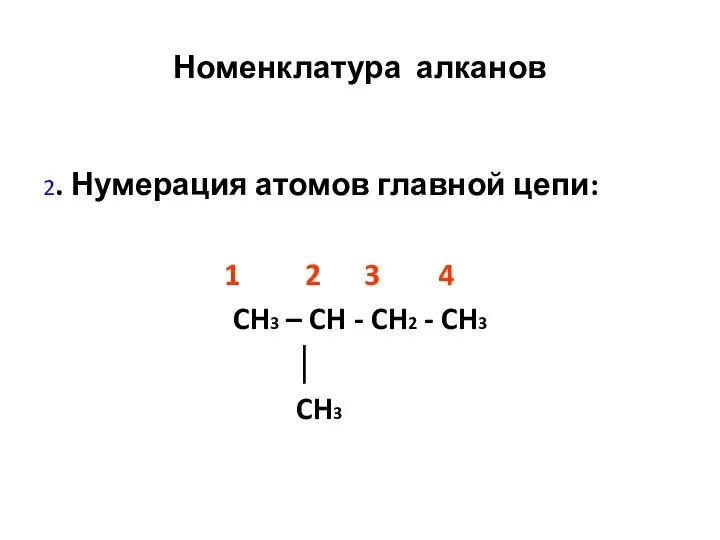
- 7. Номенклатура алканов 2. Нумерация атомов главной цепи: 1 2 3 4 CH3 – CH - CH2
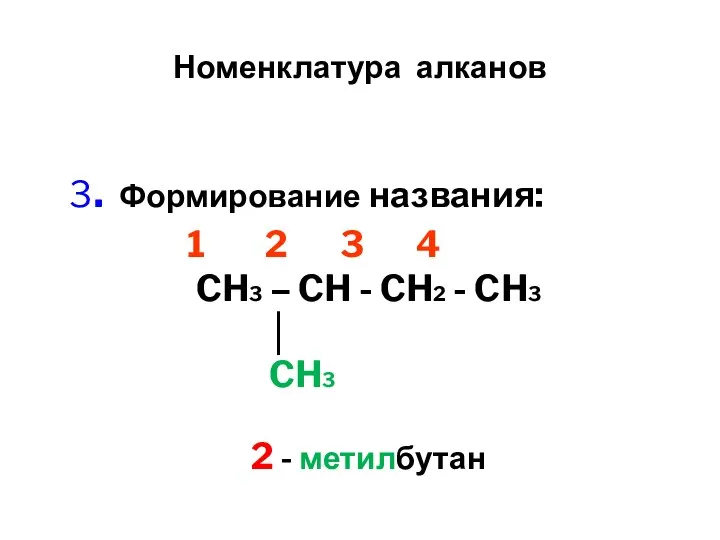
- 8. Номенклатура алканов 3. Формирование названия: 1 2 3 4 CH3 – CH - CH2 - CH3
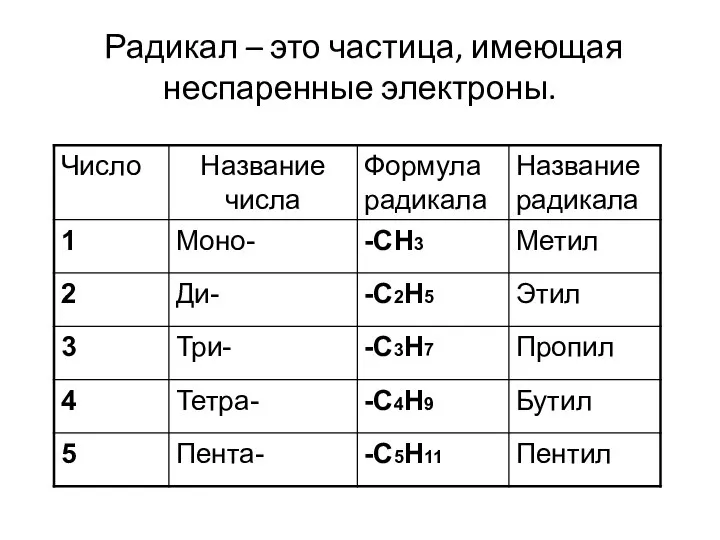
- 9. Радикал – это частица, имеющая неспаренные электроны.
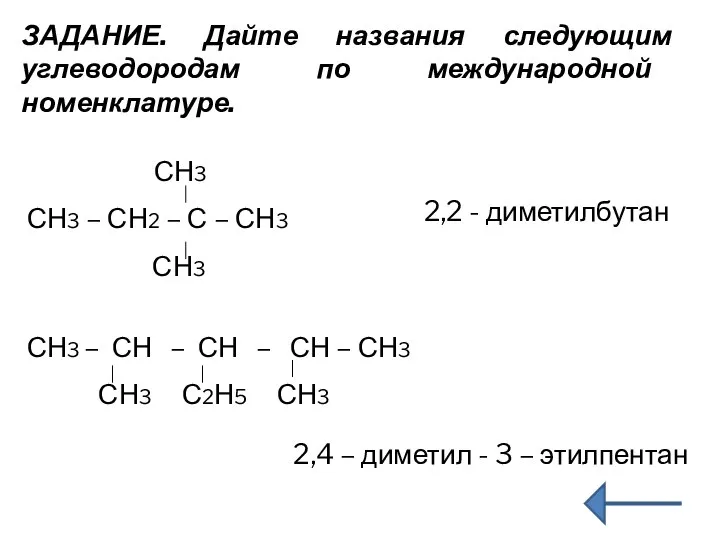
- 10. ЗАДАНИЕ. Дайте названия следующим углеводородам по международной номенклатуре. СН3 СН3 – СН2 – С – СН3
- 11. Напишите структурные формулы следующих алканов: а) 2,3-диметилпентан; б) З-метил-3-этилпентан; в) 2,3,4-триметил-З-пропил-гексан; г) 2,2,4,6-тетраметилгептан; д) 2-метил-3,3-диэтилоктан.
- 12. Строение алканов метан
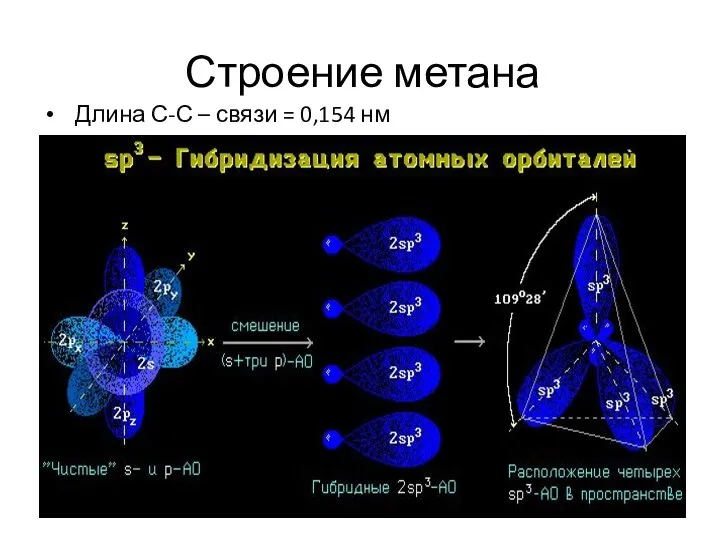
- 13. Строение метана Длина С-С – связи = 0,154 нм
- 14. Строение метана- правильный тетраэдр
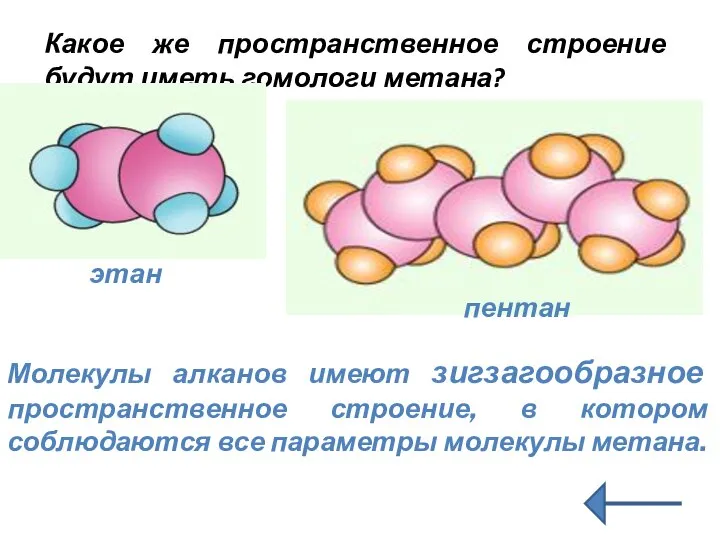
- 15. Какое же пространственное строение будут иметь гомологи метана? этан пентан Молекулы алканов имеют зигзагообразное пространственное строение,
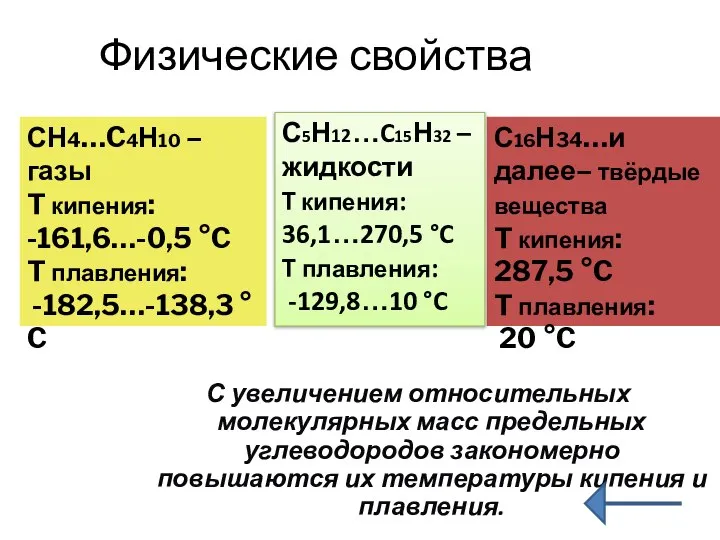
- 16. Физические свойства С увеличением относительных молекулярных масс предельных углеводородов закономерно повышаются их температуры кипения и плавления.
- 17. Получение алканов 1 –выделение углеводородов из природного сырья 2- гидрирование циклоалканов и непредельных углеводородов 3- декарбоксилирование
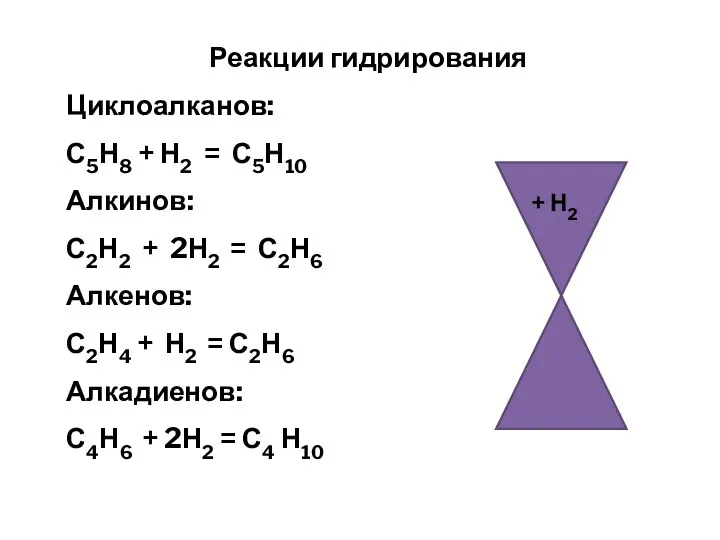
- 18. Реакции гидрирования Циклоалканов: С5Н8 + Н2 = С5Н10 Алкинов: С2Н2 + 2Н2 = С2Н6 Алкенов: С2Н4
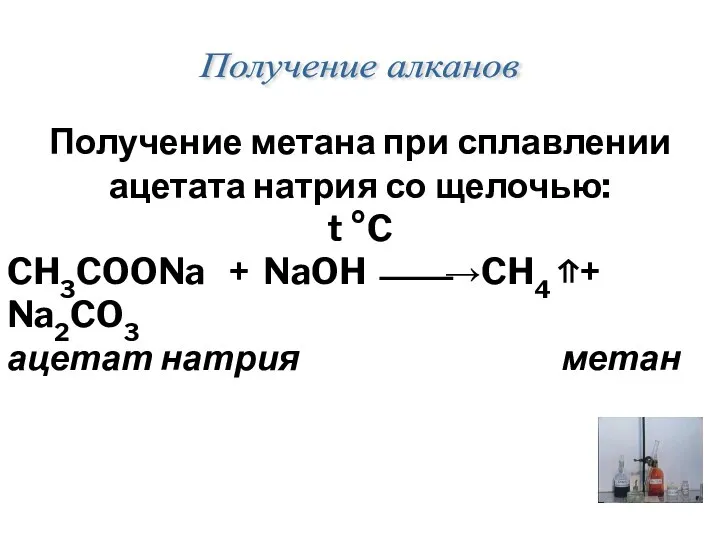
- 19. Получение метана при сплавлении ацетата натрия со щелочью: t °C CH3COONa + NaOH ⎯⎯→CH4 ⇑+ Na2CO3
- 20. Синтез Вюрца проводят с целью получения алканов с более длинной углеродной цепью. Например: получение этана из
- 21. Метан в лаборатории можно получить гидролизом карбида алюминия Al4C3 + 12H2O = 4Al(OH)3 + 3CH4
- 22. Химические свойства алканов
- 23. Свойства метана: 1) метан не вступает в реакцию окисления при действии водного раствора KMnO4; 2) метан
- 24. СН4 + Сl2 CH3Cl + HCl + Q t Реакции протекают по радикальному механизму. С Н
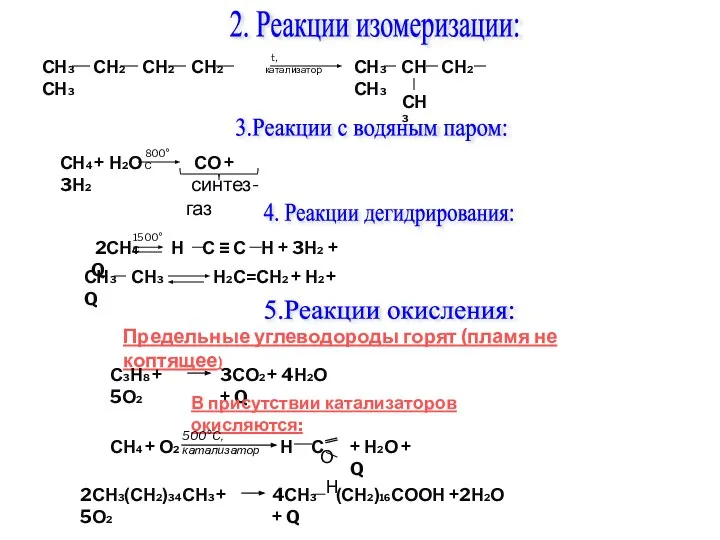
- 25. 2. Реакции изомеризации: СН3 СН2 СН2 СН2 СН3 t, катализатор СН3 СН СН2 СН3 СН3 3.Реакции
- 26. Применение Получение ацетилена Горючее для дизельных и турбореактивных двигателей Получение растворителей В металлургии А также сырьё
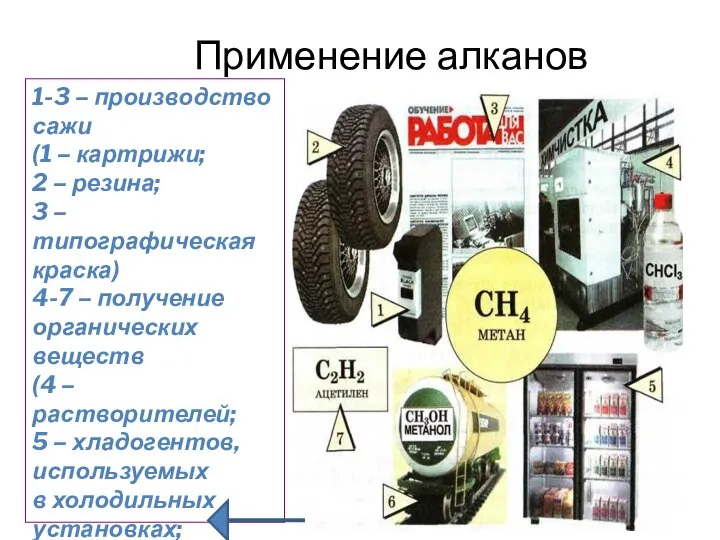
- 27. Применение алканов 1-3 – производство сажи (1 – картрижи; 2 – резина; 3 – типографическая краска)
- 28. Проверка знаний Какие углеводороды относят к алканам? Запишите формулы возможных изомеров гексана и назовите их по
- 30. Скачать презентацию












 Химический состав и пищевая ценность кофе
Химический состав и пищевая ценность кофе Представители солей. Важнейшие соли, используемые человеком в жизни. МОУ лицей №18 Иванова И. Учитель химии Калинина Л.А.
Представители солей. Важнейшие соли, используемые человеком в жизни. МОУ лицей №18 Иванова И. Учитель химии Калинина Л.А. Бумага - важнейший элемент человеческой культуры, основа просвещения и воспитания человека.
Бумага - важнейший элемент человеческой культуры, основа просвещения и воспитания человека.  Гидролиз солей
Гидролиз солей Лиофильные и лиофобные дисперсные системы
Лиофильные и лиофобные дисперсные системы Основания и соли
Основания и соли Презентация Жидкие кристаллы
Презентация Жидкие кристаллы  Органічні сполуки в побуті
Органічні сполуки в побуті  Химический элемент селен
Химический элемент селен Краски. Виды красок
Краски. Виды красок Выращивание кристаллов неорганических веществ Проект Кийко Елизаветы ученицы 3 Б класса МОУ «Гимназия №17 г.
Выращивание кристаллов неорганических веществ Проект Кийко Елизаветы ученицы 3 Б класса МОУ «Гимназия №17 г. Химическая связь. Природа химической связи
Химическая связь. Природа химической связи Металлокомплексный катализ. (Лекция 16)
Металлокомплексный катализ. (Лекция 16) Хроматография талдау әдістері
Хроматография талдау әдістері Презентация по химии Тема : « Большое приключение маленькой спички»
Презентация по химии Тема : « Большое приключение маленькой спички» Анализ консервантов в пищевых продуктах
Анализ консервантов в пищевых продуктах Соединения железа
Соединения железа Клеточная и системная детоксикация
Клеточная и системная детоксикация Imperfections in Solids
Imperfections in Solids Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований
Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований Бериллий, магний и щелочноземельные металлы
Бериллий, магний и щелочноземельные металлы Этиленгликоль. Физические свойства
Этиленгликоль. Физические свойства Диены. Сопряженные диены
Диены. Сопряженные диены Очистка и контроль качества природных и сточных вод. Изотопный состав и структура жидкой воды
Очистка и контроль качества природных и сточных вод. Изотопный состав и структура жидкой воды Гранулирование. Виды грануляции
Гранулирование. Виды грануляции Презентация по Химии "Отбеливатели" - скачать смотреть
Презентация по Химии "Отбеливатели" - скачать смотреть  Презентация по Химии "Презентация Химия вокруг нас" - скачать смотреть
Презентация по Химии "Презентация Химия вокруг нас" - скачать смотреть  Комплексті қосылыстар
Комплексті қосылыстар