Содержание
- 2. Я, Кузьмина Ирина Викторовна, кандидат технических наук с большим опытом преподавания в высшей школе, обобщила полезную
- 3. Вернуться к содержанию Для выхода из программы нажмите «Esc» на клавиатуре Переход к тому действию, о
- 4. Содержание Инструкция по использованию интерфейса Вода и ее свойства. Изотопный состав воды. Структура жидкой воды. Водородные
- 5. Вода и ее свойства Изотопный состав и структура жидкой воды
- 6. Вода – главное и наиболее распространенное химическое соединение на нашей планете – обязательный компонент всех живых
- 7. Наибольшие запасы воды содержатся в гидросфере – 96 % в мировом океане, остальные запасы воды –
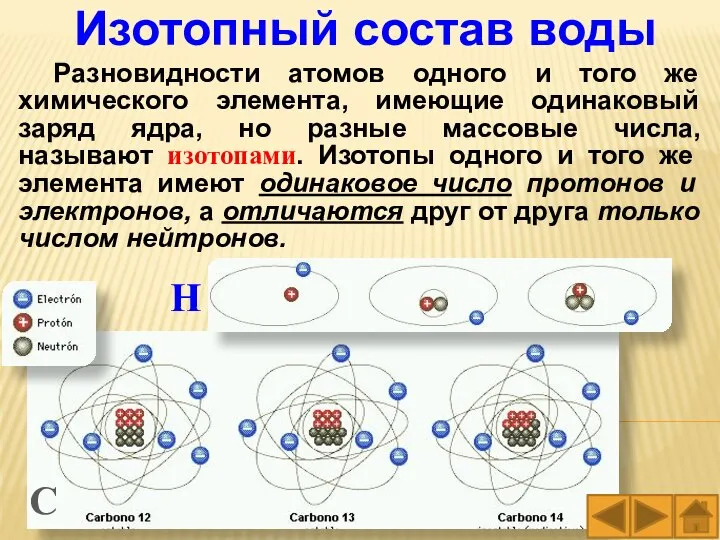
- 8. Изотопный состав воды Разновидности атомов одного и того же химического элемента, имеющие одинаковый заряд ядра, но
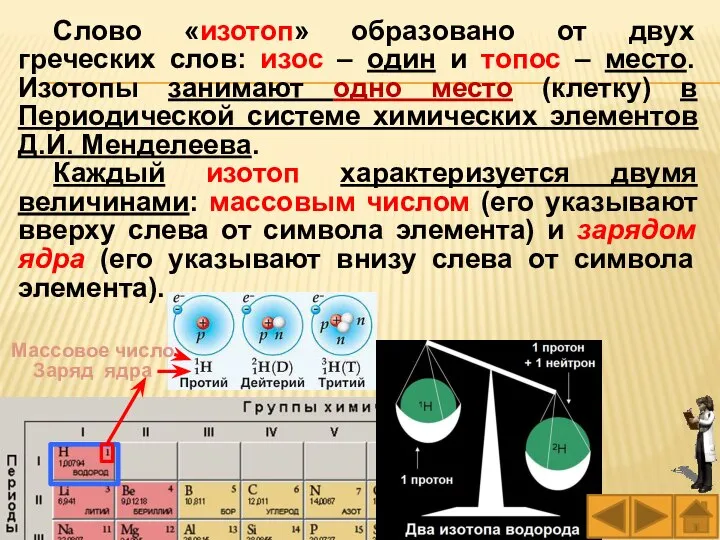
- 9. Слово «изотоп» образовано от двух греческих слов: изос – один и топос – место. Изотопы занимают
- 10. Массовые числа изотопов всегда выражают целыми числами. Но в природе содержание каждого изотопа различно, поэтому относительные
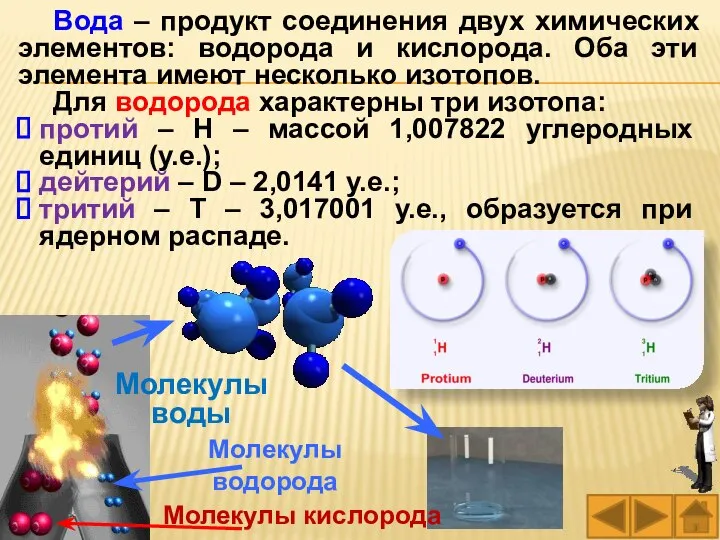
- 11. Молекулы воды Молекулы водорода Молекулы кислорода Вода – продукт соединения двух химических элементов: водорода и кислорода.
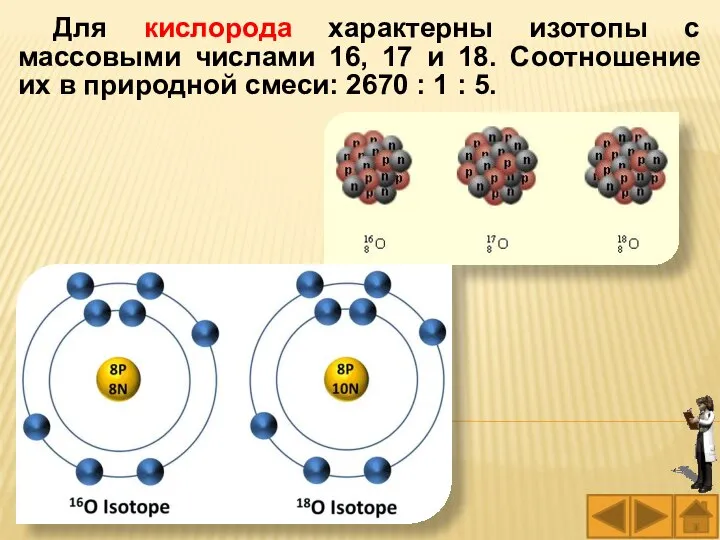
- 12. Для кислорода характерны изотопы с массовыми числами 16, 17 и 18. Соотношение их в природной смеси:
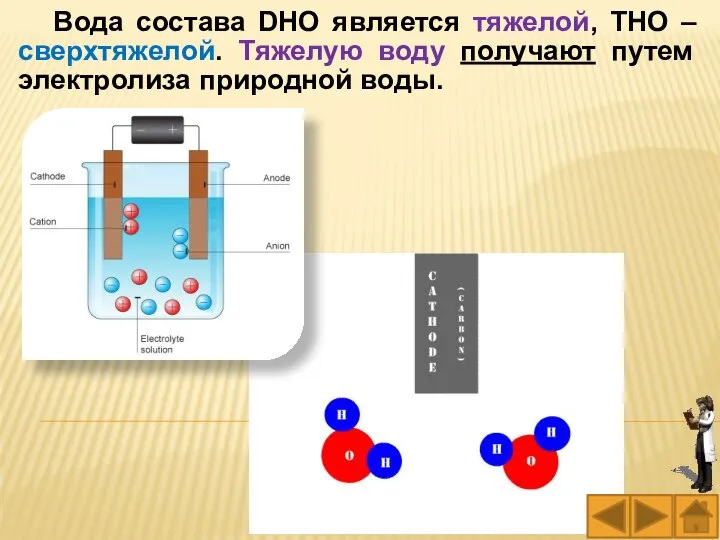
- 13. Вода состава DНО является тяжелой, ТНО – сверхтяжелой. Тяжелую воду получают путем электролиза природной воды.
- 14. По свойствам тяжелая вода отличается от обычной: замерзает при температуре –3,8 °С, кипит при температуре 101,4
- 15. Вода – это смесь девяти видов молекул, поэтому в зависимости от их количественного соотношения все ее
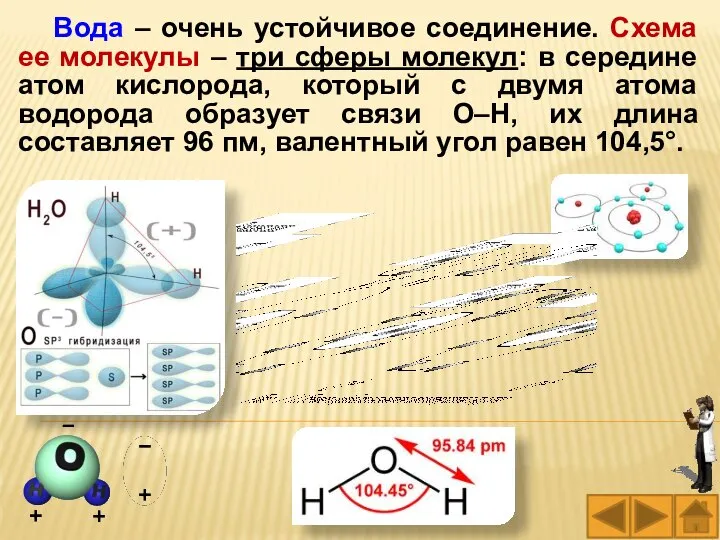
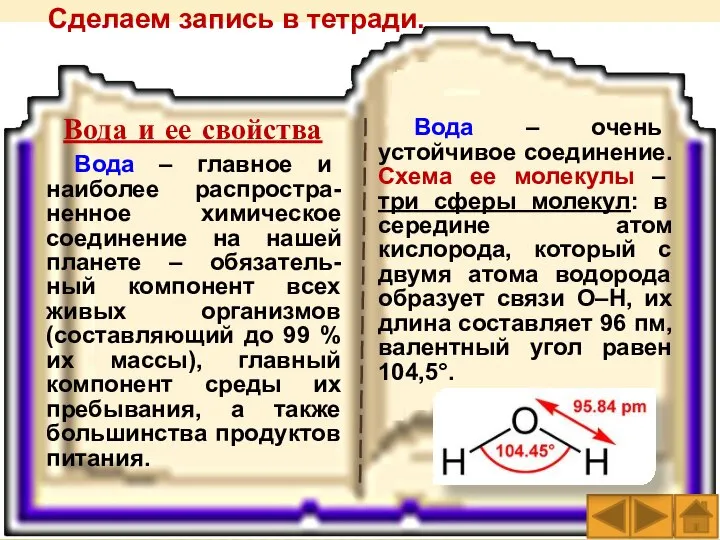
- 16. Вода – очень устойчивое соединение. Схема ее молекулы – три сферы молекул: в середине атом кислорода,
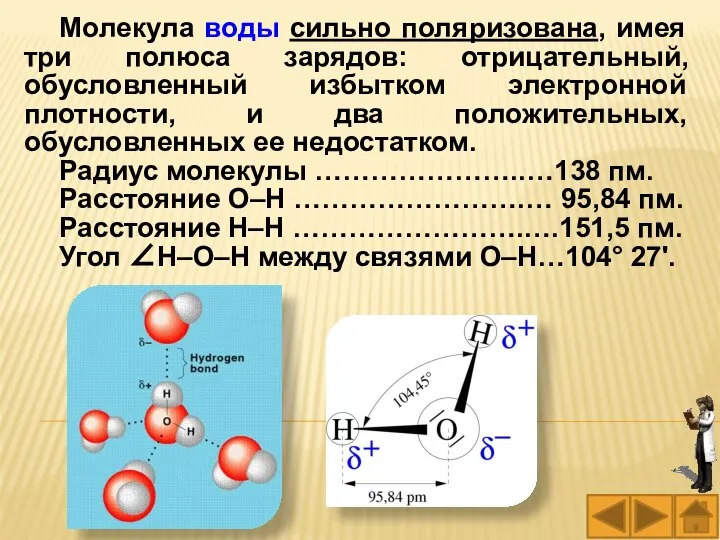
- 17. Молекула воды сильно поляризована, имея три полюса зарядов: отрицательный, обусловленный избытком электронной плотности, и два положительных,
- 19. Сделаем запись в тетради. Вода и ее свойства Вода – главное и наиболее распростра-ненное химическое соединение
- 20. Сделаем запись в тетради. Разновидности ато-мов одного и того же химического элемента, имеющие одинаковый заряд ядра,
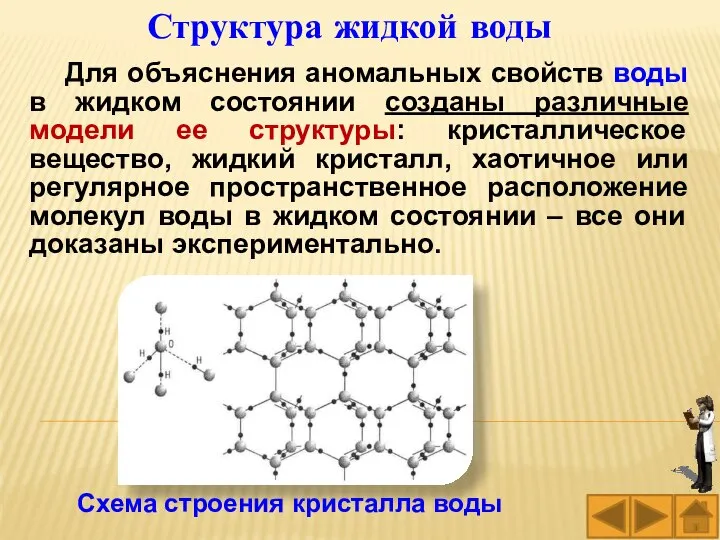
- 21. Структура жидкой воды Для объяснения аномальных свойств воды в жидком состоянии созданы различные модели ее структуры:
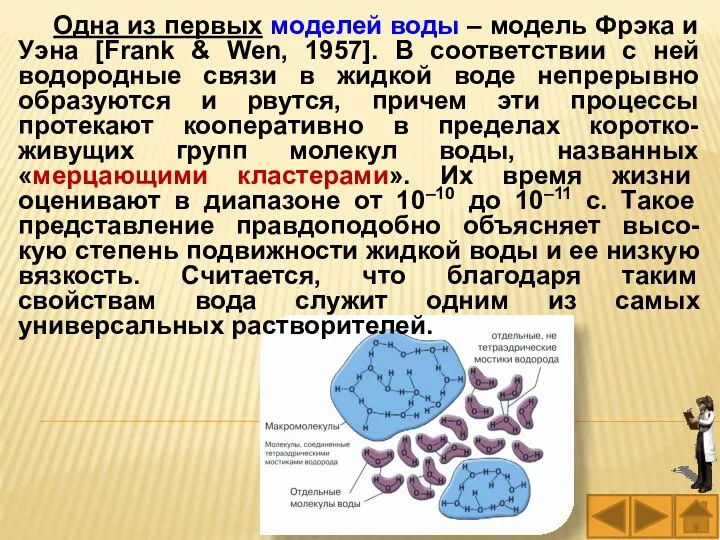
- 22. Одна из первых моделей воды – модель Фрэка и Уэна [Frank & Wen, 1957]. В соответствии
- 23. В 1999 г. известный российский исследователь воды С.В. Зенин защитил в Институте медико-биологических проблем РАН докторскую
- 24. С.В. Зенин проводил исследования тремя химическими методами:
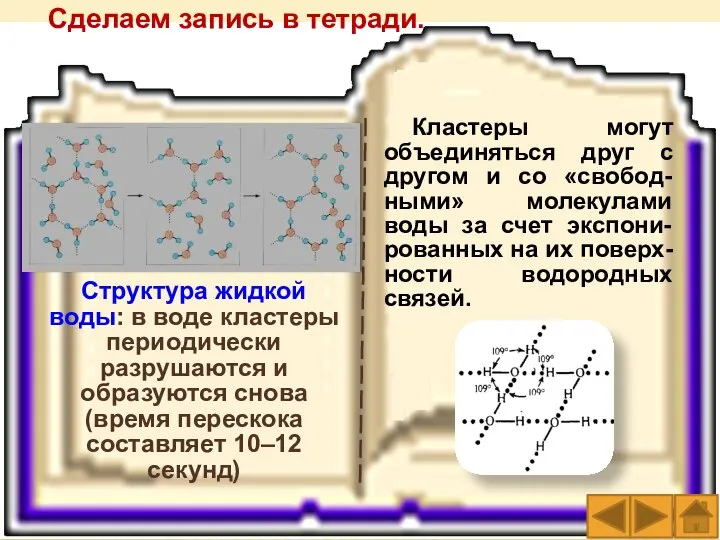
- 25. Молекулы воды объединя-ются в группы, которые называются кластерами. Ученые предположили, что именно кластеры являются своеобразными ячейками
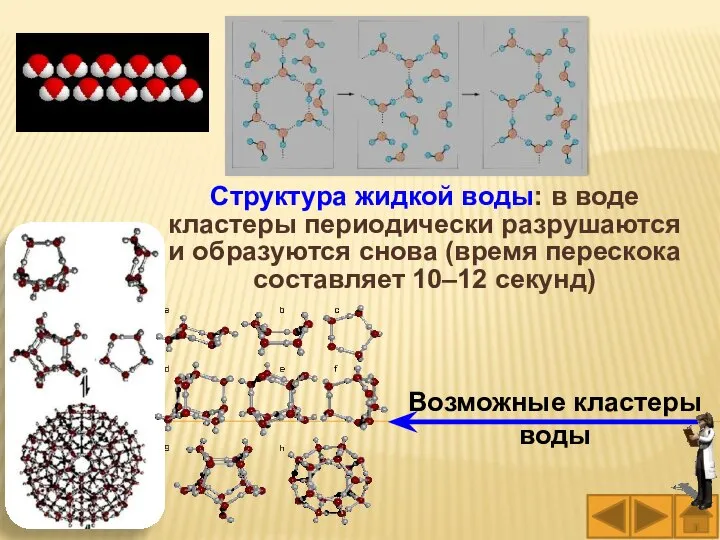
- 26. Возможные кластеры воды Структура жидкой воды: в воде кластеры периодически разрушаются и образуются снова (время перескока
- 27. Поллинг полагает, что вода имеет клатратную структуру, характерную для газовых гидратов, центральная молекула в которых окружена
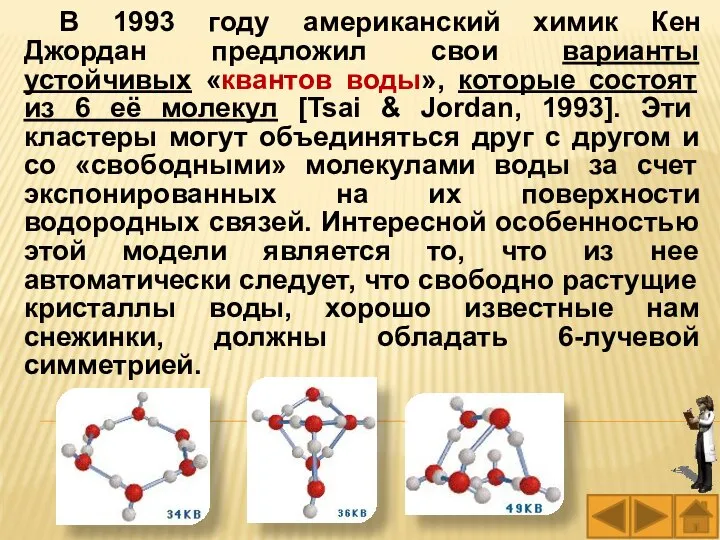
- 28. В 1993 году американский химик Кен Джордан предложил свои варианты устойчивых «квантов воды», которые состоят из
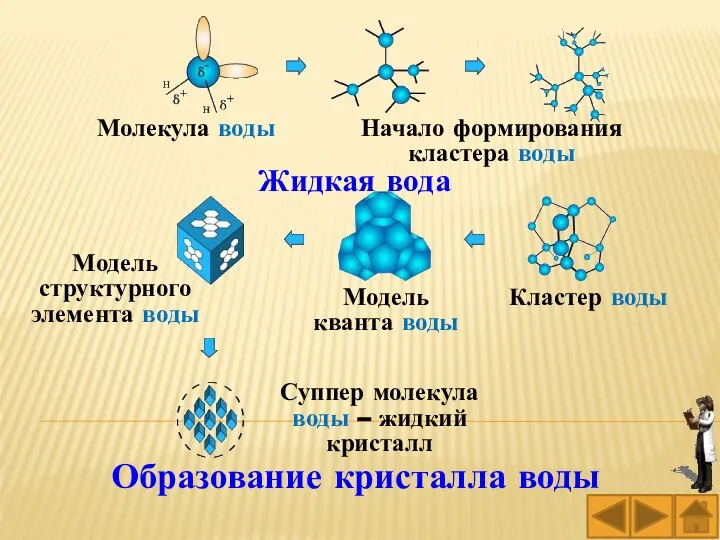
- 29. Жидкая вода Образование кристалла воды Молекула воды Начало формирования кластера воды Кластер воды Модель кванта воды
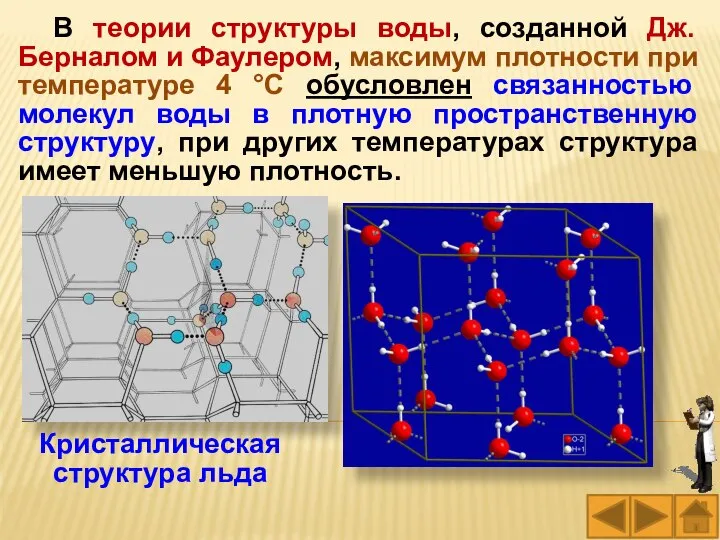
- 30. В теории структуры воды, созданной Дж. Берналом и Фаулером, максимум плотности при температуре 4 °С обусловлен
- 31. Структура воды искажается при попадании в нее примесей – как способных взаимодейст-вовать с диполями воды, так
- 32. При повышении температуры амплитуда колебаний молекул воды в кристалле увеличивается и его объем возрастает – плотность
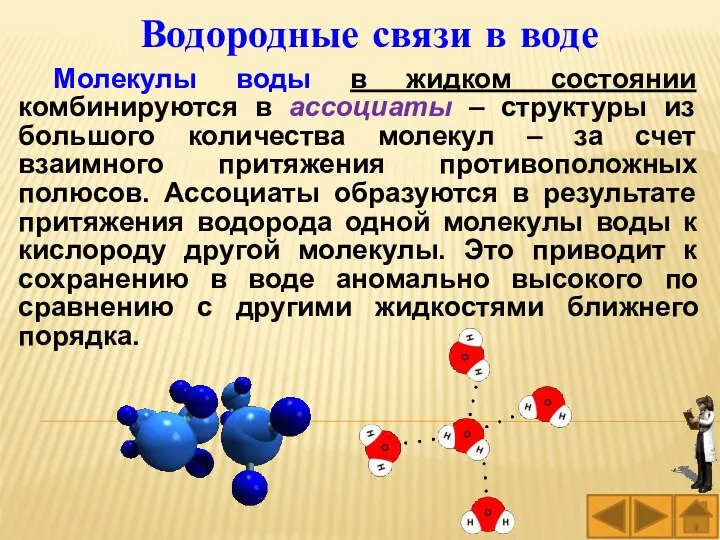
- 33. Водородные связи в воде Молекулы воды в жидком состоянии комбинируются в ассоциаты – структуры из большого
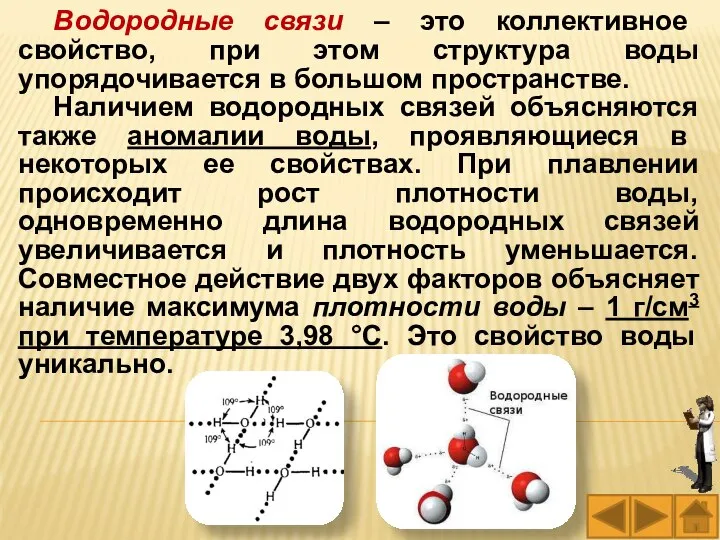
- 34. Водородные связи – это коллективное свойство, при этом структура воды упорядочивается в большом пространстве. Наличием водородных
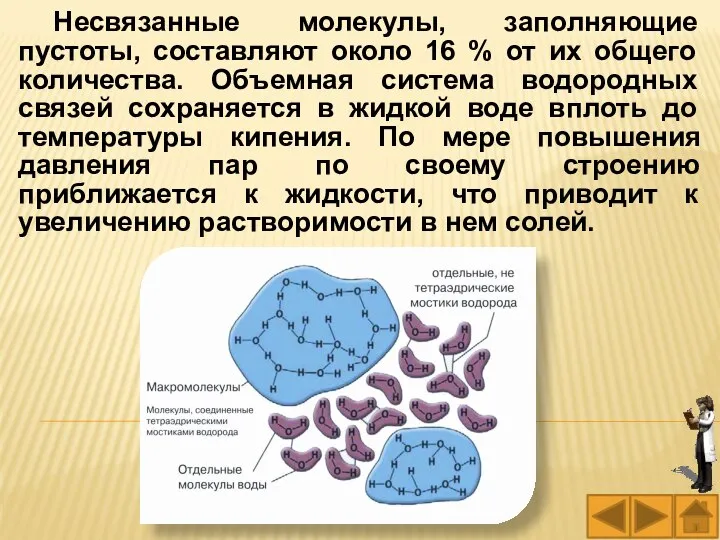
- 35. Несвязанные молекулы, заполняющие пустоты, составляют около 16 % от их общего количества. Объемная система водородных связей
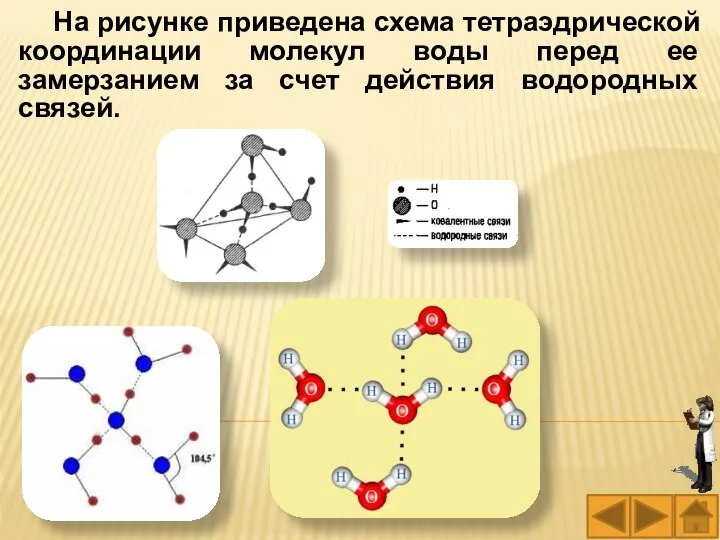
- 36. На рисунке приведена схема тетраэдрической координации молекул воды перед ее замерзанием за счет действия водородных связей.
- 37. Сделаем запись в тетради. Структура жидкой воды Для объяснения аномальных свойств во-ды в жидком состоянии созданы
- 38. Сделаем запись в тетради. Структура жидкой воды: в воде кластеры периодически разрушаются и образуются снова (время
- 39. Физические свойства воды Вода – единственное химическое соеди-нение, которое в природе может находиться в жидком, твердом
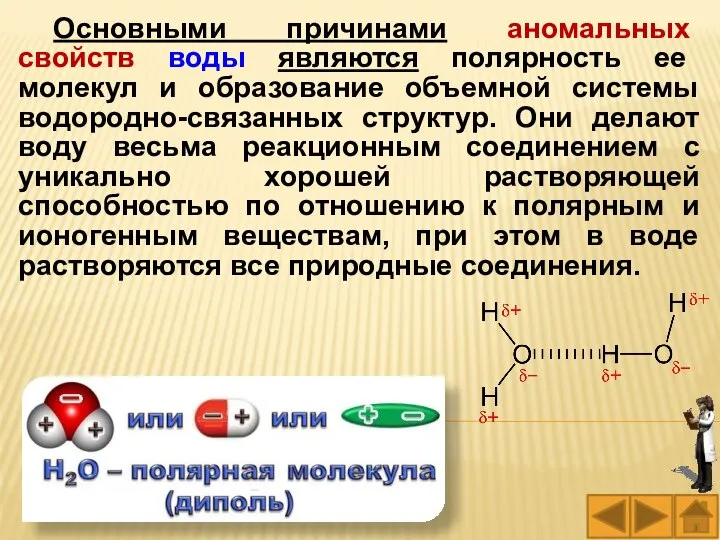
- 40. Основными причинами аномальных свойств воды являются полярность ее молекул и образование объемной системы водородно-связанных структур. Они
- 41. Коэффициент объемного расширения имеет отрицательные значения при температурах ниже 3,98 °С, теплоемкость при плавлении возрастает почти
- 42. Вязкость воды при повышении давления снижается аномально быстро в области малых температур при нагревании (что не
- 43. Сделаем запись в тетради. Физические свойства воды Вода – это смесь девяти видов молекул, поэтому в
- 44. Сделаем запись в тетради. Не образующие связей молекулы воды до 30–60 °С обладают возмож-ностью сохранять льдо-подобный
- 45. Сделаем запись в тетради. Наличием водородных связей объясняются аномалии воды: при плавлении происходит рост плотности воды,
- 46. Свойства водных растворов. Химическое равновесие Химические реакции обратимы, т.е. их течение возможно в прямом и обратном
- 47. Равновесное состояние нарушается при воздействии внешних факторов – изменении концентрации продуктов реакции и температуры. Так как
- 48. Направление смещение химического равновесия можно определить с помощью принципа Ле–Шателье: если на систему, находящуюся в равновесии,
- 49. При увеличении температуры равновесие смещается в сторону эндотермической реакции и, наоборот, при уменьшении температуры – в
- 50. При увеличении концентрации исходных веществ равновесие системы смещается вправо, в сторону образования конечных продуктов, а при
- 51. Принцип смещения равновесия в гомогенных системах применим и к гетерогенным системам для характеристики равновесных состояний в
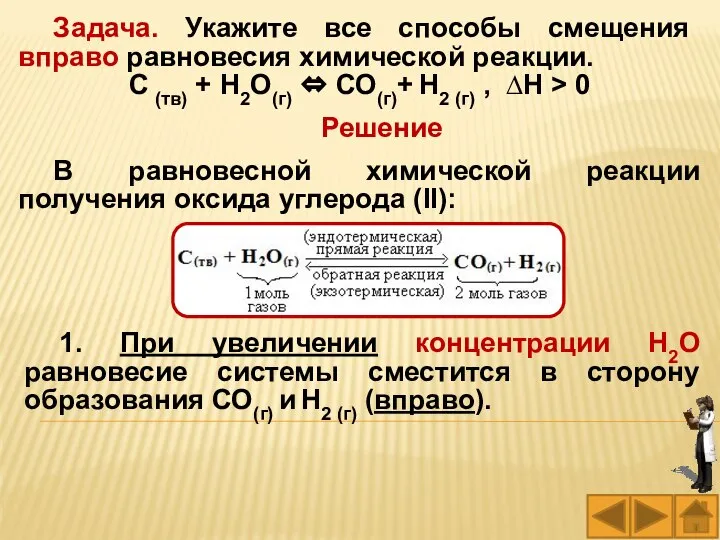
- 52. Задача. Укажите все способы смещения вправо равновесия химической реакции. С (тв) + Н2О(г) ⇔ СО(г)+ Н2
- 53. 2. При уменьшении давления в системе равновесие сместится вправо, т.к. исходные вещества занимают меньший объем, чем
- 54. 4. При введении катализатора или его замене положение равновесия не меняется, так как катализатор изменяет энергию
- 55. В первой половине 19 в. ввел понятие об электролитах и неэлектролитах английский физик и химик Майкл
- 56. Сванте Август Аррениус (1859-1927) Основные положения теории электроли-тической диссоциации (распада на ионы) разработаны в 1887 г.
- 57. Иван Алексеевич Каблуков (1857-1942) Владимир Александрович Кистяковский (1865 –1952) Дальнейшее развитие представления об электролитической диссоциации получили
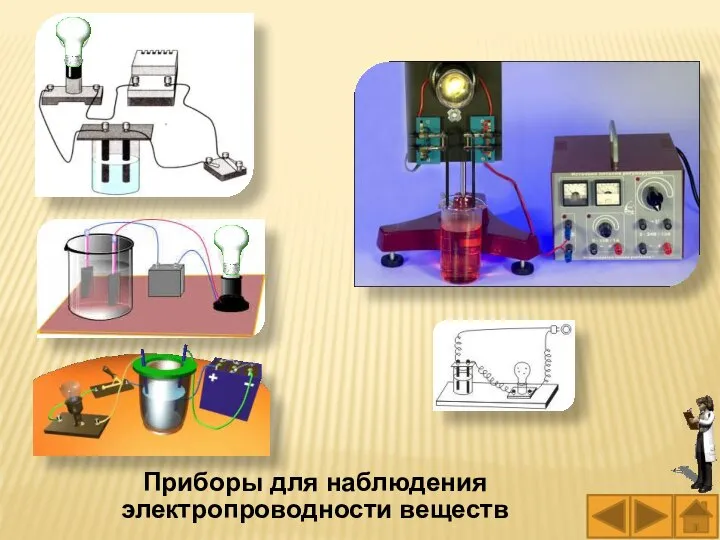
- 58. Вам известно из курса физики и повседневной жизни, что водные растворы и расплавы одних веществ проводят
- 59. Приборы для наблюдения электропроводности веществ
- 61. Электролитическая диссоциация – это распад электролита на свободно перемещаю-щиеся ионы при растворении его в воде или
- 63. Дистиллированная вода, которая имеет молекулярную структуру, является хорошим изолятором (неэлектролитом), т.к. в ней нет свободных электри-ческих
- 64. Тем не менее, вода незначительно диссоци-ирует. Традиционная форма записи дис-социации воды на ионы водорода и гидроксила
- 65. Вспомним: при написании ионно-молекуляр-ных уравнений нельзя расписывать на ионы: нерастворимые и малорастворимые вещест-ва; твердые вещества; газы;
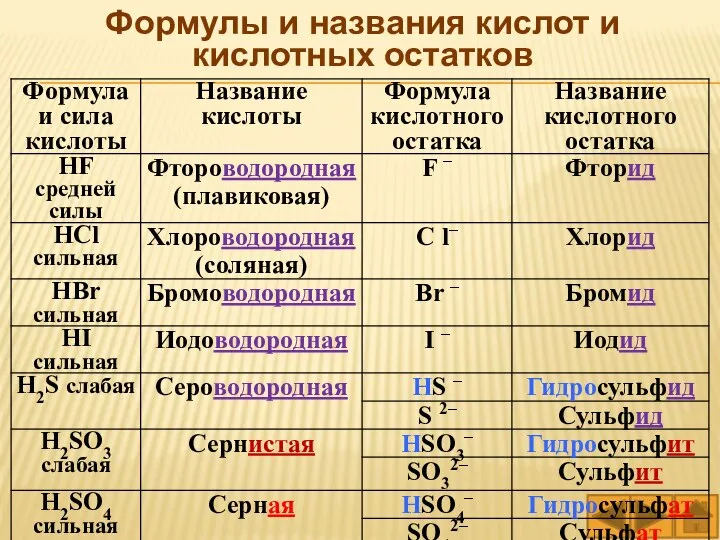
- 66. Формулы и названия кислот и кислотных остатков
- 67. Формулы и названия кислот и кислотных остатков
- 68. Классическая реакция нейтрализации в молекулярной форме записи процесса: NaOH + НСl ⇔ NaCl + Н2O при
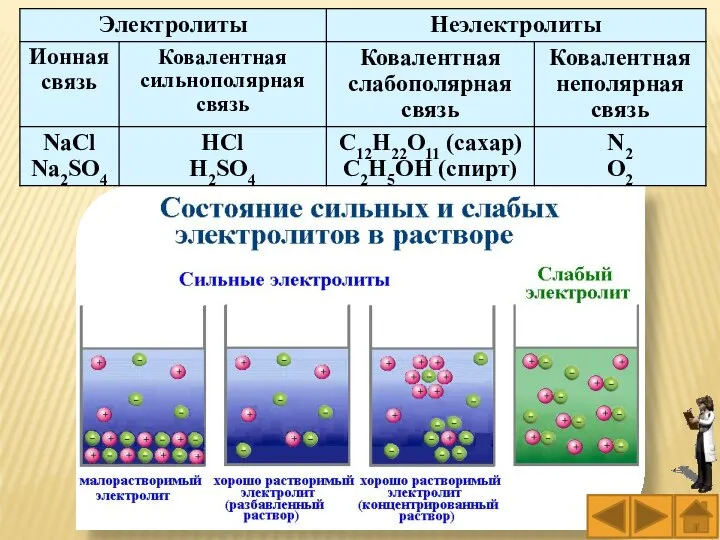
- 69. Возможность распада растворённого вещества на ионы определяется его природой. Распадаются на ионы немолекулярные (ионные) соединения (например,
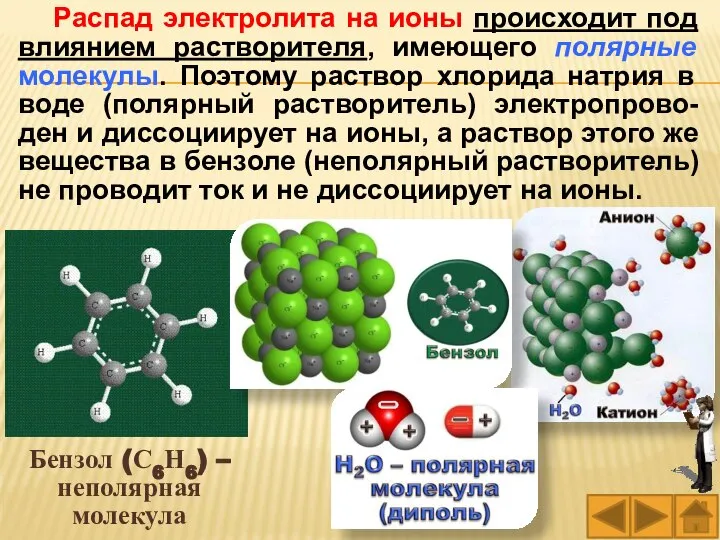
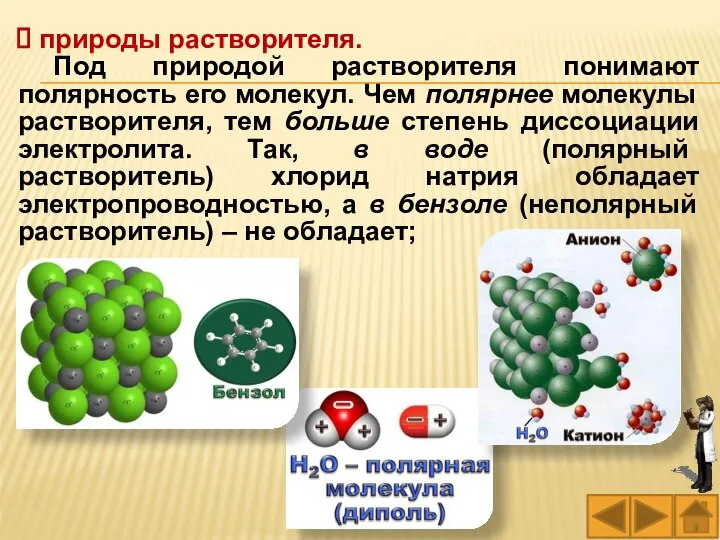
- 70. Бензол (С6Н6) – неполярная молекула Распад электролита на ионы происходит под влиянием растворителя, имеющего полярные молекулы.
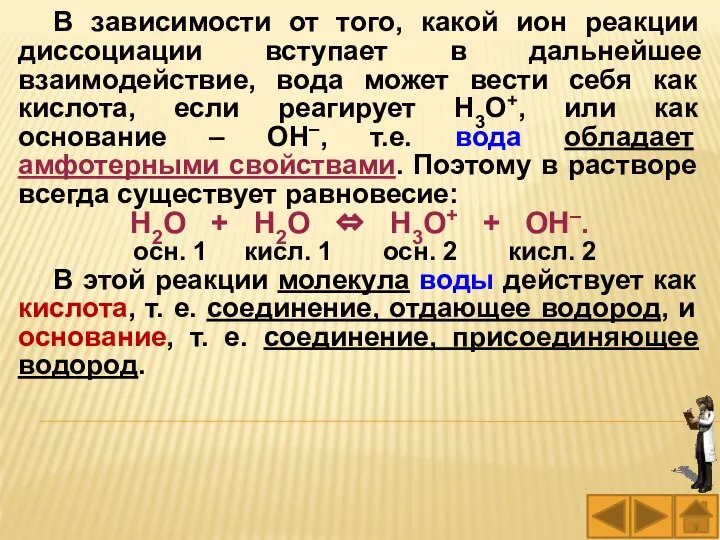
- 71. В зависимости от того, какой ион реакции диссоциации вступает в дальнейшее взаимодействие, вода может вести себя
- 72. Насколько полно электролит диссоциирует на ионы, показывает его степень диссоциации, которую обозначают греческой буквой α («альфа»).
- 73. Степень диссоциации зависит от: концентрации электролита в растворе. С уменьшением концентрации электролита (при разбавлении раствора водой)
- 74. природы растворителя. Под природой растворителя понимают полярность его молекул. Чем полярнее молекулы растворителя, тем больше степень
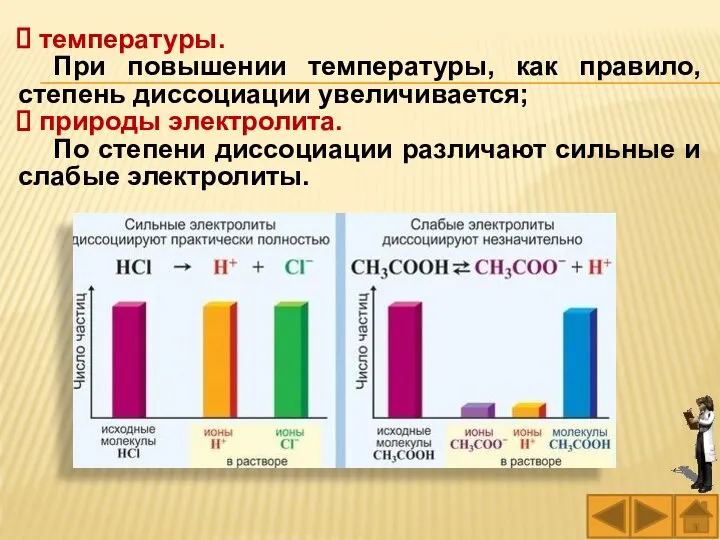
- 75. температуры. При повышении температуры, как правило, степень диссоциации увеличивается; природы электролита. По степени диссоциации различают сильные
- 77. Классификация электролитов по степени их диссоциации
- 78. Сильные электролиты при растворении в воде практически полностью диссоциируют на ионы независимо от их концентрации в
- 79. Слабые электролиты в водных растворах лишь частично (обратимо) диссоциируют на ионы. Поэтому в уравнениях диссоциации слабых
- 80. Среду любого водного раствора можно охарактеризовать содержанием ионов водорода Н+ или гидроксид-ионов ОН–. Водные растворы могут
- 81. Кислотная среда – это среда, в которой число ионов водорода больше числа гидроксид-ионов. Например, все кислоты
- 82. Щелочная среда – это среда, в которой число ионов водорода меньше числа гидроксид-ионов. Например, щелочную среду
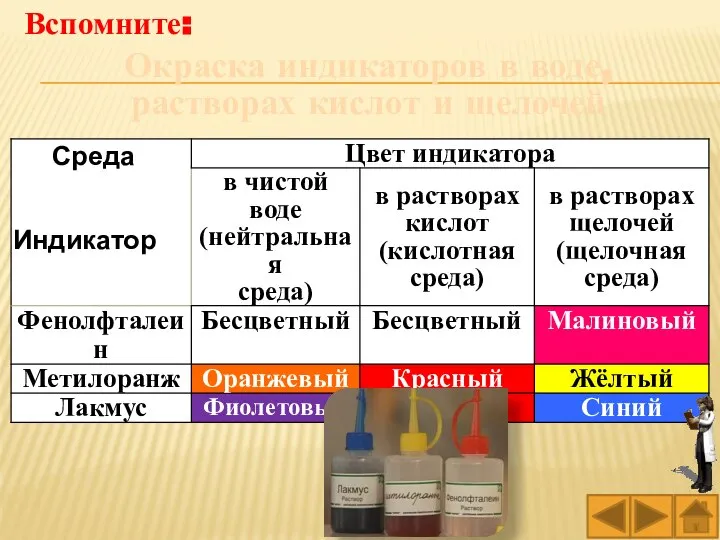
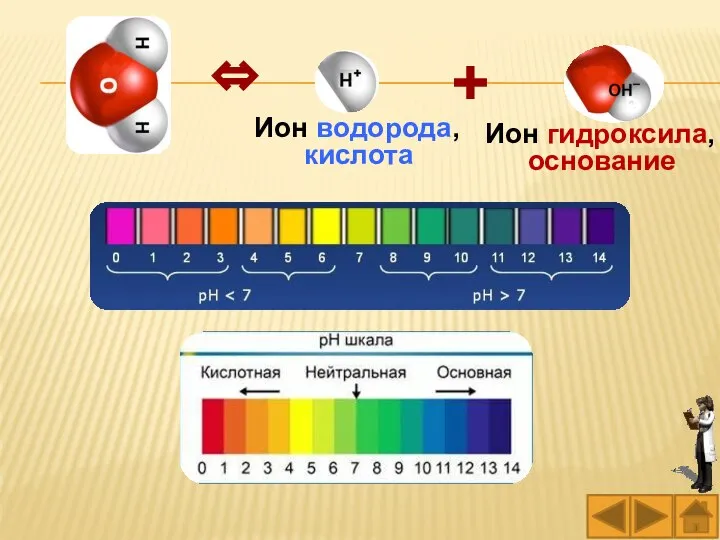
- 83. Окраска индикаторов в воде, растворах кислот и щелочей Вспомните:
- 84. Кислота Вода Щелочь Метиловый оранжевый (метилоранж) Фенолфталеин Кислота Вода Щелочь
- 85. Лакмус Лакмус в воде
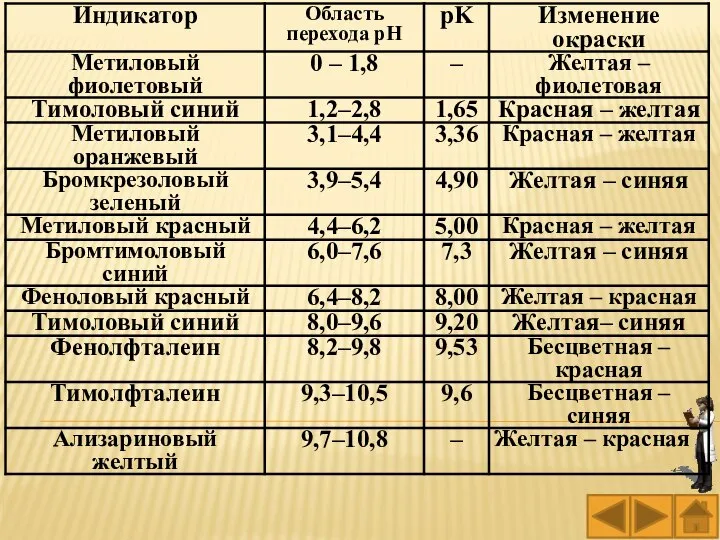
- 86. Индикатор меняет окраску в определенном интервале значений рН. Интервал перехода окраски индикатора: ΔрН = рКинд ±
- 88. Лакмус в аналитической химии при титровании не используется, так как имеет широкую область перехода окраски (5,0
- 89. Состояние равновесия процесса диссоциа-ции воды характеризуется константой диссоциации: Концентрация ионов и молекул в уравнении выражается в
- 90. Традиционно в курсах общей химии отмечается, что нейтральная реакция среды, когда [Н3О+] = [ОН–], при температуре
- 91. Для оценки кислотности, нейтральности и щелочности – активной реакции среды водных растворов – удобно пользоваться не
- 92. Значение рН раствора можно определить с помощью универсального индикатора и более точно методом титрования (рассмотрим позже).
- 93. Ион водорода, кислота + Ион гидроксила, основание ⇔
- 95. Алексеев Л.С. Контроль качества воды: учебник. – 3-е изд., перераб. и доп. – М.: ИНФРА-М, 2014.–
- 96. http://www.ecology-portal.ru/publ/4-1-0-789 http://www.vodoobmen.ru/13-prop.html http://www.o8ode.ru/article/dwater/pi_water/ http://www.ibe-techno.com/e/piwater/piwater.html http://www.piwater.net/ http://www.pi-water.com/new/en_water_DrPi_WhatIsPi.html http://www.medicinform.net/biochemistry/voda_1.htm http://missis-lanaluk.hiblogger.net/ http://www.o8ode.ru/article/energo/emotoenergy/remem.htm http://structuravody.ru/index.php?id=71 http://www.vodoobmen.ru/13-prop.html. Использованные источники
- 97. Габриелян О. С., Остроумов И. Г. Химия для профессий и специальностей технического профиля: учебник для студ.
- 98. http://www.webqc.org/periodictable-Rutherfordium-Rf.html https://ru.wikipedia.org/wiki/%D0%9B%D1%8C%D1%8E%D0%B8%D1%81,_%D0%93%D0%B8%D0%BB%D0%B1%D0%B5%D1%80%D1%82_%D0%9D%D1%8C%D1%8E%D1%82%D0%BE%D0%BD http://podelise.ru/docs/index-24513145-1.html http://www.syl.ru/article/150485/mod_stepen-dissotsiatsii-elektrolityi-i-polojeniya-teorii-elektroliticheskoy-dissotsiatsii Новошннский И. И., Новошинская Н. С. Химия: учебник для 10(11) класса общеобразователь-ных
- 99. http://ppt4web.ru/khimija/ehlektroliticheskaja-dissociacija.html http://www.tryphonov.ru/tryphonov5/terms5/pK4.htm http://demexp.pspu.ru/digital_resources?page=3 http://autosquad.ru/kak-polzovatsya-areometrom http://rpp.nashaucheba.ru/docs/index-53922.html http://fizhim.com/prigotovlenie-rastvora-i-izmerenie-e/ http://pogrebok.net/shop/termometry_areometry/areometr_dlya_soli/ http://lib.convdocs.org/docs/index-63955.html?page=7 http://ru.convdocs.org/docs/index-160605.html http://www.gastroscan.ru/handbook/117/2846 http://liidweb.com/node/7683 Использованные источники
- 100. http://www.kristallikov.net/page5.html http://texvedkom.org/archives/115 http://wiseparents.ru/eksperiment-s-kapustoj-ili-kak-menya-obvinili-v-besxozyajstvenosti/ http://interactions.iciq.es/divulgaciocientifica/es/2013/01/06/larc-de-sant-marti-de-la-col-llombarda/ Использованные источники
- 102. Скачать презентацию








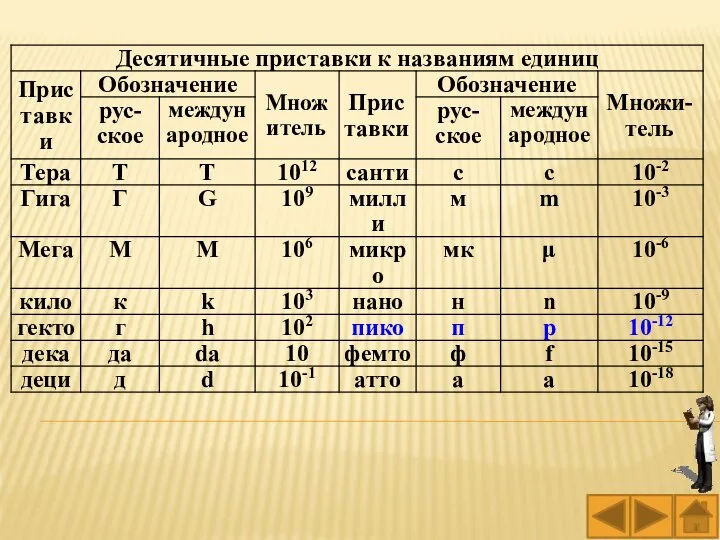


























































 Решение задач на нахождение молекулярной формулы газообразного алкана
Решение задач на нахождение молекулярной формулы газообразного алкана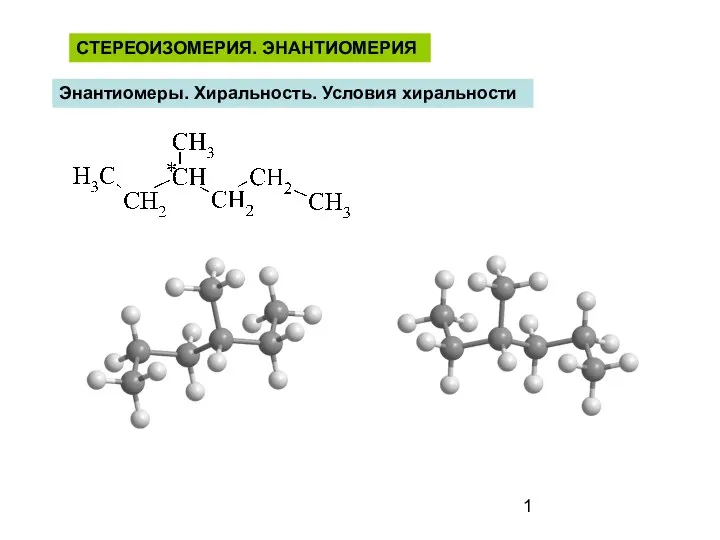 Стереоизомерия. Энантиомерия. Энантиомеры. Хиральность. Условия хиральности
Стереоизомерия. Энантиомерия. Энантиомеры. Хиральность. Условия хиральности Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Кинетика химических реакций. Основные понятия и законы химической кинетики
Кинетика химических реакций. Основные понятия и законы химической кинетики Кристаллы. Виды
Кристаллы. Виды Фуллерен, его свойства, производство и применение
Фуллерен, его свойства, производство и применение Алканы. Строение алканов
Алканы. Строение алканов 6-я группа элементов. 9 класс
6-я группа элементов. 9 класс Презентация Углерод Carboneum происходит от лат. carbo — уголь.
Презентация Углерод Carboneum происходит от лат. carbo — уголь. Интересные свойства редких металлов
Интересные свойства редких металлов Химические реакции. по фазовому составу
Химические реакции. по фазовому составу Совместимость электродных материалов в новой электрохимической системе Li4Ti5O12/Li3V2(PO4)3 с традиционным электролитом для
Совместимость электродных материалов в новой электрохимической системе Li4Ti5O12/Li3V2(PO4)3 с традиционным электролитом для Рекомендации по подготовке учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии
Рекомендации по подготовке учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии Гидролиз
Гидролиз Презентация по Химии "Діопсид силікати" - скачать смотреть
Презентация по Химии "Діопсид силікати" - скачать смотреть  Дисперсные системы: общая характеристика и классификация
Дисперсные системы: общая характеристика и классификация Алюминий – металл будущего
Алюминий – металл будущего Анализ качества неорганических лекарственных средств количественно определяемых методами редоксиметрии
Анализ качества неорганических лекарственных средств количественно определяемых методами редоксиметрии Химические реакции. Закон сохранения массы веществ
Химические реакции. Закон сохранения массы веществ Видалення забруднень із поверхні тканини Виконали: Сидорова Анастасія Труба Альона
Видалення забруднень із поверхні тканини Виконали: Сидорова Анастасія Труба Альона  Общая характеристика металлов. Металлическая связь
Общая характеристика металлов. Металлическая связь Обобщение по теме: «Азот»( урок-сказка) Тайны царства Азота
Обобщение по теме: «Азот»( урок-сказка) Тайны царства Азота Аттестационная работа. Программа элективного курса по химии экологическая химия
Аттестационная работа. Программа элективного курса по химии экологическая химия Железо и его соединения
Железо и его соединения Нітрати – токсичні речовини
Нітрати – токсичні речовини  Неорганическая химия 8 класс г. Азов школа №9 учитель: Карасёв Евгений Владимирович
Неорганическая химия 8 класс г. Азов школа №9 учитель: Карасёв Евгений Владимирович  Дисперсные системы. Свойства коллоидных растворов
Дисперсные системы. Свойства коллоидных растворов Строение твердых и жидких металлов. Зональная ликвация
Строение твердых и жидких металлов. Зональная ликвация