Содержание
- 2. Цели урока. Образовательная – познакомить учащихся с основными химическими свойствами белков на основе проведения опытов и
- 3. Задачи урока. Учащиеся должны изучить химические свойства белков, этапы синтеза белка в клетке и роль белков
- 4. Белки – это высокомолекулярные органические соединения, представляющие собой биополимер, состоящий из мономеров, которыми являются аминокислоты соединенные
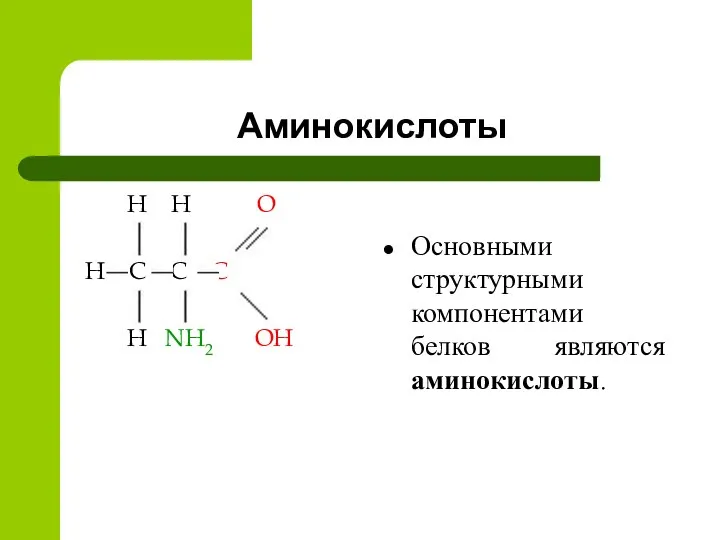
- 5. Аминокислоты H H O H C C C H NH2 OH Основными структурными компонентами белков являются
- 6. Образование пептидной связи NH2 – CH2 – COOH + NH2 – CH2 – COOH = NH2
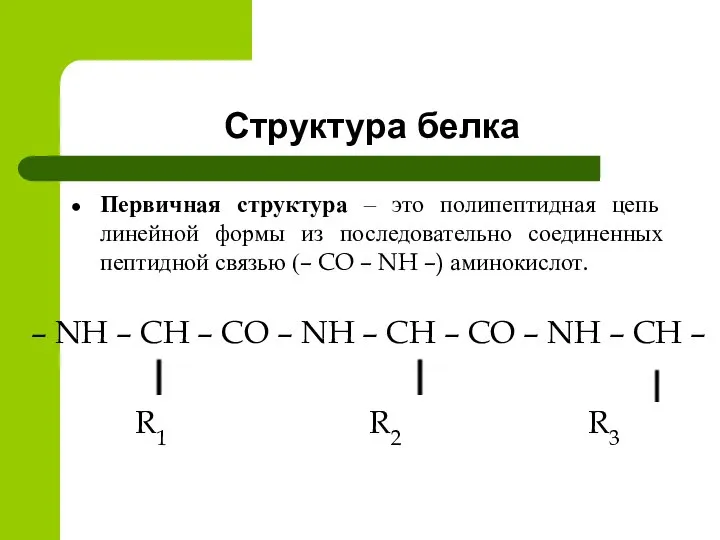
- 7. Структура белка Первичная структура – это полипептидная цепь линейной формы из последовательно соединенных пептидной связью (–
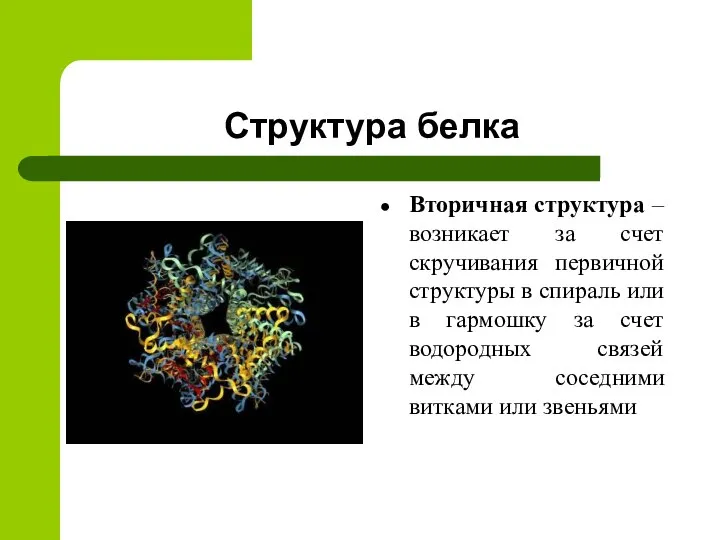
- 8. Структура белка Вторичная структура – возникает за счет скручивания первичной структуры в спираль или в гармошку
- 9. Структура белка Третичная структура – это глобулярная форма, образующаяся за счет гидрофобных связей между радикалами аминокислот
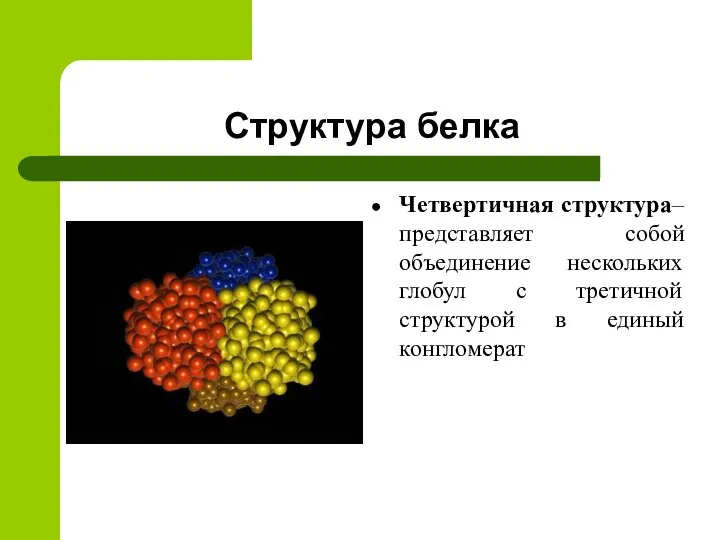
- 10. Структура белка Четвертичная структура– представляет собой объединение нескольких глобул с третичной структурой в единый конгломерат
- 11. Свойства белков Белки могут быть как растворимы, так и нерастворимы в воде в зависимости от их
- 12. Свойства белков Водорастворимые белки образуют коллоидные растворы
- 13. Свойства белков При обработке хлоридом натрия белки высаливаются из раствора. Этот процесс обратим.
- 14. Свойства белков Кислоты, щелочи и высокая температура разрушают структуру белков и приводят к их денатурации. Белки
- 15. Свойства белков Поместите кусочек прессованного творога в пробирку и добавьте несколько капель азотной кислоты. Осторожно нагрейте.
- 16. Свойства белков. Налейте в пробирку 2 мл яичного белка. Добавьте такой же объем концентрированного раствора гидроксида
- 17. Новые понятия: Гидролиз белков – разрушение первичной структуры белка. Денатурация – полное разрушение пространственной структуры белка.
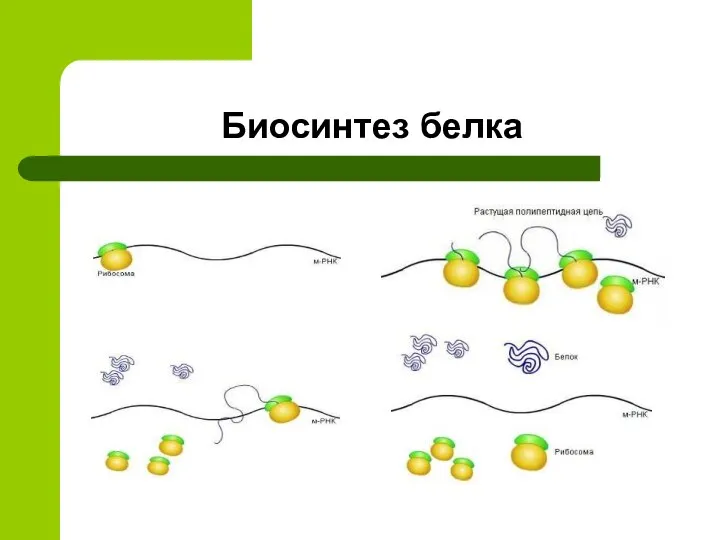
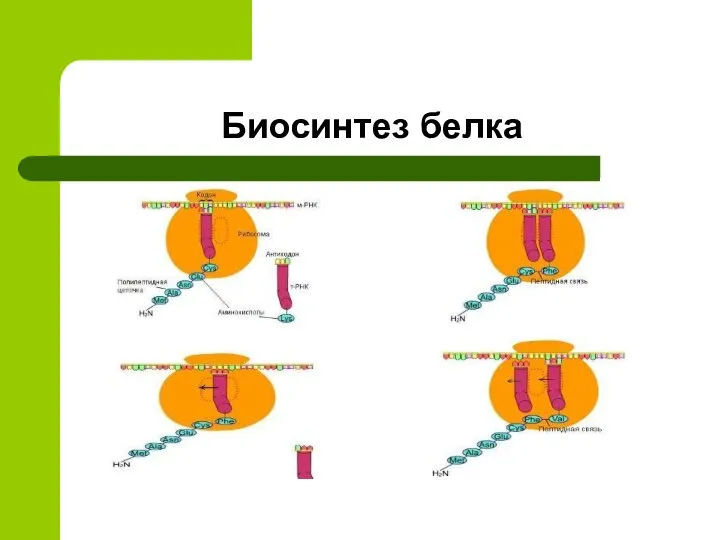
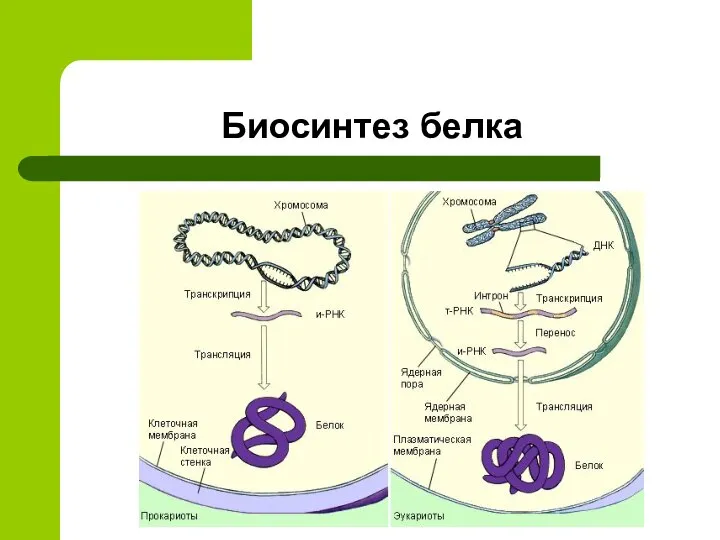
- 18. Биосинтез белка
- 19. Биосинтез белка
- 20. Биосинтез белка
- 22. Скачать презентацию










 Химия и повседневная жизнь человека
Химия и повседневная жизнь человека «Азот»және «Фосфор»элементтерін салыстырыңдар,мәліметтерді кестеге толтырыңдар
«Азот»және «Фосфор»элементтерін салыстырыңдар,мәліметтерді кестеге толтырыңдар ЦІКАВІ ФАКТИ ПРО ЗОЛОТО
ЦІКАВІ ФАКТИ ПРО ЗОЛОТО  Химическая связь
Химическая связь Белки. Классификация белков. (Тема 2)
Белки. Классификация белков. (Тема 2) Извлечение как единство процессов десорбции, растворения и диффузии. Теоретические основы извлечения
Извлечение как единство процессов десорбции, растворения и диффузии. Теоретические основы извлечения Organic compounds: nomenclature
Organic compounds: nomenclature Химическая стойкость тугоплавких металлов в различных реагентах
Химическая стойкость тугоплавких металлов в различных реагентах Процессы проявления и фиксирования
Процессы проявления и фиксирования Растворы электролитов
Растворы электролитов КВН В МИРЕ ВЕЩЕСТВ
КВН В МИРЕ ВЕЩЕСТВ Предмет и задачи биохимии. Ферменты. Регуляция активности ферментов. (Лекция 3)
Предмет и задачи биохимии. Ферменты. Регуляция активности ферментов. (Лекция 3) Жизненный Путь Дмитрия Ивановича Менделеева Выполнила ученица 10-А класса Рипка Елизавета
Жизненный Путь Дмитрия Ивановича Менделеева Выполнила ученица 10-А класса Рипка Елизавета  Вещества и явления в окружающем мире
Вещества и явления в окружающем мире Аттестационная работа. Проектная и исследовательская деятельность как способ формирования химических знаний и умений
Аттестационная работа. Проектная и исследовательская деятельность как способ формирования химических знаний и умений Химические реакции разложения и соединения
Химические реакции разложения и соединения Нефть как дисперсная система
Нефть как дисперсная система Органічні сполуки в живій природі
Органічні сполуки в живій природі  Основы кристаллографии
Основы кристаллографии Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства.
Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства.  ПРИРОДНЫЕ ЯДЫ
ПРИРОДНЫЕ ЯДЫ Химическая связь и ее типы
Химическая связь и ее типы Вода - Н2О
Вода - Н2О Иондық және ковалентті байланысы бар қосылыстардың электролиттік диссоциациясы
Иондық және ковалентті байланысы бар қосылыстардың электролиттік диссоциациясы Характеристики элемента по его положению в ПСХЭ Д.И.Менделеева
Характеристики элемента по его положению в ПСХЭ Д.И.Менделеева Яблоки и здоровье человека
Яблоки и здоровье человека Презентация по Химии "Предмет химии" - скачать смотреть
Презентация по Химии "Предмет химии" - скачать смотреть  Презентация по Химии "ХИМИЯ НА КУХНЕ" - скачать смотреть бесплатно
Презентация по Химии "ХИМИЯ НА КУХНЕ" - скачать смотреть бесплатно