Содержание
- 2. Цели урока: Изучить свойства металлов 3 А группы на примере алюминия. Дать характеристику элемента по его
- 3. «Серебро из глины» Немецкий учёный Ф. Велер (1827 г.) получил алюминий при нагревании хлорида алюминия со
- 4. Из истории открытия В период открытия алюминия - металл был дороже золота. Англичане хотели почтить богатым
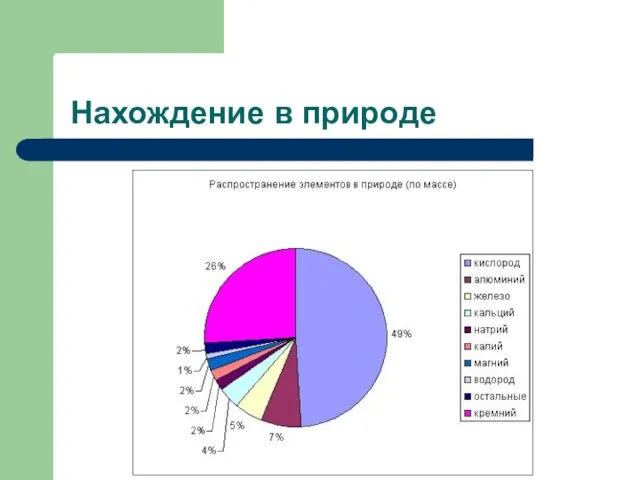
- 5. Нахождение в природе
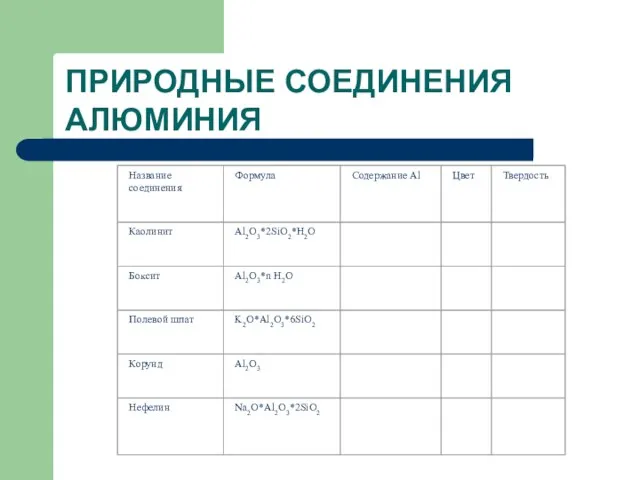
- 6. ПРИРОДНЫЕ СОЕДИНЕНИЯ АЛЮМИНИЯ
- 7. Физические свойства Алюминий – металл серебристо- белого цвета, лёгкий ( q- 2,7 г./ см.3), плавится при
- 8. Химические свойства Алюминий восстанавливает все элементы, находящиеся справа от него в электрохимическом ряду напряжения металлов, простые
- 9. Применение алюминия Al
- 11. Скачать презентацию






 Щелочные металлы
Щелочные металлы Винная кислота
Винная кислота Презентация по Химии "Горение кислорода" - скачать смотреть
Презентация по Химии "Горение кислорода" - скачать смотреть  Амины - производные аммиака
Амины - производные аммиака Минерал гранат
Минерал гранат Живопись Англии 17 века
Живопись Англии 17 века  Алканы
Алканы Галогены. Хлор
Галогены. Хлор Конструкционные материалы на основе легких металлов: сплавы алюминия
Конструкционные материалы на основе легких металлов: сплавы алюминия Барометр – анероид. Атмосферное давление на различных высотах. Манометры
Барометр – анероид. Атмосферное давление на различных высотах. Манометры Тест по неорганической химии
Тест по неорганической химии Использование химии в медицине
Использование химии в медицине Кремний және оның қосылыстары
Кремний және оның қосылыстары Эрбий. Жалпы сипаттамасы
Эрбий. Жалпы сипаттамасы Анод + Катод = Электролиз Выполнил: ученик 11М класса МОУ лицея №6 Аббязов Эрик
Анод + Катод = Электролиз Выполнил: ученик 11М класса МОУ лицея №6 Аббязов Эрик Азотсодержащие органические соединения
Азотсодержащие органические соединения Моделирование фазовых систем. Тройные взаимные системы
Моделирование фазовых систем. Тройные взаимные системы Факторы, влияющие на смещение химического равновесия (концентрация реагентов, температура, давление )
Факторы, влияющие на смещение химического равновесия (концентрация реагентов, температура, давление ) Гетероорганические углеводороды нефти и асфальто-смолистые вещества
Гетероорганические углеводороды нефти и асфальто-смолистые вещества Поверхностные явления
Поверхностные явления Кондуктометрия. Приборы кондуктометрии. Достоинства метода. Классификация
Кондуктометрия. Приборы кондуктометрии. Достоинства метода. Классификация Химические реакции. Реакции по тепловому эффекту
Химические реакции. Реакции по тепловому эффекту МОУ «Средняя школа № 14» г. Кимры Тверской Области урок химии в 11 классе Учитель: Иванова Ирина Викторовна
МОУ «Средняя школа № 14» г. Кимры Тверской Области урок химии в 11 классе Учитель: Иванова Ирина Викторовна  Кислородсодержащие органические соединения. Спирты. Фенолы. Альдегиды
Кислородсодержащие органические соединения. Спирты. Фенолы. Альдегиды Презентация по Химии "Теория тарелок. Хроматографические идентификация. Количественный анализ" - скачать смотреть
Презентация по Химии "Теория тарелок. Хроматографические идентификация. Количественный анализ" - скачать смотреть  Растворение. Растворимость веществ в воде
Растворение. Растворимость веществ в воде Бензол. Получение бензола. Химические свойства бензола. Применение бензола на основе его свойств
Бензол. Получение бензола. Химические свойства бензола. Применение бензола на основе его свойств Химические вещества парабены
Химические вещества парабены