Содержание
- 2. Амінокислоти – гетерофункціональні сполуки, молекули яких містять одночасно аміногрупу і карбоксильну. Загальна формула амінокислот:
- 3. Різноманітні пептиди і білки складаються із залишків α-амінокислот. Частіше за все термін "амінокислота" застосовують для позначення
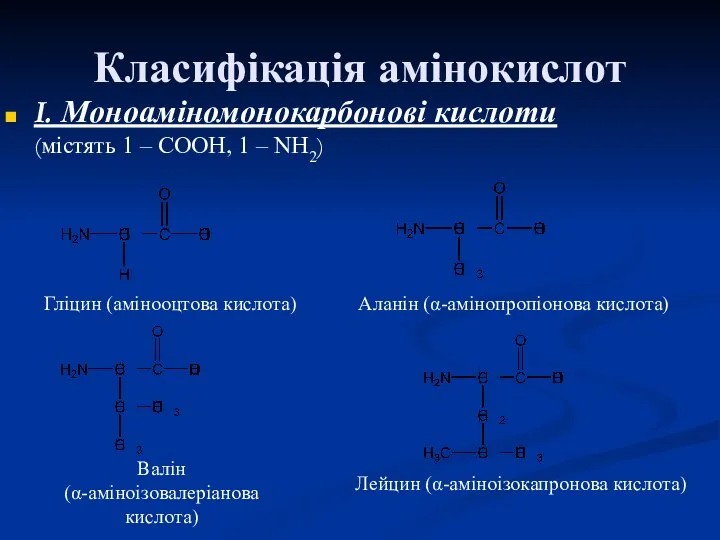
- 4. Класифікація амінокислот I. Моноаміномонокарбонові кислоти (містять 1 – СООН, 1 – NH2) Гліцин (амінооцтова кислота) Аланін
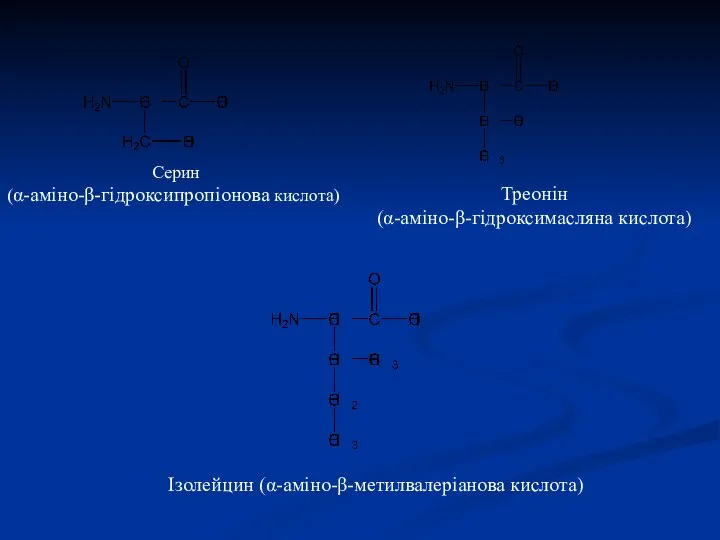
- 5. Треонін (α-аміно-β-гідроксимасляна кислота) Серин (α-аміно-β-гідроксипропіонова кислота) Ізолейцин (α-аміно-β-метилвалеріанова кислота)
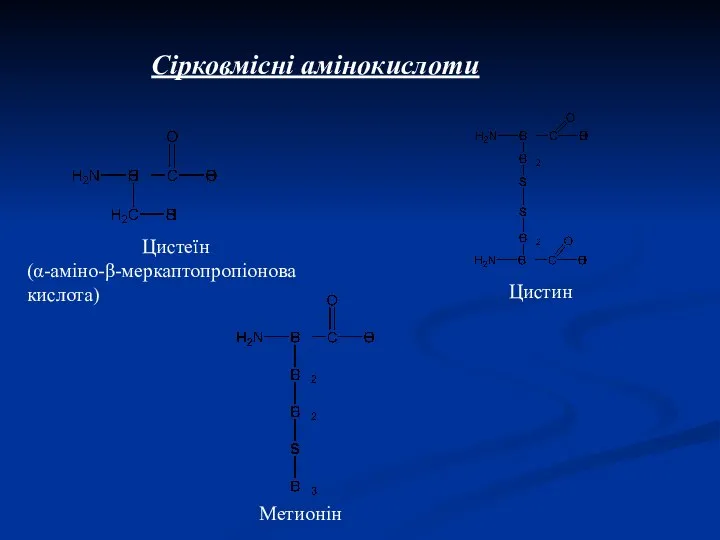
- 6. Сірковмісні амінокислоти Цистеїн (α-аміно-β-меркаптопропіонова кислота) Цистин Метионін
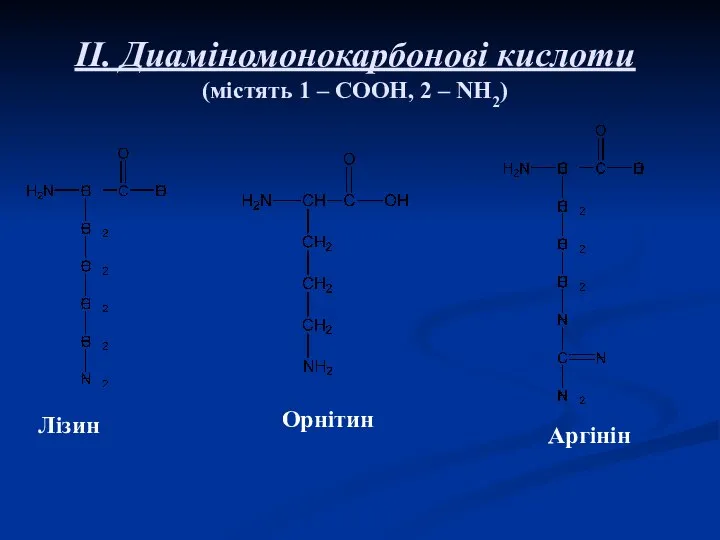
- 7. II. Диаміномонокарбонові кислоти (містять 1 – СООН, 2 – NH2) Лізин Орнітин Аргінін
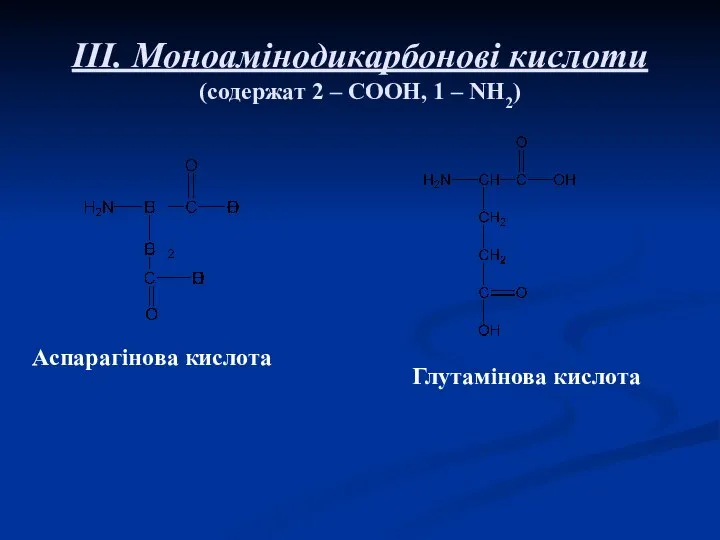
- 8. III. Моноамінодикарбонові кислоти (содержат 2 – СООН, 1 – NH2) Аспарагінова кислота Глутамінова кислота
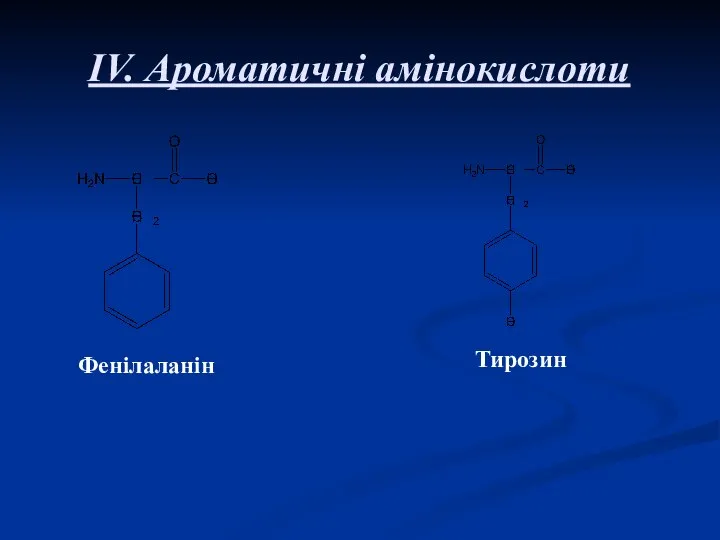
- 9. IV. Ароматичні амінокислоти Фенілаланін Тирозин
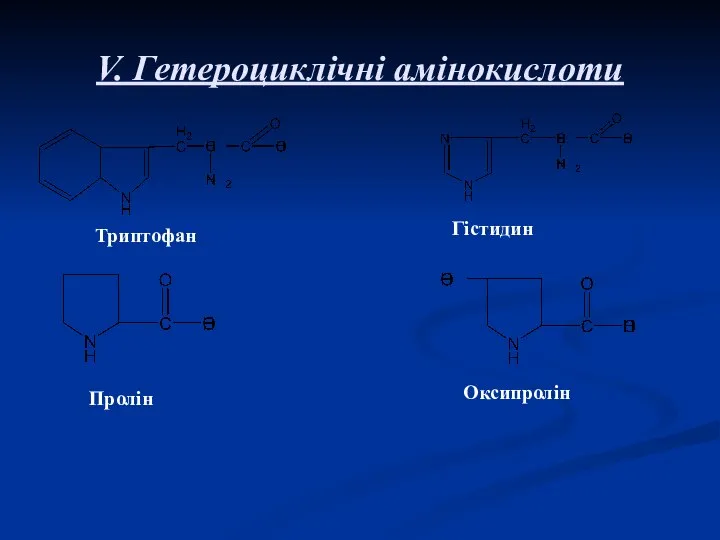
- 10. V. Гетероциклічні амінокислоти Триптофан Гістидин Пролін Оксипролін
- 11. Амінокислоти Замінні Гліцин Аланін Серин Цистеїн Аспарагінова кислота Глутамінова кислота Тирозин Пролін Аспарагін Глутамін Незамінні Треонін
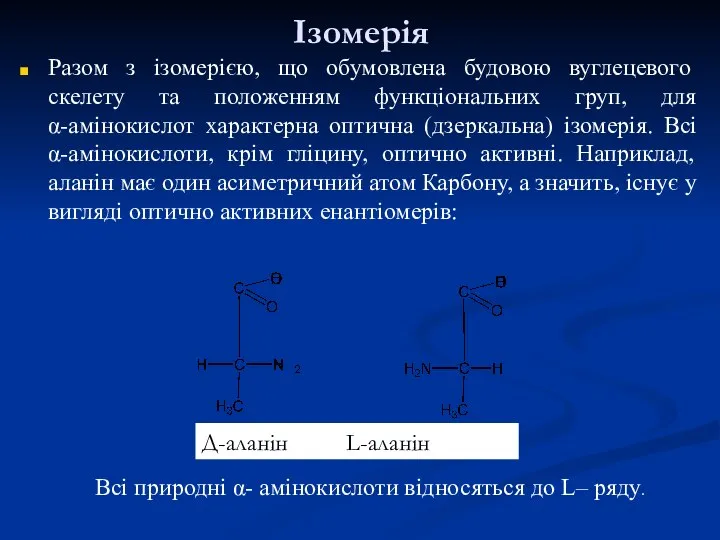
- 12. Ізомерія Разом з ізомерією, що обумовлена будовою вуглецевого скелету та положенням функціональних груп, для α-амінокислот характерна
- 13. Фізичні властивості Амінокислоти представляють собою кристалічні речовини з високими (вище 250°С) температурами плавлення, які мало відрізняються
- 16. Хімічні властивості 1. Дисоціація амінокислот: а) Моноаміномонокарбонові кислоти гліцин Білки, в складі яких переважає такий тип
- 17. б) Диаміномонокарбонові кислоти лізин в) Моноамінодикарбонові кислоти Аспарагінова кислота Білки, в складі яких переважає такий тип
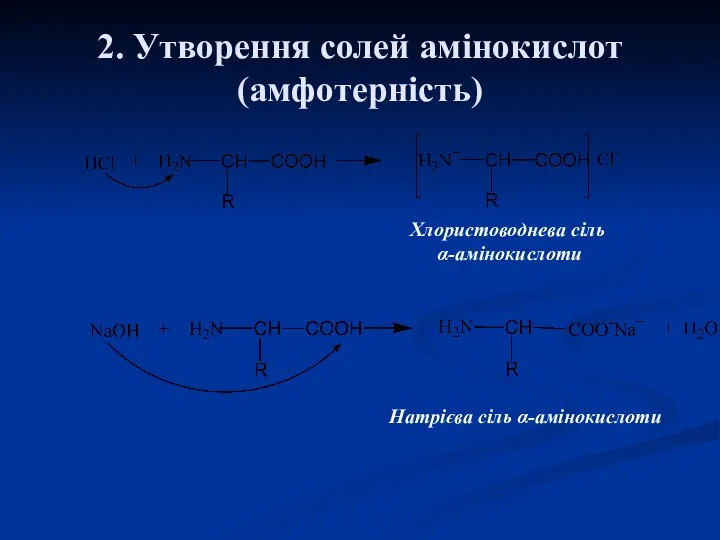
- 18. 2. Утворення солей амінокислот (амфотерність) Хлористоводнева сіль α-амінокислоти Натрієва сіль α-амінокислоти
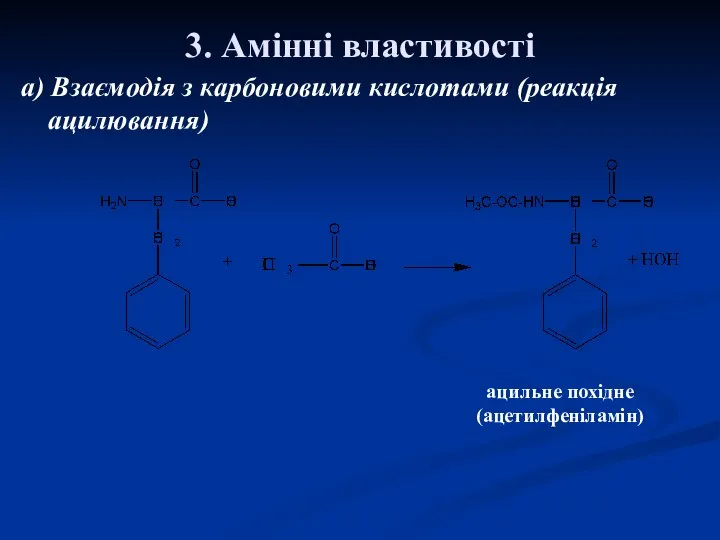
- 19. 3. Амінні властивості а) Взаємодія з карбоновими кислотами (реакція ацилювання) ацильне похідне (ацетилфеніламін)
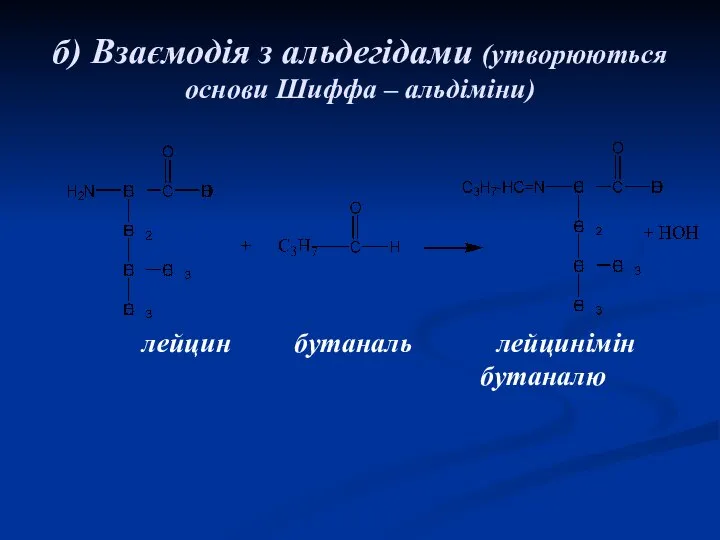
- 20. б) Взаємодія з альдегідами (утворюються основи Шиффа – альдіміни) лейцин бутаналь лейцинімін бутаналю
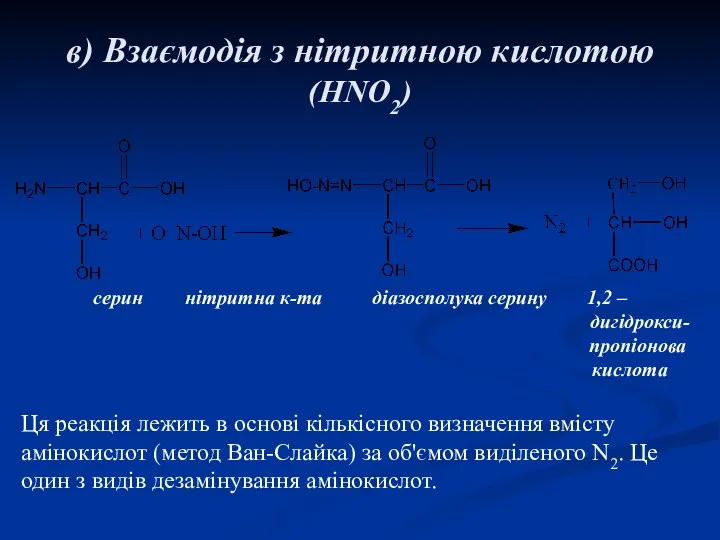
- 21. в) Взаємодія з нітритною кислотою (HNO2) серин нітритна к-та діазосполука серину 1,2 – дигідрокси- пропіонова кислота
- 22. 4. Реакції за карбоксилом (кислотні властивості амінокислот) Подібно карбоновим кислотам, амінокислоти за рахунок карбоксильної групи утворюють
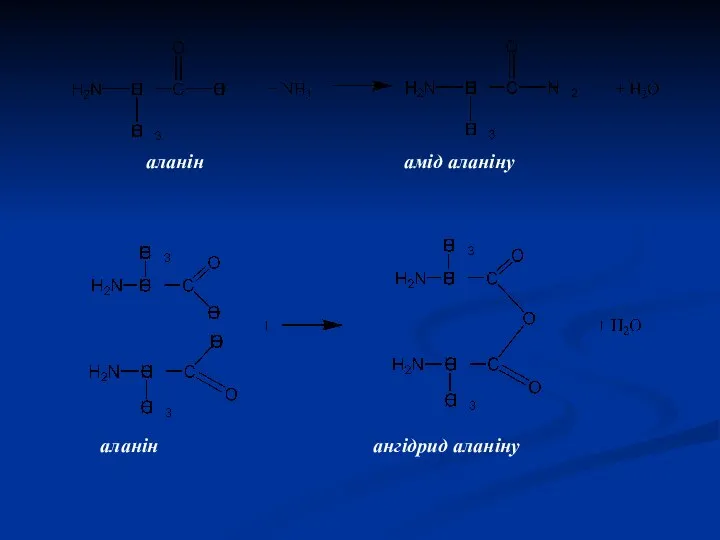
- 23. аланін амід аланіну аланін ангідрид аланіну
- 24. серин хлорангідрид серину
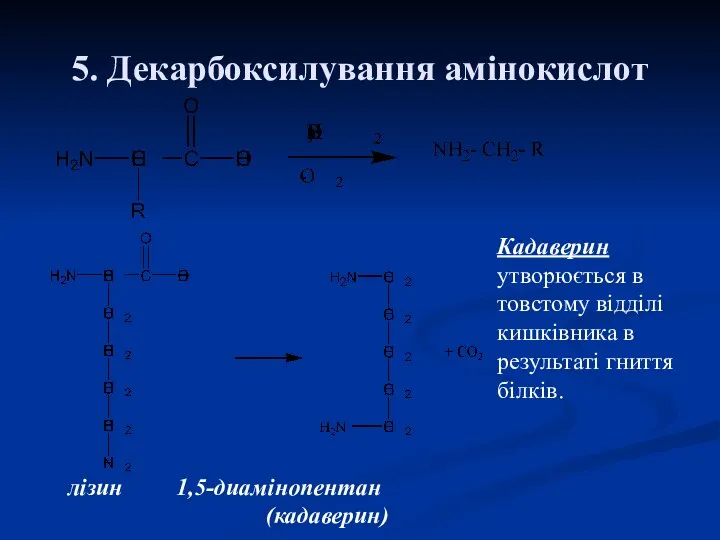
- 25. 5. Декарбоксилування амінокислот лізин 1,5-диамінопентан (кадаверин) Кадаверин утворюється в товстому відділі кишківника в результаті гниття білків.
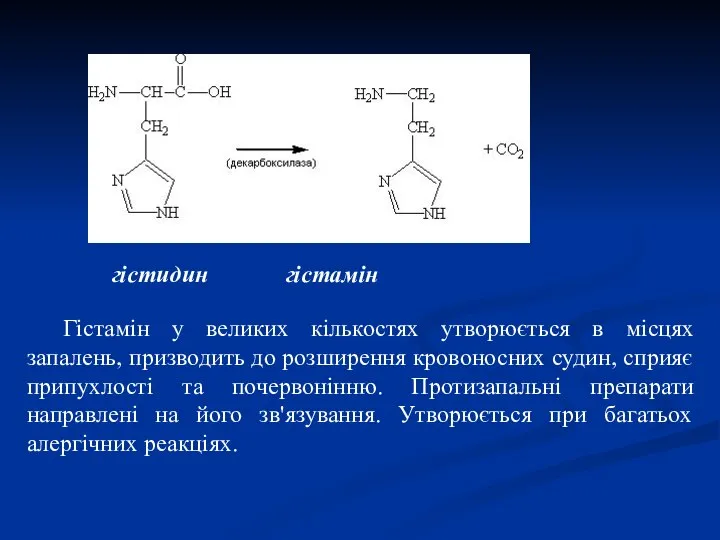
- 26. гістидин гістамін Гістамін у великих кількостях утворюється в місцях запалень, призводить до розширення кровоносних судин, сприяє
- 27. 6. Специфічні властивості амінокислот Різне розташування карбоксильних і аміногруп в молекулах амінокислот надає їм деяких відмінних
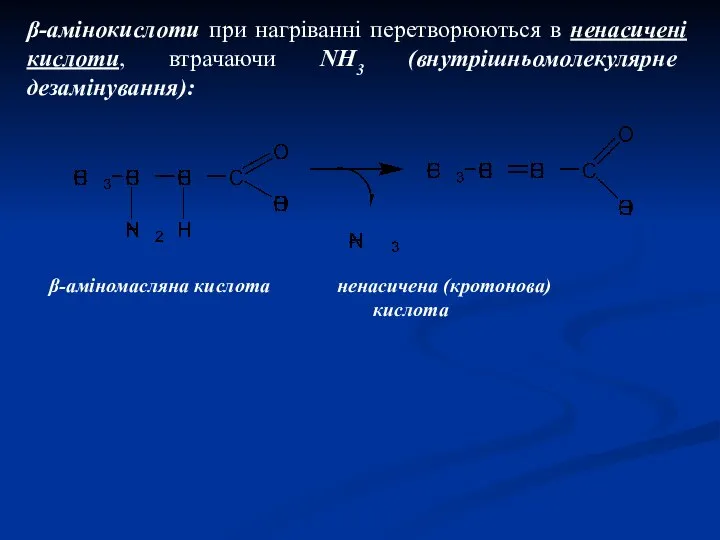
- 28. β-амінокислоти при нагріванні перетворюються в ненасичені кислоти, втрачаючи NH3 (внутрішньомолекулярне дезамінування): β-аміномасляна кислота ненасичена (кротонова) кислота
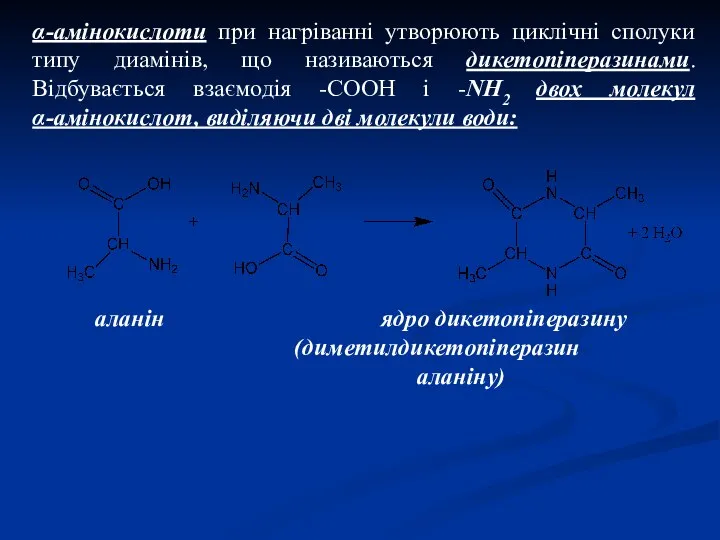
- 29. α-амінокислоти при нагріванні утворюють циклічні сполуки типу диамінів, що називаються дикетопіперазинами. Відбувається взаємодія -СООН і -NH2
- 30. 7. Утворення поліпептидів Метионін треонін цистеїн пептидные связи трипептид (метионіл-треоніл-цистеїн, мет-тре-цис)
- 31. Біологічна роль амінокислот 1. Амінокислоти називають «цеглинками життя», тобто білки складаються із залишків амінокислот. 2. Амінокислоти
- 32. Якісна реакція на амінокислоти мідна сіль гліцину Характерною особливістю амінокислот є здатність до утворення внутрішньокомплексних солей
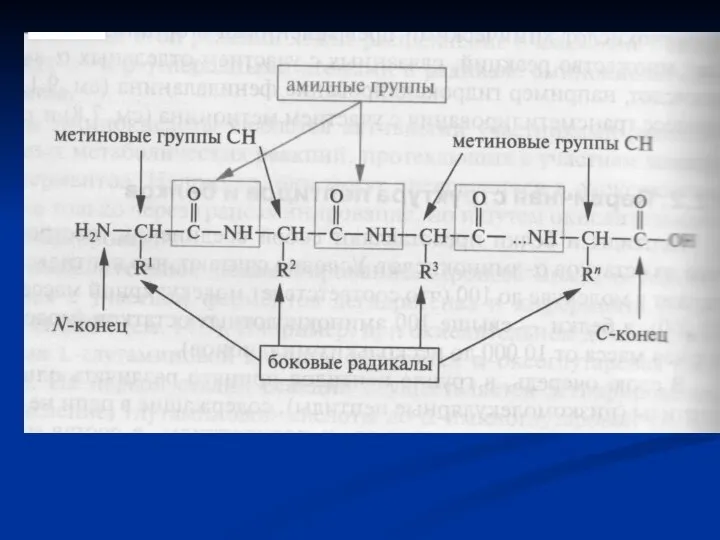
- 33. Пептиди і білки Пептиди і білки представляють собою високомолекулярні органічні сполуки, які побудовані із залишків α-
- 35. Пептиди Пептид складається з двох або більшої кількості амінокислотних залишків, сполучених пептидними зв'язками (дипептид, трипептид ….).
- 36. Білки Білки – біологічні полімерні молекули, мономерами яких є амінокислоти, сполучені пептидними зв'язками. Індивідуальність білкових молекул
- 38. Скачать презентацию

















 Готовимся к экзамену по химии. 9 класс
Готовимся к экзамену по химии. 9 класс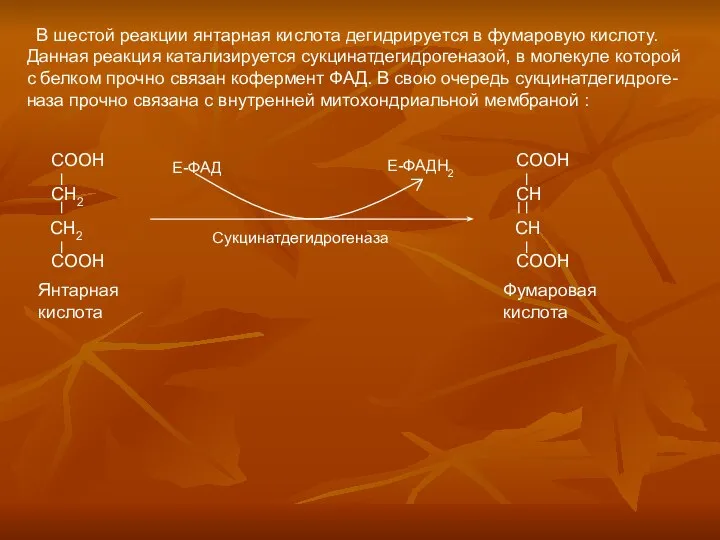 Аэробное окисление углеводов. (Часть 2)
Аэробное окисление углеводов. (Часть 2) Оксиды азота
Оксиды азота Классификация кислот
Классификация кислот Қатты күйдегі препараттар
Қатты күйдегі препараттар Полиамиды. Классификация по методу получения
Полиамиды. Классификация по методу получения Химический элемент платина
Химический элемент платина Щелочные металлы
Щелочные металлы Растворы (дисперсные системы)
Растворы (дисперсные системы) Тақырыпқа байланысты білімді жүйелеу
Тақырыпқа байланысты білімді жүйелеу II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra
II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях
Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях Генетичний зв'язок
Генетичний зв'язок Презентация по Химии "РАСТВОРЫ" - скачать смотреть бесплатно
Презентация по Химии "РАСТВОРЫ" - скачать смотреть бесплатно Органічні розчинники. Їх застосування
Органічні розчинники. Їх застосування Получение этилена и опыты с ним. (Практическая работа 2)
Получение этилена и опыты с ним. (Практическая работа 2) Презентация по Химии "Ковалентная химическая связь" - скачать смотреть бесплатно
Презентация по Химии "Ковалентная химическая связь" - скачать смотреть бесплатно Основы химической термодинамики
Основы химической термодинамики Определение свободной поверхностной энергии тонких пленок оксидов
Определение свободной поверхностной энергии тонких пленок оксидов Внеурочная работа по химии. Краеведение
Внеурочная работа по химии. Краеведение Азотная кислота
Азотная кислота Жоғары температурағы асқын өткізгіштер
Жоғары температурағы асқын өткізгіштер Введение в биоорганическую химию. Пространственное и электронное строение органических соединений
Введение в биоорганическую химию. Пространственное и электронное строение органических соединений Исследовательская работа на тему: Удивительные свойства воды
Исследовательская работа на тему: Удивительные свойства воды “Кількість речовини. Молярна маса. Молярний об’єм” Урок хімії у 8 класі КЗ Верхівцевського НВК Учитель Кукса Наталія Миколаївна.
“Кількість речовини. Молярна маса. Молярний об’єм” Урок хімії у 8 класі КЗ Верхівцевського НВК Учитель Кукса Наталія Миколаївна.  Степень окисления
Степень окисления Презентация по Химии "Щавелевая кислота" - скачать смотреть
Презентация по Химии "Щавелевая кислота" - скачать смотреть  Количества вещества
Количества вещества