Содержание
- 2. Содержание Основные понятия химической термодинамики Внутренняя энергия. Первое начало термодинамики Тепловые эффекты химических реакций. Энтальпия Основы
- 3. Химическая термодинамика изучает переходы энергии из одной формы в другую, от одной части системы к другой
- 4. Основные понятия химической термодинамики Система – вещество или совокупность веществ, находящихся во взаимодействии, реально или мысленно
- 5. Типы систем по характеру взаимодействия с внешней средой Открытая – система, для которой возможен обмен веществом
- 11. Взаимосвязь между параметрами системы – уравнение состояния Пример: уравнение состояния идеального газа (уравнение Клапейрона-Менделеева) Параметры состояния
- 12. Функции состояния внутренняя энергия U энтальпия H энтропия S энергия Гиббса G Свойства функций состояния: численные
- 13. Внутренняя энергия (U) - сумма кинетической энергии движения и потенциальной энергии взаимодействия структурных единиц (молекул, атомов,
- 20. ► Изохорический процесс – процесс, происходящий в физической системе при постоянном объеме (V = const). -
- 21. ► Изобарический процесс – процесс, происходящий в физической системе при постоянном давлении (P = const). -
- 22. ► Изобарический процесс – процесс, происходящий в физической системе при постоянном давлении (P = const). -
- 23. Стандартные условия Все вещества, участвующие в реакции, чистые Температура 298 К Парциальные давления газов или атмосферное
- 24. Термохимические уравнения - уравнения химических реакций, записанные с указанием значения энтальпии ΔH (кДж) и агрегатного состояния
- 25. Энтальпия образования - энтальпия реакции образования одного моля данного вещества из простых веществ, устойчивых в стандартных
- 26. Закон Гесса энтальпии реакций, протекающих при постоянном давлении или при постоянном объеме, не зависят от пути
- 28. 2Fe(к) + 3/2 O2(г) = Fe2O3(к), 2Fe(к) + O2(г) = 2FeO(к), 2FeO(к) + 1/2O2(г) = Fe2O3(к),
- 29. Расчет стандартной энтальпии реакции FeO(к) + H2(г) = Fe(к) + H2O(г) (1) по известным термохимическим уравнениям
- 30. Закон Гесса. Следствие 1 Энтальпия реакции равна разности сумм энтальпий образования продуктов реакции и исходных веществ
- 36. Заключение Химическая термодинамика изучает энергетические эффекты химических реакций Объектами изучения химической термодинамики являются разнообразные системы, для
- 38. Скачать презентацию



































 Требования, особенности, оценка знаний по химии. ОГЭ - 2016
Требования, особенности, оценка знаний по химии. ОГЭ - 2016 Смазывающие вещества
Смазывающие вещества Водородная связь
Водородная связь Неметаллы. Положение неметаллов в ПСХЭ Д.И. Менделеева. Галогены
Неметаллы. Положение неметаллов в ПСХЭ Д.И. Менделеева. Галогены Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований
Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований Металдар мен бейметалдар, олардың қосылыстарының қасиеттерінің период және топ бойынша өзгеруі
Металдар мен бейметалдар, олардың қосылыстарының қасиеттерінің период және топ бойынша өзгеруі Практическая работа по химии. Строение пламени
Практическая работа по химии. Строение пламени Эндогенная серия. Вулканогенно-осадочная группа
Эндогенная серия. Вулканогенно-осадочная группа Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД)
Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД) Класифікація органічних сполук за будовою вуглецевого скелету та природою функціональних груп
Класифікація органічних сполук за будовою вуглецевого скелету та природою функціональних груп “Проценты”, “Массовая доля” при решении задач. Интегрированный урок химии и математики
“Проценты”, “Массовая доля” при решении задач. Интегрированный урок химии и математики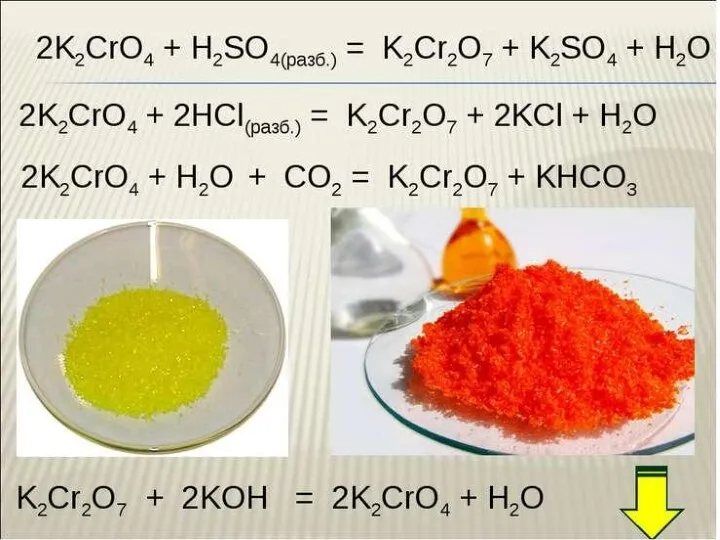 Хром. Соединения хрома
Хром. Соединения хрома История изучения структуры белка Лайнус Полинг считается первым учёным, который смог успешно предсказать вторичную структуру
История изучения структуры белка Лайнус Полинг считается первым учёным, который смог успешно предсказать вторичную структуру Алкены. Строение. Изомерия. Химические свойства. Получение. Учитель химии ГОУ СОШ №277 Кировского района г. Санкт-Петербурга Елен
Алкены. Строение. Изомерия. Химические свойства. Получение. Учитель химии ГОУ СОШ №277 Кировского района г. Санкт-Петербурга Елен Алкалоиды, как лекарственные вещества. Источники получения. Методы установления строения. Классификация. (Тема 9)
Алкалоиды, как лекарственные вещества. Источники получения. Методы установления строения. Классификация. (Тема 9) Типы изомерии
Типы изомерии Синтетические моющие средства
Синтетические моющие средства Кадмий (Cadmium)
Кадмий (Cadmium) Тема: «Бишофит – новый старый антигололедный реагент» Авторы: Гончаревич Анастасия Клокова Татьян
Тема: «Бишофит – новый старый антигололедный реагент» Авторы: Гончаревич Анастасия Клокова Татьян Химия и физика полимеров. Курс лекций
Химия и физика полимеров. Курс лекций Строение вещества. Химические элементы
Строение вещества. Химические элементы Графен. Классические и квантовые низкоразмерные системы. Ковалентная химическая связь: σ- и π-электроны
Графен. Классические и квантовые низкоразмерные системы. Ковалентная химическая связь: σ- и π-электроны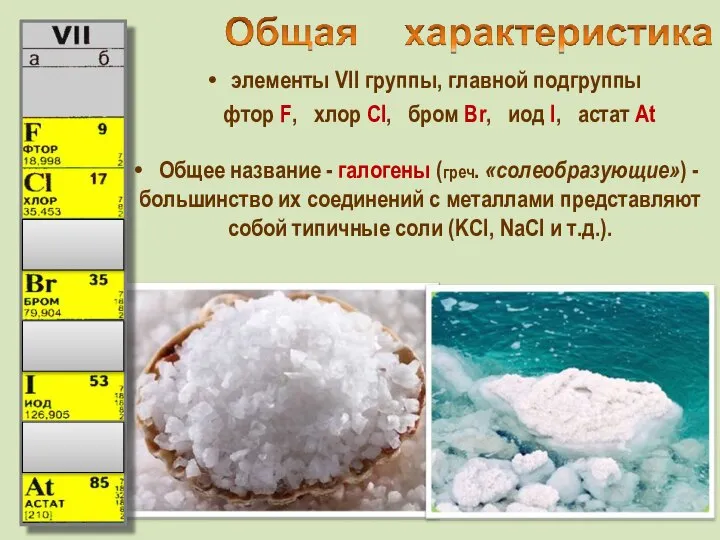 Элементы VII группы
Элементы VII группы Уроки зельеварения. Задача 6
Уроки зельеварения. Задача 6 Основные положения МКТ МКТ- молекулярно-кинетическая теория
Основные положения МКТ МКТ- молекулярно-кинетическая теория  Промышленное получение аминокислот и их применение в медицине и диетологии
Промышленное получение аминокислот и их применение в медицине и диетологии Положение кислорода и серы в Периодической системе химических элементов, строение атомов. Строение простых веществ. Аллотропия
Положение кислорода и серы в Периодической системе химических элементов, строение атомов. Строение простых веществ. Аллотропия Физическая и коллоидная химия
Физическая и коллоидная химия