Содержание
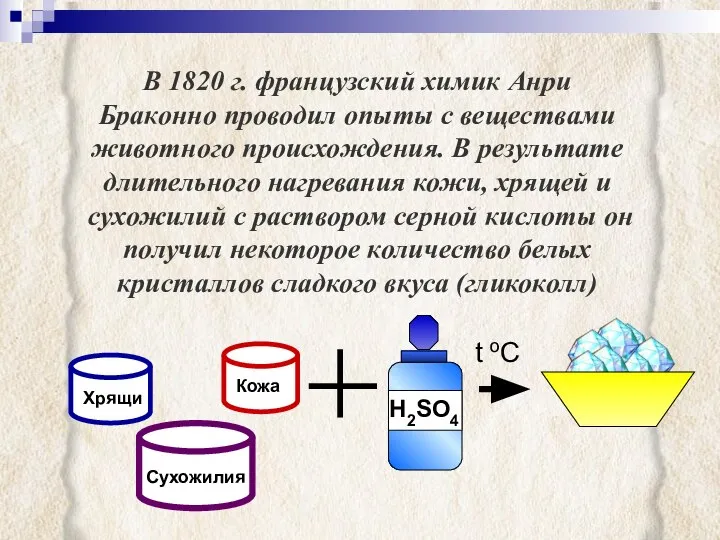
- 2. В 1820 г. французский химик Анри Браконно проводил опыты с веществами животного происхождения. В результате длительного
- 3. Гликоколл долгое время считался «родственником» углеводов, пока в 1838 г. голландский химик Г.Мульдер не обнаружил в
- 4. Аминокислоты – это производные углеводорода, содержащие аминогруппу (NH2) и карбоксильную группу (COOH) Общая формула: R (NH2
- 5. Классификацияаминокислот Моноаминомонокарбоновые кислоты Диаминомонокарбоновые кислоты Моноаминодикарбоновые кислоты NH2-R-COOH (NH2)2-R-COOH NH2-R-(COOH)2
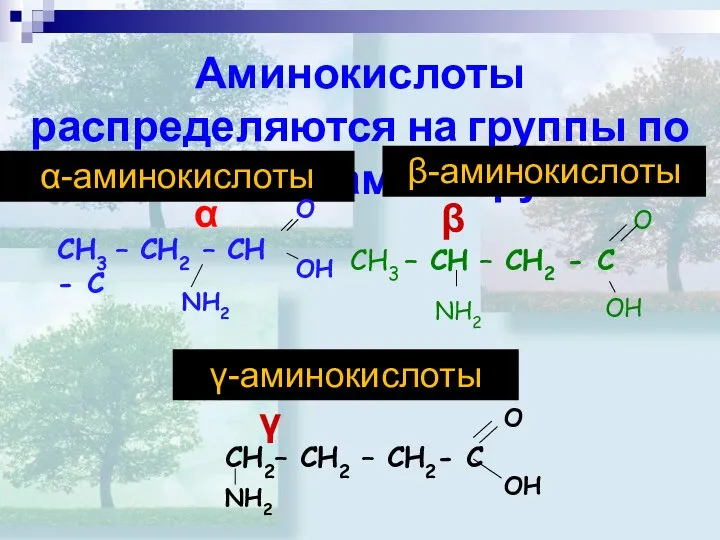
- 6. Аминокислоты распределяются на группы по положению аминогруппы: γ-аминокислоты α-аминокислоты β-аминокислоты
- 7. Номенклатура аминокислот I. ИЮПАКовская номенклатура (международная) II. Рациональная номенклатура
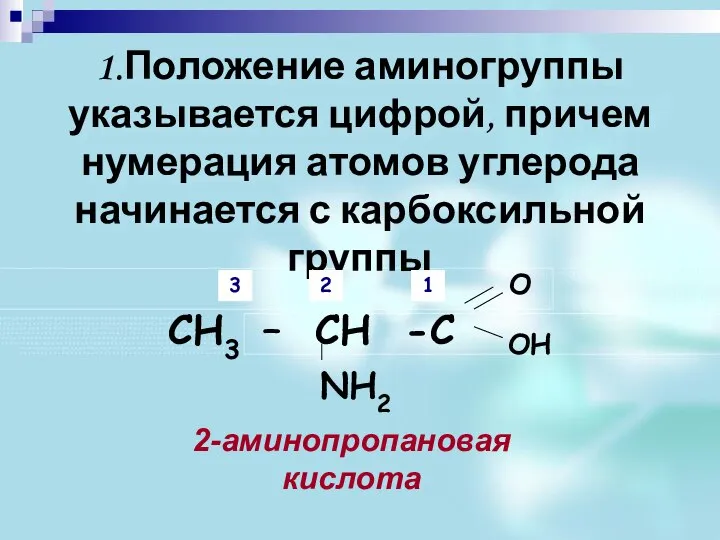
- 8. 1.Положение аминогруппы указывается цифрой, причем нумерация атомов углерода начинается с карбоксильной группы 1 2 3 2-аминопропановая
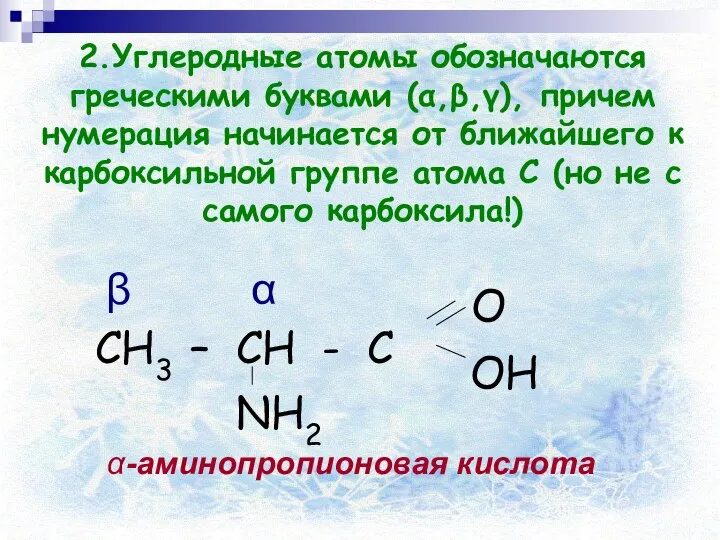
- 9. 2.Углеродные атомы обозначаются греческими буквами (α,β,γ), причем нумерация начинается от ближайшего к карбоксильной группе атома C
- 10. Изомерия: 1. Углеродного скелета 2. Положения функциональной группы 3. Межклассовая изомерия
- 11. 1. Изомерия углеродного скелета 2-аминобутановая кислота α-аминомасляная кислота C4H9O2N 2-амино,2-метилпропановая кислота α-амино,α-метилпропионовая кислота
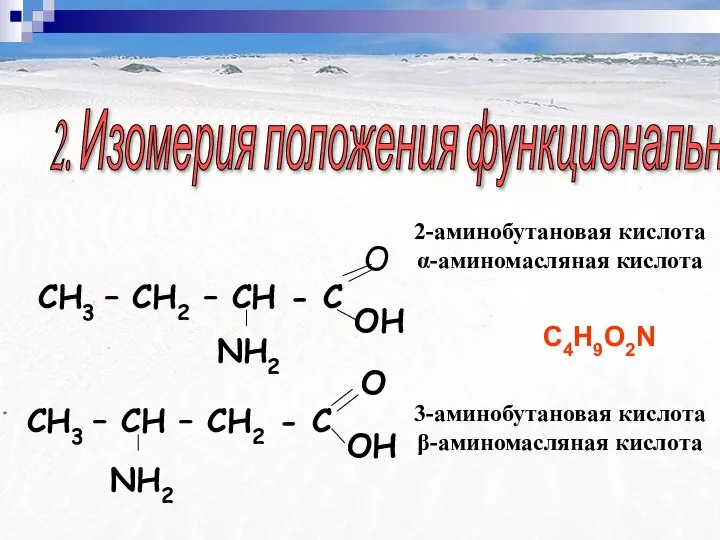
- 12. 2. Изомерия положения функциональной группы C4H9O2N 2-аминобутановая кислота α-аминомасляная кислота 3-аминобутановая кислота β-аминомасляная кислота
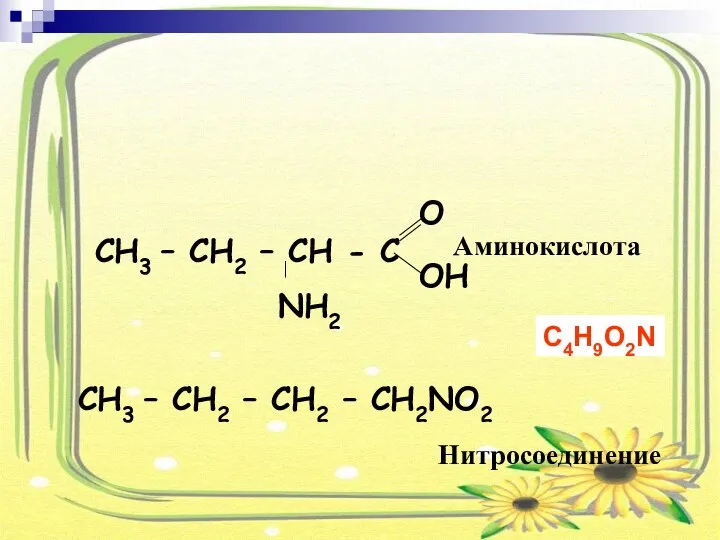
- 13. 3. Межклассовая изомерия CH3 – CH2 – CH2 – CH2NO2 Аминокислота Нитросоединение C4H9O2N
- 14. У α-aминoкиcлoт при атоме C-2 (C-α) имеются 4 различных зaмecтитeля: каpбокcильнaя группа, аминогруппа, вoдopoдный атом и
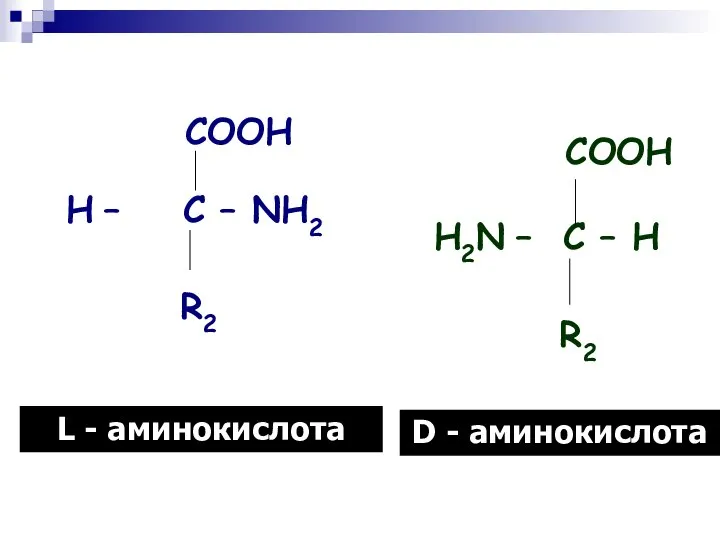
- 15. L - аминокислота D - аминокислота
- 17. Проекционные фoрмyлы вывoдятcя из тpeхмepной cтpyктypы cледyющим образом: тетраэдр пoвoрачивaют таким образом, чтобы наиболее окиcлeннaя гpyппa
- 18. Аминокислоты представляют собой твердые кристаллические вещества, хорошо растворимые в воде и мало растворимые в органических растворителях.
- 19. Химические свойства Аминокислоты — это органические амфотерные соединения. Они содержат в составе молекулы две функциональные группы
- 20. Поэтому аминокислоты реагируют как с кислотами, так и с основаниями (т.е. являются амфотерными соединениями): 1.Аминокислоты как
- 21. 2. С оксидами металлов 1. С активными металлами 3. Реакция нейтрализации 4. С солью слабых кислот
- 22. 1.Взаимодействие с активными металлами:
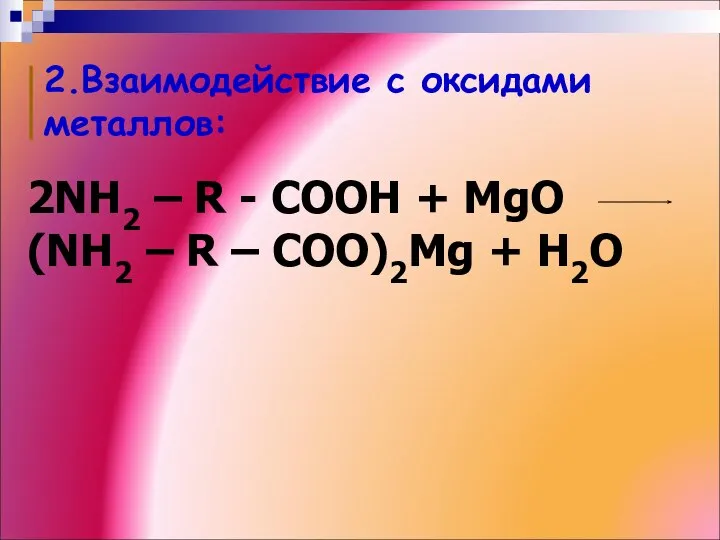
- 23. 2.Взаимодействие с оксидами металлов: 2NH2 – R - COOH + MgO (NH2 – R – COO)2Mg
- 24. 3.Реакция нейтрализации: NH2 – R - COOH + NaOH NH2 – R – COONa + H2O
- 25. 4.Взаимодействие с солью слабых кислот (угольная кислота): 2NH2 – R - COOH + Na2CO3 2NH3 –
- 26. 5.Реакция этерификация: 2NH2 – R - COOH + HOR 2NH2 – R – COOR + H2O
- 27. Аминокислоты как основания
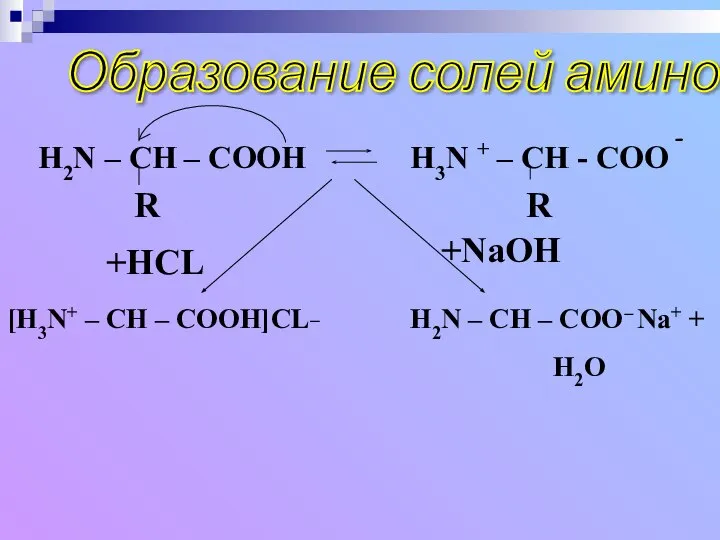
- 28. Образование солей аминокислот -
- 29. При растворении аминокислот в воде карбоксильная группа отщепляет ион водорода, который может присоединиться к аминогруппе. При
- 30. Кислотно-основные превращения аминокислот в различных средах можно изобразить следующей схемой:
- 31. Водные растворы аминокислот имеют нейтральную, щелочную или кислую среду в зависимости от количества функциональных групп
- 32. Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир: H2N—CH(R)— COOH +
- 33. Аминокислоты способны к конденсации с образованием пептидов. Пептиды — это продукты конденсации двух или более молекул
- 34. Пептидная связь Полученное соединение называют дипептидом: Аминокислота Аминокислота Дипептид +
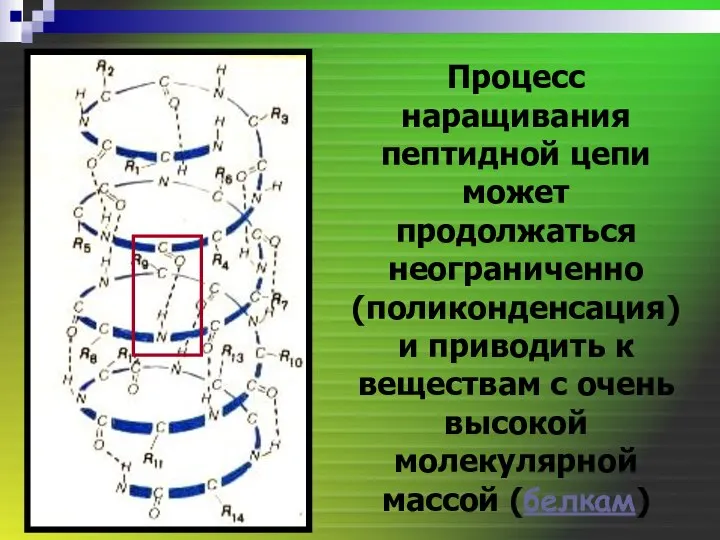
- 35. Процесс наращивания пептидной цепи может продолжаться неограниченно (поликонденсация) и приводить к веществам с очень высокой молекулярной
- 36. - это азотосодержащие высокомолекулярные органические вещества со сложным составом и строением молекул. Белки являются основной составной
- 37. 1) Все α -аминокислоты окисляются нингидрином с образованием продуктов, окрашенных в сине-фиолетовый цвет. Эта реакция является
- 38. 2) При нагревании ароматических аминокислот с концентрированной азотной кислотой происходит нитрование бензольного кольца и образуются соединения,
- 39. 3). К раствору белка добавляют раствор сульфата меди образуется осадок голубого цвета. 4). К раствору белка
- 40. Основное свойство пептидов — способность к гидролизу. При гидролизе происходит полное или частичное расщепление пептидной цепи
- 41. Способы получения: 1. Гидролиз белковых веществ обычно дает сложные смеси аминокислот. Однако разработан ряд методов, позволяющих
- 42. 2.Замещение галогена на аминогруппу в соответствующих галогенкислотах: СН3-СН-СООН + NН3 СI СН3 -СН-СООН + НСI NН2
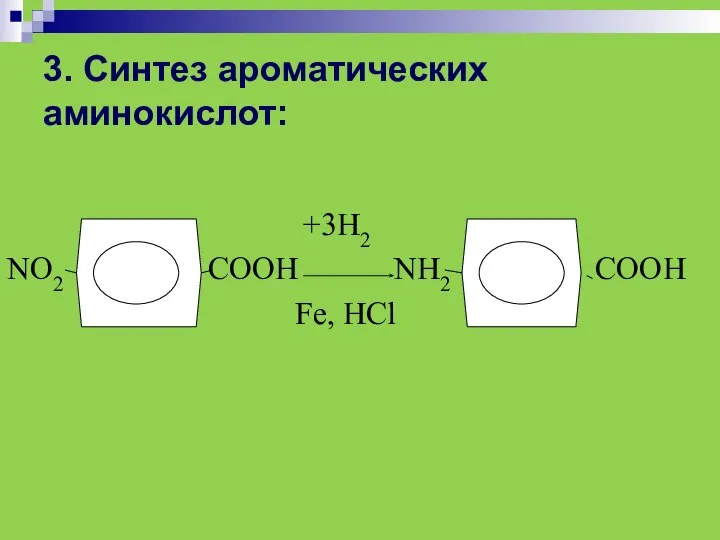
- 43. 3. Синтез ароматических аминокислот: +3Н2 NО2 СООН NН2 СООН Fе, НСl
- 44. В природе обнаружено около 300 разных аминокислот. Наибольший интерес представляют 20 α-аминокислот, входящих в состав белковых
- 45. Аланин Валин Лейцин Изолейцин Метионин Фенилаланин Триптофан Треонин Лизин Цистеин Тирозин Пролин Аспарагин Аспарагиновая к-та Глутамин
- 46. Триптофан Естественный релаксант, помогает бороться с бессонницей, вызывая нормальный сон (триптофан распадается до серотонина - нейромедиатора,
- 47. Метионин Способствует понижению уровня холестерина, усиливая выработку лецитина печенью; понижает уровень жиров в печени, защищает почки;
- 48. Треонин Необходим для синтеза иммуноглобулинов и антител. участвует в борьбе с отложением жира в печени; поддерживает
- 49. Валин Один из главных компонентов в росте и синтезе тканей тела. Используется для лечения депрессии, т.к.
- 50. Фенилаланин Поддерживает нас в в состоянии бодрствования и восприимчивости; уменьшает чувство голода и снимает боль; работает
- 51. Изолейцин Играет важную роль в формирования мышечной ткани; играет значительную роль в получении энергии за счет
- 52. Лейцин Необходим для построения и развития мышечной ткани; синтеза протеина организмом; для укрепления иммунной системы; понижает
- 53. Лизин Обеспечивает должное усвоение кальция; участвует в образовании коллагена ( из которого затем формируются хрящи и
- 54. Серин Участвует в запасании печенью и мышцами гликогена; активно участвует в усилении иммунной системы, обеспечивая ее
- 55. Цистеин Необходим для роста волос и ногтей; играет важную роль в формировании вторичной структуры белков за
- 56. Пролин Крайне важен для суставов и для сердца; дефицит этой аминокислоты может заметно повысить утомляемость. Свободный
- 57. Гистидин Почти на 60 процентов всасывается через кишечник; играет важную роль в метаболизме белков, в синтезе
- 58. Аспарагин/Аспарагиновая кислота Аспарагин служит сырьем для производства аспарагиновой кислоты, которая участвует в работе иммунной системы и
- 59. Глутамин/Глутаминовая кислота Глутамин образуется из глутаминовой кислоты путем присоединения аммиака. Глутамин весьма важен как переносчик энергии
- 60. Аргинин Вызывает замедление развития опухолей и раковых образований; очищает печень; помогает выделению гормона роста; укрепляет иммунную
- 61. Глицин Участвует в обеспечении кислородом процесса образования новых клеток; очень важен для создания соединительных тканей; он
- 62. Тирозин необходим для нормальной работы надпочечников, щитовидной железы и гипофиза, создания красных и белых кровяных телец;
- 63. Аланин Является важным источником энергии для головного мозга и центральной нервной системы; укрепляет иммунную систему путем
- 64. Предприимчивые японцы давно заметили, что добавление в пищу приправы из сушеных водорослей усиливает ее вкус и
- 65. Аминокислоты и их производные используются в качестве лекарственных средств в медицине. В аптеке можно купить глицин
- 66. Производимый в больших количествах лизин и метионин используются как добавка в рацион сельскохозяйственных животных. Синтетические аминокислоты
- 68. Скачать презентацию






















































 ОСНОВАНИЯ, ИХ КЛАССИФИКАЦИЯ И СВОЙСТВА Составил: учитель химии МОУ «Средняя общеобразовательная школа №92 с углубленным изуче
ОСНОВАНИЯ, ИХ КЛАССИФИКАЦИЯ И СВОЙСТВА Составил: учитель химии МОУ «Средняя общеобразовательная школа №92 с углубленным изуче Аммиак NH3
Аммиак NH3  Алюминий и его соединения. Строение атома
Алюминий и его соединения. Строение атома Применение ацетилена
Применение ацетилена ПУТИ ОБМЕНА ОТДЕЛЬНЫХ АМИНОКИСЛОТ
ПУТИ ОБМЕНА ОТДЕЛЬНЫХ АМИНОКИСЛОТ Белки плазмы крови, их биологическая роль. Методы разделения белков плазмы крови. Диспротеинемии. Выполнила студентка 6 курса МБФ
Белки плазмы крови, их биологическая роль. Методы разделения белков плазмы крови. Диспротеинемии. Выполнила студентка 6 курса МБФ Презентация по Химии "«Углеводы»" - скачать смотреть
Презентация по Химии "«Углеводы»" - скачать смотреть  Химическая промышленность Донецкой области
Химическая промышленность Донецкой области Кристаллические решетки
Кристаллические решетки Энергетика химических процессов. (Лекция 2)
Энергетика химических процессов. (Лекция 2) Дисперсные системы. Лиофобные дисперсные системы (часть 1)
Дисперсные системы. Лиофобные дисперсные системы (часть 1) Химическая кинетика. Лекция 9
Химическая кинетика. Лекция 9 Гума
Гума  Биохимия почек и мочи. (Лекция 10)
Биохимия почек и мочи. (Лекция 10) Процеси гниття. Хімізм процесу гниття
Процеси гниття. Хімізм процесу гниття Горение топлива
Горение топлива Биологически активные гетероциклические соединения. Нуклеиновые кислоты
Биологически активные гетероциклические соединения. Нуклеиновые кислоты Металловедение. Теория сплавов
Металловедение. Теория сплавов Классификация дисперсных систем. Коллигативные свойства растворов. Растворимость газов в воде. Термодинамика
Классификация дисперсных систем. Коллигативные свойства растворов. Растворимость газов в воде. Термодинамика Иммунохимические методы детекции
Иммунохимические методы детекции Производство серной кислоты
Производство серной кислоты Cellulase. Introduction (source)
Cellulase. Introduction (source) Investigation of the conditions for the synthesis of a silver - containing composite
Investigation of the conditions for the synthesis of a silver - containing composite Гидрокси(окси) кислоты
Гидрокси(окси) кислоты Растворы. Классификация дисперсных систем
Растворы. Классификация дисперсных систем Синтетические каучуки
Синтетические каучуки Материалы с высокими упругими свойствами
Материалы с высокими упругими свойствами Магистерская диссертация. Синтез новых производных тиазола реакцией Ганча
Магистерская диссертация. Синтез новых производных тиазола реакцией Ганча