Содержание
- 2. Цели лекции: Обучающая - Сформировать знания о строении, номенклатуре и реакционной способности аминокислот. Развивающая – Расширять
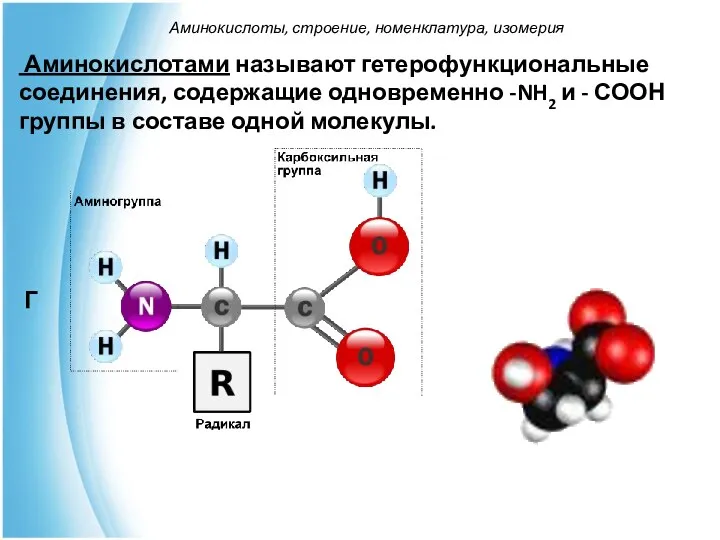
- 3. Аминокислотами называют гетерофункциональные соединения, содержащие одновременно -NH2 и - СООН группы в составе одной молекулы. Г
- 4. Аминокислоты находят широкое применение в синтетической и аналитической химии (например, трилон Б ). На основе ароматических
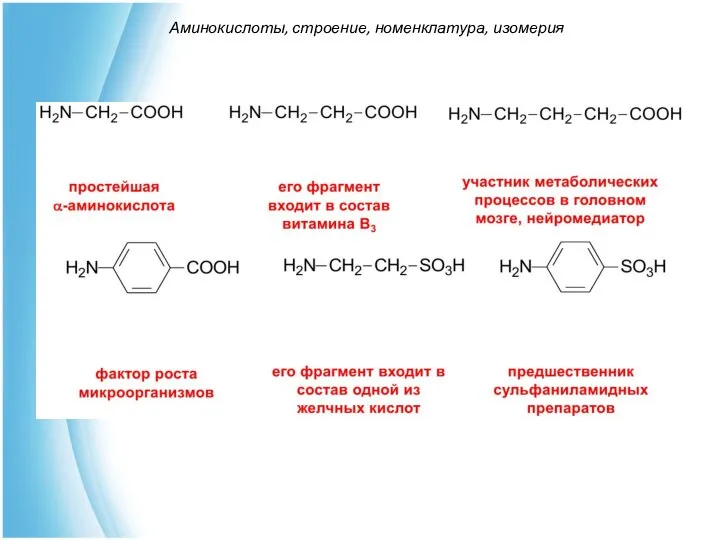
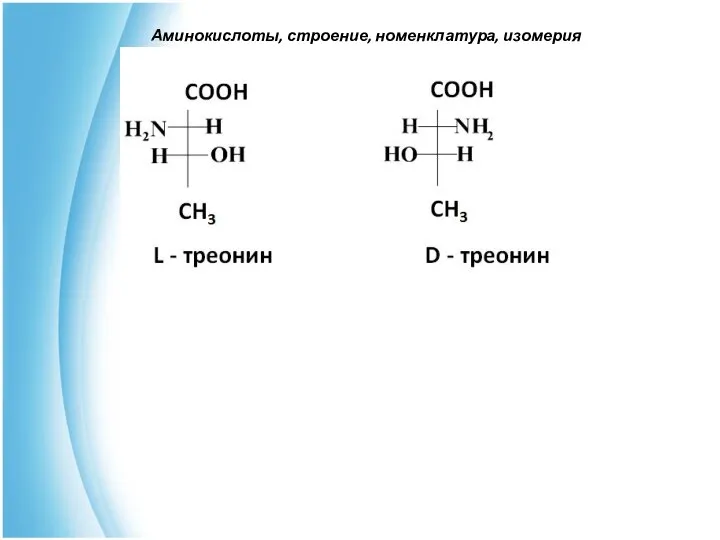
- 5. Аминокислоты, строение, номенклатура, изомерия
- 6. Аминокислоты, строение, номенклатура, изомерия
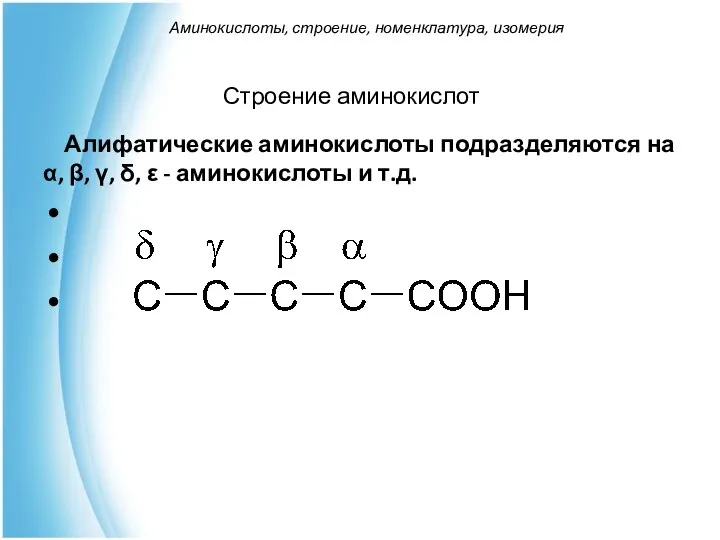
- 7. Алифатические аминокислоты подразделяются на α, β, γ, δ, ε - аминокислоты и т.д. Строение аминокислот Аминокислоты,
- 8. Аминокислоты, строение, номенклатура, изомерия
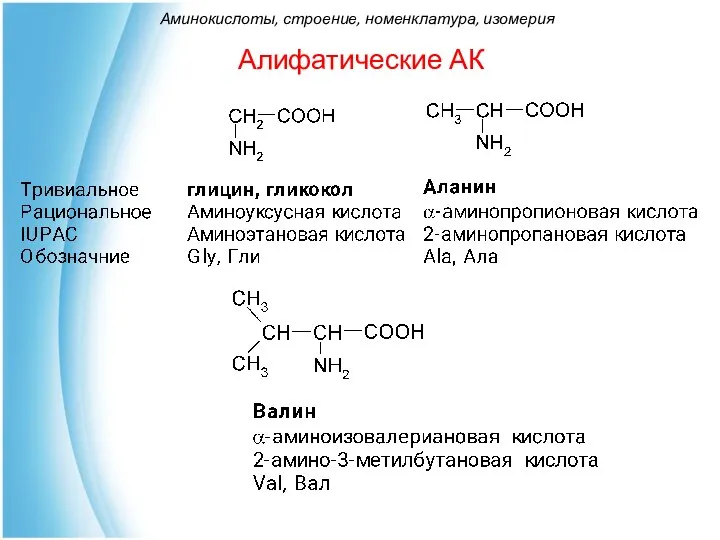
- 9. Номенклатура алифатических аминокислот 1. Тривиальная номенклатура в основном используется для широко распространённых аминокислот. 2. Рациональная 3.
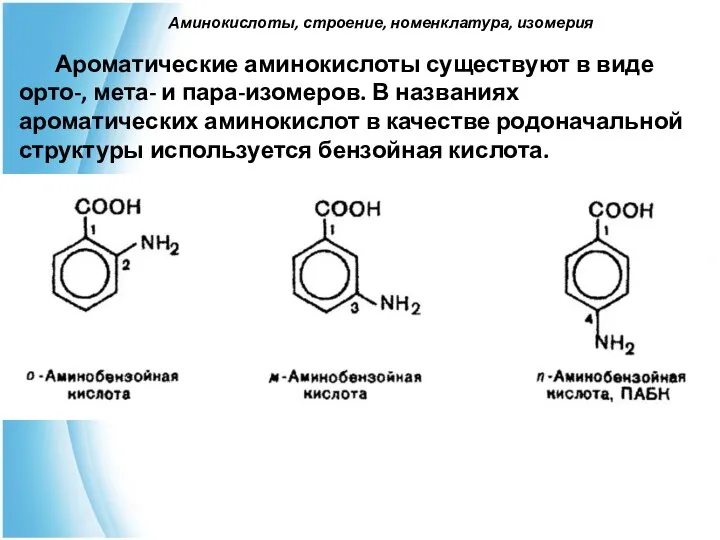
- 10. Ароматические аминокислоты существуют в виде орто-, мета- и пара-изомеров. В названиях ароматических аминокислот в качестве родоначальной
- 11. Аминокислоты, строение, номенклатура, изомерия
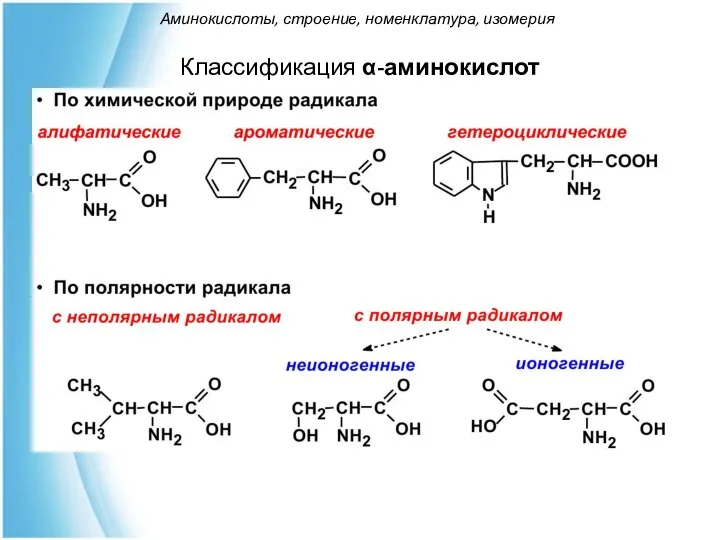
- 12. Классификация α-аминокислот Аминокислоты, строение, номенклатура, изомерия
- 13. Аминокислоты, строение, номенклатура, изомерия
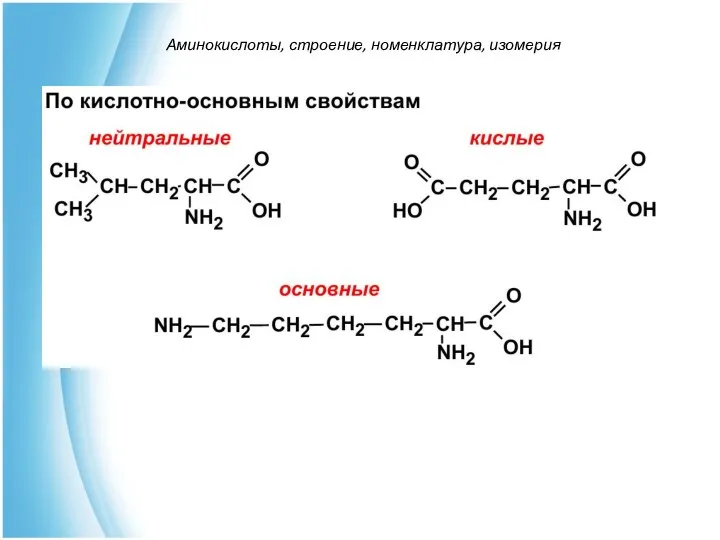
- 14. По количеству карбокси- и аминогрупп α-аминокислоты классифицируют на: Моноаминомонокарбоновые кислоты (глицин, аланин, валин, лейцин, изолейцин, серин,
- 15. Классификация по встречаемости в белках : В составе белков человека открыто 20 α – аминокислот. Все
- 16. Алифатические АК Аминокислоты, строение, номенклатура, изомерия
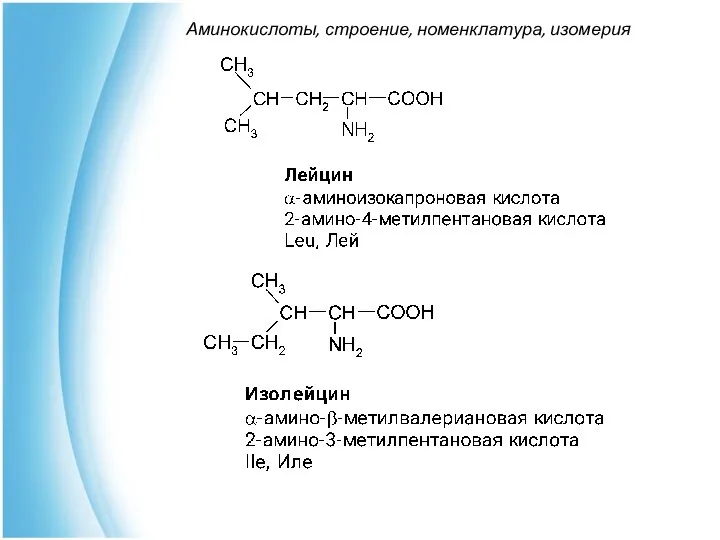
- 17. Аминокислоты, строение, номенклатура, изомерия
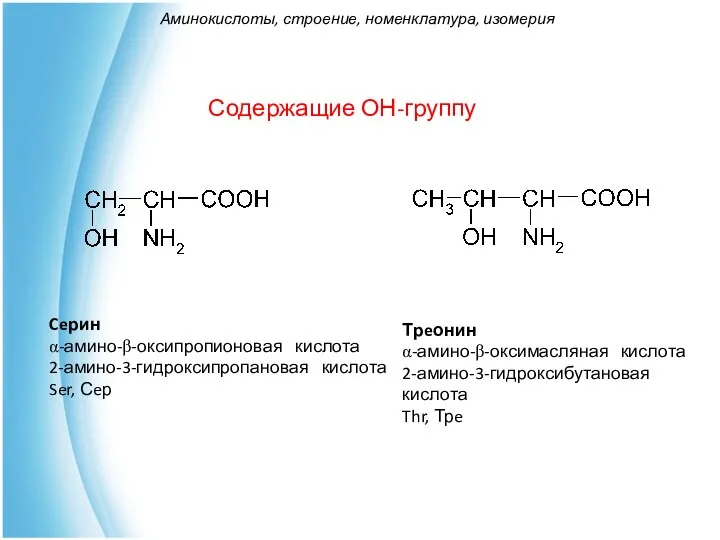
- 18. Содержащие ОН-группу Ceрин α-амино-β-оксипропионовая кислота 2-амино-3-гидроксипропановая кислота Ser, Сeр Трeонин α-амино-β-оксимасляная кислота 2-амино-3-гидроксибутановая кислота Thr, Трe
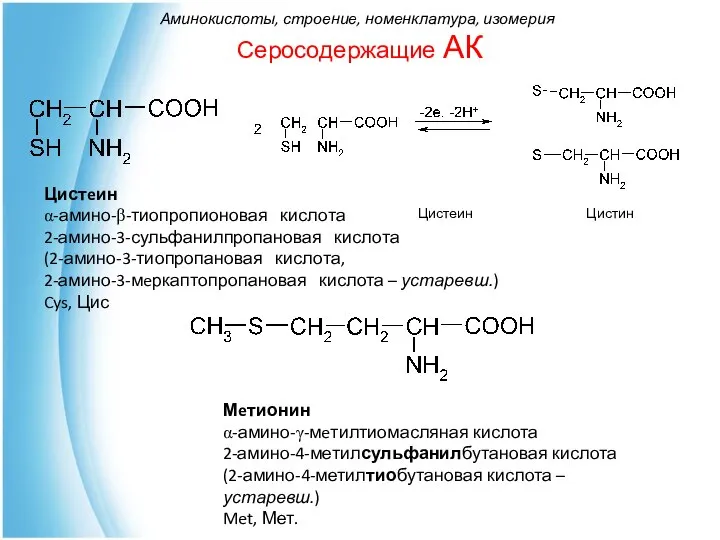
- 19. Серосодержащие АК Цистеин Цистин Мeтионин α-амино-γ-мeтилтиомасляная кислота 2-амино-4-метилсульфанилбутановая кислота (2-амино-4-метилтиобутановая кислота – устаревш.) Met, Мет. Цистeин
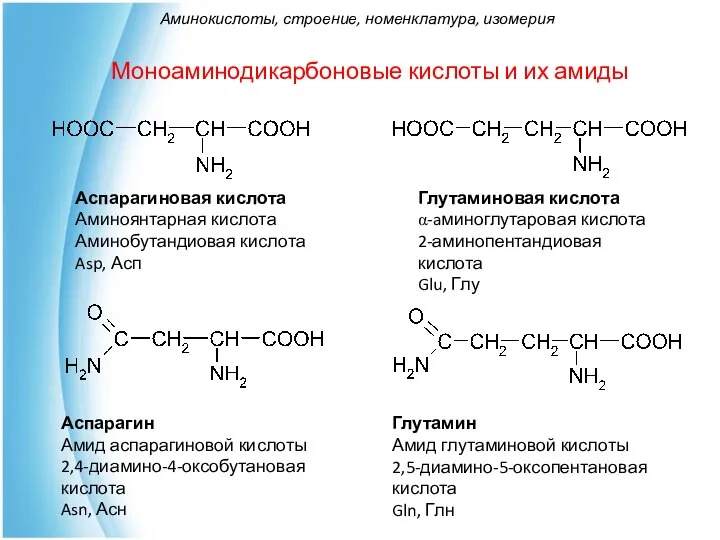
- 20. Моноаминодикарбоновые кислоты и их амиды Аспарагиновая кислота Аминоянтарная кислота Аминобутандиовая кислота Asp, Асп Глутаминовая кислота α-aминоглутаровая
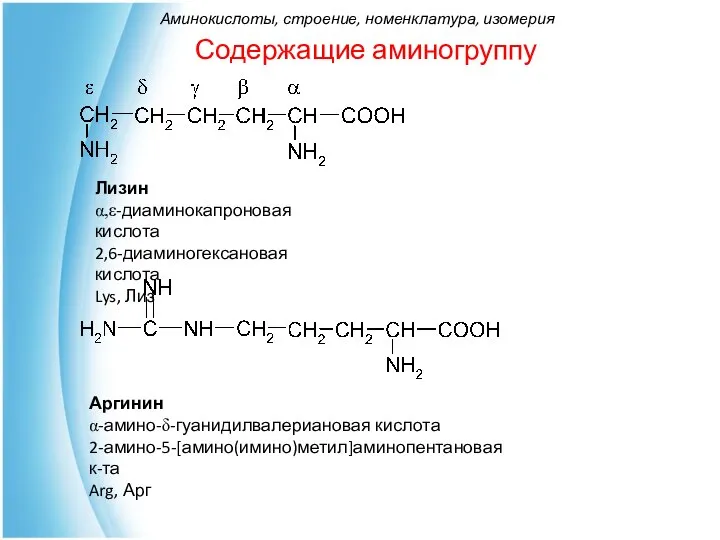
- 21. Содержащие аминогруппу Лизин α,ε-диаминокапроновая кислота 2,6-диаминогексановая кислота Lys, Лиз Аргинин α-амино-δ-гуанидилвалериановая кислота 2-амино-5-[амино(имино)метил]аминопентановая к-та Arg, Арг
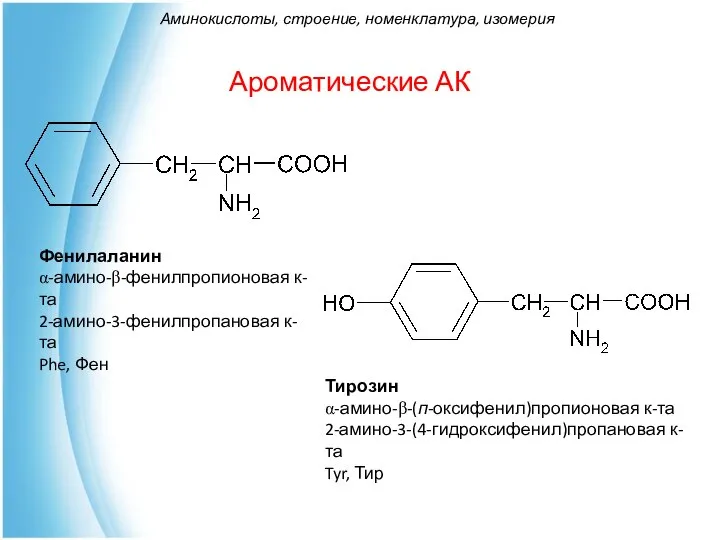
- 22. Ароматические АК Фенилаланин α-амино-β-фенилпропионовая к-та 2-амино-3-фенилпропановая к-та Phe, Фен Тирозин α-амино-β-(п-оксифенил)пропионовая к-та 2-амино-3-(4-гидроксифенил)пропановая к-та Tyr, Тир
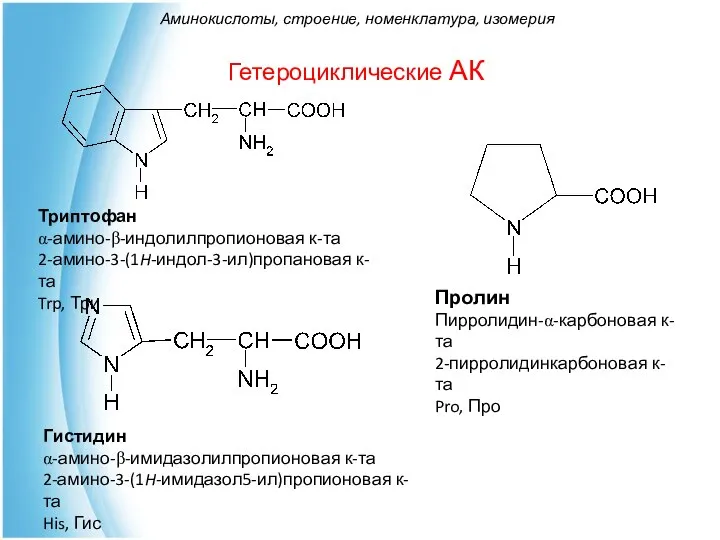
- 23. Гетероциклические АК Триптофан α-амино-β-индолилпропионовая к-та 2-амино-3-(1H-индол-3-ил)пропановая к-та Trp, Три Гистидин α-амино-β-имидазолилпропионовая к-та 2-амино-3-(1H-имидазол5-ил)пропионовая к-та His, Гис
- 24. По пищевой ценности для человека аминокислоты делятся на: заменимые и незаменимые. Основным источником α - аминокислот
- 25. По характеру катаболизма (биохимической роли): 1). глюкогенные – при распаде дают метаболиты, не повышающие уровень кетоновых
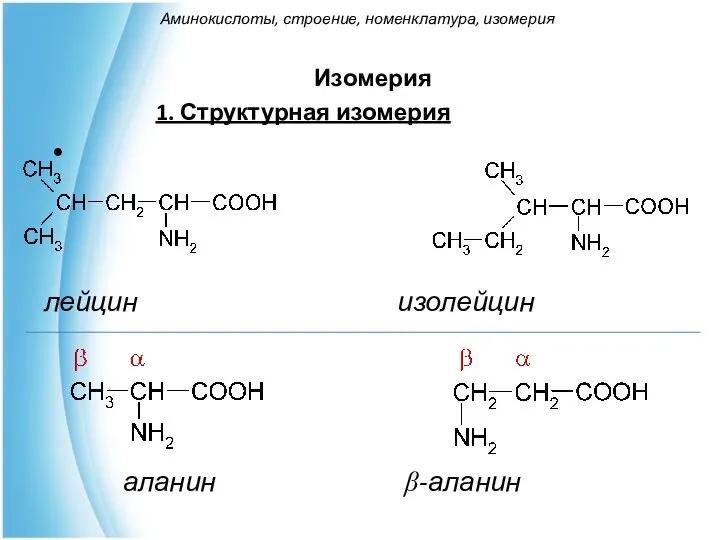
- 26. Изомерия 1. Структурная изомерия лейцин изолейцин аланин β-аланин Аминокислоты, строение, номенклатура, изомерия
- 27. Аминокислоты, строение, номенклатура, изомерия 2. Стереоизомерия α - Аминокислоты - хиральные соединения. Исключение составляет глицин Относительная
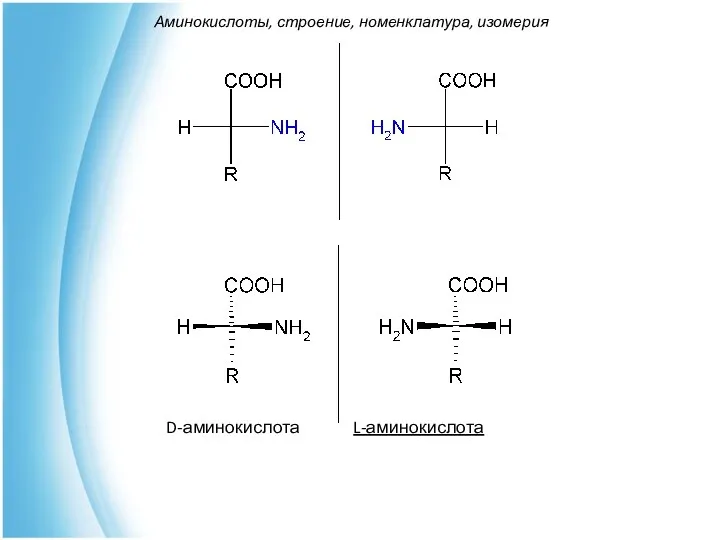
- 28. D-аминокислота L-аминокислота Аминокислоты, строение, номенклатура, изомерия
- 29. Аминокислоты, строение, номенклатура, изомерия
- 30. Физические и химические свойства Физические свойства α-Аминокислоты - кристаллические вещества. Имеют высокие температуры плавления (выше 200°
- 31. Физические и химические свойства Физические свойства α-Аминокислоты - кристаллические вещества. Имеют высокие температуры плавления (выше 200°
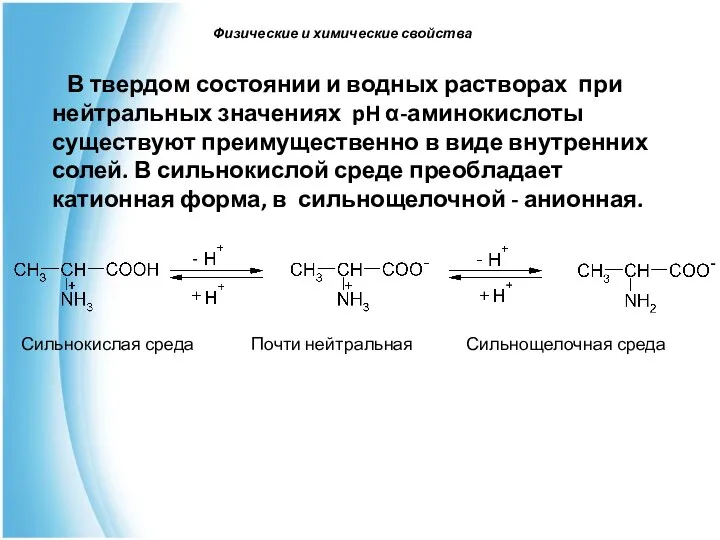
- 32. В твердом состоянии и водных растворах при нейтральных значениях pH α-аминокислоты существуют преимущественно в виде внутренних
- 33. Положение равновесия аминокислоты в водном растворе при определенном значении pH существенно зависит от строения радикала. Значение
- 34. Для моноаминомонокарбоновых кислот pI ≈ 5-6 pI моноаминодикарбоновых кислот (Asp, Glu) ≈ 3 pI диаминомонокарбоновых кислот
- 35. Физические и химические свойства Химические свойства 1. Кислотно-основные свойства. α-Аминокислоты - амфотерные соединения, вступают в реакции
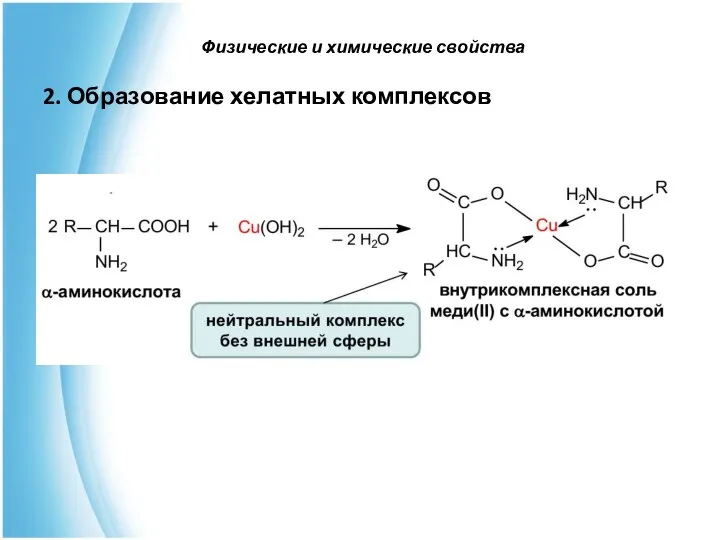
- 36. 2. Образование хелатных комплексов Физические и химические свойства
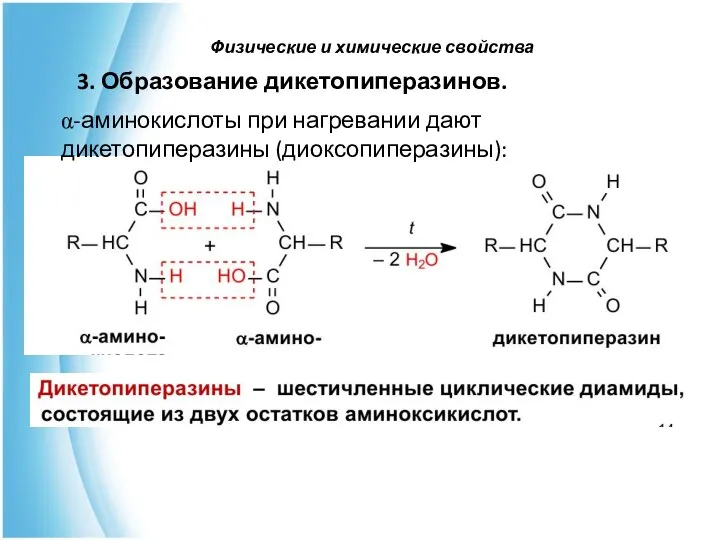
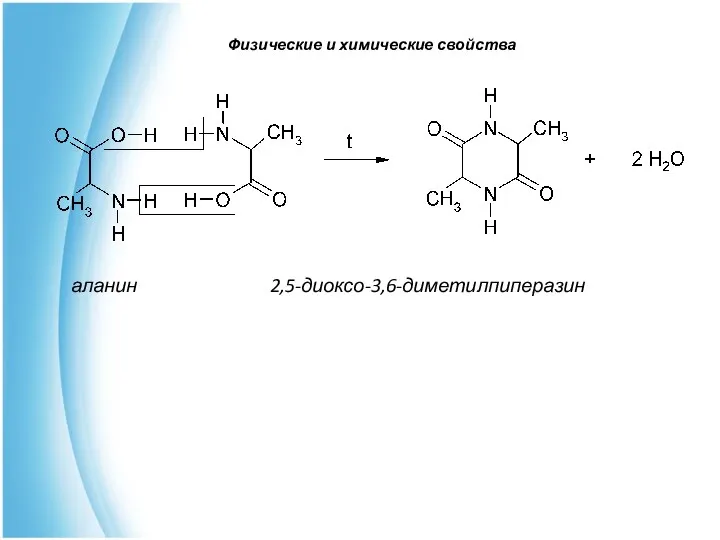
- 37. Физические и химические свойства 3. Образование дикетопиперазинов. α-аминокислоты при нагревании дают дикетопиперазины (диоксопиперазины):
- 38. аланин 2,5-диоксо-3,6-диметилпиперазин Физические и химические свойства
- 39. γ- и δ-аминокислоты при нагревании отщепляют воду, циклизуются с образованием лактамов – циклических амидов: γ-аминомасляная кислота
- 40. 5. Реакция поликонденсации ( образование пептидов): Физические и химические свойства
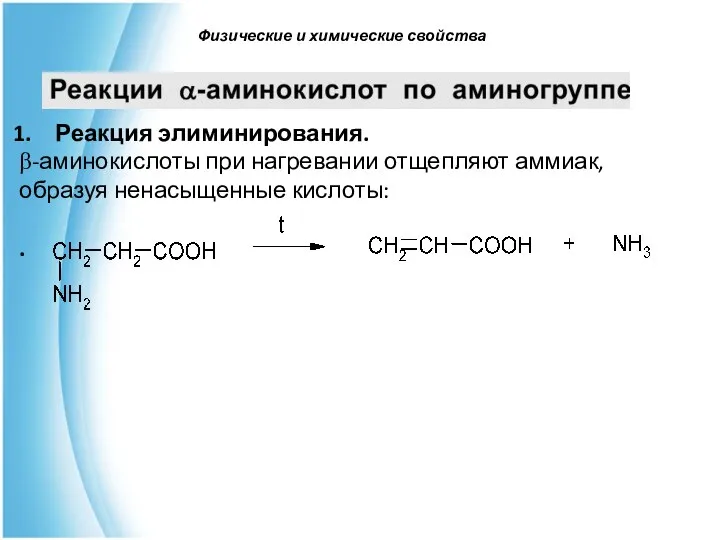
- 41. Реакция элиминирования. β-аминокислоты при нагревании отщепляют аммиак, образуя ненасыщенные кислоты: . Физические и химические свойства
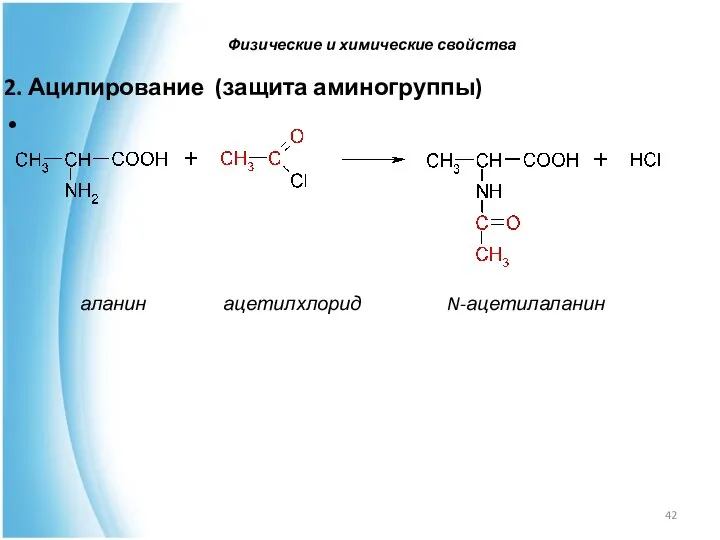
- 42. 2. Ацилирование (защита аминогруппы) аланин ацетилхлорид N-ацетилаланин Физические и химические свойства
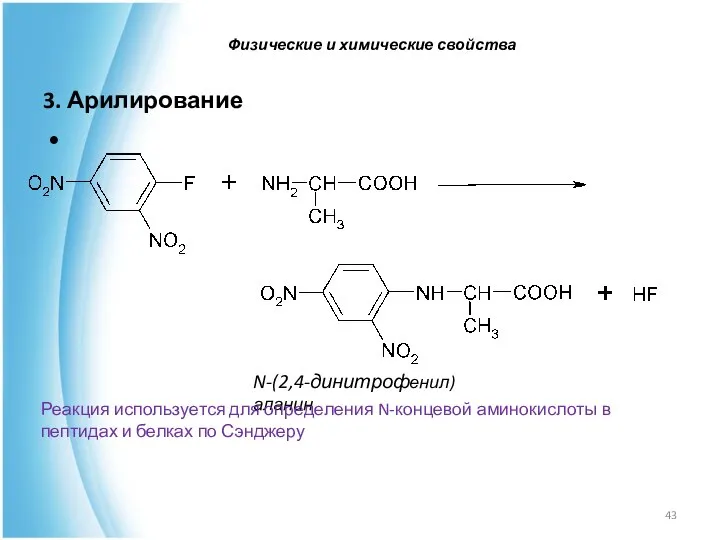
- 43. 3. Арилирование N-(2,4-динитрофенил)аланин Реакция используется для определения N-концевой аминокислоты в пептидах и белках по Сэнджеру Физические
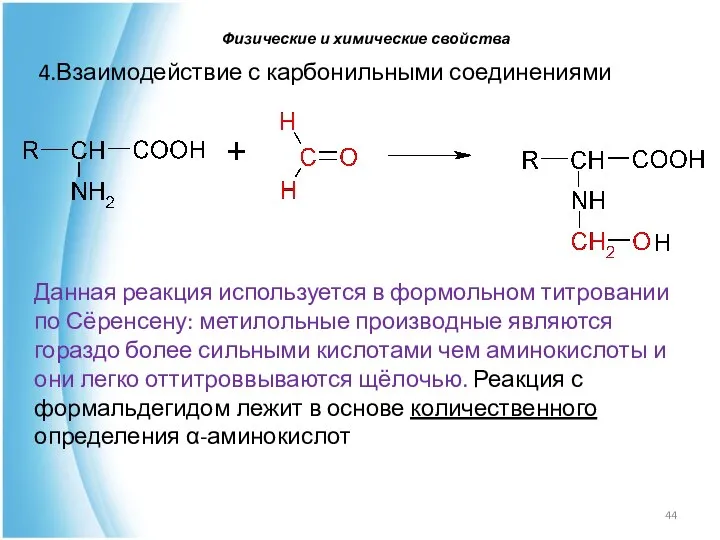
- 44. Данная реакция используется в формольном титровании по Сёренсену: метилольные производные являются гораздо более сильными кислотами чем
- 45. 5. Взаимодействие с азотистой кислотой α -аминокислота α-гидроксикислота Реакция с азотистой кислотой используется определения аминокислот по
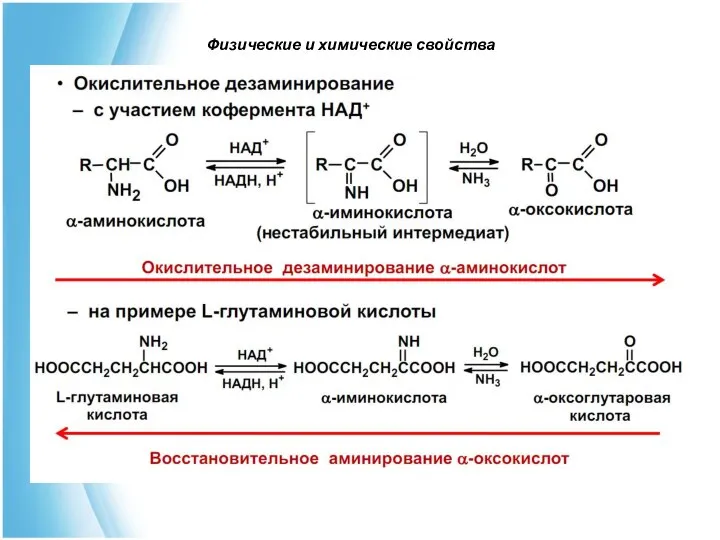
- 46. Физические и химические свойства 6. Дезаминирование - это реакция удаления аминогруппы путем окислительного, восстановительного, гидролитического или
- 47. Физические и химические свойства
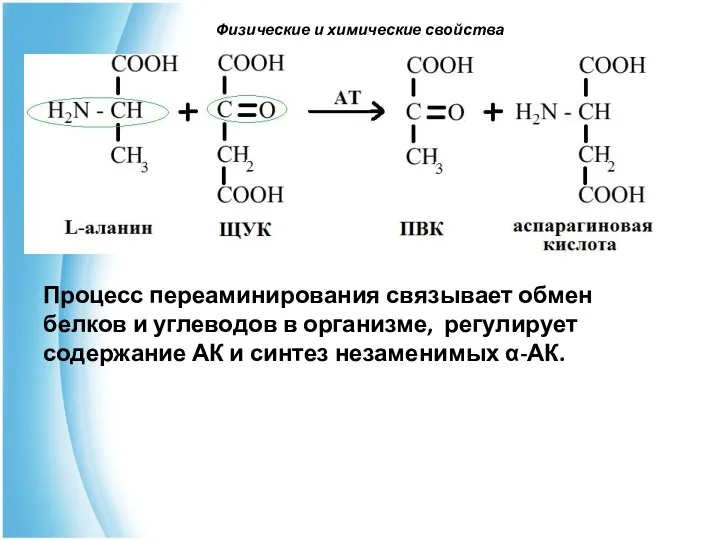
- 48. Физические и химические свойства 7.Переаминирование (трансаминирование) - это путь синтеза необходимых АК из α-кетонокислот. При этом
- 49. Физические и химические свойства Процесс переаминирования связывает обмен белков и углеводов в организме, регулирует содержание АК
- 50. 1. Образование сложных эфиров Реакция используется для защиты карбоксильной группы в синтезе пептидов Физические и химические
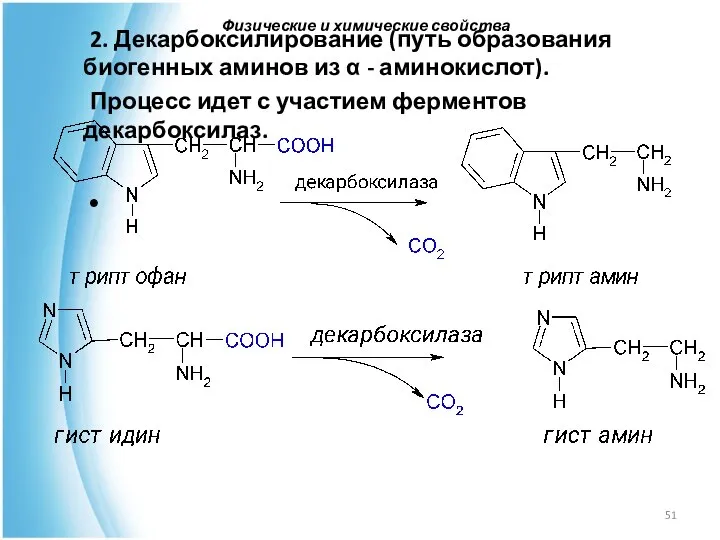
- 51. 2. Декарбоксилирование (путь образования биогенных аминов из α - аминокислот). Процесс идет с участием ферментов декарбоксилаз.
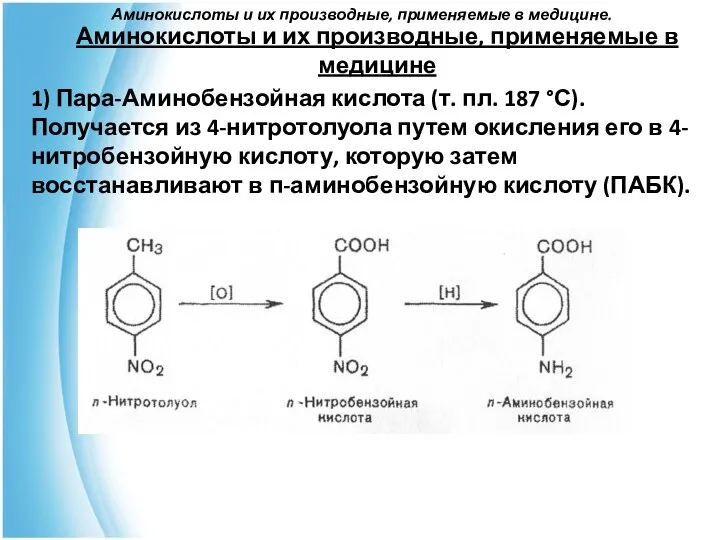
- 52. Аминокислоты и их производные, применяемые в медицине. Аминокислоты и их производные, применяемые в медицине 1) Пара-Аминобензойная
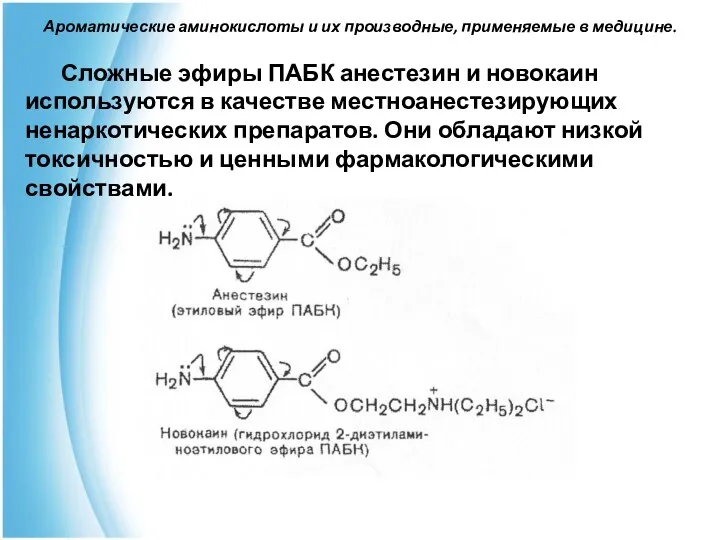
- 53. Ароматические аминокислоты и их производные, применяемые в медицине. Сложные эфиры ПАБК анестезин и новокаин используются в
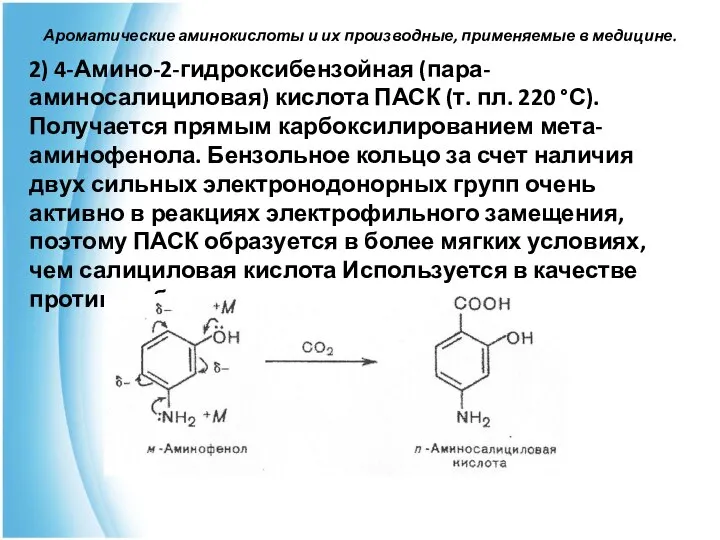
- 54. Ароматические аминокислоты и их производные, применяемые в медицине. 2) 4-Амино-2-гидроксибензойная (пара-аминосалициловая) кислота ПАСК (т. пл. 220
- 55. Ароматические аминокислоты и их производные, применяемые в медицине. 3) Антраниловая (о-аминобензойная кислота). Бесцветное кристаллическое вещество (т.
- 57. Скачать презентацию























 Реакционная способность фенольных антиоксидантов при взаимодействии с пероксирадикалами
Реакционная способность фенольных антиоксидантов при взаимодействии с пероксирадикалами Химия
Химия Железо и его соединения
Железо и его соединения Физико-химические методы анализа
Физико-химические методы анализа Дисперсные системы в медицине и пищевой промышленности
Дисперсные системы в медицине и пищевой промышленности Выполнил: А. М. Галенко, учитель химии МОУ СОШ № 67 г. Волгограда
Выполнил: А. М. Галенко, учитель химии МОУ СОШ № 67 г. Волгограда  Хроматографические методы анализа. Метод газовой хроматографии
Хроматографические методы анализа. Метод газовой хроматографии Схема катаболизма углеродного скилета аминокислот
Схема катаболизма углеродного скилета аминокислот Коллоидты жүйелердің коагуляциялық және кристаллизациялық құрылымдары
Коллоидты жүйелердің коагуляциялық және кристаллизациялық құрылымдары Строение атома алюминия. Физические и химические свойства алюминия
Строение атома алюминия. Физические и химические свойства алюминия Цифровые лаборатории «Архимед» в изучении биологии и химии
Цифровые лаборатории «Архимед» в изучении биологии и химии Термодинамика. Химическая термодинамика
Термодинамика. Химическая термодинамика Химический состав продуктов питания
Химический состав продуктов питания Цинк и его сплавы. Антифрикционные сплавы, их маркировка и область применения. Олово, свинец и их свойства. (Тема 10)
Цинк и его сплавы. Антифрикционные сплавы, их маркировка и область применения. Олово, свинец и их свойства. (Тема 10) Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады) Химические элементы O2 и N2
Химические элементы O2 и N2 Колообіг нітрогену Колообіг речовин — основна властивість, характерна риса біосфери.
Колообіг нітрогену Колообіг речовин — основна властивість, характерна риса біосфери.  Карбоновые кислоты
Карбоновые кислоты Сущность процесса электролитической диссоциации
Сущность процесса электролитической диссоциации 6 классов ферментов и тривиальные названия некоторых основных групп
6 классов ферментов и тривиальные названия некоторых основных групп Методы контроля и анализа веществ
Методы контроля и анализа веществ Интегрированный урок биологии и химии с применением информационных технологий
Интегрированный урок биологии и химии с применением информационных технологий Химический элемент алюминий
Химический элемент алюминий Дисперсные системы
Дисперсные системы Химия. Введение
Химия. Введение Кристаллы вокруг нас
Кристаллы вокруг нас Свойства нейтральных атомов. Лекция 4
Свойства нейтральных атомов. Лекция 4 Молекулы и атомы. Простые и сложные вещества
Молекулы и атомы. Простые и сложные вещества