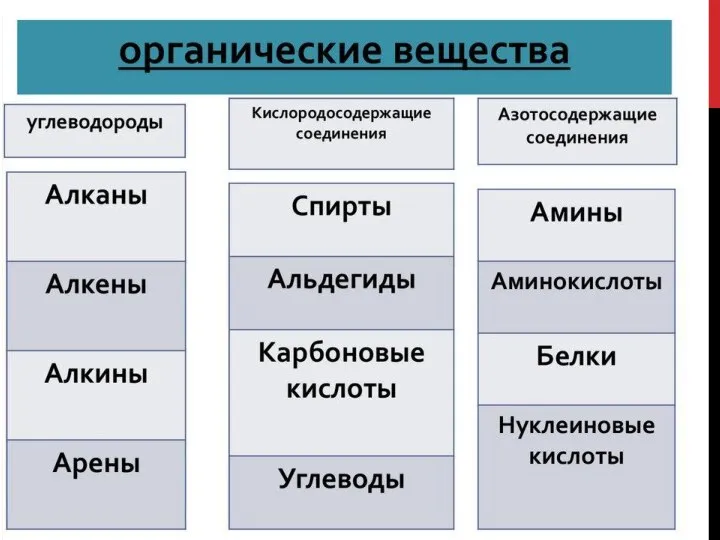
Содержание
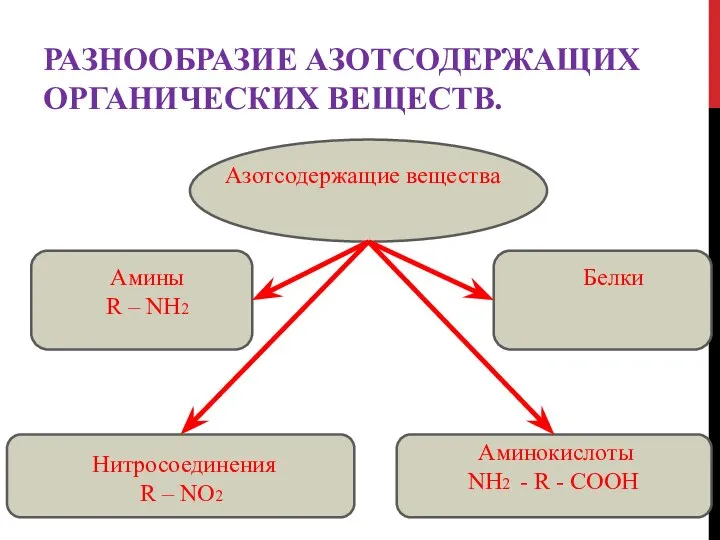
- 3. РАЗНООБРАЗИЕ АЗОТСОДЕРЖАЩИХ ОРГАНИЧЕСКИХ ВЕЩЕСТВ. Азотсодержащие вещества Амины R – NH2 Нитросоединения R – NO2 Аминокислоты NH2
- 6. ИСТОРИЯ ИЗУЧЕНИЯ АМИНОВ. Август Вильгельм Гофман (1818 – 1892) Шарль Адольф Вюрц (1817 – 1884) Первооткрывателями
- 7. ИСТОРИЯ ИЗУЧЕНИЯ АМИНОВ. Николай Николаевич Зинин ( 1812 – 1880) Русский химик – органик. Открыл метод
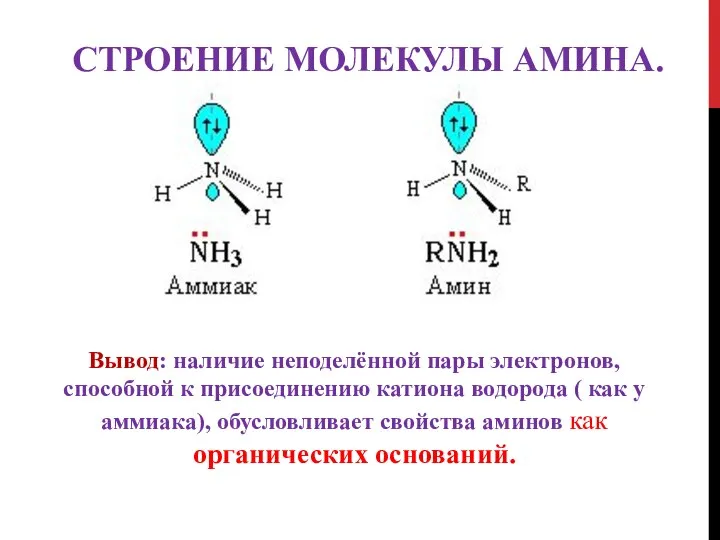
- 8. СТРОЕНИЕ МОЛЕКУЛЫ АМИНА. Вывод: наличие неподелённой пары электронов, способной к присоединению катиона водорода ( как у
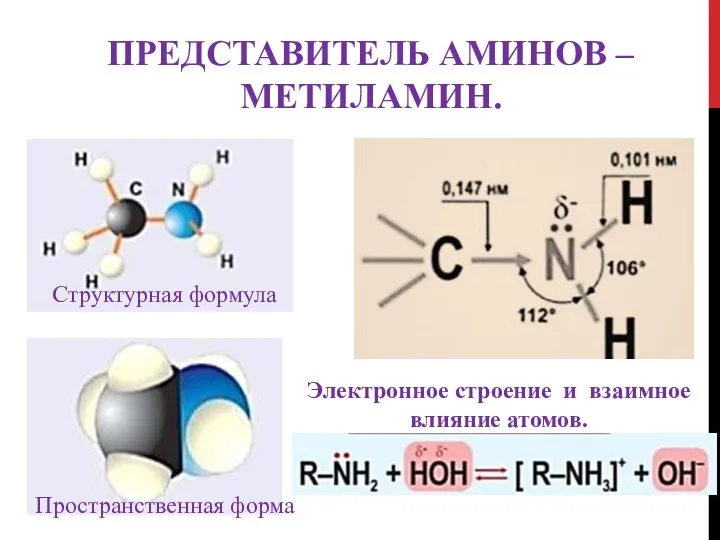
- 9. ПРЕДСТАВИТЕЛЬ АМИНОВ – МЕТИЛАМИН. Структурная формула Пространственная форма Электронное строение и взаимное влияние атомов.
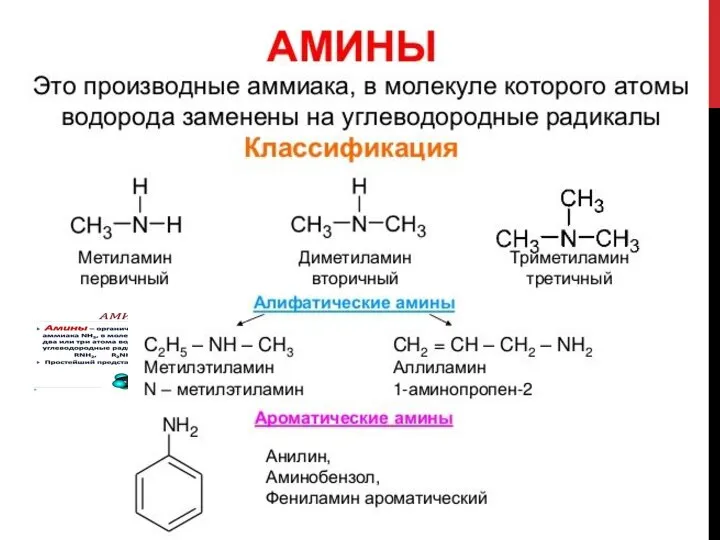
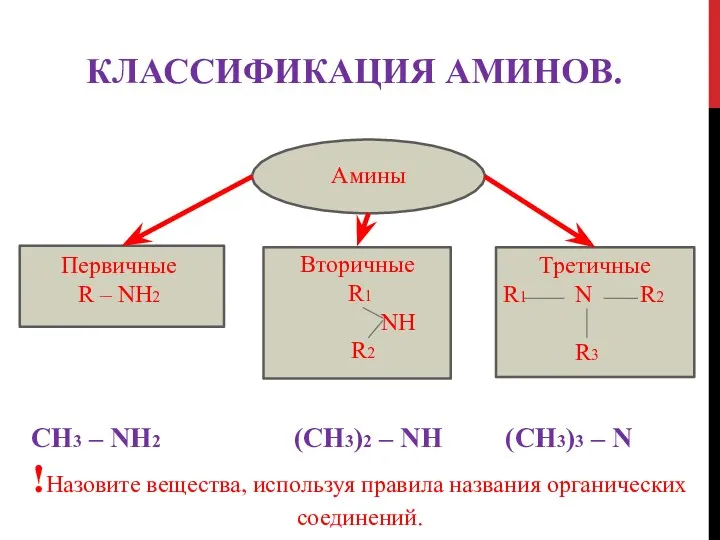
- 10. КЛАССИФИКАЦИЯ АМИНОВ. Амины Первичные R – NH2 Вторичные R1 NH R2 Третичные R1 N R2 R3
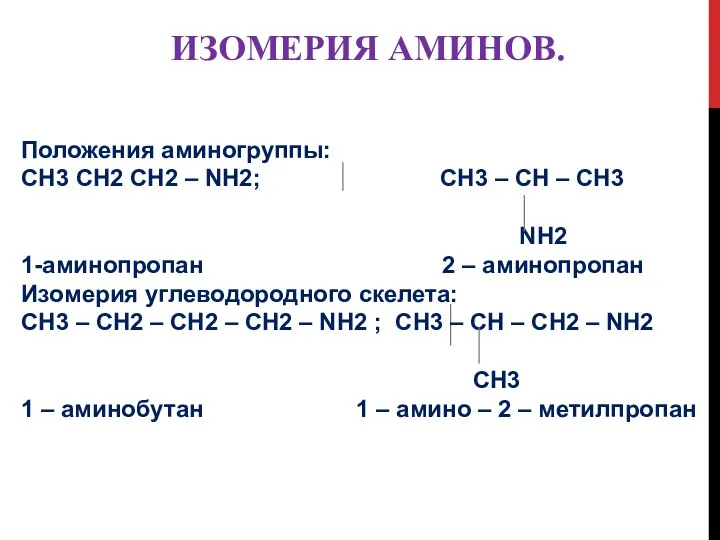
- 11. ИЗОМЕРИЯ АМИНОВ. Положения аминогруппы: CH3 CH2 CH2 – NH2; CH3 – CH – CH3 NH2 1-аминопропан
- 12. ПОЛУЧЕНИЕ АМИНОВ. 1 способ 2 способ 3 способ
- 13. ПОЛУЧЕНИЕ АМИНОВ. 4 способ !При реакции Гофмана группа (Ar) R: мигрирует от атома углерода к соседнему
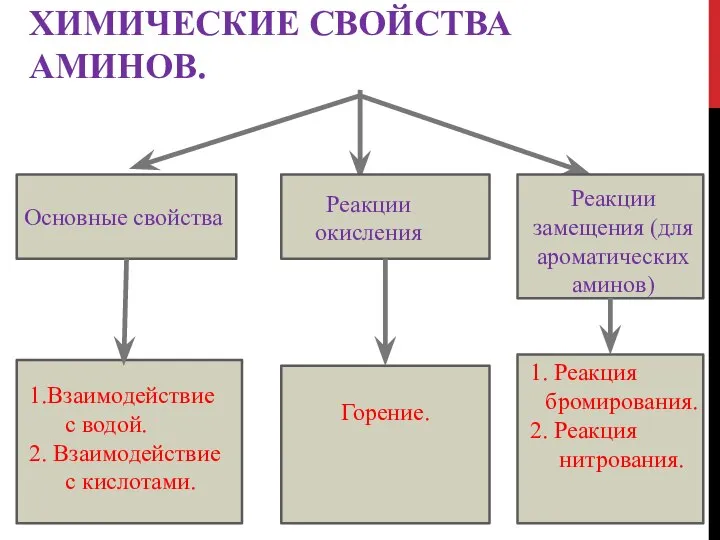
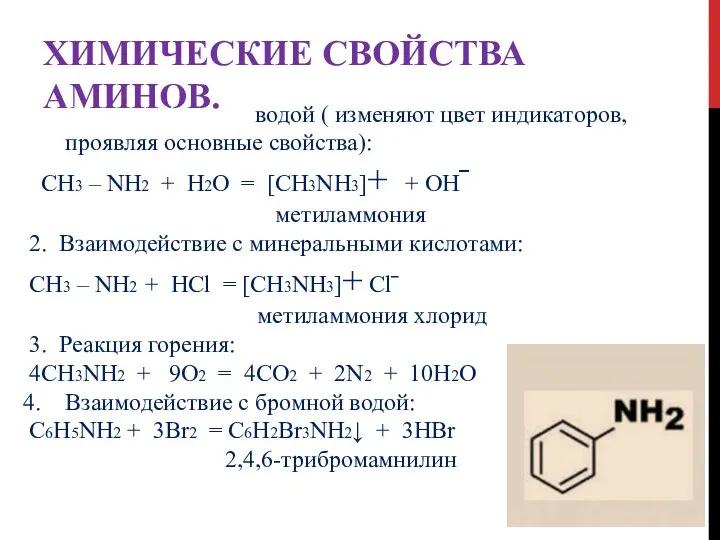
- 14. ХИМИЧЕСКИЕ СВОЙСТВА АМИНОВ. Основные свойства Реакции окисления Реакции замещения (для ароматических аминов) 1.Взаимодействие с водой. 2.
- 15. ХИМИЧЕСКИЕ СВОЙСТВА АМИНОВ. Взаимодействие с водой ( изменяют цвет индикаторов, проявляя основные свойства): CH3 – NH2
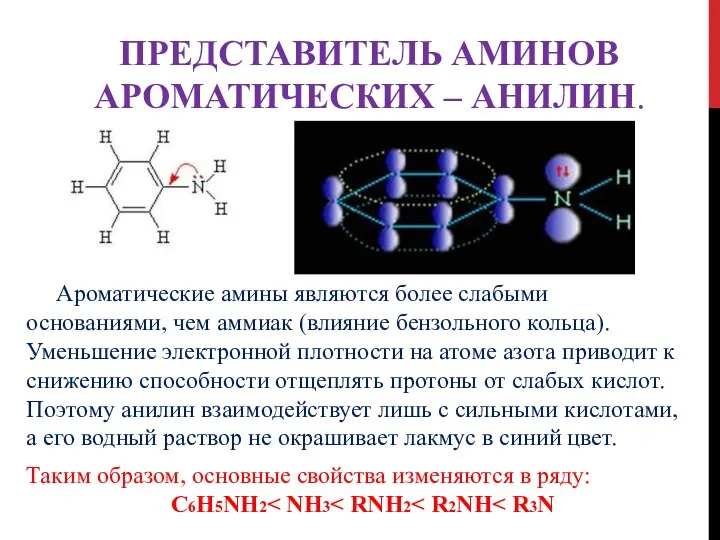
- 16. ПРЕДСТАВИТЕЛЬ АМИНОВ АРОМАТИЧЕСКИХ – АНИЛИН. Ароматические амины являются более слабыми основаниями, чем аммиак (влияние бензольного кольца).
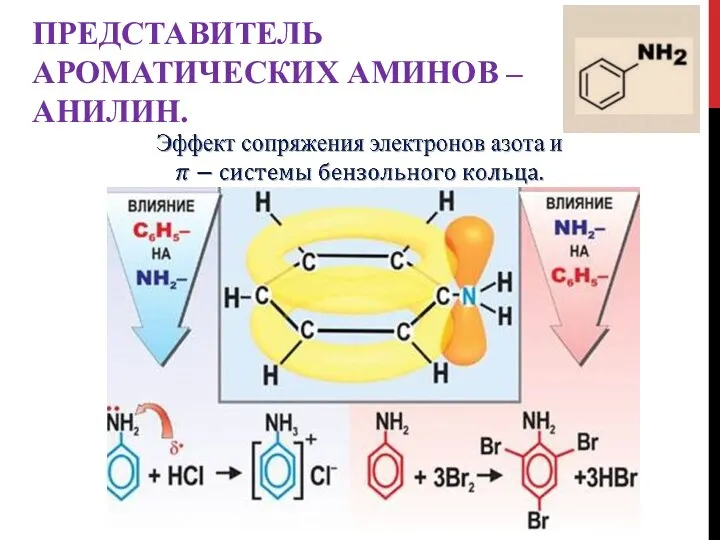
- 17. ПРЕДСТАВИТЕЛЬ АРОМАТИЧЕСКИХ АМИНОВ – АНИЛИН.
- 19. ГЛАВНЫЕ ТЕЗИСЫ.
- 22. Скачать презентацию







 Метасоматические горные породы
Метасоматические горные породы Скорость химической реакции
Скорость химической реакции Презентация по Химии "Cинтетичні волокна" - скачать смотреть бесплатно
Презентация по Химии "Cинтетичні волокна" - скачать смотреть бесплатно Минералы. Значение минералов и задачи минералогии
Минералы. Значение минералов и задачи минералогии Методы решения ОВР с участием органических соединений
Методы решения ОВР с участием органических соединений Энергетическое топливо и его классификация
Энергетическое топливо и его классификация Презентация по Химии "«Свойства комплексных соединений»" - скачать смотреть
Презентация по Химии "«Свойства комплексных соединений»" - скачать смотреть  Пентозофосфатный цикл
Пентозофосфатный цикл Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Химический элемент медь. (11 класс)
Химический элемент медь. (11 класс) Альдегиды и кетоны
Альдегиды и кетоны Мельхіор, Нейзильбер, застосування і склад інших сплавів для приборів в ТВКП
Мельхіор, Нейзильбер, застосування і склад інших сплавів для приборів в ТВКП Кислотность органических соединений. Типы химических реакций
Кислотность органических соединений. Типы химических реакций Praktická cvičení z biochemie
Praktická cvičení z biochemie Химия Изучение коррозии и защиты металлов
Химия Изучение коррозии и защиты металлов Вікторина для ерудитів
Вікторина для ерудитів Ничто так не утомляет, как выполненная на совесть чужая работа Макс Фрай
Ничто так не утомляет, как выполненная на совесть чужая работа Макс Фрай Обмен липидов - 2
Обмен липидов - 2 Алкены. Строение, номенклатура, изомерия, физические и химические свойства алкенов
Алкены. Строение, номенклатура, изомерия, физические и химические свойства алкенов Презентация по Химии "карбон қышқылдары" - скачать смотреть бесплатно
Презентация по Химии "карбон қышқылдары" - скачать смотреть бесплатно Периодическая система элементов Д.И. Менделеева
Периодическая система элементов Д.И. Менделеева Катаболизм пищевых и тканевых липидов. (Лекция 7)
Катаболизм пищевых и тканевых липидов. (Лекция 7) Аналитические методы
Аналитические методы Насыщенные (предельные) углеводороды. Алканы (парафины)
Насыщенные (предельные) углеводороды. Алканы (парафины) Мембранний транспорт. Рівняння Теорела. Рівняння проникності мембран
Мембранний транспорт. Рівняння Теорела. Рівняння проникності мембран Кислоты. Серная кислота-H₂SO₄
Кислоты. Серная кислота-H₂SO₄ Презентация по Химии "Сказ о том, как кот помог открыть йод" - скачать смотреть
Презентация по Химии "Сказ о том, как кот помог открыть йод" - скачать смотреть  Строение вещества. Химические элементы
Строение вещества. Химические элементы