Содержание
- 2. Цели: формирование общеучебных умений и навыков. Задачи: образовательные: изучить строение и свойства аммиака; рассмотреть донорно –
- 3. План 1.Состав молекулы аммиака 2.Строение молекулы аммиака 3.Физические свойства аммиака 4.Химические свойства аммиака 5.Получение аммиака 6.Применение
- 4. 1.Состав молекулы аммиака
- 5. 2. Строение молекулы. NH3 Молекула полярная, имеет форму треугольной пирамиды с атомом азота в вершине, ∠HNH
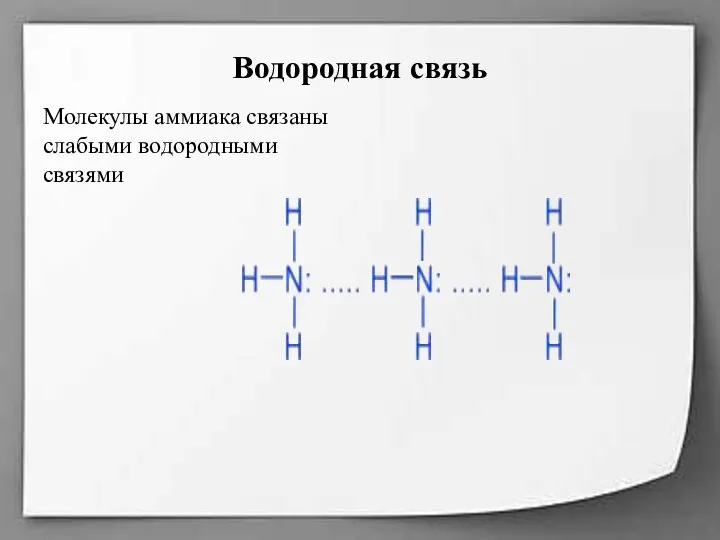
- 6. Водородная связь Молекулы аммиака связаны слабыми водородными связями
- 8. 3. Физические свойства аммиака. изучите физические свойства аммиака по учебнику; рассчитайте его плотность по воздуху Dвозд
- 9. 3.Физические свойства. NH3 – газ без цвета, с резким запахом, почти в два раза легче воздуха,
- 10. Правила собирания аммиака
- 11. 4. Химические свойства аммиака I.Реакции, идущие без изменения степени окисления. 1)Растворение аммиака в воде. NH3 +
- 12. Растворение аммиака в воде.
- 13. Образование иона аммония
- 14. 2) Взаимодействие с кислотами.
- 15. Аммиак реагирует с кислотами с образованием солей аммония. NH3 + HCl → NH4Cl 2NH3 + H2SO4
- 16. II. Реакции, идущие с изменением степени окисления. 1.Аммиак- непрочное соединение и при нагревании разлагается. 2N-3H3 ←t°→
- 17. 2.Горение аммиака в кислороде
- 18. 1. В отсутствии катализатора. 4N-3H3 + 3O2 → 2N20 + 6Н2O
- 19. 3.Каталитическое окисление аммиака
- 20. 4N-3H3 + 5O2 → 4N+2O + 6Н2O В присутствии катализатора
- 21. 4.Аммиак способен восстанавливать оксиды малоактивных металлов . 3Cu+2O + 2N-3H3 → 3Cu0 + N20 + 3Н2O
- 22. IV.Получение аммиака. Работа с учебником. Прочитайте с. 47-48 учебника. Запишите уравнения реакций получения аммиака а) в
- 23. а) в промышленности N2 + 3H2 → 2NH3 б) в лаборатории. 2NH4Cl + Ca(OH)2 –t°→ CaCl2
- 24. Распознавание аммиака
- 25. Распознавание аммиака а) по запаху; б) по посинению влажной лакмусовой бумажки в) по появлению белого дыма
- 26. 5. Применение аммиака
- 27. 5.Применение аммиака. NH3 1) в холодильных установках; 2) в медицине и быту; 3) для производства азотной
- 28. IV. Закрепление изученного материала. 1.Азот при обычных условиях – это: а) тяжелый металл; б) бесцветная маслянистая
- 30. Скачать презентацию


























 Химические волокна. Полиэфирные волокна. Лавсан
Химические волокна. Полиэфирные волокна. Лавсан Основные классы неорганических соединений
Основные классы неорганических соединений Физико-химические основы патологии клетки. Митохондрии и апоптоз
Физико-химические основы патологии клетки. Митохондрии и апоптоз Ароматические углеводороды
Ароматические углеводороды Растворы электролитов
Растворы электролитов Виды присадок к моторным топливам (керосин)
Виды присадок к моторным топливам (керосин) Тепловой эффект химических реакций
Тепловой эффект химических реакций Аспірин Даниленко, Реутенко 11-А
Аспірин Даниленко, Реутенко 11-А  ОВР в гетерогенных системах
ОВР в гетерогенных системах Генетическая связь
Генетическая связь Дгебуадзе Загра Омардибировна, учитель химии, МОУ «СОШ № 14 г.Зеленокумска» Ставропольский край
Дгебуадзе Загра Омардибировна, учитель химии, МОУ «СОШ № 14 г.Зеленокумска» Ставропольский край Технология производства простых полиэфиров
Технология производства простых полиэфиров Вибух газо- та пароповітряних сумішей на відкритому просторі та в приміщенні
Вибух газо- та пароповітряних сумішей на відкритому просторі та в приміщенні Лексикология и фразеология Однозначные и многозначные слова Прямое и переносное значение слова
Лексикология и фразеология Однозначные и многозначные слова Прямое и переносное значение слова Выращивание кристаллов из соли
Выращивание кристаллов из соли Исследовательская работа по химии Количественное содержание витамина С в ягодах клюквы и проблема сохранности в зимний период вр
Исследовательская работа по химии Количественное содержание витамина С в ягодах клюквы и проблема сохранности в зимний период вр Нуклеофильные реакции. (Лекция 7)
Нуклеофильные реакции. (Лекция 7) Расчет температуры вспышки. Классификация горючести жидкости
Расчет температуры вспышки. Классификация горючести жидкости Разложение отходов. 11 класс
Разложение отходов. 11 класс Щелочные металлы
Щелочные металлы Органика в твоих руках
Органика в твоих руках Реакции окисления-восстановления в химическом анализе. (Лекция 8.3)
Реакции окисления-восстановления в химическом анализе. (Лекция 8.3) Оценка химической обстановки при авариях на химически опасных объектах
Оценка химической обстановки при авариях на химически опасных объектах Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Моно- та дикарбонові кислоти. Функціональні похідні карбонових кислот
Моно- та дикарбонові кислоти. Функціональні похідні карбонових кислот Липиды. Фосфолипиды
Липиды. Фосфолипиды Кремнийорганические каучуки
Кремнийорганические каучуки Этапы гравиметрического анализа. (Лекция 3)
Этапы гравиметрического анализа. (Лекция 3)