Содержание
- 2. Фенолы - это ароматические углеводороды, содержащие одну, две или большее количество гидроксильных групп. Кроме фенолов существуют
- 3. В зависимости от количества гидроксильных групп различают по атомности: одноатомные; двухатомные; трехатомные; четырехатомные.
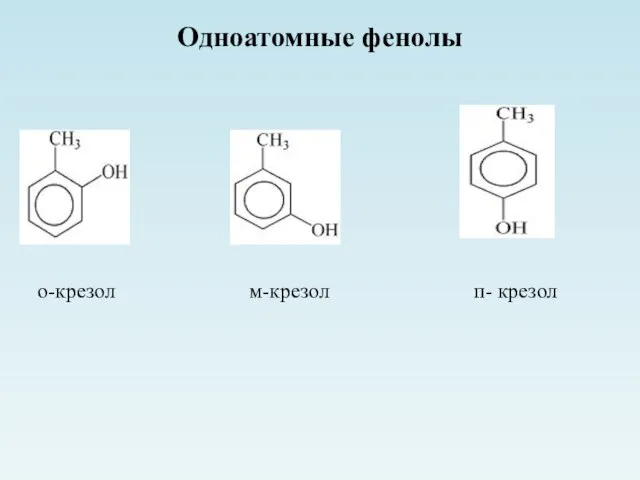
- 4. Одноатомные фенолы о-крезол м-крезол п- крезол
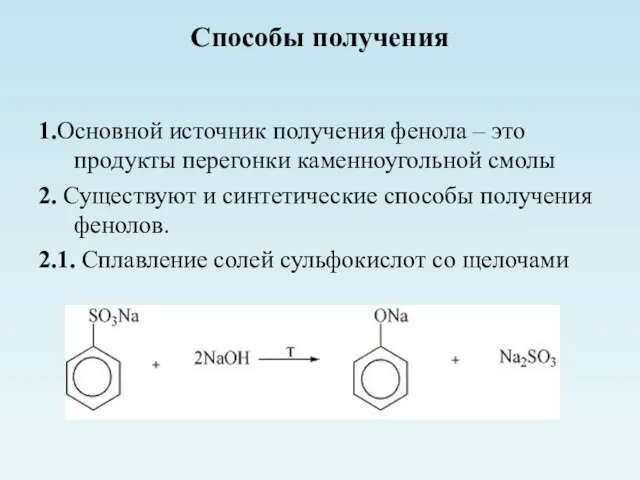
- 5. Способы получения 1.Основной источник получения фенола – это продукты перегонки каменноугольной смолы 2. Существуют и синтетические
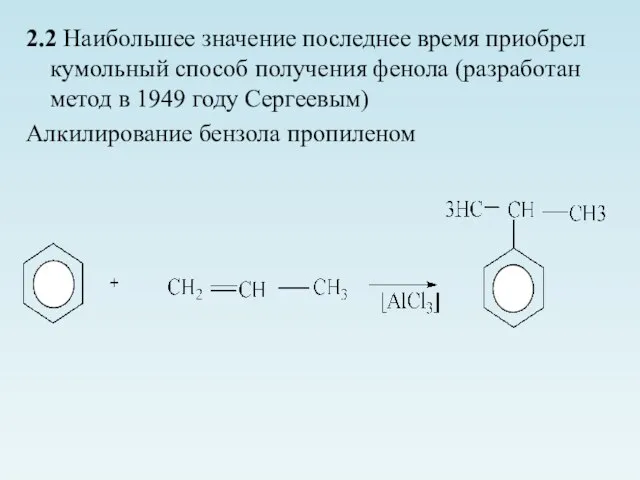
- 6. 2.2 Наибольшее значение последнее время приобрел кумольный способ получения фенола (разработан метод в 1949 году Сергеевым)
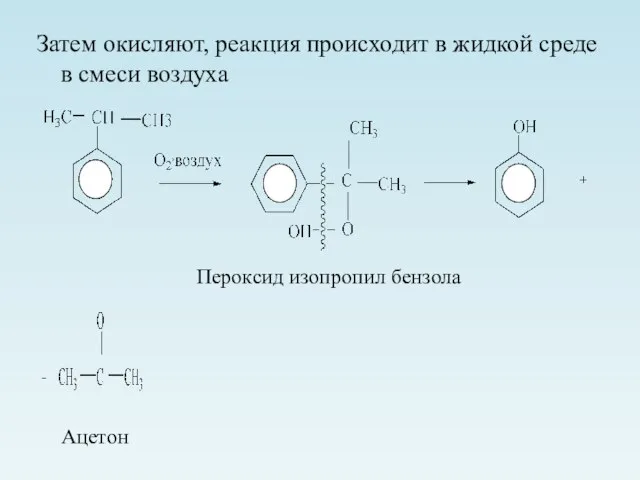
- 7. Затем окисляют, реакция происходит в жидкой среде в смеси воздуха Пероксид изопропил бензола Ацетон
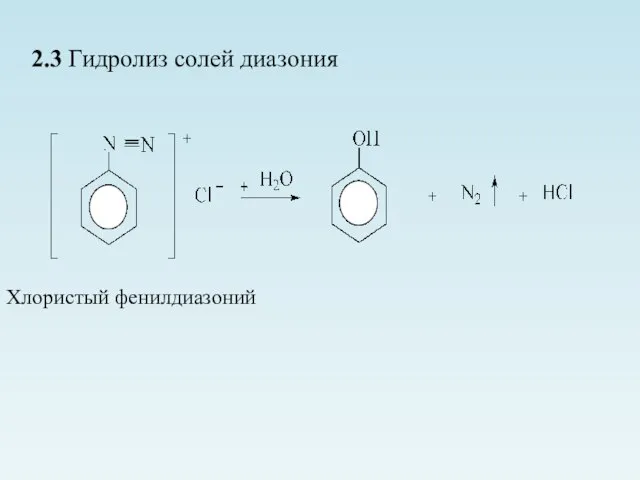
- 8. 2.3 Гидролиз солей диазония Хлористый фенилдиазоний
- 9. Физические свойства Фенолы – это бесцветные кристаллические вещества, трудно растворимые в воде, обладают характерным запахом, а
- 10. Химические свойства Химические свойства фенола определяются наличием двух функциональных групп: гидроксильная группа; ароматическое кольцо. Из-за взаимного
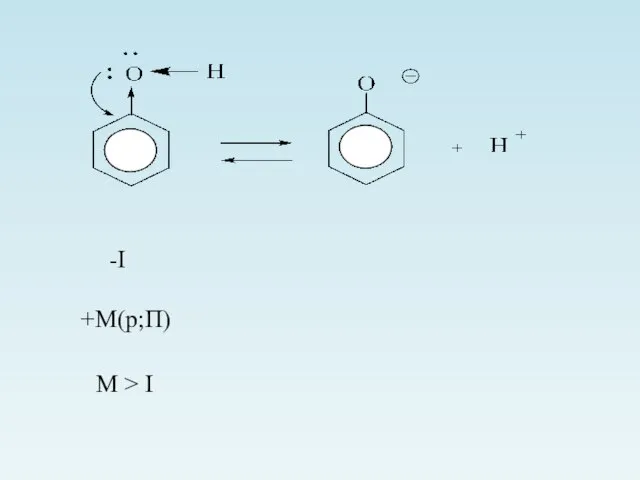
- 11. -I +М(p;П) М > I
- 12. С другой стороны, увеличению кислотных свойств способствует большая стабильность образующегося фенолят иона Вывод: электроно-акцепторные заместители увеличивают
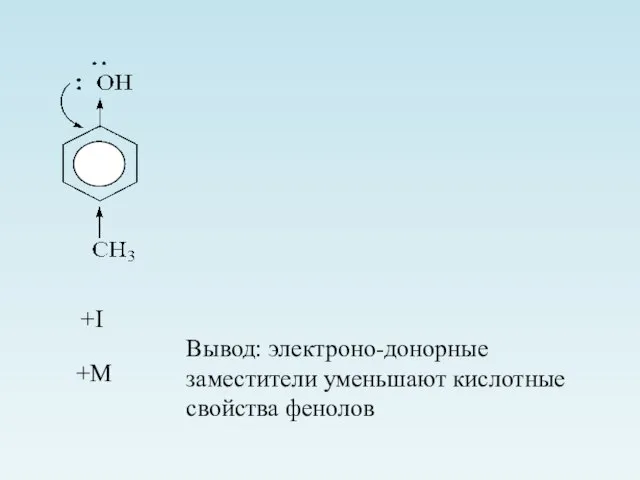
- 13. +I +М Вывод: электроно-донорные заместители уменьшают кислотные свойства фенолов
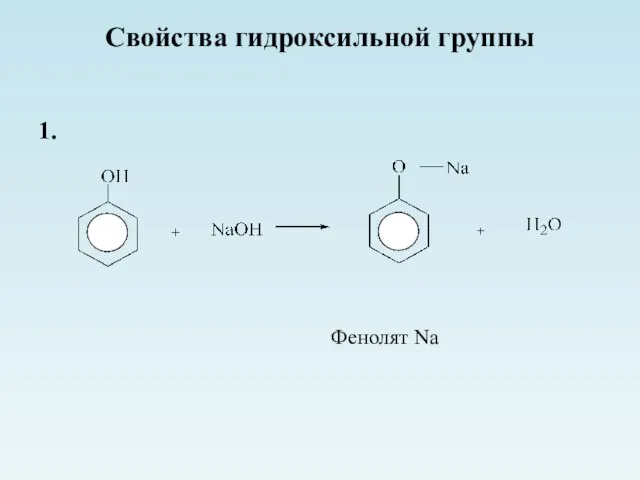
- 14. Свойства гидроксильной группы 1. Фенолят Na
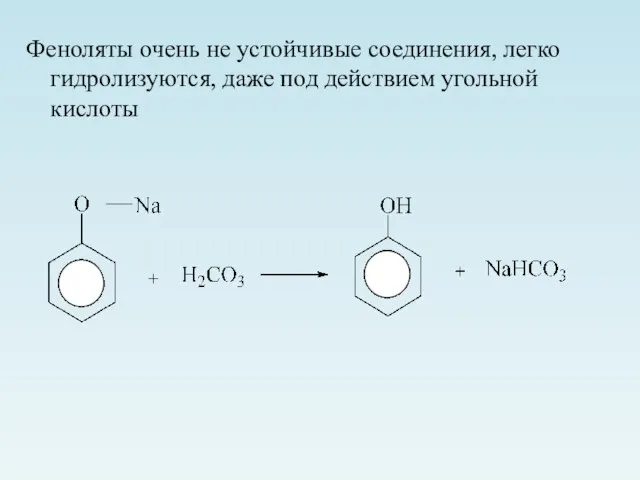
- 15. Феноляты очень не устойчивые соединения, легко гидролизуются, даже под действием угольной кислоты
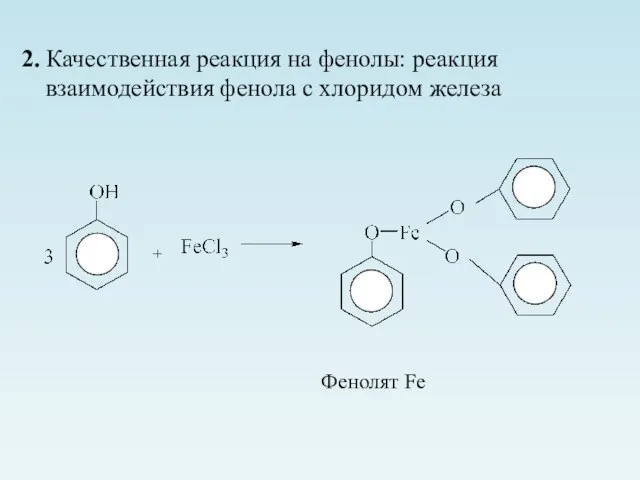
- 16. 2. Качественная реакция на фенолы: реакция взаимодействия фенола с хлоридом железа Фенолят Fe
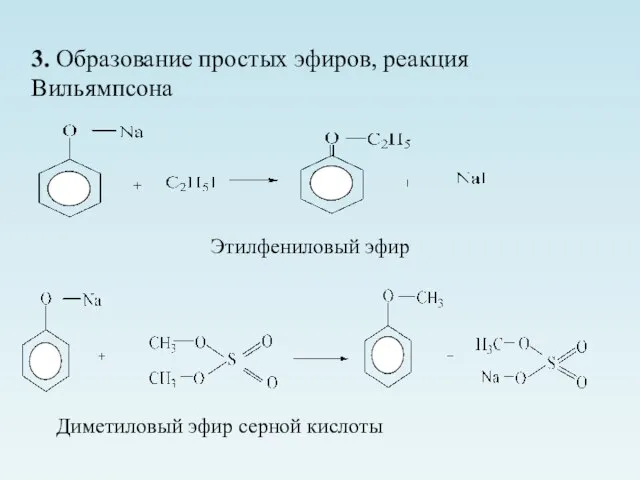
- 17. 3. Образование простых эфиров, реакция Вильямпсона Этилфениловый эфир Диметиловый эфир серной кислоты
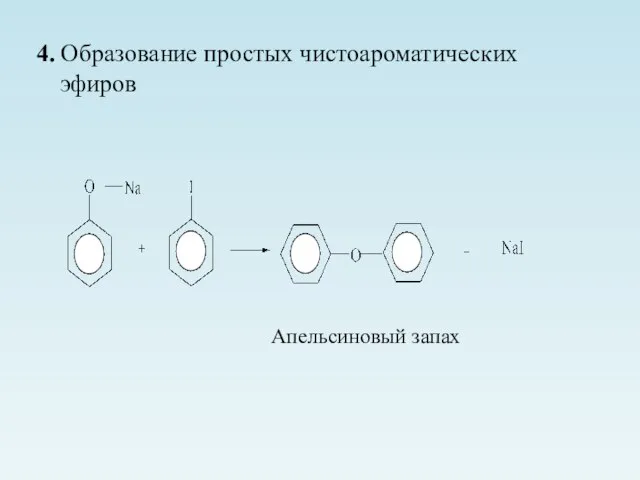
- 18. 4. Образование простых чистоароматических эфиров Апельсиновый запах
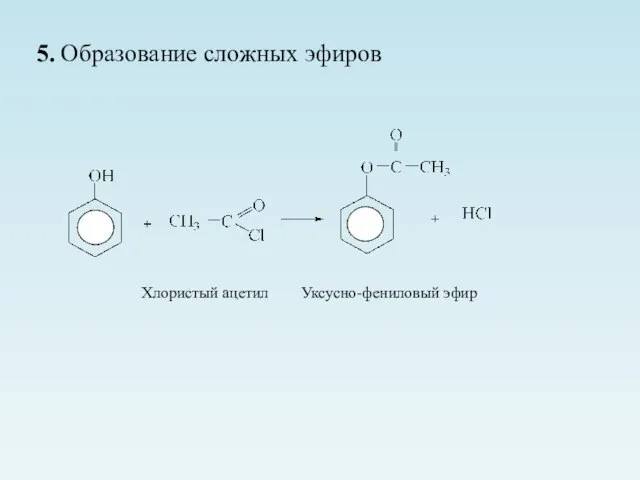
- 19. 5. Образование сложных эфиров Хлористый ацетил Уксусно-фениловый эфир
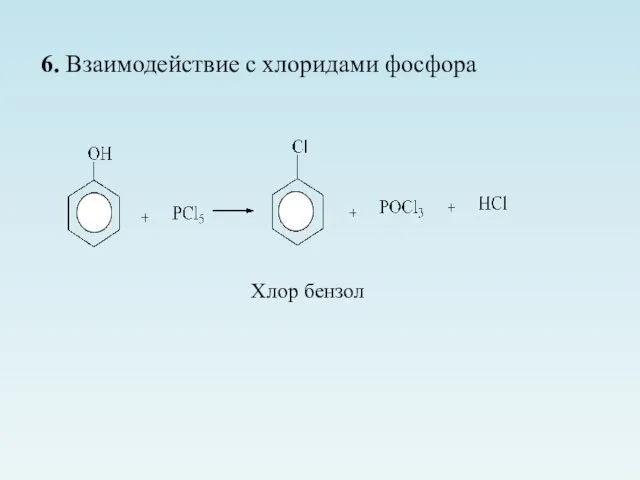
- 20. 6. Взаимодействие с хлоридами фосфора Хлор бензол
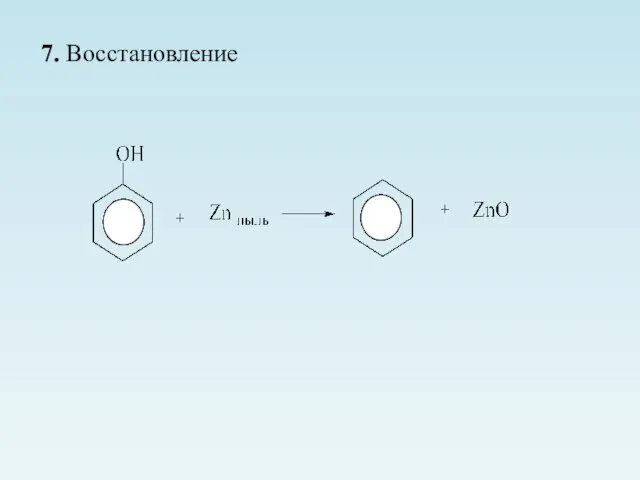
- 21. 7. Восстановление
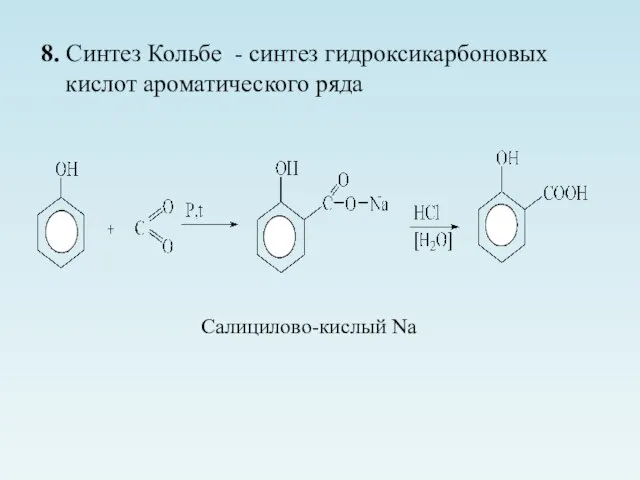
- 22. 8. Синтез Кольбе - синтез гидроксикарбоновых кислот ароматического ряда Салицилово-кислый Na
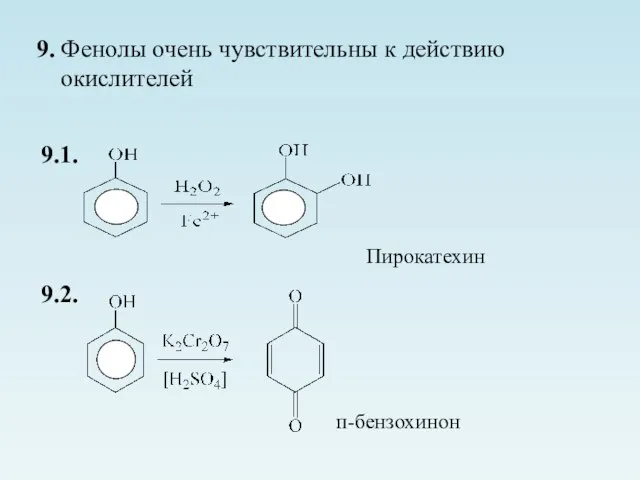
- 23. 9. Фенолы очень чувствительны к действию окислителей 9.1. Пирокатехин 9.2. п-бензохинон
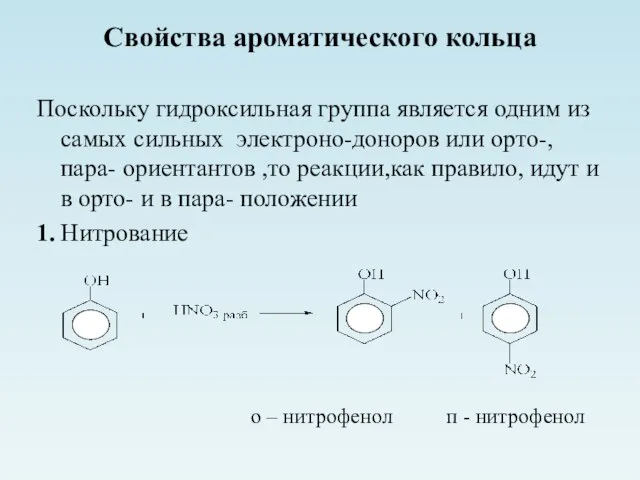
- 24. Свойства ароматического кольца Поскольку гидроксильная группа является одним из самых сильных электроно-доноров или орто-, пара- ориентантов
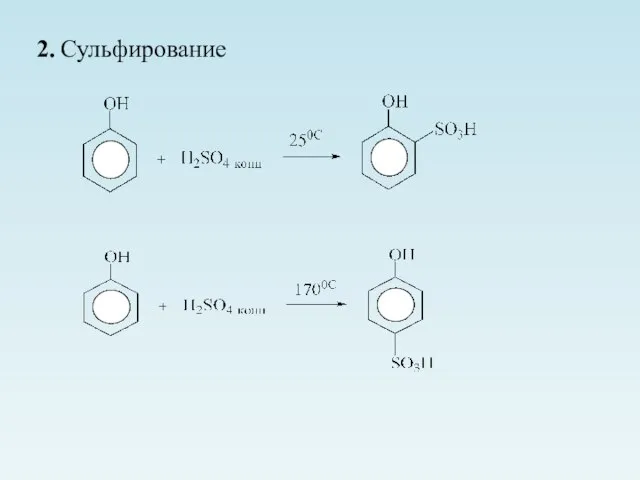
- 25. 2. Сульфирование
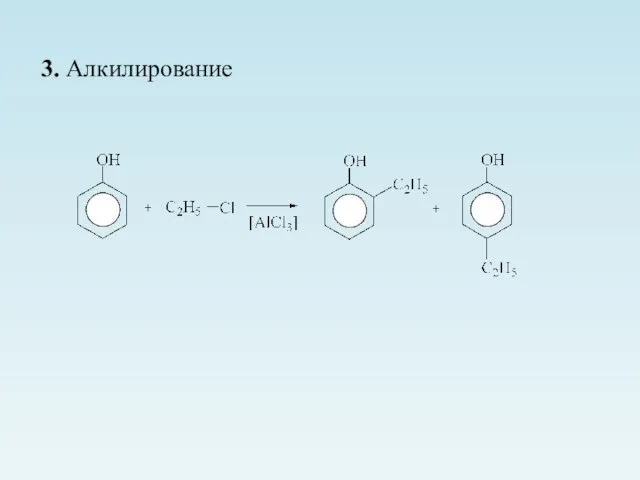
- 26. 3. Алкилирование
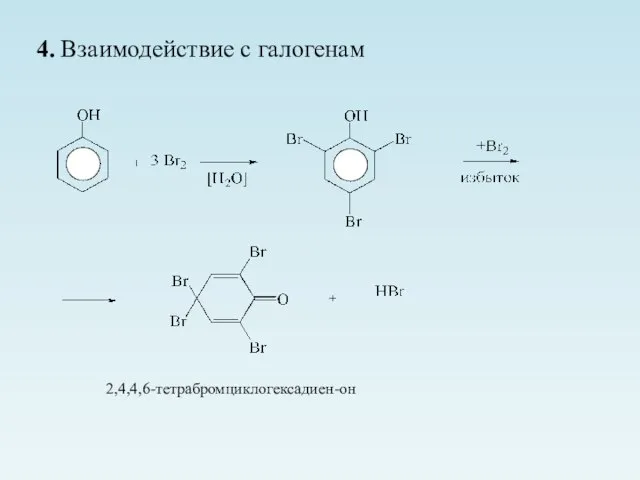
- 27. 4. Взаимодействие с галогенам 2,4,4,6-тетрабромциклогексадиен-он
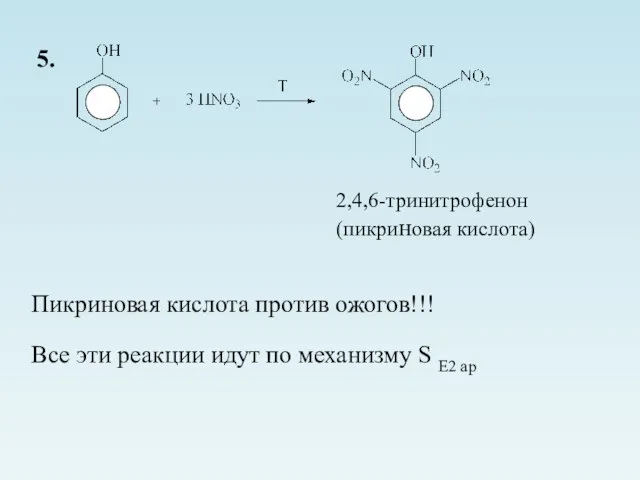
- 28. 5. 2,4,6-тринитрофенон (пикриновая кислота) Пикриновая кислота против ожогов!!! Все эти реакции идут по механизму S Е2
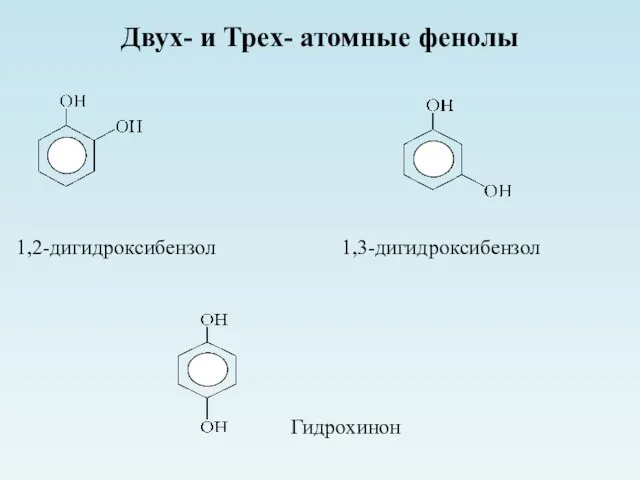
- 29. Двух- и Трех- атомные фенолы 1,2-дигидроксибензол 1,3-дигидроксибензол Гидрохинон
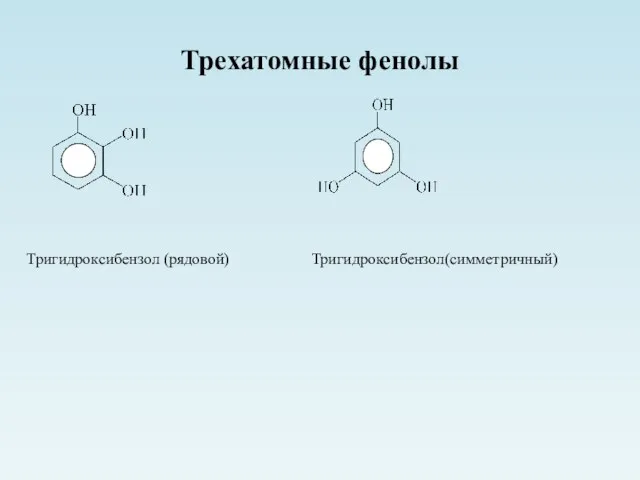
- 30. Трехатомные фенолы Тригидроксибензол (рядовой) Тригидроксибензол(симметричный)
- 31. Двух- и трех- атомные фенолы – кристаллические вещества, которые легко растворяются в воде. Проявляют все свойства
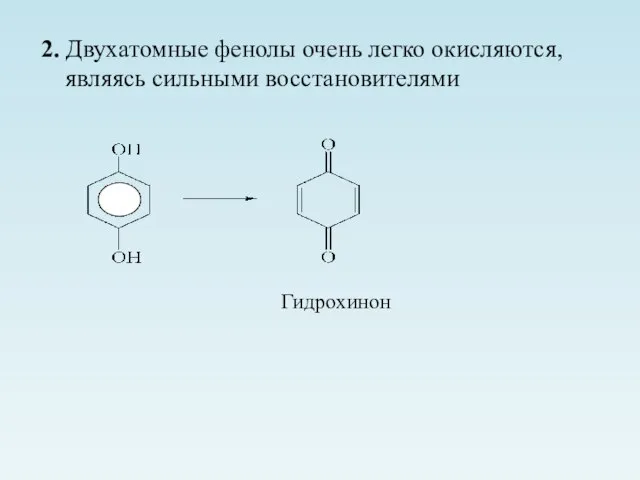
- 32. 2. Двухатомные фенолы очень легко окисляются, являясь сильными восстановителями Гидрохинон
- 34. Скачать презентацию






 6-я группа элементов. 9 класс
6-я группа элементов. 9 класс Алкадиены. Классификация алкадиенов
Алкадиены. Классификация алкадиенов Нуклеиновые кислоты
Нуклеиновые кислоты Презентация по Химии "Степень окисления" - скачать смотреть бесплатно_
Презентация по Химии "Степень окисления" - скачать смотреть бесплатно_ Сырьё для получения фенолальдегидных полимеров
Сырьё для получения фенолальдегидных полимеров Презентация по Химии "Увлекательные факты из жизни великого химика." - скачать смотреть бесплатно
Презентация по Химии "Увлекательные факты из жизни великого химика." - скачать смотреть бесплатно Разработка и исследование системы управления процессом осушки бутанола при производстве н -бутилового спирта
Разработка и исследование системы управления процессом осушки бутанола при производстве н -бутилового спирта Химическая кинетика и катализ
Химическая кинетика и катализ Ферросплавы. Феррохром
Ферросплавы. Феррохром Закон Авогадро. Молярный объем и относительные плотности газов. Уравнение Клапейрона-Менделеева
Закон Авогадро. Молярный объем и относительные плотности газов. Уравнение Клапейрона-Менделеева Нефть. Свойства, состав, переработка
Нефть. Свойства, состав, переработка Синтез ультрадисперсного мела для различных эффективных использований
Синтез ультрадисперсного мела для различных эффективных использований К 180-летию со дня рождения Д.И. Менделеева
К 180-летию со дня рождения Д.И. Менделеева Кислоты, их классификация и свойства Презентация к уроку химии для 8 класса Учитель МОУ «Куженерская средняя общеобразовате
Кислоты, их классификация и свойства Презентация к уроку химии для 8 класса Учитель МОУ «Куженерская средняя общеобразовате Электроды 1 рода
Электроды 1 рода Homecredit Bank. Показатели и зоны роста
Homecredit Bank. Показатели и зоны роста Закон действующих масс и его применение к различным типам равновесий
Закон действующих масс и его применение к различным типам равновесий ПОЛІПРОПІЛЕН ( РР) СИНТЕТИЧНИЙ ПОЛІМЕР, ПРОДУКТ ПОЛІМЕРИЗАЦІЇ ПРОПІЛЕНУ, [—СН2—СН(СН3)—]N.
ПОЛІПРОПІЛЕН ( РР) СИНТЕТИЧНИЙ ПОЛІМЕР, ПРОДУКТ ПОЛІМЕРИЗАЦІЇ ПРОПІЛЕНУ, [—СН2—СН(СН3)—]N.  Газоанализаторы. Измерительный прибор для определения качественного и количественного состава смесей газов
Газоанализаторы. Измерительный прибор для определения качественного и количественного состава смесей газов Посуда, ее виды и использование. Работу выполнила Гливинская Анастасия ученица 9 класса МБОУ «СОШ №11»
Посуда, ее виды и использование. Работу выполнила Гливинская Анастасия ученица 9 класса МБОУ «СОШ №11»  Нитраты, их влияние на организм человека
Нитраты, их влияние на организм человека Поливинилхлорид. Физические и химические свойства
Поливинилхлорид. Физические и химические свойства Азот. Открытие азота
Азот. Открытие азота Предмет химии. Вещества. 8 клвсс
Предмет химии. Вещества. 8 клвсс Тіндер-тірі организмнің иерархиялық деңгейінің ұйымдастырудың бір түрі. Олардың құрылымдық принциптері
Тіндер-тірі организмнің иерархиялық деңгейінің ұйымдастырудың бір түрі. Олардың құрылымдық принциптері Химическая термодинамика
Химическая термодинамика AgCl негізіндегі нанокомпазиттердің фотокаталитикалық белсенділігі
AgCl негізіндегі нанокомпазиттердің фотокаталитикалық белсенділігі Сахароза
Сахароза