Содержание
- 2. Электроды 2 рода Усложним конструкцию, введем в систему на границу фаз серебро – раствор труднорастворимую соль
- 3. Газовые электроды В систему вместо труднорастворимого вещества можно ввести газ, тогда получатся так называемые газовые электроды.
- 4. Кислородный электрод
- 5. Хлорный электрод Если на такую платиновую пластину, погруженную в раствор соляной кислоты, подавать газообразный хлор, получится
- 6. Электроды сравнения (водородный) (H2)Pt|H2SO4 На платине устанавливается равновесие: H2 ─ 2e ↔ 2H+ εH2 = εoH2
- 7. Red-ox электроды (+) Pt | Fe3+ Fe3+ + e ↔ Fe2+ (─) Pt | Sn2+ Sn4+
- 8. Гальванический элемент Двухэлектродная обратимая система, в которой энергия химической реакции преобразуется в электрическую, называется гальваническим элементом.
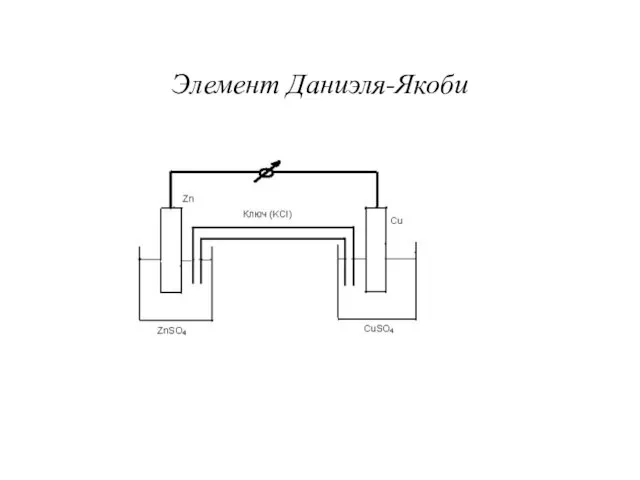
- 9. Элемент Даниэля-Якоби
- 10. Схема элемента и обозначение электродов Zn + CuSO4 ↔ ZnSO4 + Cu (─) Zn| ZnSO4 ||
- 11. Электродвижущая сила (Э.Д.С) Суммарная работа, производимая электрическим током называется электродвижущей силой (э.д.с.) элемента (Е). ∑Аi =
- 12. Виды работ А1 –работа окисления цинка (поверхность металлического цинка в контакте с раствором его соли). А1
- 13. Связь э.д.с. с потенциалами электродов А3 = А4 ≈ 0. Е • n • F =
- 14. Концентрационная цепь Cu| CuSO4 || CuSO4 | Cu (2) С1 = 1 моль/л, С2 = 0,01
- 15. Автомобильный аккумулятор
- 16. Аккумуляторные батареи
- 18. Скачать презентацию














 Видалення забруднень органічного походження з поверхні тканини
Видалення забруднень органічного походження з поверхні тканини Углерод и кремний
Углерод и кремний Алкадиены. Состав и строение
Алкадиены. Состав и строение Термодинамическое равновесие
Термодинамическое равновесие Белоктар жөніңдегі ілім дамуының қысқаша тарихы
Белоктар жөніңдегі ілім дамуының қысқаша тарихы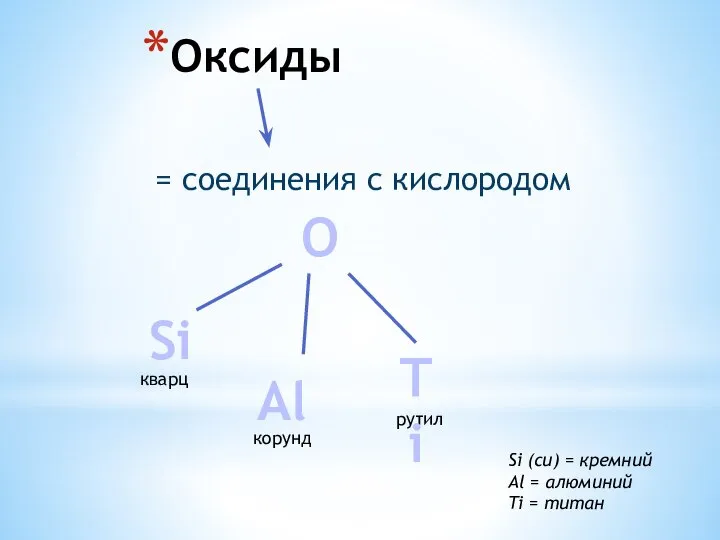 Оксиды. Кварц (SiO2). Корунд (Al2O3)
Оксиды. Кварц (SiO2). Корунд (Al2O3) Презентація на тему : “Кам’яне вугілля та продукти його переробки”
Презентація на тему : “Кам’яне вугілля та продукти його переробки”  Химиялық реакциялардың типтері
Химиялық реакциялардың типтері IV группа (побочная подгруппа)
IV группа (побочная подгруппа) Строение вещества. Химическая связь
Строение вещества. Химическая связь Спирти. Одноатомні насичені спирти (алканоли)
Спирти. Одноатомні насичені спирти (алканоли) Химический состав яблока
Химический состав яблока Химия соединения железа
Химия соединения железа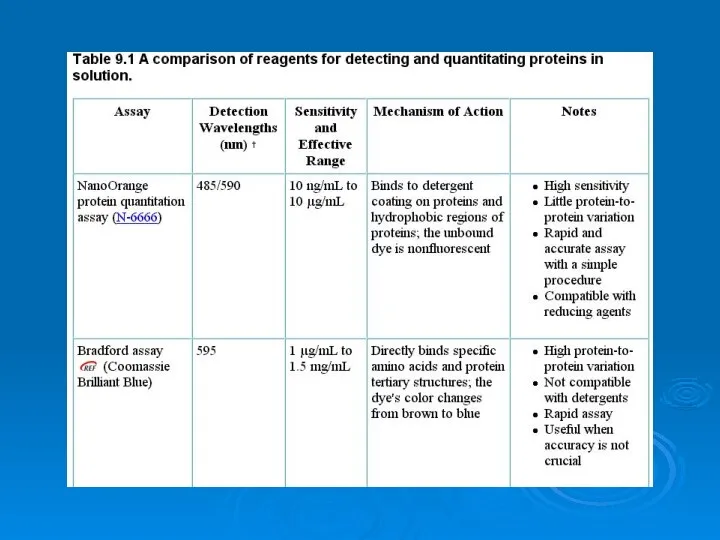 Analysis of proteins
Analysis of proteins Механизмы двухсубстатных реакций
Механизмы двухсубстатных реакций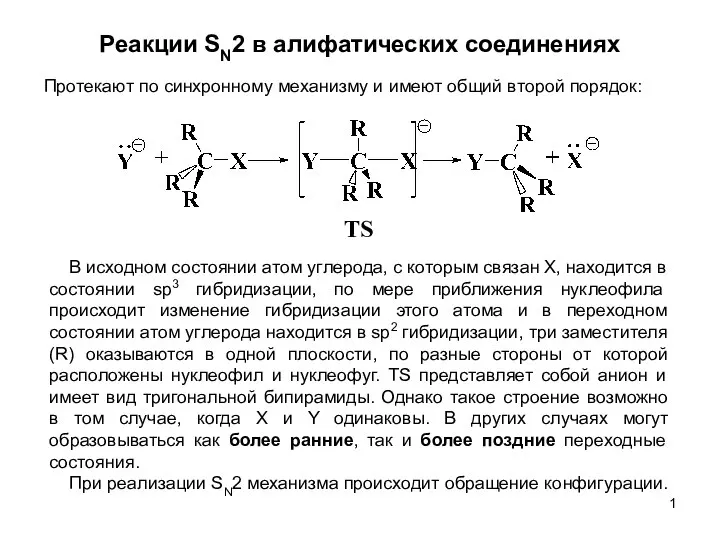 Реакции SN2 в алифатических соединениях. (Лекция 7.1)
Реакции SN2 в алифатических соединениях. (Лекция 7.1) Титриметрический анализ
Титриметрический анализ Неметаллы и их соединения
Неметаллы и их соединения Кислород. 8 класс
Кислород. 8 класс Лекарственные растения и сырье, содержащие гликозиды. (Лекция 7)
Лекарственные растения и сырье, содержащие гликозиды. (Лекция 7)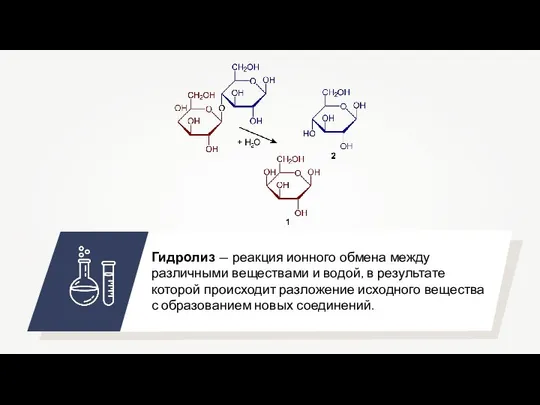 Гидролиз. Реакции гидролиза
Гидролиз. Реакции гидролиза Повторение и обобщение. Зависимость свойств веществ от типа химической связи и кристаллической решетки
Повторение и обобщение. Зависимость свойств веществ от типа химической связи и кристаллической решетки Литосфера. Физико-химические процессы в литосфере
Литосфера. Физико-химические процессы в литосфере Жиры. История открытия жиров
Жиры. История открытия жиров Галогены
Галогены Щелочноземельные металлы
Щелочноземельные металлы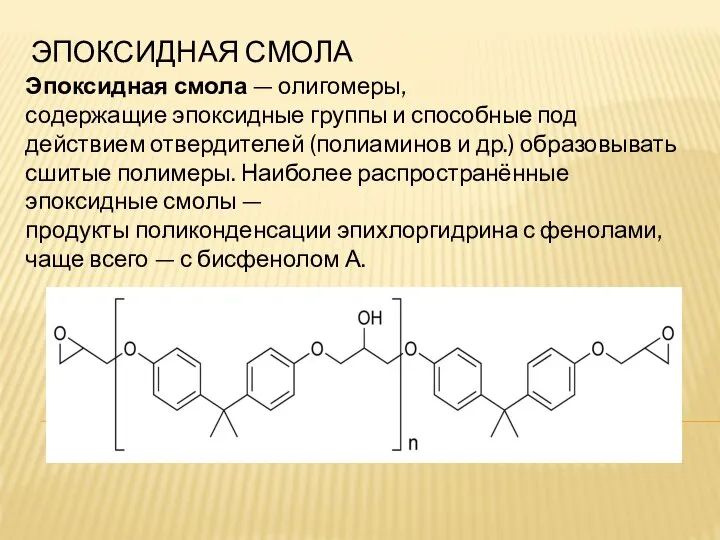 Эпоксидная смола
Эпоксидная смола Калій. Знаходження в періодичній системі і основні характеристики
Калій. Знаходження в періодичній системі і основні характеристики