Слайд 16

Металлические кристаллы
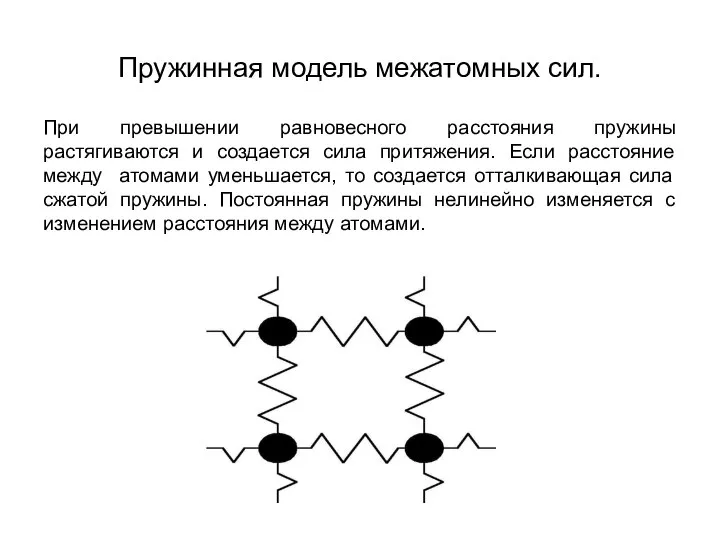
Металлические кристаллы - это кристаллы, в которых связь между
атомами обусловлена взаимодействием свободных электронов с положительно заряженными ионами кристаллической решетки. Поэтому металлические кристаллы характеризуются относительно низкой энергией связи (100–400 кДж/моль), высокой компактностью и высоким координационным числом.
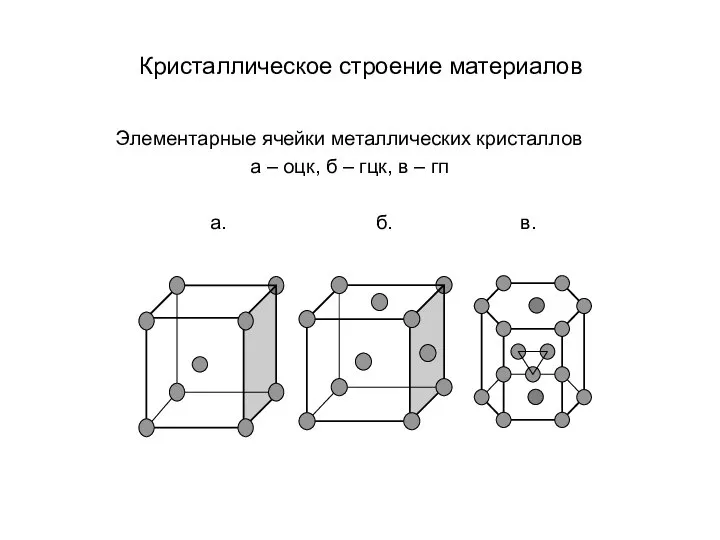
В кристаллах, состоящих из одинаковых атомов, каждый атом может иметь не более 12 соседей, что соответствует максимально возможной плотности упаковки. Координационное число 12 имеют два типа кристаллической решетки: гранецентрированная кубическая (ГЦК) и гексагональная плотноупакованная (ГП). Как ГЦК, так и ГП решетка имеют коэффициент компактности 0,74. Так как они обеспечивают наиплотнейшую упаковку и, следовательно, низкую энергию, то эти две кристаллические структуры встречаются у большого количества металлов. Например, ГЦК решетку имеют такие металлы как Ni, Cu, Ag, Pt, Al. ГП решетку имеют металлы Mg, Co, Be, Ti и др.
У некоторых металлических кристаллов атом может быть координирован с 8 соседями. Несколько меньший коэффициент компактности (0,68) вызван присутствием ковалентной компоненты межатомной связи. Такая кристаллическая решетка называется объемноцентрированной кубической (ОЦК). К металлам с ОЦК кристаллической структурой относятся Na, K, V, Cr, Nb, Mo, Ta, W.
















 Элементарные процессы роста кристаллов (лекция 2)
Элементарные процессы роста кристаллов (лекция 2) c4bf82f888b84ff1b75efb1a64c84b0f
c4bf82f888b84ff1b75efb1a64c84b0f Получение и реакции пиразина
Получение и реакции пиразина Химическое сопротивление алюминий и его сплавов
Химическое сопротивление алюминий и его сплавов Энергетический обмен
Энергетический обмен Правила поведения зимой на воде
Правила поведения зимой на воде  Классы неорганических соединений Оксиды Кислоты Соли Основания
Классы неорганических соединений Оксиды Кислоты Соли Основания Основы промышленной экологии. Занятие 2
Основы промышленной экологии. Занятие 2 Пластмассалар, пластикалық материалдар
Пластмассалар, пластикалық материалдар Ізотопи і нукліди
Ізотопи і нукліди Номенклатура органических веществ - алканов
Номенклатура органических веществ - алканов Своя игра «Знаешь ли ты химические элементы?»
Своя игра «Знаешь ли ты химические элементы?» Химическая промышленность и химические технологии
Химическая промышленность и химические технологии Л3.12 Композицитонные материалы
Л3.12 Композицитонные материалы Выделение нефтегазоматеринских пород по данным пиролиза. Построение геохимического разреза
Выделение нефтегазоматеринских пород по данным пиролиза. Построение геохимического разреза Полимеры. Классификация, применение
Полимеры. Классификация, применение Значение органической химии Кондрашов Алексей | 9 А класс
Значение органической химии Кондрашов Алексей | 9 А класс  Средние породы. Типичный андезитовый вулкан
Средние породы. Типичный андезитовый вулкан Игра «Химические элементы» (формулы и названия)
Игра «Химические элементы» (формулы и названия) Агрохимия растений
Агрохимия растений Штучні і синтетичні волокна
Штучні і синтетичні волокна  Строение и функции отдельных коферментов
Строение и функции отдельных коферментов Релаксационные свойства полимеров
Релаксационные свойства полимеров Роль металлов в нашей жизни
Роль металлов в нашей жизни Конструкционные и специальные материалы холодильной техники
Конструкционные и специальные материалы холодильной техники Предмет химии. Вещества
Предмет химии. Вещества Гидролиз солей.
Гидролиз солей.  Использование дрожжей в пищевой промышленности Федеральное государственное образовательное учреждение среднего профессионал
Использование дрожжей в пищевой промышленности Федеральное государственное образовательное учреждение среднего профессионал