Содержание
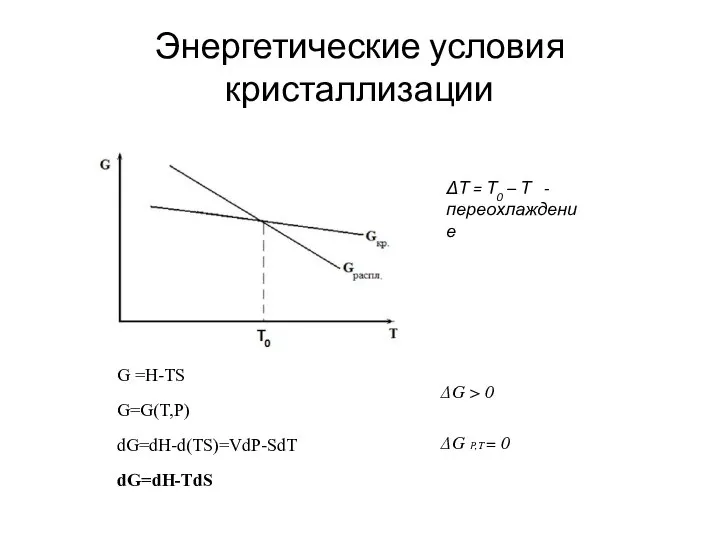
- 2. Энергетические условия кристаллизации ΔТ = Т0 – Т - переохлаждение G =H-TS G=G(T,P) dG=dH-d(TS)=VdP-SdT dG=dH-TdS ΔG
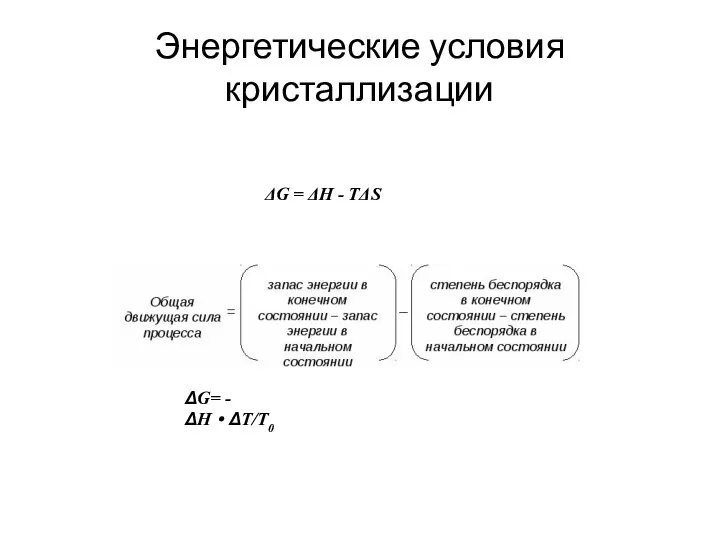
- 3. Энергетические условия кристаллизации ΔG = ΔH - TΔS ΔG= - ΔH·ΔT/T0
- 4. Энергетические условия кристаллизации Gж=Gкр → Tпл ∆G=Gж-тв ∆T=Tпл–T кр - степень переохлаждения ΔG= - ΔH·ΔT/T0
- 5. Энергетические условия кристаллизации ΔT=T-T0 - переохлаждение ΔP=P-P0 – пересыщение Δс=с-с0 - пересыщение
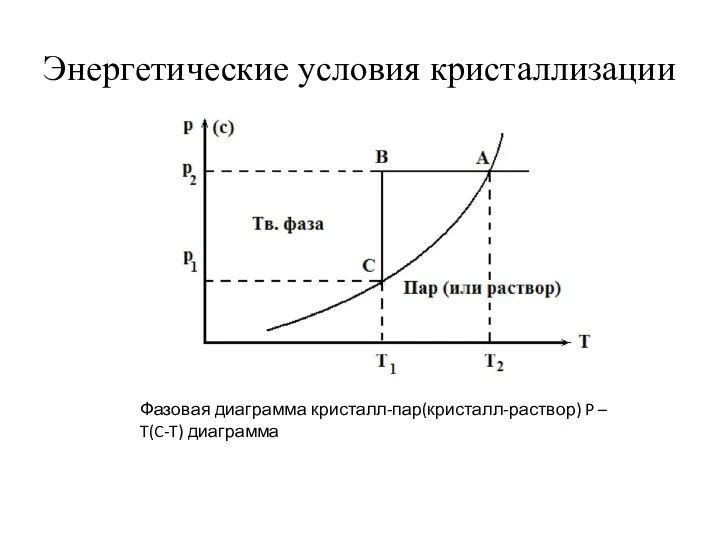
- 6. Энергетические условия кристаллизации Фазовая диаграмма кристалл-пар(кристалл-раствор) P – T(C-T) диаграмма
- 7. Энергетические условия кристаллизации Фаза – однородная часть, характеризующаяся определенным составом, кристаллической решеткой и отделенная от других
- 8. Эвтектика греч. éutektos — легкоплавящийся) — нонвариантная (при постоянном давлении) точка в системе из n компонентов,
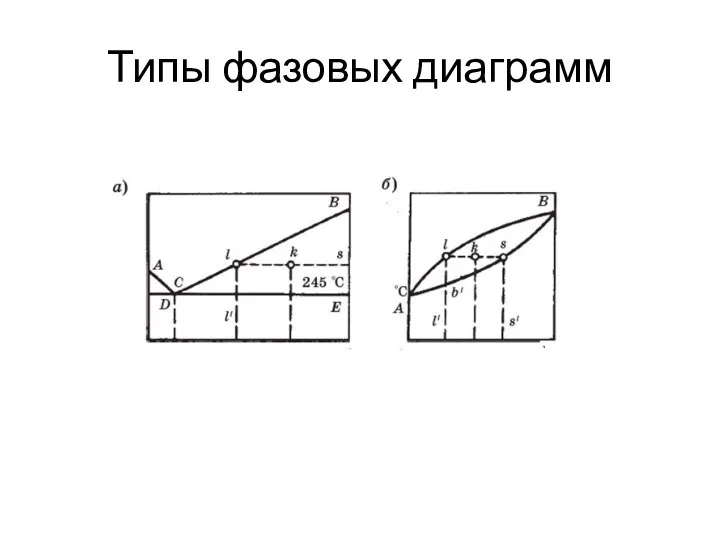
- 9. Типы фазовых диаграмм
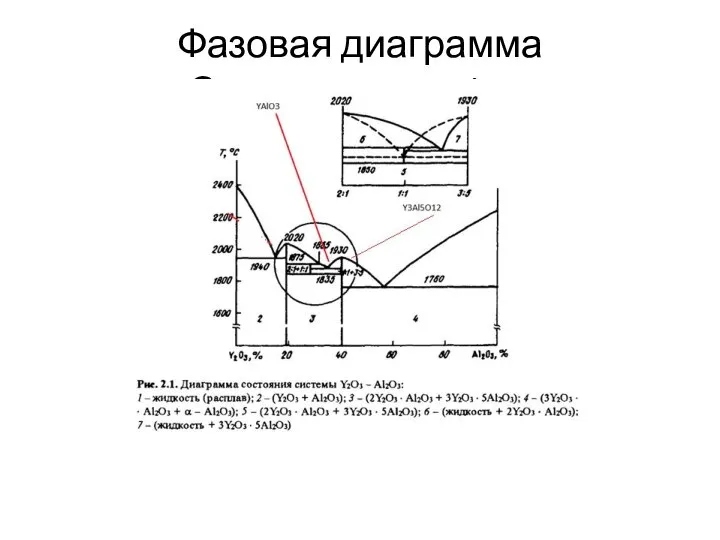
- 10. Фазовая диаграмма Системы Y2O3-Al2O3
- 11. Кинетика кристаллизации Гиббс – теория зарождения центров кристаллизации. Переход из неравновесного(метастабильного) состояния Метастабильное состояние – появление
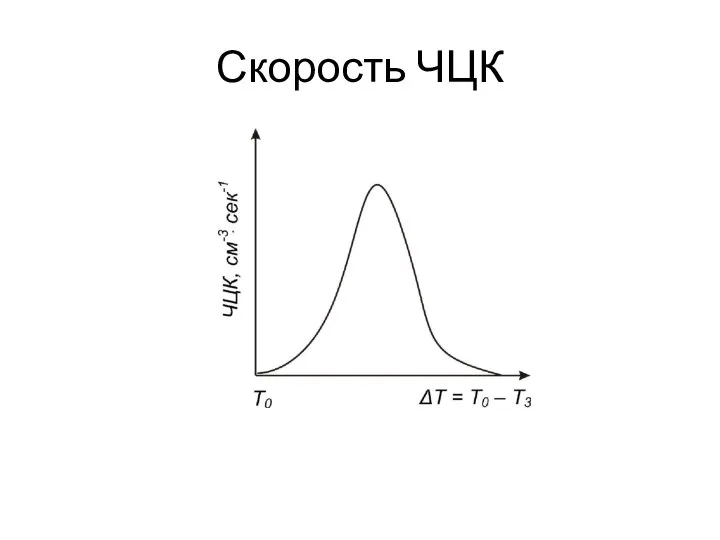
- 12. Скорость ЧЦК
- 13. Кинетика кристаллизации Определение ЧЦК
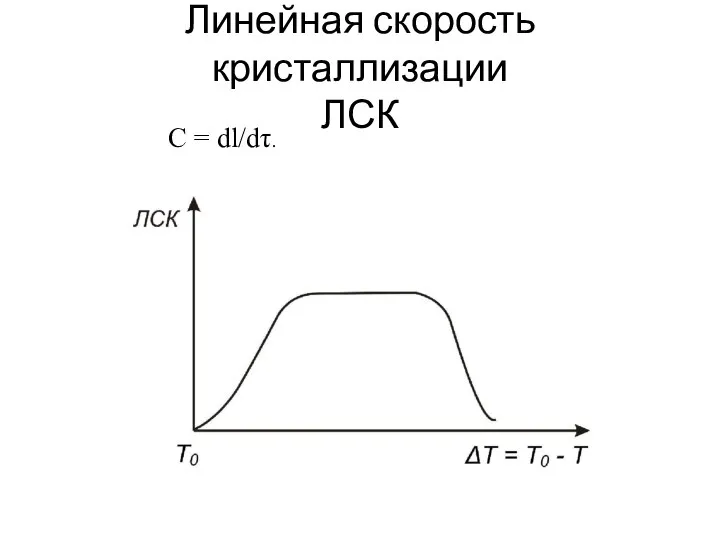
- 14. Линейная скорость кристаллизации ЛСК С = dl/dτ.
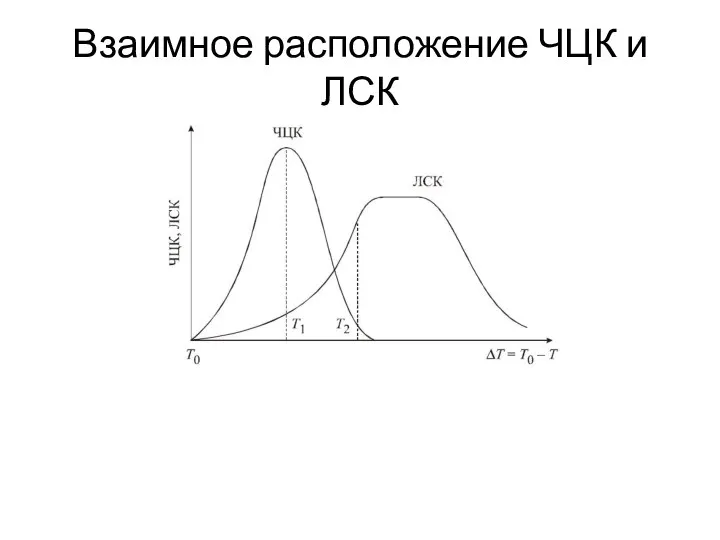
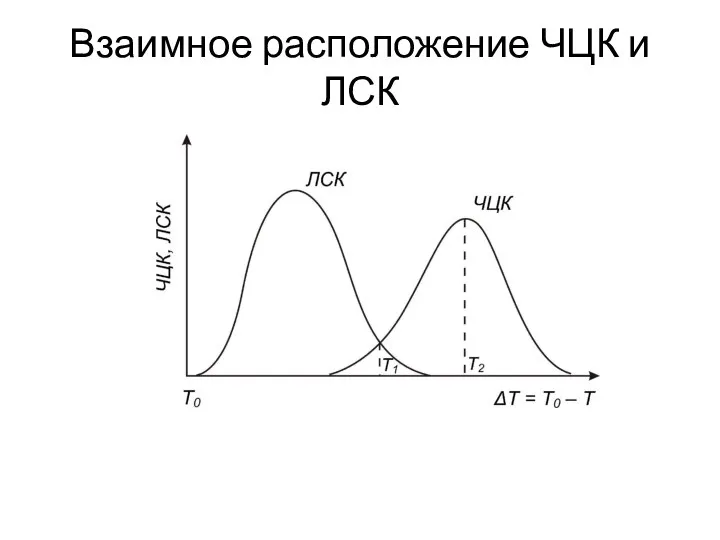
- 15. Взаимное расположение ЧЦК и ЛСК
- 16. Взаимное расположение ЧЦК и ЛСК
- 17. Взаимное расположение ЧЦК и ЛСК
- 18. Влияние давления на ЧЦК и ЛСК
- 19. Определение температурного интервала кристаллизации методом принудительной кристаллизации
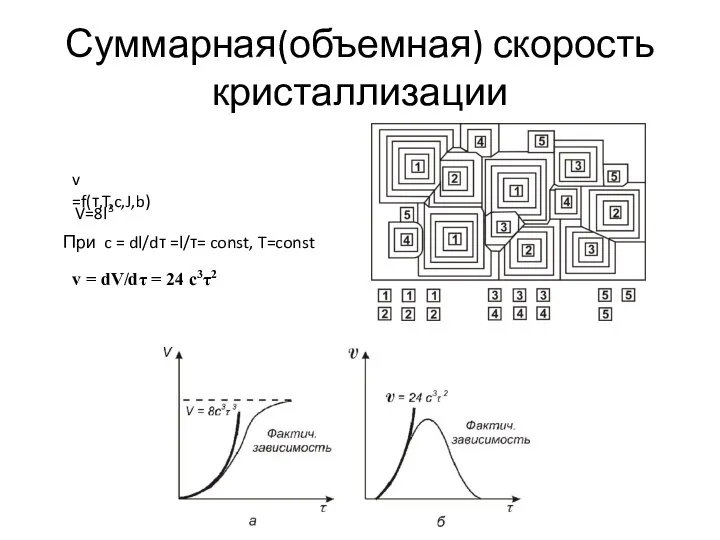
- 20. Суммарная(объемная) скорость кристаллизации v =f(τ,T,c,J,b) V=8l3 При c = dl/dτ =l/τ= const, T=const v = dV/dτ
- 21. Огранка кристалла и скорость роста граней Vc>Vb>Va Vc : Va = 3 Анизотропия скорости роста кристалла
- 22. Огранка кристалла и скорость роста граней Геометрический отбор Методы Бриджмана, Обреимова-Шубникова, Стокбаргера
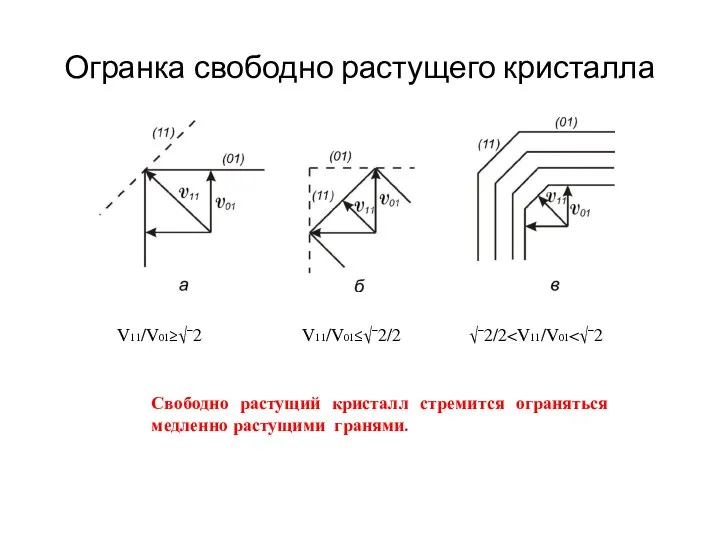
- 23. Огранка свободно растущего кристалла V11/V01≥√¯2 V11/V01≤√¯2/2 √¯2/2 Свободно растущий кристалл стремится ограняться медленно растущими гранями.
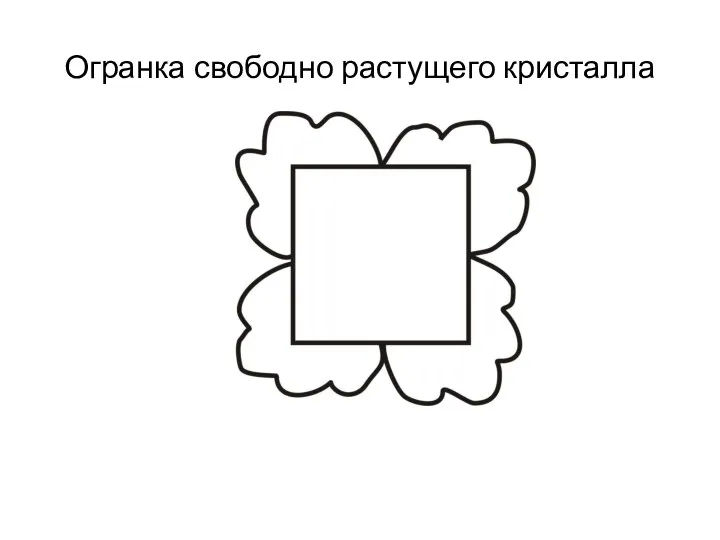
- 24. Огранка свободно растущего кристалла
- 25. Огранка свободно растущего кристалла
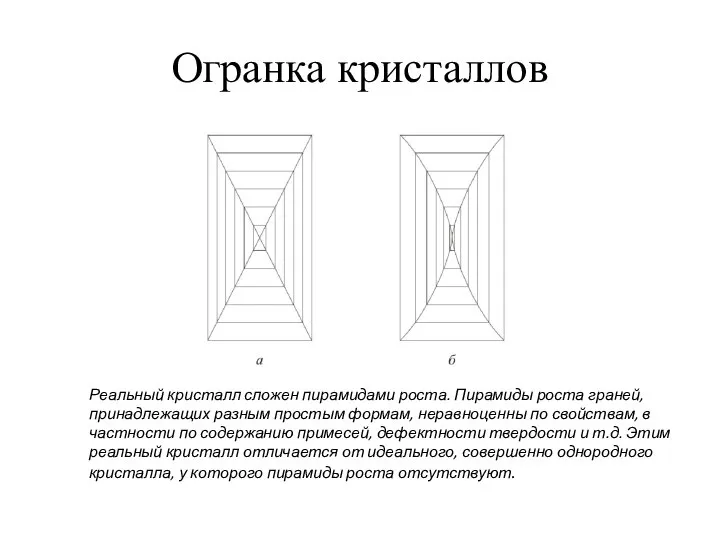
- 26. Огранка кристаллов Реальный кристалл сложен пирамидами роста. Пирамиды роста граней, принадлежащих разным простым формам, неравноценны по
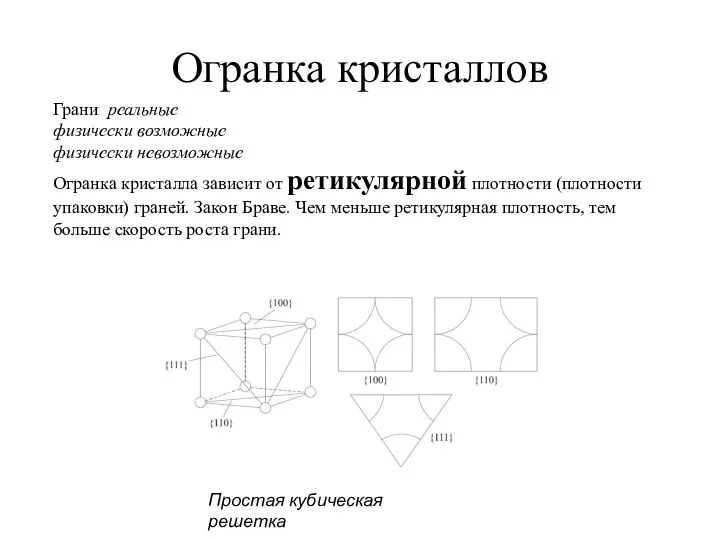
- 27. Огранка кристаллов Грани реальные физически возможные физически невозможные Огранка кристалла зависит от ретикулярной плотности (плотности упаковки)
- 28. Огранка кристаллов Объемноцентрированая решетка. Максимальная ретикулярная плотность для грани [110]
- 29. Огранка кристаллов Гранецентрированная решетка . Максимальная ретикулярная плотность для грани [110]
- 30. Огранка кристаллов Форм роста много Равновесная форма кристалла одна . Образована плотноупакованным гранями Пример. Алмаз.Равновесная форма
- 31. Огранка кристаллов Принцип Гиббса-Вульфа- Кюри Принцип Гиббса-Вульфа-Кюри. Равновесная форма кристалла соответствует минимуму свободной объемной и поверхностной
- 32. Теорема Вульфа σi/hi = const В равновесном кристалле расстояния от центра кристалла до граней пропорциональны их
- 33. Метод Шубникова определения равновесной формы кристалла С медленно растущих граней, принадлежащих равновесной, форме, при растворении удаляется
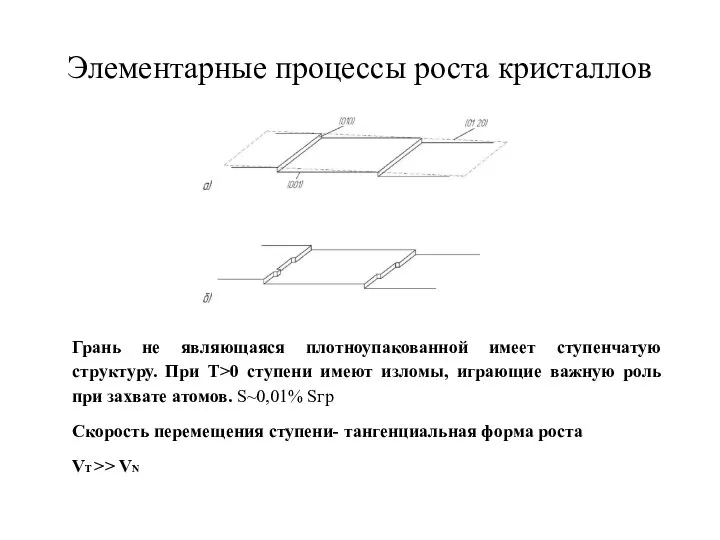
- 34. Элементарные процессы роста кристаллов Грань не являющаяся плотноупакованной имеет ступенчатую структуру. При T>0 ступени имеют изломы,
- 35. Рост шероховатых граней
- 36. Элементарные процессы роста кристаллов F- гладкие грани K,S – шероховатые грани Скорость роста для шероховатых граней
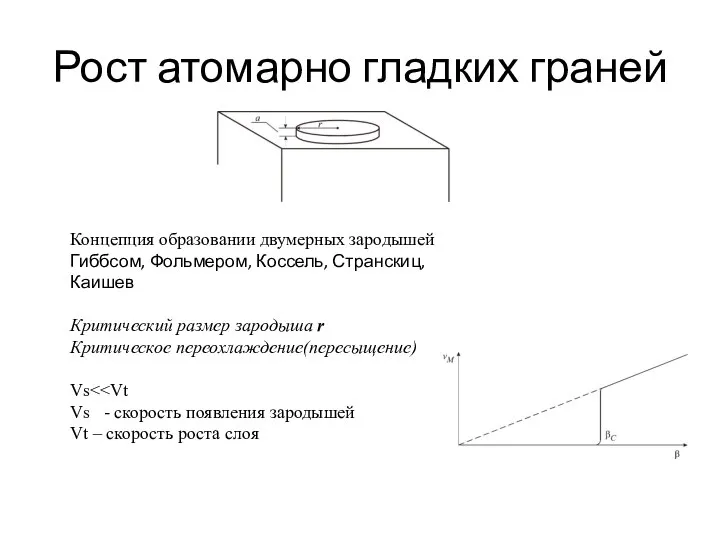
- 37. Рост атомарно гладких граней Концепция образовании двумерных зародышей Гиббсом, Фольмером, Коссель, Странскиц, Каишев Критический размер зародыша
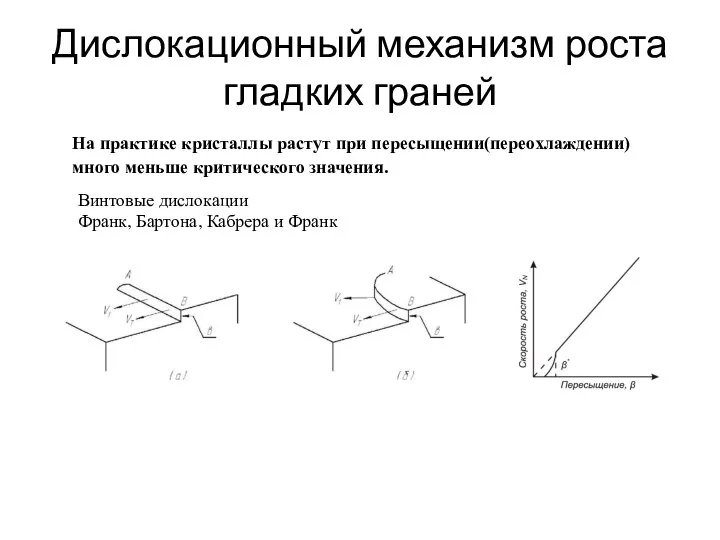
- 38. Дислокационный механизм роста гладких граней Винтовые дислокации Франк, Бартона, Кабрера и Франк На практике кристаллы растут
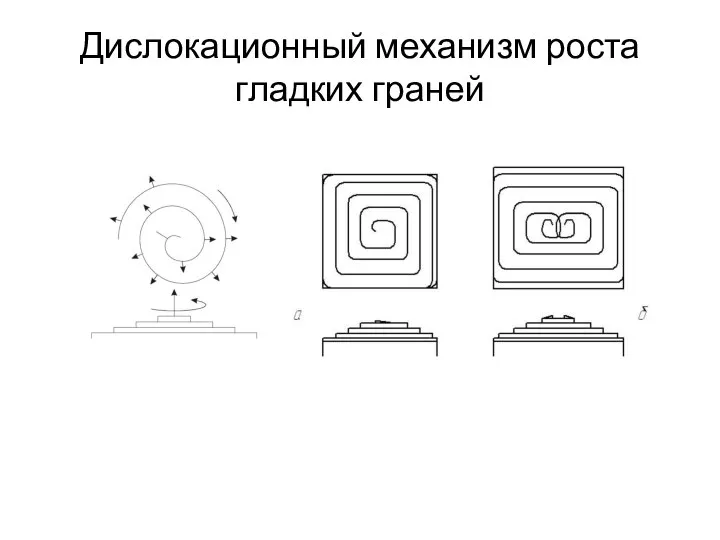
- 39. Дислокационный механизм роста гладких граней
- 40. Установка «Гранат-2», компоненты теплового узла и Компоненты теплового узла: 1 — нагревательный элемент, 2 — блок
- 41. Монокристалл алюмо-иттриевого граната, легированного ванадием
- 42. Срезы були алюмоиттриевого граната с ванадием а,б,в — срез кристалла (просветленная пластина), г — готовое изделие
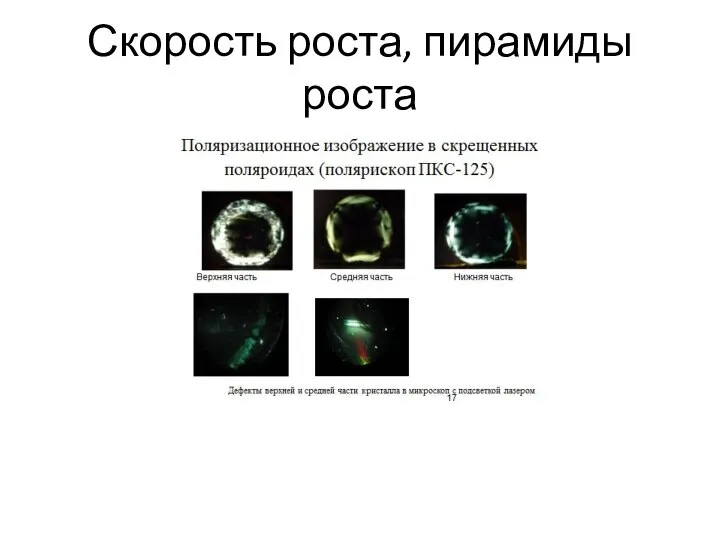
- 43. Скорость роста, пирамиды роста
- 44. Свойства кристаллов соединений Al2O3-Y2O3
- 46. Скачать презентацию












![Огранка кристаллов Объемноцентрированая решетка. Максимальная ретикулярная плотность для грани [110]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405746/slide-27.jpg)
![Огранка кристаллов Гранецентрированная решетка . Максимальная ретикулярная плотность для грани [110]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405746/slide-28.jpg)










 принцип работы, применение в технике и быту
принцип работы, применение в технике и быту Тест: Азот
Тест: Азот Общая характеристика элементов VII А группы
Общая характеристика элементов VII А группы Кристаллические и аморфные тела
Кристаллические и аморфные тела Презентация по Химии "Простые вещества – металлы" - скачать смотреть бесплатно
Презентация по Химии "Простые вещества – металлы" - скачать смотреть бесплатно EdExcel Unit C2 – Discovering Chemistry
EdExcel Unit C2 – Discovering Chemistry Химический состав и пищевая ценность кофе
Химический состав и пищевая ценность кофе История развития биохимического знания и биохимии как науки
История развития биохимического знания и биохимии как науки Кинетика химических реакций
Кинетика химических реакций Получение наночастиц в сверхкритическом флюиде
Получение наночастиц в сверхкритическом флюиде Небелковые азотистые компаненты крови
Небелковые азотистые компаненты крови Неделя специальности "Аналитический контроль качества химических соединений"
Неделя специальности "Аналитический контроль качества химических соединений" Классификация неорганических веществ
Классификация неорганических веществ Презентация Изомерия
Презентация Изомерия 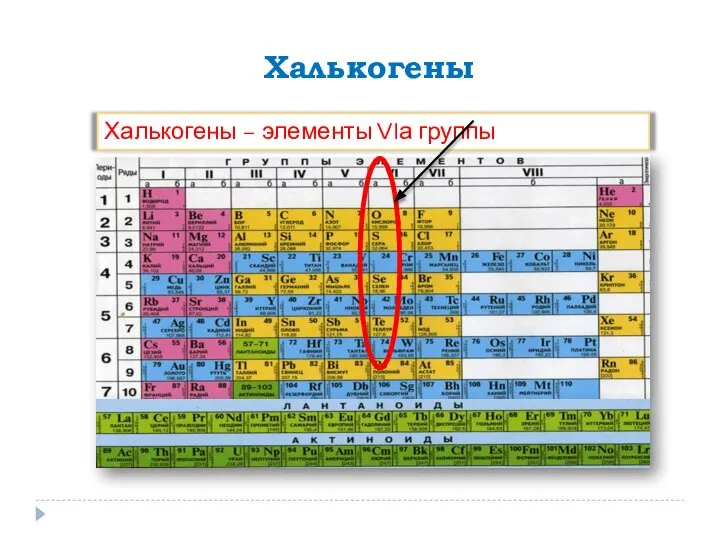 Кислород. Сера
Кислород. Сера Презентация по Химии "Дефицит пресной воды. Миф или реальность?" - скачать смотреть
Презентация по Химии "Дефицит пресной воды. Миф или реальность?" - скачать смотреть 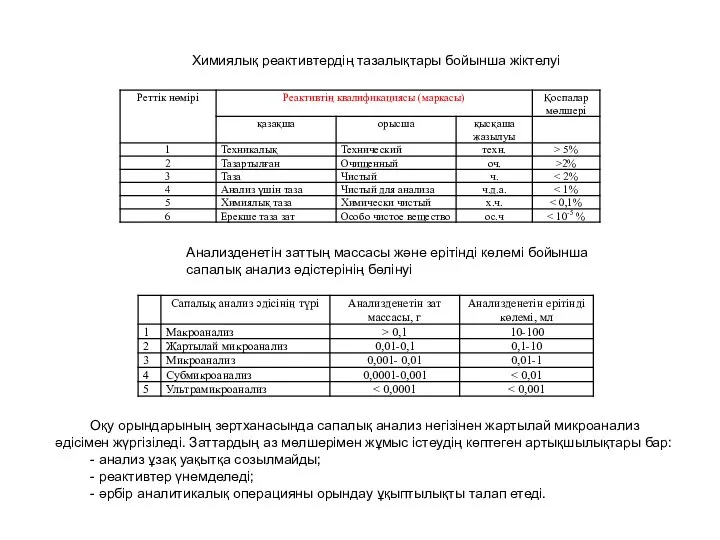 Химиялық реактивтердің тазалықтары бойынша жіктелуі
Химиялық реактивтердің тазалықтары бойынша жіктелуі КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен липид
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен липид Пластичний обмін
Пластичний обмін  Информационно – исследовательский проект Кристаллы вокруг нас.
Информационно – исследовательский проект Кристаллы вокруг нас. Значение минеральных веществ и витаминов в питании человека
Значение минеральных веществ и витаминов в питании человека КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМ
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМ Углерод
Углерод Презентация по химии Оксиды
Презентация по химии Оксиды  Среднее (полное) общее образование. Химия. Изучение химии на базовом уровне
Среднее (полное) общее образование. Химия. Изучение химии на базовом уровне Ртуть и её соединения
Ртуть и её соединения Презентация по Химии "Производство стекла" - скачать смотреть
Презентация по Химии "Производство стекла" - скачать смотреть  Протеины: плюсы и минусы
Протеины: плюсы и минусы