Содержание
- 2. ЦЕЛИ: Дать общую характеристику элементов 5 группы главной подгруппы. изучить свойства азота и область его применения
- 3. Почему назвали “азот”? Соединения азота - селитра, азотная кислота, аммиак - были известны задолго до получения
- 4. Нахождение в природе. Азот – один из распространенных элементов на Земле. - в атмосфере - 4•1051
- 5. Физические свойства азота Азот немного легче воздуха; плотность 1,2506 кг/м3 (при н.у.), tпл.= - 209,8оС, tкип.=
- 6. Химические свойства азота С Ме: N2+6Li (об.усл.) —> 2Li3N N2+3Mg (об.усл.) —> Mg3N2 N2+2Al —> 2AlN
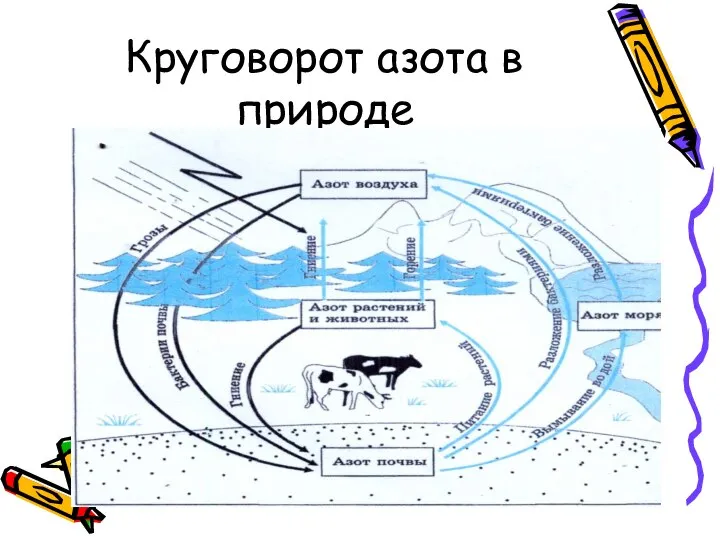
- 7. Круговорот азота в природе
- 8. Применение азота: создание инертных сред в металлургии; синтез аммиака и азотной кислоты; производство минеральных удобрений; производство
- 9. Азот – друг или враг? Азот – “безжизненный”. Азот – главный элемент жизни. Что можно сказать
- 10. Определите коэффициенты в уравнениях реакций методом электронного баланса: а) NH3+ O2→NO+H2O б) NH3+ O2→N2+H2O Рассчитайте объем
- 12. Скачать презентацию








 Презентация к уроку химии по теме «Спирты» 10 класс. УМК Габриеляна О.С. Базовый уровень
Презентация к уроку химии по теме «Спирты» 10 класс. УМК Габриеляна О.С. Базовый уровень Исследовательская работа Химические средства в быту
Исследовательская работа Химические средства в быту Творческий проект учащихся 7 класса Совхозной СОШ . Руководитель: учитель технологии Фотеева О.И.
Творческий проект учащихся 7 класса Совхозной СОШ . Руководитель: учитель технологии Фотеева О.И.  Исследовательская работа по химии “Минеральные краски’’
Исследовательская работа по химии “Минеральные краски’’ Методы окислительно-восстановительного титрования (Редоксиметрия)
Методы окислительно-восстановительного титрования (Редоксиметрия) Металлорудные ресурсы
Металлорудные ресурсы Химико-технологические процессы современных производств
Химико-технологические процессы современных производств Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства.
Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства.  Презентация по Химии "«Сахароза»" - скачать смотреть бесплатно
Презентация по Химии "«Сахароза»" - скачать смотреть бесплатно харчові Добавки
харчові Добавки  Классификация, виды бензинов и их свойства
Классификация, виды бензинов и их свойства Пожарная безопасность в жилом доме
Пожарная безопасность в жилом доме  Омега 3
Омега 3 Радиационная стойкость материалов
Радиационная стойкость материалов Важнейшие классы неорганических веществ, их свойства и способы получения
Важнейшие классы неорганических веществ, их свойства и способы получения Каталитические процессы нефтепереработки
Каталитические процессы нефтепереработки N-(2-амино-3,5-дибромбензил)-N-метилциклогексанамина гидрохлорид
N-(2-амино-3,5-дибромбензил)-N-метилциклогексанамина гидрохлорид Состав краски
Состав краски Презентация по Химии "Природня родина: Лужноземельні." - скачать смотреть бесплатно
Презентация по Химии "Природня родина: Лужноземельні." - скачать смотреть бесплатно Важнейшие соединения щелочных металлов, их свойства и применение.
Важнейшие соединения щелочных металлов, их свойства и применение. Основні принципи мас-спектрометрії
Основні принципи мас-спектрометрії Полимерные реагенты в бурении
Полимерные реагенты в бурении Водород, нахождение в природе. Получение водорода и его физические свойства
Водород, нахождение в природе. Получение водорода и его физические свойства Основні методи синтезу та стабілізації наносистем
Основні методи синтезу та стабілізації наносистем Factors affecting the rate of chemical reaction
Factors affecting the rate of chemical reaction Фосфориты. Добыча фосфоритов
Фосфориты. Добыча фосфоритов Физико-химическая и механическая миграция
Физико-химическая и механическая миграция Растворы. Первичные понятия
Растворы. Первичные понятия