Содержание
- 2. Азот и природа Большая часть азота находится в природе в свободном состоянии. Свободный азот, как известно,
- 3. Химические свойства азота Из-за наличия прочной тройной связи молекулярный азот малоактивен, а соединения азота термически малоустойчивы
- 4. Взаимодействие азота с металлами При обычных условиях молекулярный азот реагирует лишь с некоторыми сильными восстановителями, например,
- 5. Физические свойства азота При обычных условиях азот – бесцветный газ, без вкуса и запаха, абсолютно безвреден,
- 7. Скачать презентацию
Слайд 2
Азот и природа
Большая часть азота находится в природе в свободном
Азот и природа
Большая часть азота находится в природе в свободном
состоянии. Свободный азот, как известно, является главной составной частью воздуха, который содержит около 78% азота по объему. Неорганические соединения азота не встречаются в природе в больших количествах, если не считать натриевую селитру NaNO3, образующую мощные пласты на побережье Тихого океана в Чили. Почва содержит незначительные количества азота, преимущественно в виде солей азотной кислоты. Но в виде сложных органических соединений — белковых веществ — азот входит в состав тела каждого растения и животного. Из белковых веществ построены самые важные части клеток — протоплазма и ядро. Изумительные превращения, которым подвергаются белковые вещества в клетках растений и животных, составляют основу всех жизненных процессов. Без белка нет жизни, а так как азот является обязательной составной частью белка, то понятно, какую важную роль играет этот элемент в природе.
Слайд 3
Химические свойства азота
Из-за наличия прочной тройной связи молекулярный азот малоактивен, а
Химические свойства азота
Из-за наличия прочной тройной связи молекулярный азот малоактивен, а
соединения азота термически малоустойчивы и относительно легко разлагаются при нагревании с образованием свободного азота.
Слайд 4
Взаимодействие азота с металлами
При обычных условиях молекулярный азот реагирует лишь с
Взаимодействие азота с металлами
При обычных условиях молекулярный азот реагирует лишь с
некоторыми сильными восстановителями, например, литием:
6Li + N2 = 2Li3N.
Для образования нитрида магния из простых веществ требуется нагревание до 300 °С:
3Mg + N2 = Mg3N2.
Нитриды активных металлов представляют собой ионные соединения, которые гидролизуются водой с образованием аммиака.
Взаимодействие с кислородом
Только под действием электрического разряда азот реагирует с кислородом:
O2 + N2 = 2NO.
Взаимодействие с водородом
Реакция с водородом протекает при температуре порядка 400 °С и давлении 200 атм в присутствии катализатора – металлического железа:
3H2 + N2 = 2NH3.
Взаимодействие с другими неметаллами
При высоких температурах реагирует с другими неметаллами, например, с бором:
2B + N2 = 2BN.
Азот непосредственно не взаимодействует с галогенами и серой, но галогениды и сульфиды могут быть получены косвенным путем. С водой, кислотами и щелочами азот не взаимодействует.
Слайд 5
Физические свойства азота
При обычных условиях азот – бесцветный газ, без вкуса
Физические свойства азота
При обычных условиях азот – бесцветный газ, без вкуса
и запаха, абсолютно безвреден, немного легче воздуха, мало растворим в воде. Температура плавления -210 °С, температура кипения -196 °С.
Газообразный азот состоит из двухатомных молекул. Между атомами в молекуле реализуется тройная связь, вследствие этого молекула азота чрезвычайно прочная, энергия химической связи составляет 945 кДж/моль. Даже при 3000 °С степень распада молекулы азота на атомы достигает всего 0,1 %.
Структура твердого азота построена из двухатомных молекул, связанных слабыми силами межмолекулярного взаимодействия.




 Презентация по Химии "Гидролиз солей" - скачать смотреть бесплатно
Презентация по Химии "Гидролиз солей" - скачать смотреть бесплатно Нуклеиновые кислоты
Нуклеиновые кислоты Химический состав молока
Химический состав молока Двойной электрический слой. Теория Гельмгольца
Двойной электрический слой. Теория Гельмгольца Обзор основных методов исследования супрамолекулярных объектов
Обзор основных методов исследования супрамолекулярных объектов Способы перегонки
Способы перегонки Сера. Свойства серы
Сера. Свойства серы Цирконий. Схема получения чистого циркония
Цирконий. Схема получения чистого циркония Виконали: Алексеенко О.В. Перегонцева А.А.
Виконали: Алексеенко О.В. Перегонцева А.А.  Фенолы. Классификация фенолов
Фенолы. Классификация фенолов Возведение наземных стальных резервуаров
Возведение наземных стальных резервуаров Хроматография. (Лекция 4)
Хроматография. (Лекция 4) Соединения алюминия
Соединения алюминия Диссоциация кислот, оснований и солей
Диссоциация кислот, оснований и солей Химия неметаллов
Химия неметаллов Конструкционные функциональные волокнистые композиты. Стеклопластики
Конструкционные функциональные волокнистые композиты. Стеклопластики Химические источники тока
Химические источники тока “ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман
“ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман  Соль – основа жизни
Соль – основа жизни Аэрозольдер, ұнтақтар, суспензиялар, эмульсиялар, көбіктер
Аэрозольдер, ұнтақтар, суспензиялар, эмульсиялар, көбіктер Синтетические моющие средства, порошки, омыление, выпадение в осадок мыла, жиров
Синтетические моющие средства, порошки, омыление, выпадение в осадок мыла, жиров Методика изучения современной теории строения органических веществ
Методика изучения современной теории строения органических веществ Химическая физика горения
Химическая физика горения Химия вопросы и ответы
Химия вопросы и ответы Презентация по Химии "Алюминий и его соединения" - скачать смотреть
Презентация по Химии "Алюминий и его соединения" - скачать смотреть  Степень окисления
Степень окисления Презентация Каучук Органическая химия 10 класс
Презентация Каучук Органическая химия 10 класс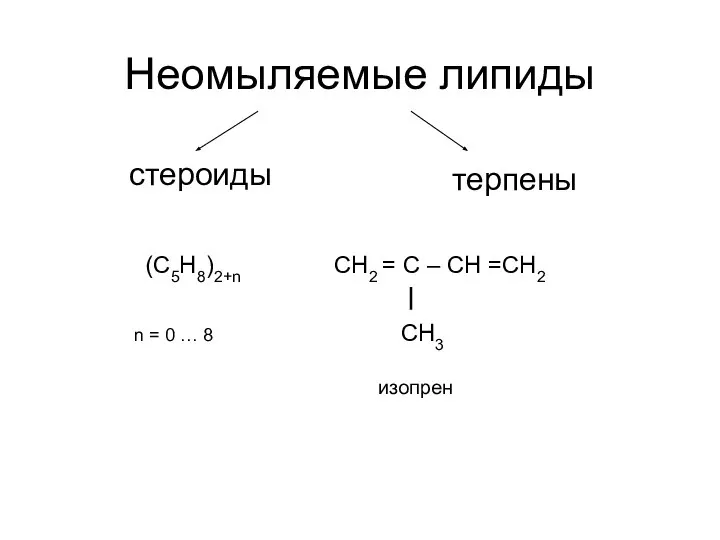 Неомыляемые липиды. Стероиды
Неомыляемые липиды. Стероиды