Содержание
- 2. Амины органические соединения, содержащие в своём составе аминогруппу –NH2 или замещённую аминогруппу (-NHR или NR2) производные
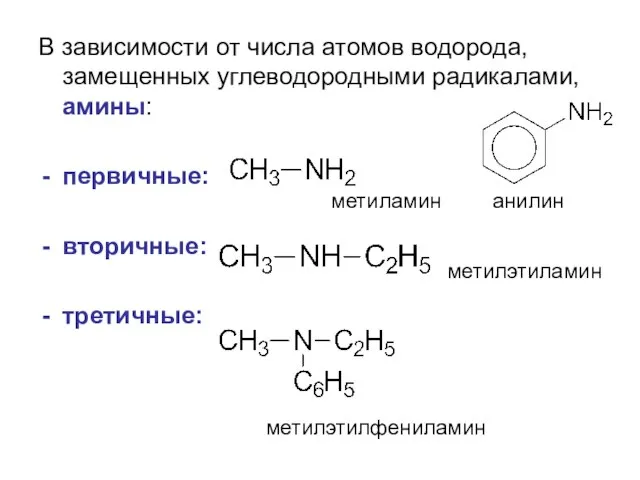
- 3. В зависимости от числа атомов водорода, замещенных углеводородными радикалами, амины: первичные: вторичные: третичные: метилэтиламин метиламин анилин
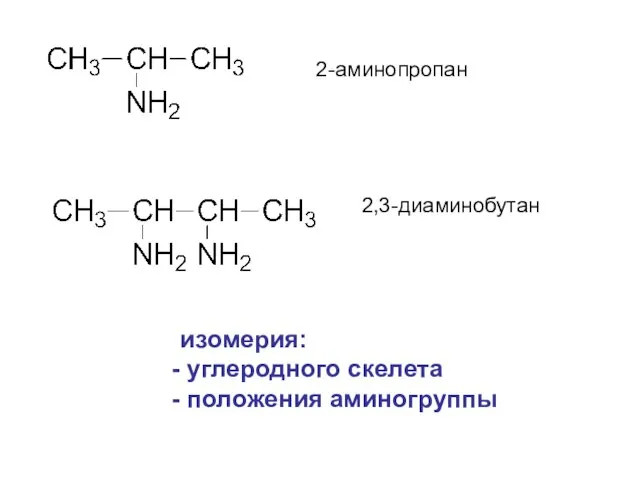
- 4. 2-аминопропан 2,3-диаминобутан изомерия: углеродного скелета положения аминогруппы
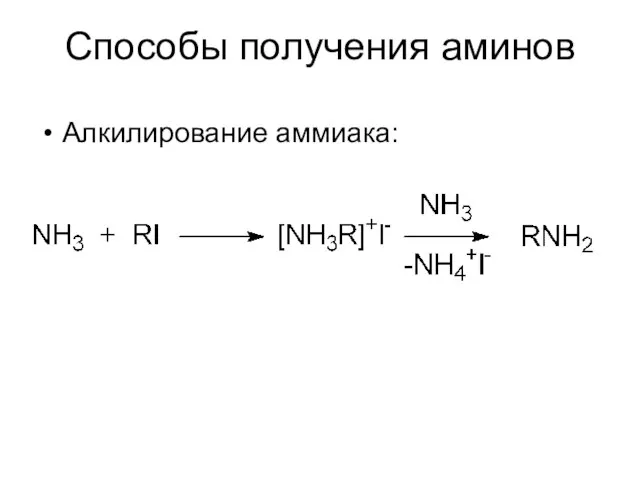
- 5. Способы получения аминов Алкилирование аммиака:
- 6. Восстановление азотсодержащих соединений:
- 7. Расщепление амидов кислот гипобромитами: Биогенные амины образуются путём декарбоксилирования α-аминокислот
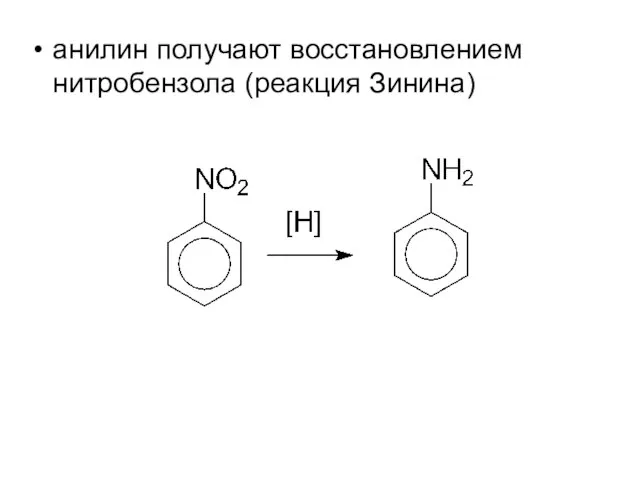
- 8. анилин получают восстановлением нитробензола (реакция Зинина)
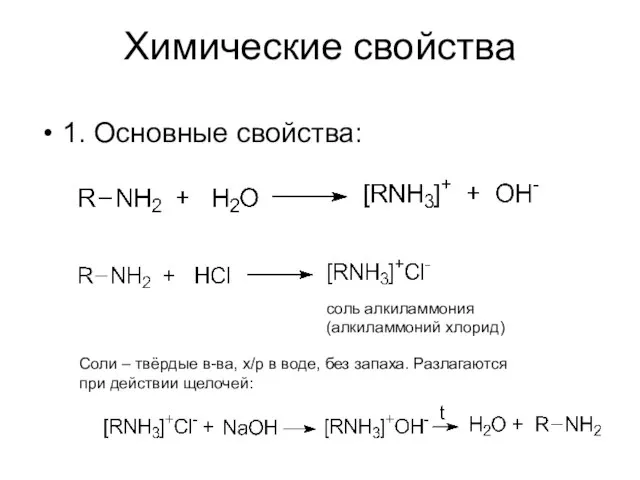
- 10. Химические свойства 1. Основные свойства: соль алкиламмония (алкиламмоний хлорид) Соли – твёрдые в-ва, х/р в воде,
- 11. Амины жирного ряда обладают более выраженными основными свойствами, чем аммиак. У аминов ароматического ряда основные свойства
- 12. 2. Взаимодействие с азотистой кислотой проходит с образованием различных продуктов для аминов разного строения. Это качественная
- 13. первичные алифатические:
- 14. вторичные алифатические: нитрозосоединение
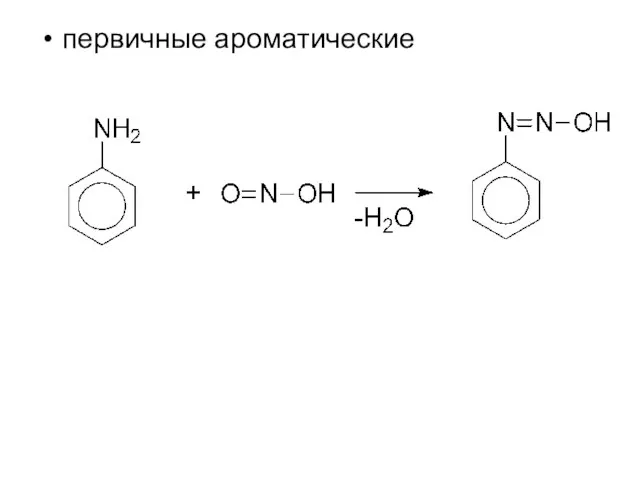
- 15. первичные ароматические
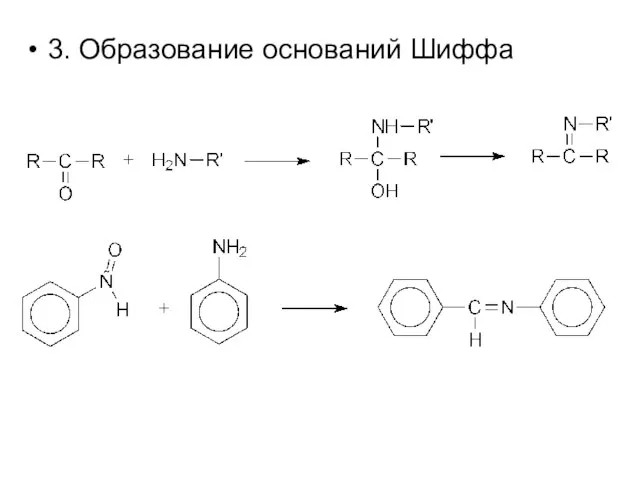
- 16. 3. Образование оснований Шиффа
- 17. 4. Ацилирование аминов (образование ацильных производных) Ацилирующие средства: карбоновые кислоты, галогенангидриды карбоновых кислот, ангидриды карбоновых кислот
- 18. 5. Реакции электрофильного замещения для ароматических аминов а) галогенирование
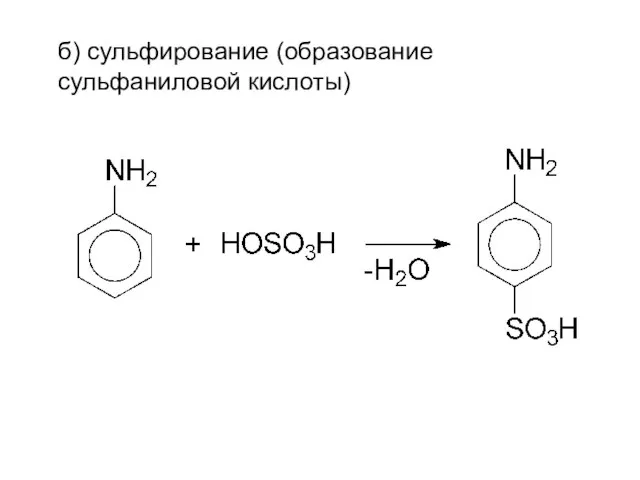
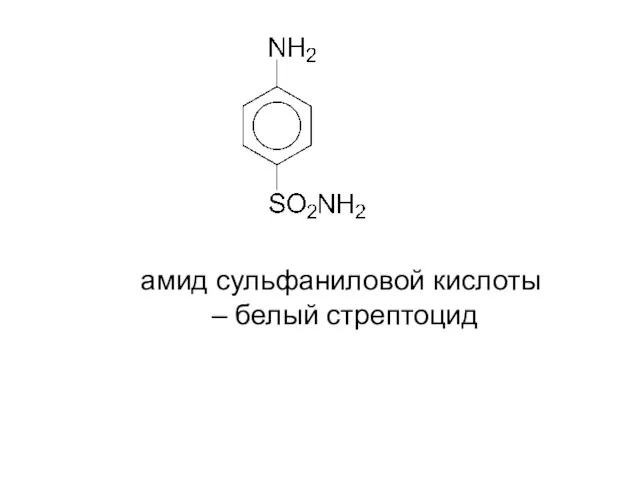
- 19. б) сульфирование (образование сульфаниловой кислоты)
- 20. амид сульфаниловой кислоты – белый стрептоцид
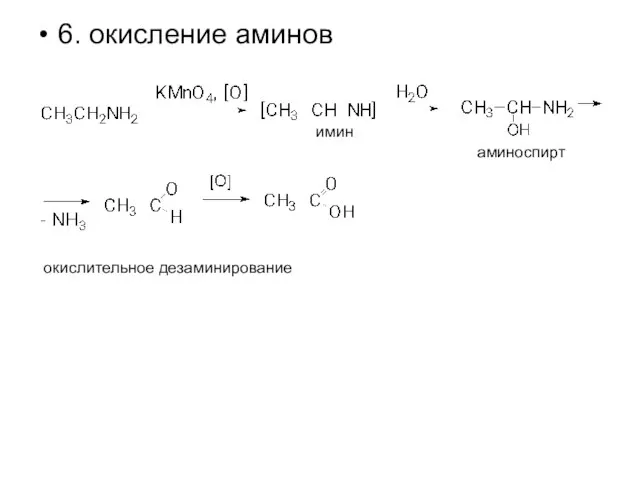
- 21. 6. окисление аминов окислительное дезаминирование имин аминоспирт
- 22. Аминоспирты коламин (этаноламин) холин (триметил-β-гидроксиэтилгидрат аммония):
- 23. Амиды кислот См. лекцию по карбоновым кислотам
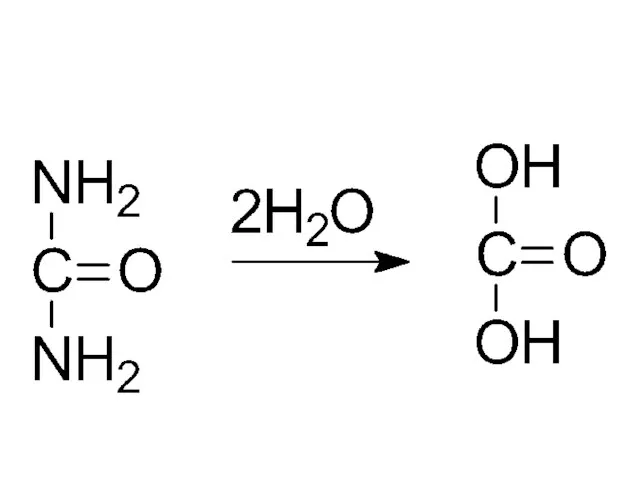
- 24. мочевина
- 31. Гетероциклические соединения. Гетероциклическими называют циклические органические соединения, в состав цикла которых, помимо атомов углерода, входят один
- 32. Классификационные признаки: природа гетероатома число гетероатомов размер цикла степень насыщенности
- 33. Пятичленные гетероциклы с одним гетероатомом Пиррол Фуран Тиофен
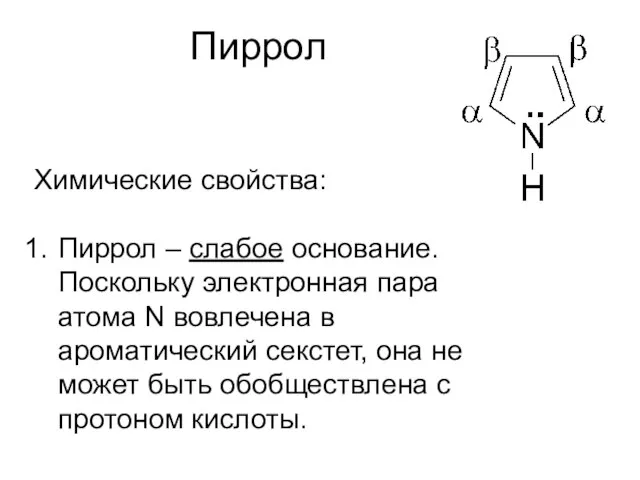
- 34. Пиррол Химические свойства: Пиррол – слабое основание. Поскольку электронная пара атома N вовлечена в ароматический секстет,
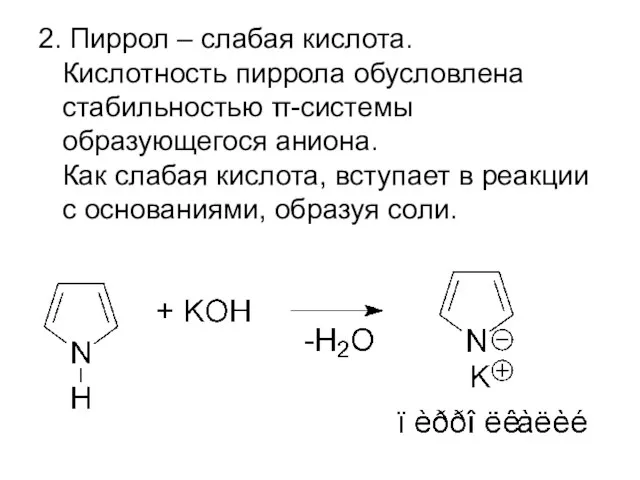
- 35. 2. Пиррол – слабая кислота. Кислотность пиррола обусловлена стабильностью π-системы образующегося аниона. Как слабая кислота, вступает
- 36. Соли разлагаются водой:
- 37. 3. Пиррол является ацидофобным соединением (не выдерживает присутствия кислот). В присутствии кислот осмоляется:
- 38. 4. Пиррол, являясь типично ароматическим соединением, вступает в реакции электрофильного замещения. Причём обладает высокой реакционной способностью.
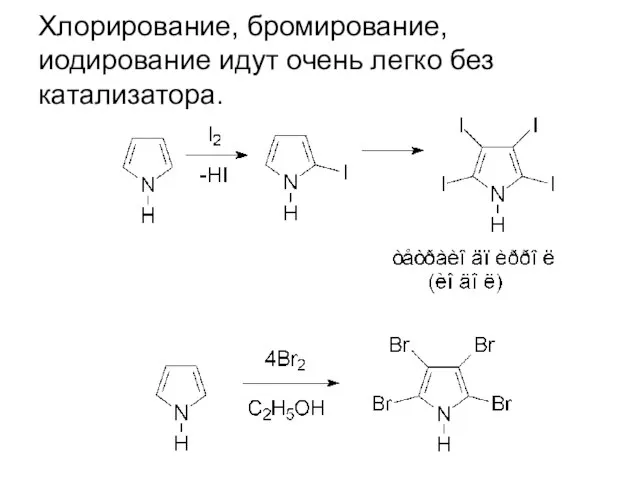
- 40. Хлорирование, бромирование, иодирование идут очень легко без катализатора.
- 41. 5. Восстановление Пирролидин – циклический вторичный амин – сильное основание. Его ядро входит в состав ряда
- 42. Тетрапиррольные соединения Порфин
- 43. Гем
- 44. Фуран ТГФ
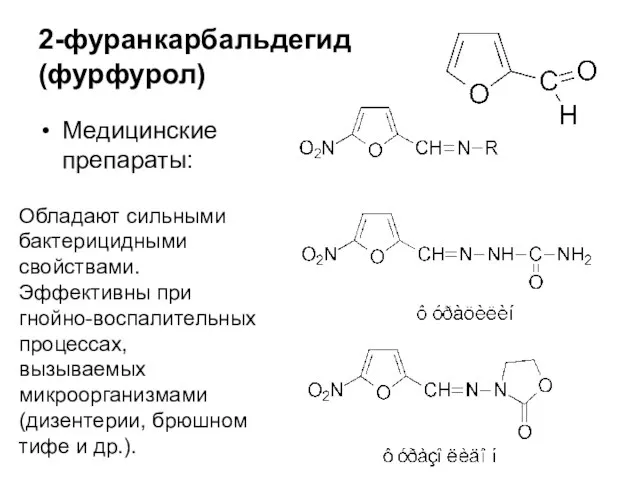
- 45. 2-фуранкарбальдегид (фурфурол) Медицинские препараты: Обладают сильными бактерицидными свойствами. Эффективны при гнойно-воспалительных процессах, вызываемых микроорганизмами (дизентерии, брюшном
- 46. От слова фуран происходит название циклической формы моносахаридов. Например: Рибоза – рибофураноза, Глюкоза – глюкофураноза.
- 47. Тиофен Производные тиофена входят в состав ихтиоловой мази (противовоспалительное, антисептическое, местное обезболивающее действие). Тетрагидротиофеновое кольцо входит
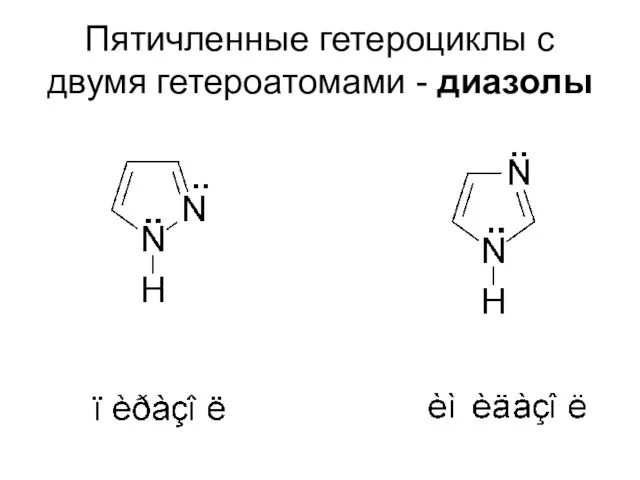
- 48. Пятичленные гетероциклы с двумя гетероатомами - диазолы
- 49. Основные свойства усиливаются в ряду: имидазол >пиразол >> пиррол
- 51. Медико-биологическое значение производных имидазола и пиразола
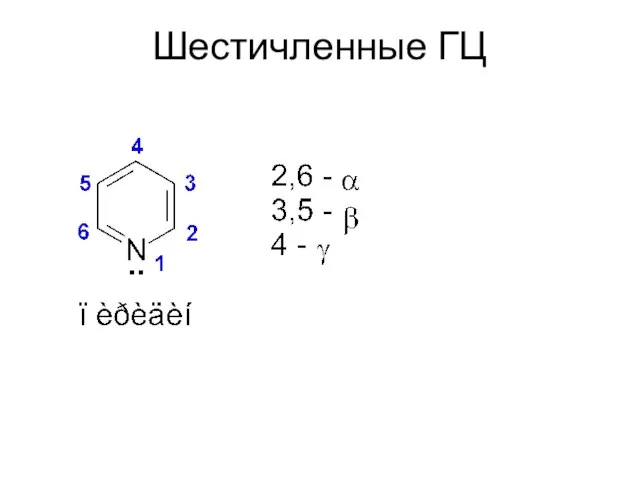
- 54. Шестичленные ГЦ
- 55. SE
- 56. Основные свойства пиридиний-катион
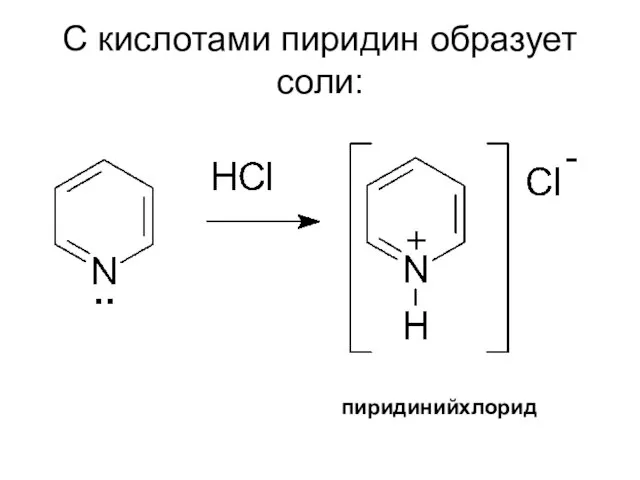
- 57. С кислотами пиридин образует соли: пиридинийхлорид
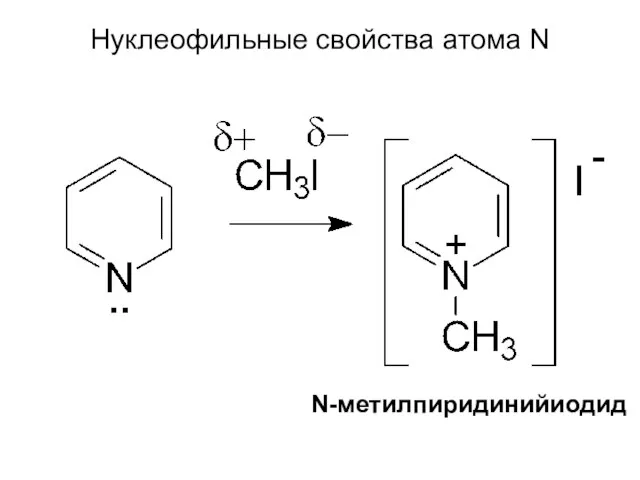
- 58. Нуклеофильные свойства атома N N-метилпиридинийиодид
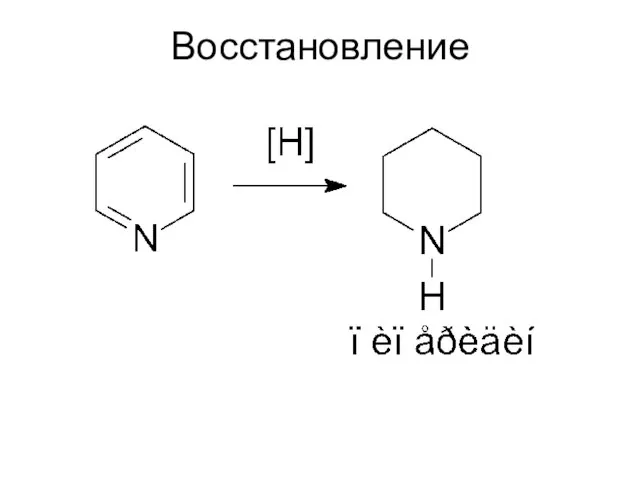
- 59. Восстановление
- 60. Некоторые формы витамина В6
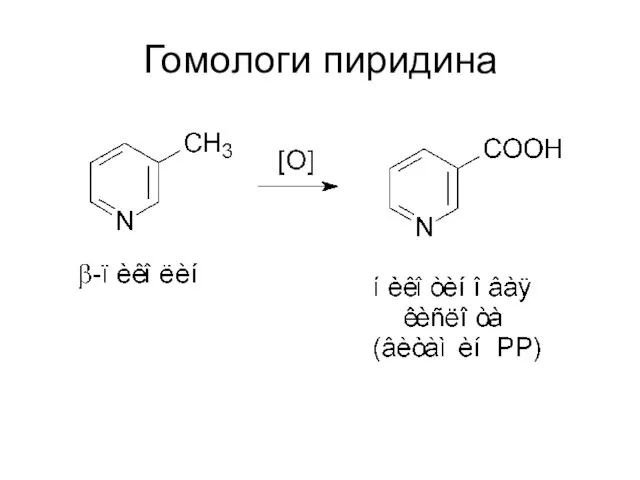
- 61. Гомологи пиридина
- 63. α-пиран α-пиран γ-пиран
- 64. Из строения молекулы видно, что пиран не обладает ароматическим характером. Пирановое кольцо лежит в основе циклических
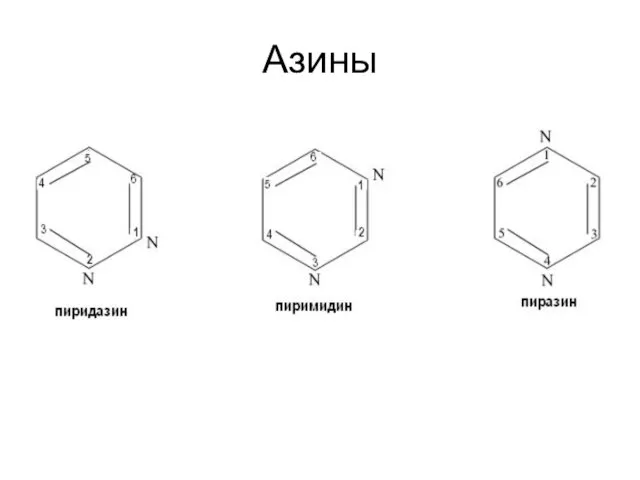
- 65. Азины
- 67. Барбитуровая к-та Барбитуровая к-та
- 68. ГЦ с конденсированными ядрами индол скатол
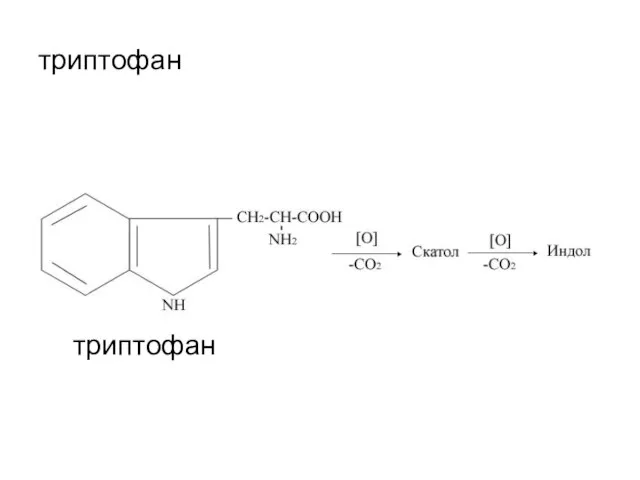
- 69. триптофан триптофан
- 71. Индол обладает слабыми основными свойствами:
- 73. Бензимидазол
- 74. Хинолин. Изохинолин.
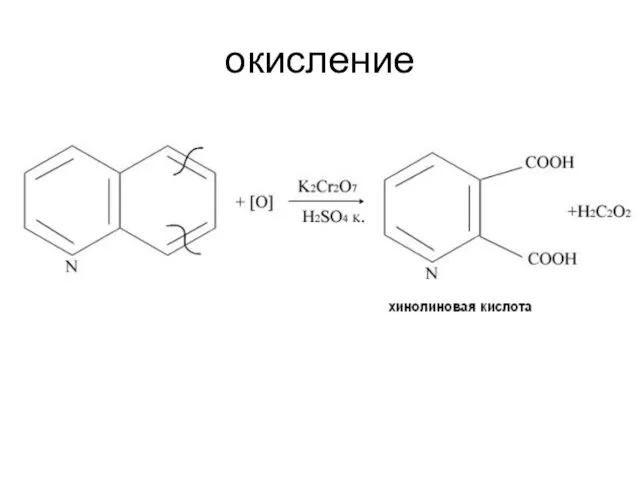
- 75. окисление
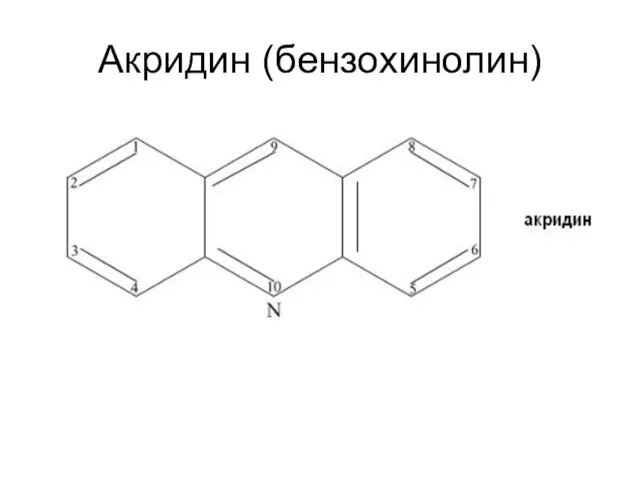
- 76. Акридин (бензохинолин)
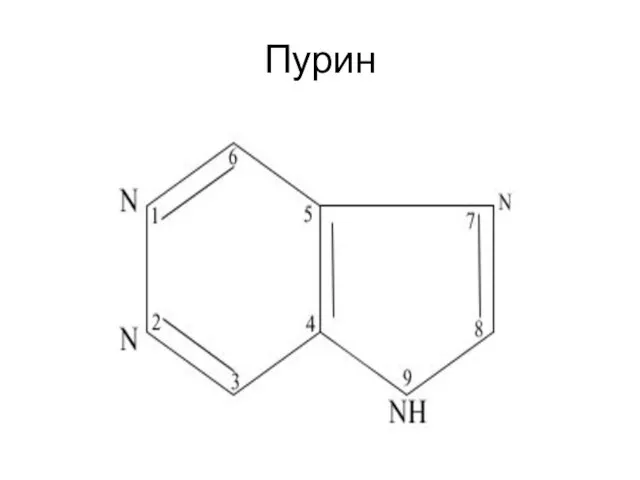
- 77. Пурин
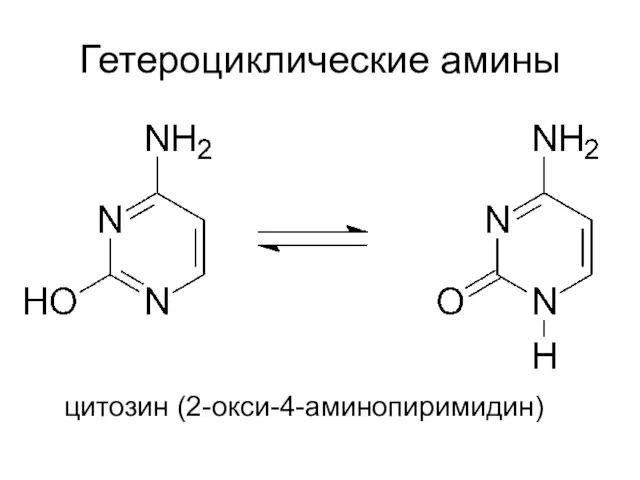
- 78. Гетероциклические амины цитозин (2-окси-4-аминопиримидин)
- 79. аденин (6-аминопурин) гуанин (2-амино-6-оксипурин)
- 81. Скачать презентацию



















































 Электролит және бейэлектролит ерітінділердің коллигативті қасие
Электролит және бейэлектролит ерітінділердің коллигативті қасие Топливный элемент
Топливный элемент Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії
Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії Получение меламина из карбамида
Получение меламина из карбамида Бензол и его свойства
Бензол и его свойства Новітні досягнення в хімії (9 клас)
Новітні досягнення в хімії (9 клас) Электронные конфигурации атомов
Электронные конфигурации атомов Степень окисления химических элементов
Степень окисления химических элементов Презентация на тему: Хром
Презентация на тему: Хром Растворы
Растворы Сравнение нормативов некоторых веществ
Сравнение нормативов некоторых веществ Презентация по Химии "Химический КВН" - скачать смотреть
Презентация по Химии "Химический КВН" - скачать смотреть  Характеристика 1-й аналитической группы анионов
Характеристика 1-й аналитической группы анионов Строение и свойства циклоалканов
Строение и свойства циклоалканов Коррозия металлов (9 класс)
Коррозия металлов (9 класс) Тема: “Обобщение сведений об основных классах неорганических соединений”.
Тема: “Обобщение сведений об основных классах неорганических соединений”. Проблемно-исследовательские технологии обучения химии
Проблемно-исследовательские технологии обучения химии Картофельное пюре быстрого приготовления
Картофельное пюре быстрого приготовления Кислоты 9-10 класс - Презентация_
Кислоты 9-10 класс - Презентация_ Лужні метали. Фізичні та хімічні властивості простих речовин. Біологічна роль елементів.
Лужні метали. Фізичні та хімічні властивості простих речовин. Біологічна роль елементів.  Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД)
Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД) Презентация по Химии "Спирты. Польза и вред" - скачать смотреть
Презентация по Химии "Спирты. Польза и вред" - скачать смотреть  Металдар арасындағы беттік керіліс
Металдар арасындағы беттік керіліс Органічні розчинники
Органічні розчинники Обезвреживающая функция печени
Обезвреживающая функция печени Биологическое оружие Преподаватель-организатор ОБЖ Белобородов М.М.
Биологическое оружие Преподаватель-организатор ОБЖ Белобородов М.М.  Микроскопическая симметрия. Пространственные решетки. Решетки Бравэ
Микроскопическая симметрия. Пространственные решетки. Решетки Бравэ Островные силикаты (Орто)
Островные силикаты (Орто)