Содержание
- 3. Биологическое окисление – это совокупность реакций окисления, протекающих в живых системах. Первые представления о биологическом окислении
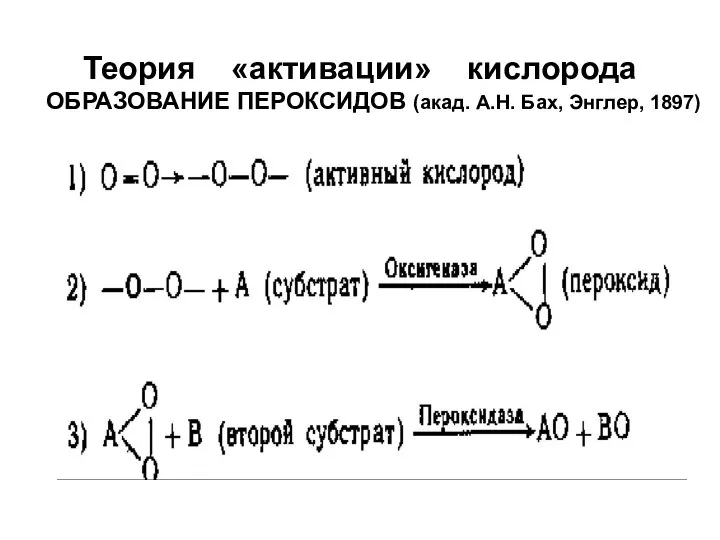
- 4. Теория «активации» кислорода ОБРАЗОВАНИЕ ПЕРОКСИДОВ (акад. А.Н. Бах, Энглер, 1897)
- 5. Варбург Активирование кислорода – ключевой процесс в тканевом дыхании 1912г – цитохромоксидаза Бателли, Штерн – дегидрогеназы
- 6. Теория активирования водорода (акад. В.И. Палладин, 1912) А*Н2 (субстрат) ½ О2 Н2О ДГ Кейлин, 1933 –
- 7. СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ Биологическое окисление - процесс переноса электронов. Если акцептором электронов является кислород,
- 8. Биологическое окисление Процесс транспорта электронов Процесс многоступенчатый Процесс полиферментативный Конечный продукт тканевого дыхания –Н2О Энергия выделяется
- 9. Биологическое окисление многоступенчатый процесс транспорта электронов (на начальных этапах и протонов) осуществляемый комплексом ферментов, сопряженный с
- 10. ФЕРМЕНТЫ И КОФЕРМЕНТЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ Биологическое окисление начинается с ДЕГИДРИРОВАНИЯ
- 11. Этап осуществляется с помощью: НАД – зависимые дегидрогеназы ФАД – зависимые дегидрогеназы Это первичные акцепторы водорода
- 12. В НАД и НАДФ рабочей частью является витамин РР - НИКОТИНАМИД. НАД + 2Н + 2е
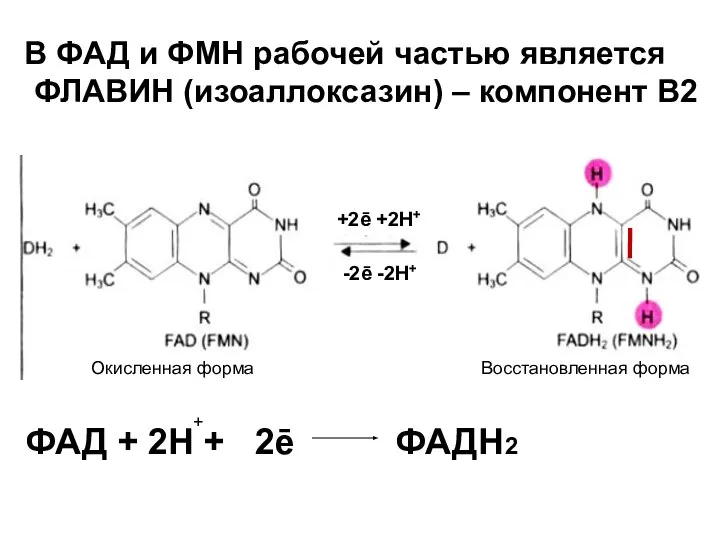
- 13. В ФАД и ФМН рабочей частью является ФЛАВИН (изоаллоксазин) – компонент В2 ФАД + 2Н +
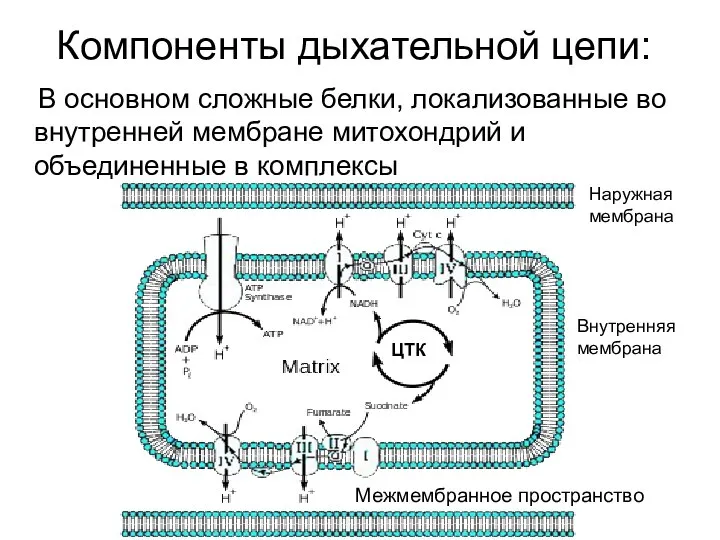
- 14. Компоненты дыхательной цепи: В основном сложные белки, локализованные во внутренней мембране митохондрий и объединенные в комплексы
- 15. Комплекс ферментов переноса электронов и протонов от субстрата к кислороду называется ЭЛЕКТРОНТРАНСПОРТНАЯ ЦЕПЬ (ЭТЦ), или ЦЕПЬ
- 16. Компоненты дыхательной цепи: В основном сложные белки, локализованные во внутренней мембране митохондрий и объединенные в комплексы
- 17. КОМПОНЕНТЫ ДЫХАТЕЛЬНОЙ ЦЕПИ: Комплекс I (НАДН-дегидрогеназа) Комплекс II (СДГ) Убихинон (кофермент Q) Комплекс III (цитохромы b,
- 18. Комплекс I (НАДН-дегидрогеназа) Флавинзависимый фермент (кофермент ФМН) Единственный Субстрат – кофермент НАДН2 Содержит железо-серные белки Донор
- 19. Комплекс II (СДГ) Флавинзависимый фермент (кофермент ФАД) Донор протонов и электронов для убихинона
- 20. Схема строения сукцинатдегидрогеназы Кольман Я., Рём К. Г. Наглядная биохимия. — 4-е изд.. — М.: БИНОМ.
- 21. Убихинон (кофермент Q) Quinone – хинон Ubiquitos – вездесущий У млекопитающих 10 звеньев изопрена (коэнзим Q10)
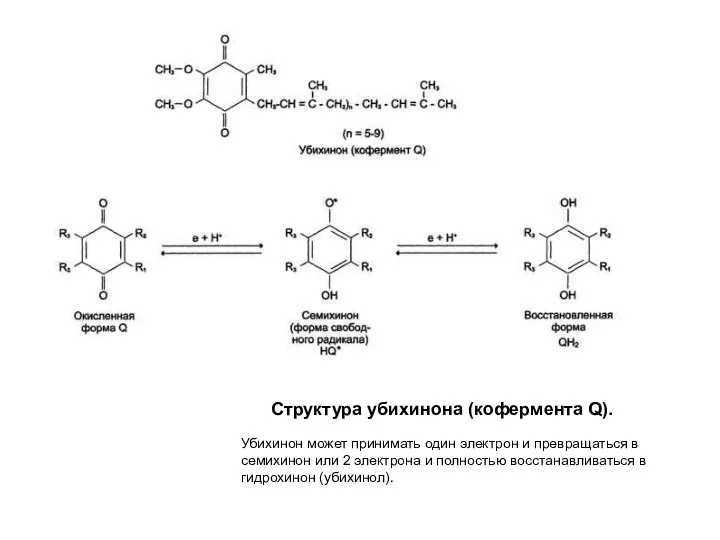
- 22. Структура убихинона (кофермента Q). Убихинон может принимать один электрон и превращаться в семихинон или 2 электрона
- 23. Цитохромы – сложные белки, небелковая часть – гем Каждый цитохром транспортирует только 1 электрон Главную роль
- 24. Комплекс III (коэнзим Q – дегидрогеназа) В составе цитохромы b, с1 Акцептор электронов от коэнзима Q
- 25. Цитохром с Не объединяется в комплекс Акцептор электронов от комплекса III Донор электронов для комплекса IV
- 26. Комплекс IV (цитохромоксидаза) Содержит цитохромы а, а3, ионы меди Акцептор электронов от цитохрома с Донор электронов
- 28. Полная ЭТЦ - взаимодействие субстрата с НАД. Укороченная ЭТЦ - взаимодействие субстрата с ФАД Порядок компонентов
- 29. Окислительно-восстановительный потенциал *Выражается в вольтах; *Чем отрицательнее E0´, тем меньше сродство к электронам; *Связан с изменением
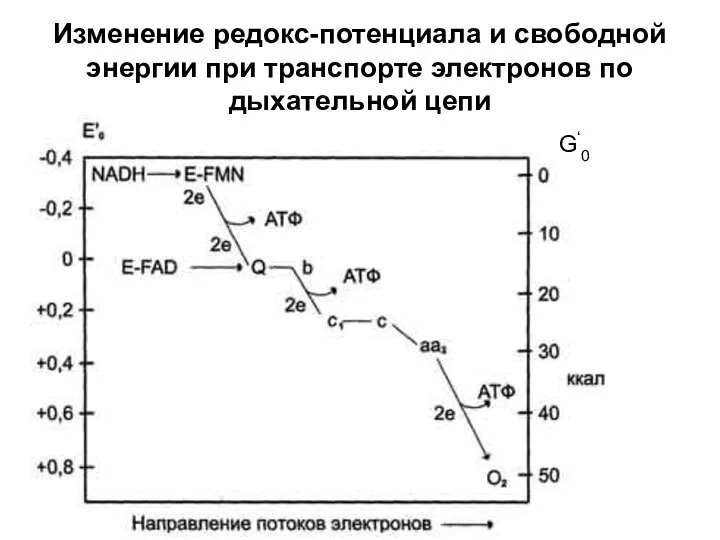
- 30. Изменение редокс-потенциала и свободной энергии при транспорте электронов по дыхательной цепи G‘0
- 31. ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ. Процесс образования АТФ из АДФ и Н3РО4 за счёт энергии переноса электронов в дыхательной
- 32. В дыхательной цепи выделяются 3 пункта, где может образоваться АТФ: 1.НАД→ KоQ 2.ЦИТ. b → ЦИТ.
- 33. МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ Теория ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ Питер МИТЧЕЛЛ, 1961
- 34. Основные положения теории: 1.Мембрана МИТОХОНДРИЙ непроницаема для протонов. 2.Образуется электрохимический потенциал в процессе транспорта электронов и
- 35. Процесс транспорта электронов происходит во внутренней мембране. Первые реакции окисления происходят в матриксе. Протоны переносятся в
- 37. Во время дыхания создаётся ЭЛЕКТРО-ХИМИЧЕСКИЙ потенциал: концентрационный (протонный) разности потенциалов (электрический)
- 38. Электрический и концентрационный потенциал составляют ПРОТОНДВИЖУЩУЮ силу, которая перемещает протоны обратно в матрикс митохондрий. Через протонные
- 39. УСЛОВИЯ ОБРАЗОВАНИЯ АТФ: 1. Целостность мембраны - непроницаемость её для протонов. 2. Наличие специальных каналов. 3.
- 40. СОПРЯЖЕНИЕ ОКИСЛЕНИЯ И ФОСФОРИЛИРОВАНИЯ. разобщение ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ (свободное окисление) окисление идёт, а ФОСФОРИЛИРОВАНИЯ нет, вся энергия
- 41. Разобщение ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ (свободное окисление) окисление идёт, а ФОСФОРИЛИРОВАНИЯ нет, вся энергия выделяется в виде тепла.
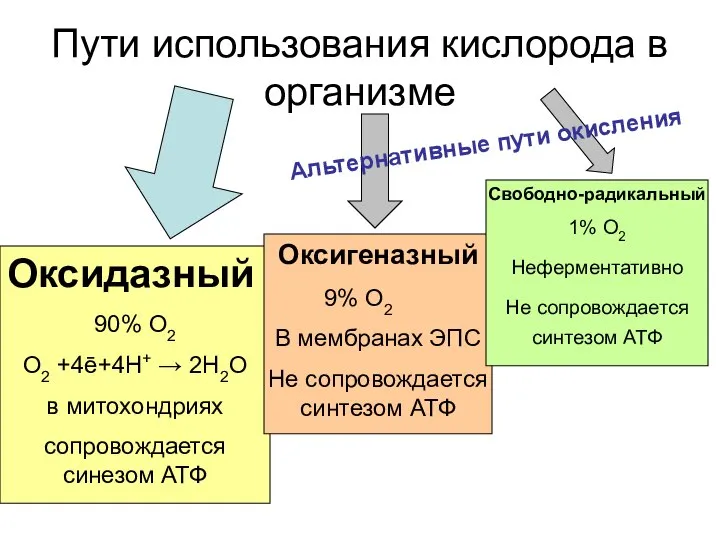
- 42. Пути использования кислорода в организме Оксидазный 90% О2 О2 +4ē+4Н+ → 2Н2О в митохондриях сопровождается синезом
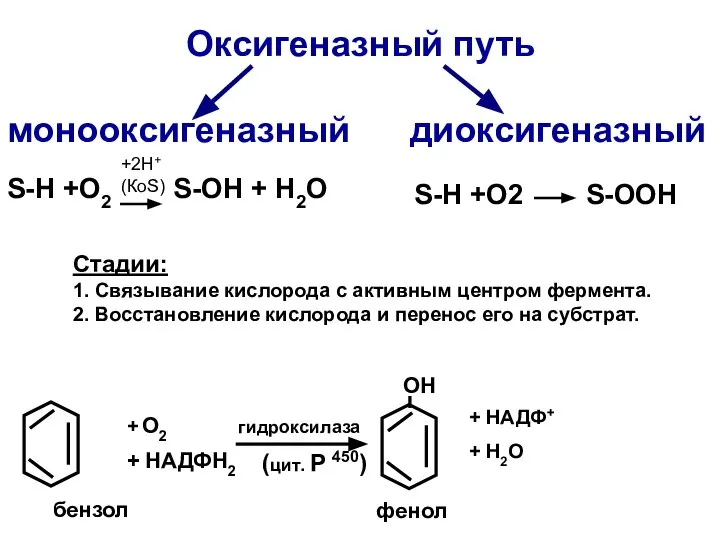
- 43. Оксигеназный путь монооксигеназный диоксигеназный S-Н +O2 S-OH + H2O S-Н +O2 S-OOH бензол + О2 +
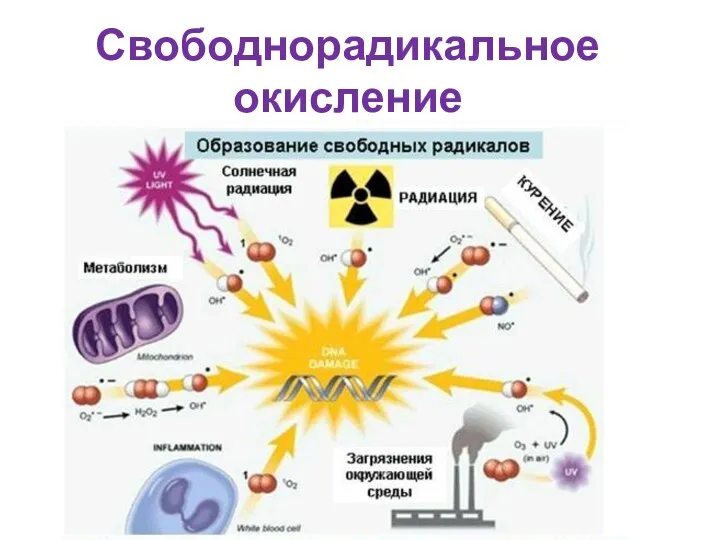
- 44. Свободнорадикальное окисление
- 45. Свободный радикал – молекула или её часть, имеющая неспаренный электрон на внешней электронной орбитали (возбужденное состояние
- 46. Источники свободных радикалов микросомальное окисление, окисление аминокислот, нуклеотидов оксидазами, неполное восстановление кислорода в дыхательной цепи, воздействие
- 47. Свойства свободных радикалов Являются нестабильными, короткоживущими молекулами Обладают очень высокой реакционной способностью Взаимодействуют с большинством органических
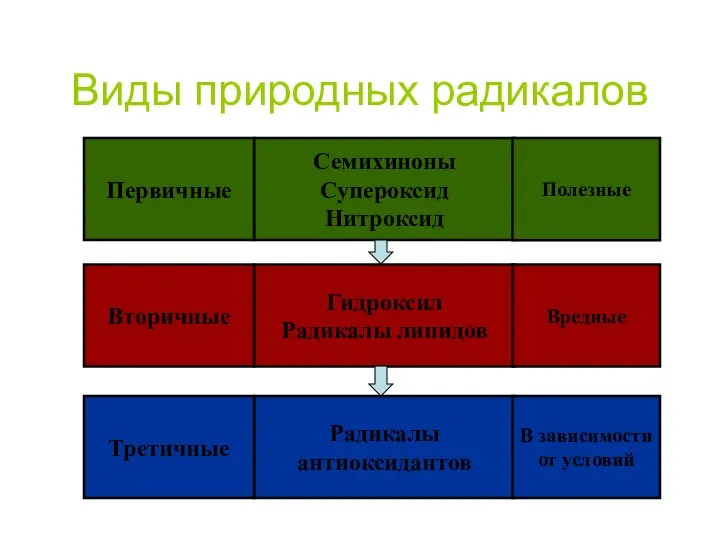
- 48. Виды природных радикалов
- 49. Значение процессов свободно-радикального окисления В НОРМЕ изменение свойств мембран; Фагоцитоз; окисление чужеродных соединений ПРИ ПАТОЛОГИИ разрушение
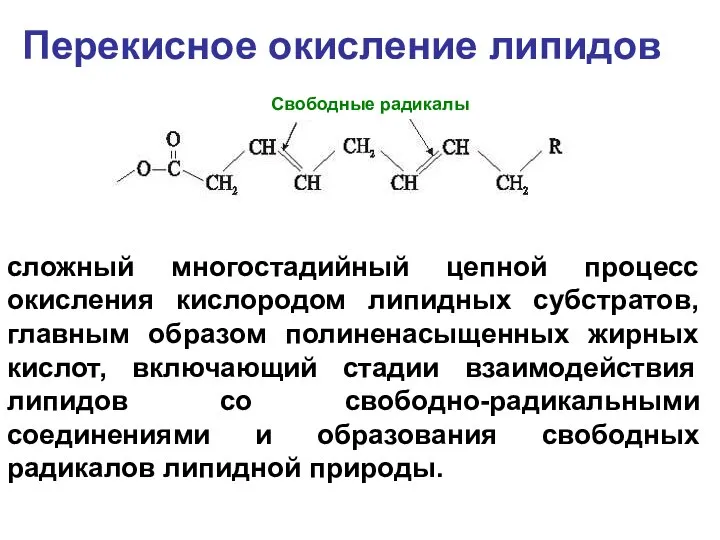
- 50. Перекисное окисление липидов сложный многостадийный цепной процесс окисления кислородом липидных субстратов, главным образом полиненасыщенных жирных кислот,
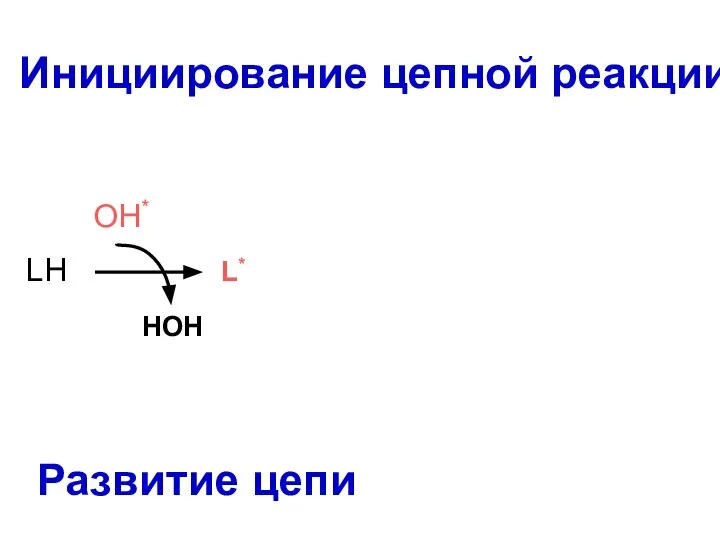
- 51. Основные стадии перекисного окисления липидов (ПОЛ) инициирование цепной реакции; развитие и разветвление цепи; разрушение структуры липидов;
- 52. Инициирование цепной реакции L* LOO* OO LH L* LOOH HOH LH OH* Развитие цепи
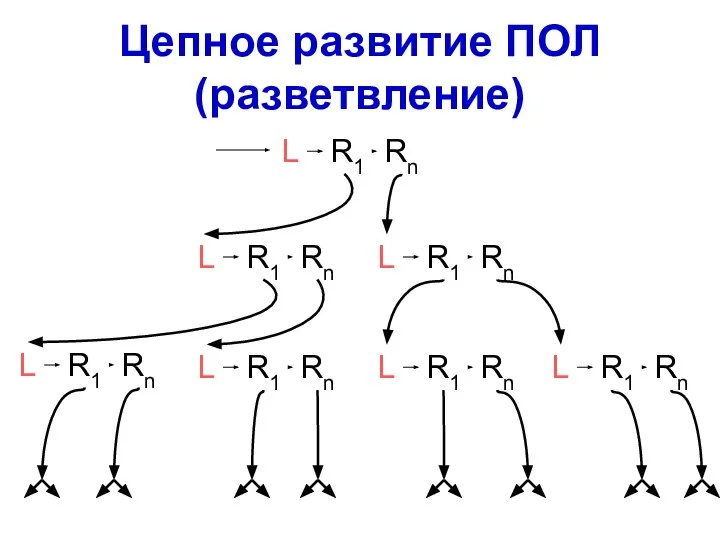
- 53. Цепное развитие ПОЛ (разветвление)
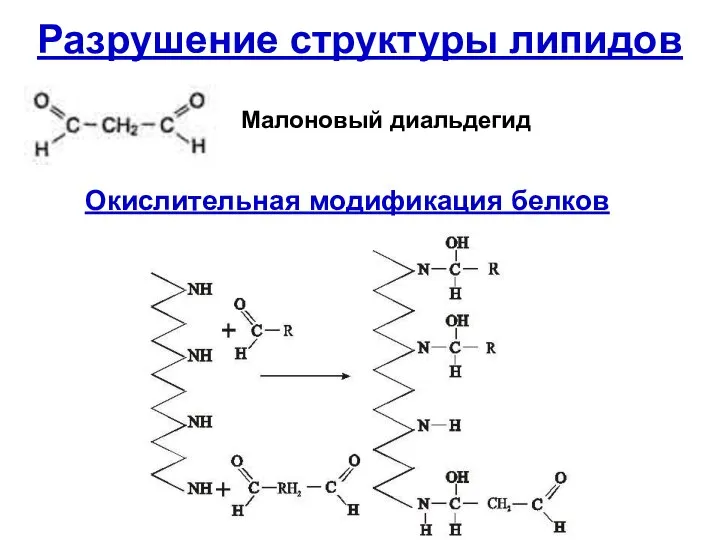
- 54. Разрушение структуры липидов Малоновый диальдегид Окислительная модификация белков
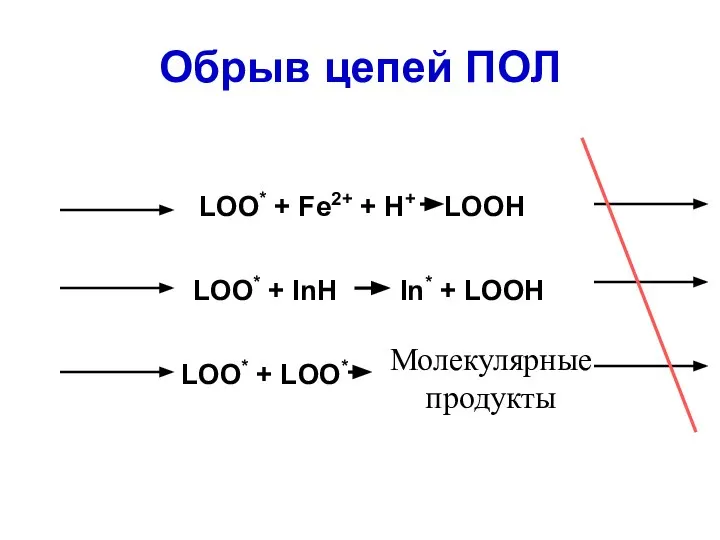
- 55. Обрыв цепей ПОЛ LOO* + Fe2+ + H+ LOOH
- 56. Механизмы защиты от свободных радикалов Предусматривают наличие в клетках антиоксидантной системы – системы, предназначенной для обезвреживания
- 57. Ферментативная антиоксидантная система Супероксиддисмутаза Каталаза Глутатионзависимые ферменты: Глутатионпероксидаза Глутатионредуктаза Глутатион-S-трансфераза
- 58. Неферментативная антиоксидантная система Витамины: Е (токоферол), С (аскорбат),биофлавоноиды Пептиды и белки: глутатион, церулоплазмин SH – соединения
- 59. К активации свободнорадикальных процессов в организме приводят: НЕДОСТАТОК БИОАНТИОКСИДАНТОВ ИНТОКСИКАЦИИ (КУРЕНИЕ, АЛКОГОЛЬ И ДР.) ХРОНИЧЕСКИЙ СТРЕСС
- 61. Скачать презентацию












































 Методика изучения периодического закона, периодической системы Д.И. Менделеева и строения атома
Методика изучения периодического закона, периодической системы Д.И. Менделеева и строения атома Презентация Валентность и степень окисления 8 класс
Презентация Валентность и степень окисления 8 класс Organic Compounds
Organic Compounds Чистые вещества и смеси
Чистые вещества и смеси Обобщение темы Строение атома и вещества
Обобщение темы Строение атома и вещества Презентация по Химии "Кремний" - скачать смотреть бесплатно
Презентация по Химии "Кремний" - скачать смотреть бесплатно Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха
Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха Пищевые кислоты
Пищевые кислоты Комплексные соединения
Комплексные соединения Использование химии в медицине
Использование химии в медицине Производство сульфата аммония (лекция)
Производство сульфата аммония (лекция) Презентация к открытому уроку Учитель химии МОУ «Гимназия №1» г. Саратов Шишкина И.Ю.
Презентация к открытому уроку Учитель химии МОУ «Гимназия №1» г. Саратов Шишкина И.Ю. СЕРА СЕРА 9 класс
СЕРА СЕРА 9 класс Галогены (солеобразующие)
Галогены (солеобразующие) Любовь, что движет Солнце и Светила Интегрированный урок по химии и литературе Подготовили: учитель химии Акимова О.В.
Любовь, что движет Солнце и Светила Интегрированный урок по химии и литературе Подготовили: учитель химии Акимова О.В.  Окислительно-восстановительные процессы
Окислительно-восстановительные процессы Каменск Уральский техникум торговли и сервиса
Каменск Уральский техникум торговли и сервиса Предельные углеводороды. Химические свойства. 10 класс
Предельные углеводороды. Химические свойства. 10 класс Proteins. Functions, structure, classification
Proteins. Functions, structure, classification оксиды - св-ва — уч-ся
оксиды - св-ва — уч-ся Техника безопасности на уроках химии_
Техника безопасности на уроках химии_ Альдегиды
Альдегиды Хромотография, явления, атомы и молекулы. 8 класс
Хромотография, явления, атомы и молекулы. 8 класс Effect receiving modes, and heat treatment on the structure and properties of the magnetic powder of strontium hexaferrite
Effect receiving modes, and heat treatment on the structure and properties of the magnetic powder of strontium hexaferrite Галогены
Галогены α – амин қышқылдары. Пептидтер. Ақуыздар
α – амин қышқылдары. Пептидтер. Ақуыздар Каучук. Применение
Каучук. Применение Биологическая коррозия и защита строительных материалов и конструкций от биоповреждений
Биологическая коррозия и защита строительных материалов и конструкций от биоповреждений