Содержание
- 2. Биохимия растений Биохимия микроорганизмов Биохимия животных Биохимия человека Объект исследования и разделы
- 3. Биохимия человека Эволюционная Космическая Фармацевтическая всасывание лекарств, их биотрансформация, обезвреживание Клиническая биохимия Скрининг, диагностика, мониторинг, эффективность
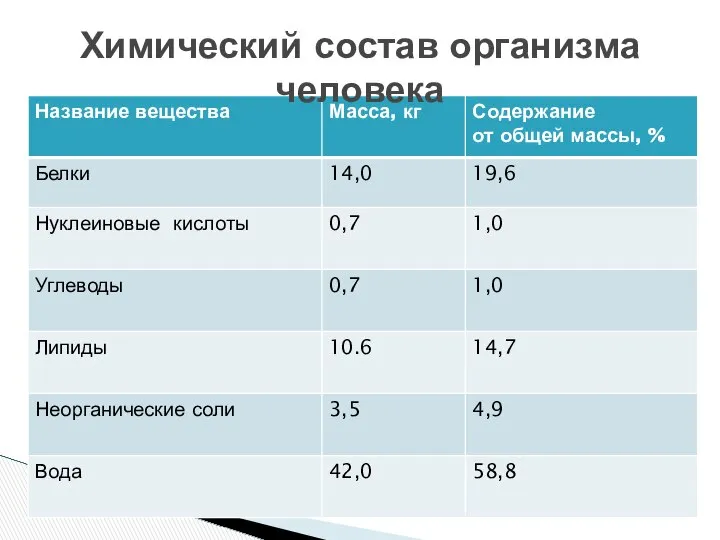
- 5. Химический состав организма человека
- 6. Структурная (пластическая) Регуляторная (ферменты, гормоны) Генетическая Транспортная Защитная Энергетическая Депонирующая (запас и питание) Сократительная и двигательная
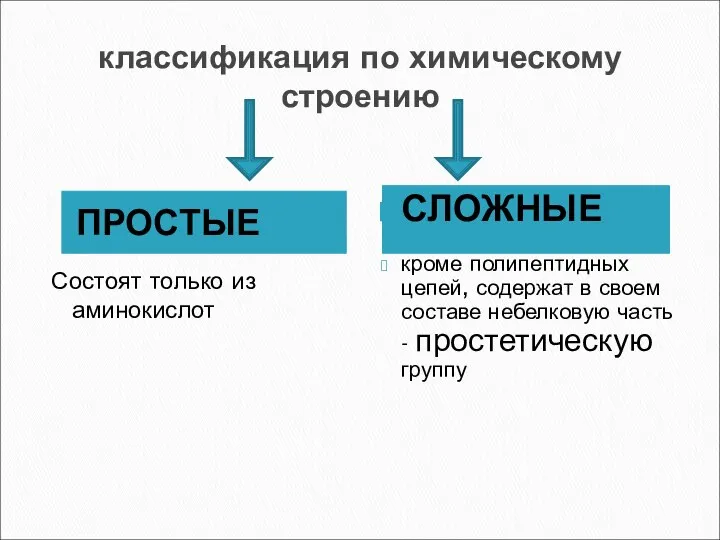
- 7. классификация по химическому строению ПРОСТЫЕ Состоят только из аминокислот СЛОЖНЫЕ кроме полипептидных цепей, содержат в своем
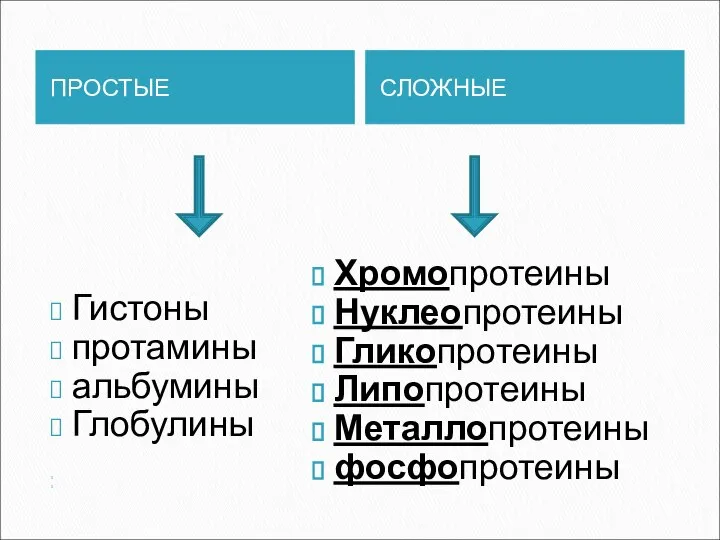
- 8. ПРОСТЫЕ СЛОЖНЫЕ Гистоны протамины альбумины Глобулины Хромопротеины Нуклеопротеины Гликопротеины Липопротеины Металлопротеины фосфопротеины
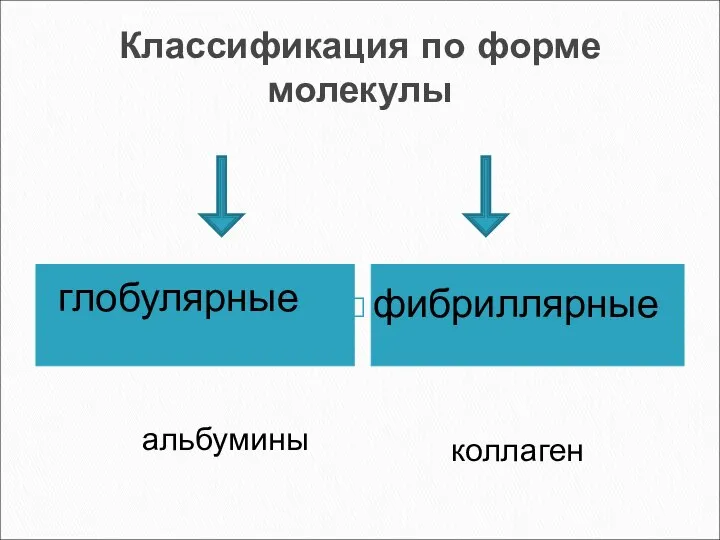
- 9. Классификация по форме молекулы глобулярные фибриллярные альбумины коллаген
- 10. Сократительные Транспортные Ферменты гормоны Классификация по функциональному (биологическому) признаку
- 11. Пептиды до 10 а.к. ММ 1000Да Олигопептиды 40 а.к. ММ 1000-4000 да Белки >40 а.к. ММ
- 12. Аминокислоты (АК) R | NH2 - Cα – COOH | H
- 13. R-CН-CООН | NH2 Аминокислоты входящие в состав -20 Модифицированные аминокислоты оксилизин, оксипролин Аминокислоты в свободном виде,
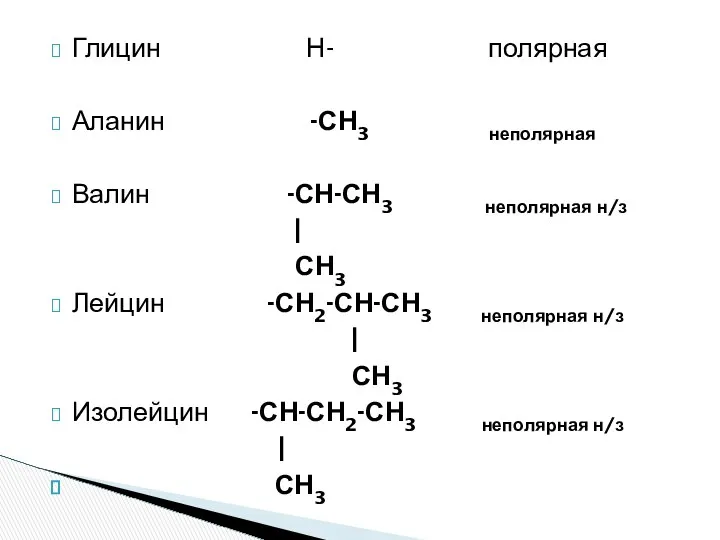
- 14. Глицин Н- полярная Аланин -СН3 неполярная Валин -СН-СН3 неполярная н/з | СН3 Лейцин -СН2-СН-СН3 неполярная
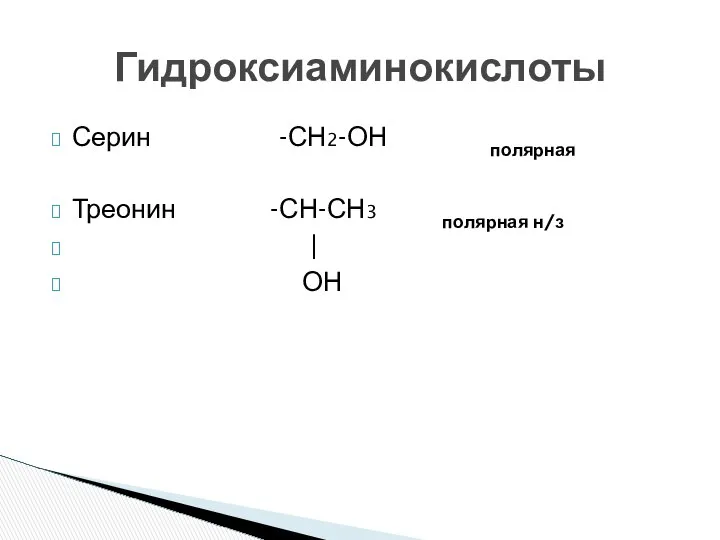
- 15. Серин -СН2-ОН полярная Треонин -СН-СН3 полярная н/з | ОН Гидроксиаминокислоты
- 16. Цистеин -СН2-SH полярная Метионин -СН2-СН2-S-СН3 неполярная н/з Cеросодержащие
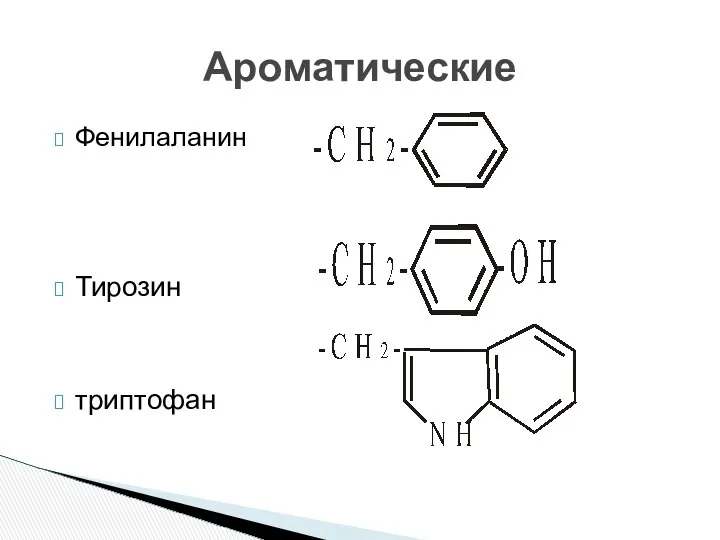
- 17. Фенилаланин Тирозин триптофан Ароматические
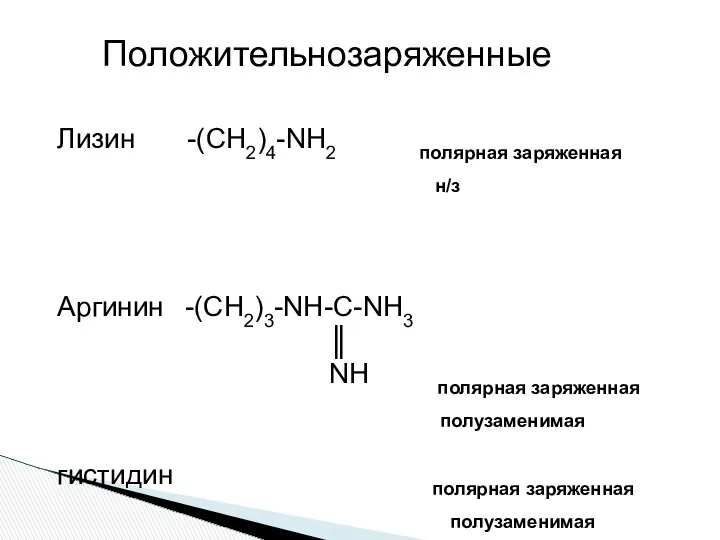
- 18. Лизин -(СН2)4-NH2 полярная заряженная н/з Аргинин -(СН2)3-NH-C-NH3 ║ NH полярная заряженная полузаменимая гистидин полярная заряженная полузаменимая
- 19. гистидин
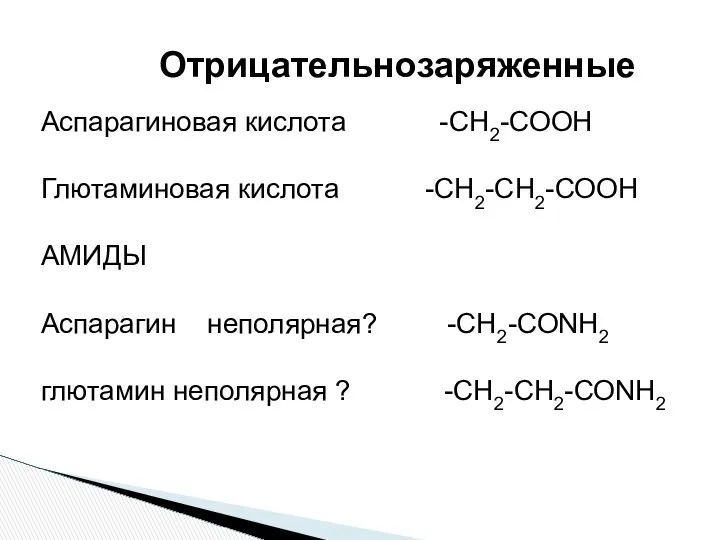
- 20. Аспарагиновая кислота -СН2-СООН Глютаминовая кислота -СН2-СН2-СООН АМИДЫ Аспарагин неполярная? -СН2-СОNH2 глютамин неполярная ? -СН2-СН2-СОNH2 Отрицательнозаряженные
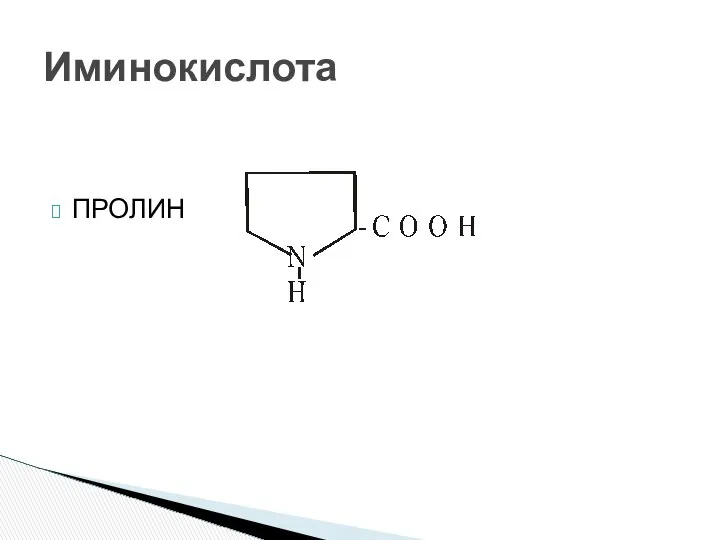
- 21. ПРОЛИН Иминокислота
- 22. Алифатические Циклические гетероциклические Классификация по химическому строению
- 23. Заряженные: Кислые, Основные Участвуют в образовании водородных связей; Обеспечивают ионные взаимодействия внутри белка; Обеспечивают ионные взаимодействия
- 24. Заменимые Незаменимые Для человека незаменимыми являются 8 аминокислот : Val, Ile, Leu, Thr, Met, Phe, Trp,
- 25. Глюкогенные глицин – на синтез углеводов асп,глу аланин,серин,тре, вал, арг гис мет Кетогенные – на синтез
- 26. Alanine Ala A Arginine Arg R Asparagine Asn N Aspartic acid Asp D Cysteine Cys C
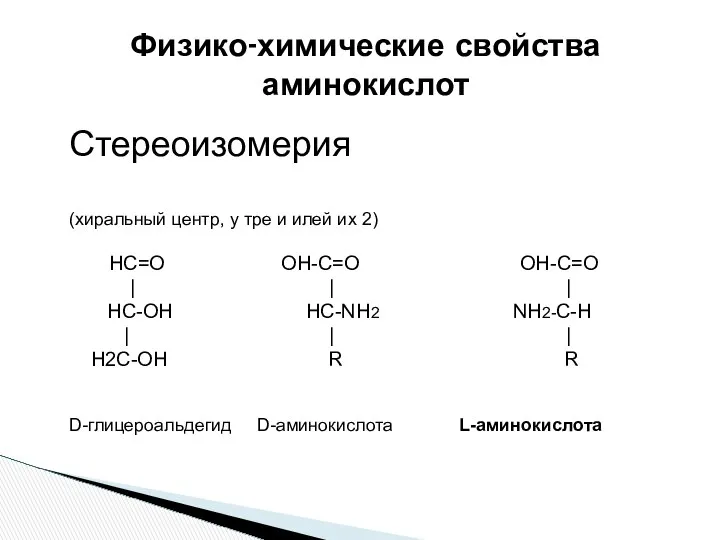
- 27. Физико-химические свойства аминокислот Стереоизомерия (хиральный центр, у тре и илей их 2) НС=О ОН-С=О ОН-С=О |
- 28. Обладают оптической активностью Левовращающие (-) гис, про, сер, тре, фен Правовращающие(+) ала, арг, глу,илей, лиз
- 29. Спектр поглощения ультрафиолетовая область тир три - 280 нм Фен - 260 Цис - 240
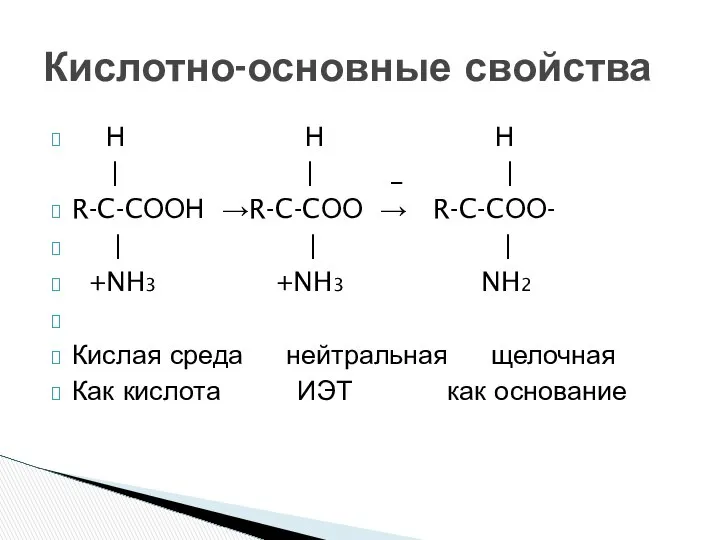
- 30. Н Н Н | | _ | R-C-CООН →R-C-CОО → R-C-CОО- | | | +NH3 +NH3
- 32. Способность к полимеризации – образование амидной (пептидной) связи
- 33. Формирование полипептидной цепи H2O
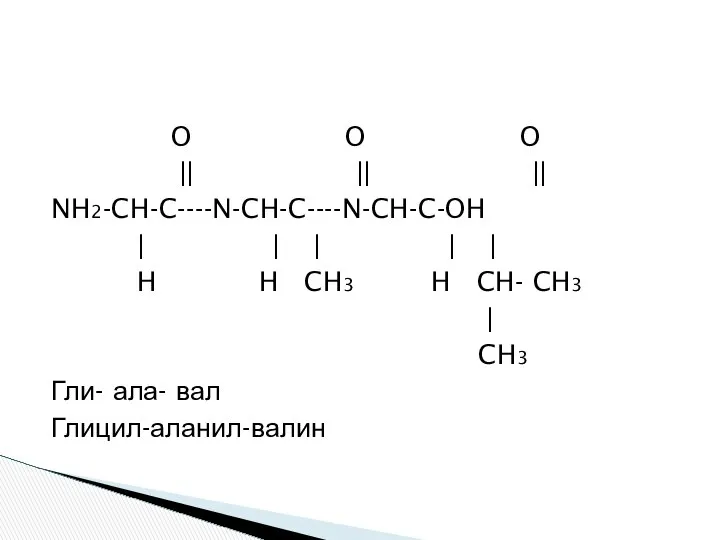
- 34. O O O || || || NH2-CH-C----N-CH-C----N-CH-C-OH | | | | | H H CH3 H
- 36. Скачать презентацию




















 Азотная кислота и ее соли. Раскаленный уголек, брошенный в концентрированную азотную кислоту, продолжает гореть, при этом выде
Азотная кислота и ее соли. Раскаленный уголек, брошенный в концентрированную азотную кислоту, продолжает гореть, при этом выде Полимеры. Классификация полимеров
Полимеры. Классификация полимеров Аскорбиновая кислота. Глютаминовая кислота. Кислота аминокапроновая
Аскорбиновая кислота. Глютаминовая кислота. Кислота аминокапроновая Установка гидрокрекинга в составе завода глубокой переработки нефти ООО «Кинеф»
Установка гидрокрекинга в составе завода глубокой переработки нефти ООО «Кинеф» Студент − это не сосуд, который надо наполнить, а факел, который надо зажечь Л. Арцимович
Студент − это не сосуд, который надо наполнить, а факел, который надо зажечь Л. Арцимович Основные закономерности химико-технологического процесса. Основные технологические понятия и определения
Основные закономерности химико-технологического процесса. Основные технологические понятия и определения Сополимеризация. Основные количественные характеристики процесса сополимеризации
Сополимеризация. Основные количественные характеристики процесса сополимеризации Минералы и их свойства
Минералы и их свойства Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Введение в органическую химию. 10 класс
Введение в органическую химию. 10 класс Циклоалканы
Циклоалканы Лакокрасочные материалы
Лакокрасочные материалы Роль липидов в формировании потребительских свойств
Роль липидов в формировании потребительских свойств Э.М. Спиридонов. Эволюция минералов серебра в зоне гипергенеза
Э.М. Спиридонов. Эволюция минералов серебра в зоне гипергенеза Минералы и их классификация
Минералы и их классификация Химическое равновесие и способы его смещения
Химическое равновесие и способы его смещения Fiber. Iron. Calcium
Fiber. Iron. Calcium Функциональные производные с кратной связью C=“Э”. Часть 1. Карбонильные соединения и имины
Функциональные производные с кратной связью C=“Э”. Часть 1. Карбонильные соединения и имины Органические вяжущие. (Лекция 12)
Органические вяжущие. (Лекция 12) Взаимодействие солей аммония со щелочами
Взаимодействие солей аммония со щелочами Презентация по Химии "ВЛИЯНИЕ ГАЗИРОВАННЫХ НАПИТКОВ НА ОРГАНИЗМ ЧЕЛОВЕКА" - скачать смотреть
Презентация по Химии "ВЛИЯНИЕ ГАЗИРОВАННЫХ НАПИТКОВ НА ОРГАНИЗМ ЧЕЛОВЕКА" - скачать смотреть  Химия. Основные понятия и законы
Химия. Основные понятия и законы «Надпровідний розчин» Опишіть, яким чином на електропровідність розчинів впливають температура, природа розчинника, природа
«Надпровідний розчин» Опишіть, яким чином на електропровідність розчинів впливають температура, природа розчинника, природа  Презентация по Химии "Алканы 10 класс" - скачать смотреть
Презентация по Химии "Алканы 10 класс" - скачать смотреть  Союз химии и медицины
Союз химии и медицины Органическая химия. Жиры
Органическая химия. Жиры Газообразные вещества
Газообразные вещества Тема урока Железо Цель урока: Рассмотреть электронное строение атома железа, дать общую характеристику его. Изучить основные
Тема урока Железо Цель урока: Рассмотреть электронное строение атома железа, дать общую характеристику его. Изучить основные